Газета «Новости медицины и фармации» 2(307) 2010
Вернуться к номеру
Железодефицитная анемия в практике терапевта
Авторы: Л.И. Дворецкий, профессор, Московская медицинская академия имени И.М. Сеченова
Версия для печати
Железодефицитная анемия (ЖДА) представляет собой клинико-гематологический синдром, характеризующийся дефицитом железа вследствие различных патологических (физиологических) процессов. Разнообразная клиническая симптоматика ЖДА, основным проявлением которой является анемический синдром, требует от врачей различных специальностей, и прежде всего интернистов, своевременной и правильной диагностики природы анемического синдрома.
Повседневная клиническая практика свидетельствует о том, что по мере тенденции к врачебной специализации, возрастания роли врачей — узких специалистов и ограничения сферы деятельности врача-интерниста в широком смысле многие больные направляются к консультантам — специалистам соответствующего профиля по чисто формальным признакам (изменения в крови или моче, выявление эрозивно-язвенного процесса в желудке при гастроскопии и т.д.). В значительной степени это касается больных с анемическим синдромом, в частности ЖДА. Среди врачей общей практики бытует мнение о том, что больные с ЖДА должны наблюдаться у гематолога, хотя при данной патологии речь идет не о заболевании системы крови, а лишь об одном из лабораторных проявлений разнообразных проблем, приводящих к развитию дефицита железа, одним из проявлений которого является анемический синдром.
Проявления ЖДА не являются клинически специфичными и характеризуются различными синдромами, знание которых необходимо врачу-интернисту независимо от его узкой специализации. Наряду с анемией, которая не всегда является ведущим синдромом, ЖДА проявляется астеническими симптомами, мышечной слабостью и синдромом эпителиопатии (сухость кожи, «заеды» в углах рта, ломкость и слоистость ногтей, выпадение волос и др.). Поражение слизистых у больных ЖДА проявляется такими симптомами, как затруднения глотания (сидеропеническая дисфагия), дизурические расстройства, развитие атрофических пангастритов с секреторной недостаточностью, нарушение белковосинтетической, энергосберегающей и ферментной функций печени. По мере развития и усугубления ЖДА развиваются нарушения со стороны сердечно-сосудистой системы в виде миокардиодистрофии, диастолической дисфункции с нарушением пассивного расслабления, гиперкинетического типа кровообращения. Указанные нарушения не всегда ассоциируются с вероятностью наличия железодефицитного состояния, что приводит к несвоевременной диагностике и лечению ЖДА.
Компетенция терапевта при ведении больных ЖДА:
Лабораторные признаки, позволяющие заподозрить и верифицировать ЖДА:
При трактовке результатов анализа крови следует обязательно обращать внимание не только на цветовой показатель, который может быть рассчитан неправильно (например, в случае ошибочного подсчета количества эритроцитов), но и на морфологическую характеристику эритроцитов (гипохромия эритроцитов и ее выраженность, микроцитоз). При использовании в лабораторной практике современных анализаторов имеется возможность непосредственного определения среднего содержания гемоглобина в одном эритроците, обозначающегося латинской аббревиатурой МСН (в норме 27–35 пг).
Гипохромный характер анемии делает весьма вероятным ее железодефицитный характер (все ЖДА являются гипохромными), однако не исключает другие патогенетические варианты анемий (не все гипохромные анемии являются железодефицитными). В связи с этим необходима дифференциальная диагностика ЖДА с другими, реже встречающимися гипохромными анемиями (сидероахрестические анемии, талассемия). Определение уровня сывороточного железа позволяет разграничить эти состояния на данном этапе диагностического поиска. На показатели сывороточного железа может влиять целый ряд факторов, маскирующих тем самым истинное содержание железа в сыворотке, что следует учитывать при трактовке полученных результатов:
Наряду с определением концентрации железа в сыворотке диагностическое значение имеет оценка общей железосвязывающей способности сыворотки (ОЖСС), отражающей степень «голодания» сыворотки и насыщения трансферрина железом. У больных ЖДА отмечаются повышение ОЖСС, значительное повышение латентной железосвязывающей способности и уменьшение процента насыщения трансферрина. Поскольку запасы железа при развитии ЖДА истощены, отмечается снижение содержания в сыворотке ферритина — железосодержащего белка, уровень которого отражает наряду с концентрацией гемосидерина величину запасов железа в депо. Снижение уровня ферритина в сыворотке является наиболее чувствительным и специфичным признаком дефицита железа.
Нозологический этап диагностического поиска при ЖДА
После верификации железодефицитного характера анемии, то есть синдрома ЖДА, необходимо выявление причины, лежащей в основе данного варианта анемического синдрома (нозологический этап диагностики). Для клинициста этот этап является наиболее трудным и ответственным, поскольку в основе имеющейся ЖДА могут лежать потенциально курабельные заболевания. Наличие в МКБ-10 рубрики «ЖДА неуточненная» оставляет для врача «лазейку» в случаях отсутствия явной причины анемии, освобождая его от тщательности и углубления диагностического поиска на этапе нозологической диагностики. Следует подчеркнуть важную роль врача-интерниста на этапах синдромной и нозологической диагностики, поскольку подавляющее большинство больных ЖДА независимо от вызванной причины обращаются прежде всего, как и многие другие пациенты, к терапевту.
Основные причины ЖДА включают:
2) нарушение всасывания:
3) повышенная потребность:
4) алиментарная недостаточность.
Лечение больных ЖДА
В случаях выявления причины ЖДА лечение должно быть направлено на устранение этой причины (в случае возможности) или коррекцию имеющихся нарушений (эрозивно-язвенные и опухолевые поражения ЖКТ, миома матки, энтериты, алиментарная недостаточность и др.).
Всем больным ЖДА показана патогенетическая терапия препаратами железа. Следует подчеркнуть ошибочность мнения о возможности коррекции дефицита железа с помощью пищевых продуктов с высоким содержанием железа, что является одним из мифов в представлениях о ведении больных ЖДА. Об этом должны быть осведомлены больные, что следует считать важным образовательным компонентом ведения данной категории пациентов. Разумеется, пища должна быть богата продуктами, содержащими железо. Однако следует иметь в виду неодинаковую степень всасываемости железа из различных продуктов. Так, например, железо, содержащееся в мясе в виде гема, всасывается на 40–50 %, в то время как из растительных продуктов, овощей, фруктов всасывается всего 3–5 % железа. Поэтому средством выбора для коррекции дефицита железа и уровня гемоглобина у больных ЖДА являются лекарственные препараты железа (ПЖ).
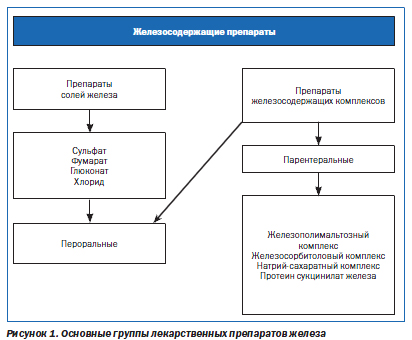
В настоящее время в распоряжении врача имеется большой арсенал лекарственных ПЖ, характеризующихся различным количеством содержащегося в них железа, наличием дополнительных компонентов, влияющих на фармакокинетику, различной лекарственной формой (рис. 1).
Путь введения препаратов железа. В большинстве случаев для коррекции дефицита железа при отсутствии специальных показаний ПЖ следует назначать внутрь. Путь введения у больных ЖДА определяется конкретной клинической ситуацией, в частности, состоянием кишечного всасывания и переносимостью пероральных ПЖ. Основным показанием для парентерального введения ПЖ следует считать наличие патологии кишечника с нарушением всасывания (различные энтериты, синдром недостаточности всасывания, резекция тонкой кишки, резекция желудка по Бильрот II с формированием «слепой петли»). ПЖ для парентерального введения могут быть средством выбора при плохой переносимости пероральных ПЖ, однако большинство современных препаратов переносится сравнительно удовлетворительно. В связи с этим принятие решения о назначении парентерального ПЖ должно осуществляться только после ряда врачебных маневров (снижение дозы ПЖ, прием вместе с пищей, смена препарата и т.д.). Темпы прироста уровня гемоглобина при назначении ПЖ внутрь и парентерально оказались приблизительно одинаковыми, в связи с чем предпочтение ПЖ в инъекционных формах в случаях необходимости более быстрого прироста уровня гемоглобина (например, при подготовке больной миомой к оперативному вмешательству) следует считать неоправданным. Многие врачи обосновывают назначение парентеральных ПЖ выраженностью анемического синдрома в расчете на их якобы больший эффект, что также не имеет достаточных оснований и не подтверждается клинической практикой.
Выбор лекарственного препарата железа. Не менее важным шагом является выбор конкретного лекарственного ПЖ для приема внутрь, тем более что в настоящее время на российском фармацевтическом рынке имеется большой арсенал ПЖ в виде различных солей железа и в меньшем количестве — в виде железосодержащих комплексов. Выбор ПЖ и оптимального режима его дозирования должен определяться количеством и биодоступностью содержащегося в нем железа, переносимостью, стоимостью. При этом необходимо иметь в виду, что адекватный прирост показателей гемоглобина у больных ЖДА может быть обеспечен поступлением в организм от 30 до 100 мг элементарного железа. Учитывая, что при развитии ЖДА всасывание железа увеличивается по сравнению с нормой и составляет 25–30 % (при нормальных запасах железа — всего 3–7 %), необходимо назначать от 100 до 300 мг элементарного железа в сутки. Применение более высоких доз не имеет смысла, поскольку всасывание железа при этом не увеличивается. С учетом этого при выборе ПЖ следует ориентироваться не на содержание в нем общего количества соединений железа, а на количество элементарного железа. Например, при назначении препаратов сульфата железа с низким содержанием элементарного железа (менее 100 мг) количество принимаемых таблеток должно быть от 3 и выше (в зависимости от содержания железа в каждой таблетке), в то время как препараты сульфата, фумарата или гидроксиполимальтозного комплекса железа с содержанием 100 мг элементарного железа можно принимать в количестве 1–2 таблетки в сутки. Основные препараты солей железа (ПСЖ) представлены сульфатом железа, глюконатом, хлоридом, фумаратом, глицинсульфатом. Наибольшей степенью абсорбции обладают препараты сульфата железа, наименьшей — глицинсульфата. Многие из ПСЖ содержат вещества, например аскорбиновую кислоту, усиливающие всасывание железа и улучшающие биодоступность препарата, а также витамины (фолиевую кислоту, цианокобаламин). Среди препаратов железосодержащих комплексов (ПЖК) на отечественном рынке имеются гидроксиполимальтозный комплекс, железосорбитоловый комплекс, протеин сукцинилат железа, железосахарозный комплекс. Необходимо учитывать, что всасывание железа из ПСЖ может уменьшаться под влиянием содержащихся в некоторых пищевых продуктах веществ — фитинов (рис, соя), фосфатов (рыба, морепродукты), танина (чай, кофе). Многие больные склонны запивать лекарства чаем, что в случаях приема ПСЖ недопустимо, поскольку образуются плохо растворимые комплексы с низкой их абсорбцией в кишечнике. Кроме того, всасывание железа из ПЖ в виде солей ухудшается при одновременном приеме ряда медикаментов (тетрациклины, антациды, соли кальция и магния). С учетом этого следует рекомендовать прием ПСЖ в различное время с другими вышеуказанными медикаментами. В то же время препараты ПЖК, в частности гидроксиполимальтозный комплекс, лишены подобных недостатков, поскольку пищевые продукты и медикаменты не оказывают влияния на всасываемость железа (в виде трехвалентной формы) из железосодержащих комплексов.
Как уже упоминалось, ПСЖ содержат двухвалентное железо, которое после поступления в кровь превращается в трехвалентное для последующего его включения в молекулу гемоглобина. Процесс превращения двухвалентного железа в трехвалентное благодаря потере одного электрона может сопровождаться образованием свободных радикалов, что обозначается как оксидативный стресс, способный оказывать негативное влияние на физиологические процессы в различных органах и тканях. В то же время ПЖК, в состав которых входит трехвалентное железо, непосредственно использующееся для построения молекулы гемоглобина, лишены возможного прооксидантного действия. Это различие между двумя группами железосодержащих препаратов постулируется как недостаток ПСЖ и дает якобы преимущество ПЖК. Между тем способность ПСЖ вызывать оксидативный стресс в отличие от ПЖК показана в эксперименте на крысах и в условиях in vitro. Реальность феномена оксидативного стресса при лечении ПСЖ в клинических условиях оставалась недоказанной. В проведенных нами исследованиях различных показателей активности свободнорадикального перекисного окисления липидов (базальная и стимулированная хемолюминисценция, малоновый диальдегид) и антиперекисной активности плазмы не выявлено активизации процессов свободноперекисного окисления у больных ЖДА на фоне лечения ПСЖ.
При выборе препарата, содержащего железо, необходимо учитывать несколько факторов. Поскольку из желудочно-кишечного тракта ионизированное железо всасывается только в двухвалентной форме и большое значение в этом процессе играет аскорбиновая кислота, то очень важно ее наличие в препарате. Существенная роль в гемопоэзе принадлежит фолиевой кислоте, усиливающей нуклеиновый обмен: для нормального обмена необходим цианокобаламин, который является основным фактором при образовании из фолиевой кислоты активной формы. Дефицит этих веществ, часто возникающий при анемиях, связанных с кровопотерями, приводит к нарушению синтеза ДНК в кроветворных клетках, тогда как включение этих компонентов в препарат увеличивает активную абсорбцию железа в кишечнике, его дальнейшую утилизацию, а также освобождает дополнительное количество трансферрина и ферритина. Все это значительно увеличивает скорость синтеза гемоглобина и повышает эффективность терапии железодефицитных состояний и железодефицитной анемии.
Продолжительность лечения. Длительность насыщающей терапии ПЖ определяется, с одной стороны, выраженностью дефицита железа и анемического синдрома, а с другой — темпами прироста и сроками нормализации гемоглобина на фоне лечения. В большинстве случаев восстановление показателей гемоглобина до нормальных происходит через 3–4 недели. Следует подчеркнуть, что у многих женщин улучшение самочувствия на фоне лечения ПЖ наблюдается раньше, чем происходит восстановление показателей гемоглобина до нормальных. В связи с этим прием ПЖ становится нерегулярным и иногда прекращается вообще. При этом не происходит полной коррекции уровня гемоглобина, и ЖДА остается фактически недолеченной. С учетом данного обстоятельства при оценке эффективности терапии необходимо ориентироваться на лабораторные показатели, то есть на уровень гемоглобина, а не на субъективные ощущения, о чем пациентки должны быть обязательно информированы.
Оценка эффективности и причин неэффективности лечения. В случаях назначения ПЖ в достаточной дозе на 7–10-й день от начала лечения наблюдается повышение количества ретикулоцитов. Достоверное повышение уровня гемоглобина отмечается через 3–4 нед. от начала лечения. Нормализация показателей гемоглобина обычно происходит в сроки 4–9 нед. Иногда наблюдается резкое скачкообразное повышение гемоглобина. Эти индивидуальные колебания могут быть обусловлены, с одной стороны, выраженностью ЖДА, степенью истощения запасов железа, а с другой — темпами прироста показателей гемоглобина на фоне назначенного ПЖ (количество содержащегося железа, биодоступность
Особые ситуации в терапевтической практике
Разнообразие клинических ситуаций у больных с наличием анемического синдрома, в частности ЖДА, требует от врача-интерниста принятия оптимального решения, основанного на патогенетических особенностях и основной причине анемии, наличии сопутствующей патологии, ответе на лечение. О подобных сложностях можно говорить при следующих ситуациях:
ЖДА у больных пожилого и старческого возраста. ЖДА наряду с В12-дефицитной анемией имеют наибольший удельный вес в структуре анемий у пожилых. Клиническое значение ЖДА у данной категории пациентов определяется еще и тем, что она нередко встречается в рамках коморбидных состояний, оказывая негативное влияние на имеющиеся сопутствующие заболевания, усугубляя и утяжеляя их клинические проявления. Это касается в первую очередь ишемической болезни сердца (утяжеление и учащение приступов стенокардии), сердечной недостаточности (рефрактерность к лечению), дисциркуляторной энцефалопатии. Нередко у пожилых больных ЖДА может сочетаться с другими патогенетическими вариантами, например В12- и фолиеводефицитной анемией. В подобных ситуациях показаны ПЖ, содержащие фолиевую кислоту. Наличие полиморбидности у пожилых влечет за собой назначение нескольких лекарственных препаратов (вынужденная полипрагмазия), что необходимо учитывать при одновременном назначении ПЖ. Не следует принимать ПЖ одновременно с препаратами кальция, пленкообразующими лекарствами (альмагель, фосфалюгель и др.).
ЖДА у больных с продолжающимися хроническими кровопотерями (носовые, маточные). Женщинам, страдающим ЖДА на фоне меноррагий при отсутствии явной гинекологической патологии как причины меноррагий и невозможности их корригировать, необходима длительная терапия ПЖ внутрь. То же касается больных с хроническими носовыми кровотечениями, например наследственной геморрагической телеангиэктазией (болезнь Рандю — Ослера). Целесообразно назначать препараты с высоким содержанием железа, позволяющим осуществлять одно- или двухразовый прием в сутки, что способствует достижению комплайенса пациентов.
ЖДА беременных. ЖДА беременных требует обязательной коррекции лекарственными ПЖ для приема внутрь, лечение ПЖ при диагностированной ЖДА должно проводиться до конца беременности. Это имеет принципиальное значение не только для коррекции анемии у беременных и профилактики осложнений в родах, послеродовых инфекций, но и главным образом для предупреждения дефицита железа у плода. Фактически назначение препаратов железа беременным является антенатальной профилактикой ЖДА. Целесообразно назначение ПЖ в сочетании с фолиевой кислотой, особенно при наличии факторов риска дефицита фолиевой кислоты (алкоголизм, прием противосудорожных препаратов, алиментарная недостаточность) или его верификации.
При непереносимости ПСЖ внутрь следует рекомендовать прием ПЖ во время еды или уменьшение дозировки. В случае сохраняющейся непереносимости рекомендуется назначение препаратов железосодержащих комплексов. Если больные не переносят препараты (сохраняются диспептические явления или кишечные расстройства), то следует назначать ПЖ парентерально.
ЖДА у больных с невыявленной причиной. Особую категорию представляют пациенты, у которых не удается выявить причину ЖДА, что может быть обусловлено как объективными (атипичное течение заболевания, скрытые кровопотери и др.), так и субъективными (недостаточный уровень обследования больных) причинами. Эффект от лечения ПЖ данной категории пациентов бывает временным, недостаточным или вообще отсутствует; последнее при очевидной клинико-гематологической картине должно служить поводом для тщательного обследования больных, прежде всего мужчин и неменструирующих женщин (возможны опухоли толстого кишечника). С учетом этого в подобных ситуациях при исключении других возможных причин неэффективности ПЖ необходимо тщательное исследование кишечника (в ряде случаев — повторное).
Таким образом, столь распространенные в практике интерниста железодефицитные состояния характеризуются неспецифическими клиническими проявлениями и лабораторными признаками. Необходима ориентировка врача в отношении лабораторных признаков ЖДА, а также основных причин развития данного синдрома. Наряду с устранением причины обязательна патогенетическая терапия ПЖ (ПСЖ и ПЖК), которые должны назначаться преимущественно внутрь. Тактика лечения ПЖ предусматривает выбор пути введения ПЖ с учетом клинической ситуации, оптимального ПЖ с достаточным содержанием в нем железа и дополнительных веществ, оценку эффективности и переносимости препарата, длительность насыщающей и обоснованность поддерживающей терапии. Своевременная верификация синдрома ЖДА и адекватная патогенетическая терапия ПЖ позволяют корригировать анемический синдром, осуществлять и обеспечивать достаточный уровень качества жизни данной категории пациентов.
