Журнал «Здоровье ребенка» 2 (23) 2010
Вернуться к номеру
Клинический случай диагностики наследственного ангионевротического отека у ребенка 14 лет
Авторы: Волосовец А.П., Кривопустов С.П., Дзюба О.Л., Сребный М.М., Макуха Н.Т., Дюденко Н.В., Национальный медицинский университет им. А.А. Богомольца, г. Киев, Киевская городская детская клиническая больница № 2
Рубрики: Педиатрия/Неонатология
Версия для печати
В аллергологическое отделение КГДКБ № 2 поступил мальчик Н., 14 лет, с жалобами на плотный отек подбородка, губ, носа, щек, отек языка, затрудняющий дыхание, ощущение сдавления в груди. Заболел остро за день до госпитализации. Связывает заболевание с приемом пищи (съел 0,5 кг трубочек с какао).
Ребенок от I беременности, I патологических родов (кесарево сечение). Рос и развивался соответственно возрасту. Братьев, сестер нет. Наследственность не отягощена (по материнской линии, достоверных сведений об отцовской линии нет). Пищевая аллергия на цитрусовые, мед. Впервые диагноз «отек Квинке» был поставлен в 2 года. Сначала отеки наблюдались с частотой 5–10 эпизодов в год, в дальнейшем они участились до 50–60 раз в год. Провоцирующими факторами выступали травмы, сильное сдавление, холод, употребление в пищу меда, сладостей, цитрусовых. Родители связывают появление отеков с погрешностями в диете (употреблением большого количества сладостей, цитрусовых). Выраженный отек, потребовавший стационарного лечения, наблюдался впервые в 9 лет, в лечении тогда применялись высокие дозы стероидов, антигистаминные препараты, но достоверного эффекта от лечения не наблюдалось. Один раз был госпитализирован в неотложном порядке в реанимационное отделение по поводу асфиксии. Ребенок многократно обследован в различных учреждениях, консультирован детскими аллергологами. При обследовании общеклинический анализ крови — без существенных изменений (эозинофилии не выявлено), общий IgE — в пределах нормы.
При объективном обследовании: состояние ребенка средней степени тяжести, он в сознании, адекватно реагирует на осмотр. Нормостенического телосложения. Наблюдается отек в нижней части лица, четко ограниченный по площади. Отек очень плотный, кожа над ним бледная, при пальпации безболезненная. Зуда в области отека нет. Слизистая ротоглотки розовая, миндалины не увеличены, язык отечный, увеличенный в размерах, с отпечатками зубов. В легких дыхание везикулярное. Тоны сердца ритмичные, звучные. Живот мягкий, доступен пальпации.
Результаты лабораторных и инструментальных исследований . Общеклинический анализ крови: Hb 154 г/л, лейкоциты 8,5 Г/л, палочкоядерных 6 %, сегментоядерных 76 %, эозинофилов 7 %, лимфоцитов 8 %, моноцитов 3 %; общеклинический анализ мочи — без особенностей; протеинограмма: общий белок 81 г/л, альбуминов 47 %, глобулинов 53 %, А/Г 0,89.
В стационаре получал лечение: адреналин, преднизолон, фуросемид, дезлоратадин в соответствующих возрастных дозах.
Учитывая незначительный эффект от предложенной схемы лечения, частые рецидивы отеков Квинке в анамнезе, во время консилиума в клинике было заподозрено наличие патологии иммунной системы, а именно наследственного ангионевротического отека (НАО). Проведены лабораторные тесты:
— ингибитор С1 эстеразы — 21,74 мг/дл (норма 23–41 мг/дл);
— система комплемента С3 — 116,7 мг/дл (норма 90–180 мг/дл);
— система комплемента С4 — 2,1 мг/дл (норма 10–40 мг/дл).
В результате обнаружился дефицит С4 фрагмента комплемента и незначительное уменьшение уровня ингибитора С1 эстеразы. Это подтверждает наличие у мальчика наследственного ангионевротического отека. В схему лечения была добавлена аминокапроновая кислота и свежезамороженная плазма в целях заместительной терапии. После улучшения состояния, исчезновения отека ребенок выписан из стационара.
Наследственный ангионевротический отек — хроническое заболевание, относящееся к группе первичных иммунодефицитов с аутосомно-доминантным наследованием и неполной пенетрантностью, связанное с качественным или количественным генетически детерминированным дефектом генов, кодирующих синтез ингибитора эстеразы компонента комплемента C1, которое проявляется в виде рецидивирующих отеков кожи и слизистых оболочек дыхательных путей, желудочно-кишечного (ЖКТ) и урогенитального трактов [3].
Впервые клинически это заболевание описано W. Osler в 1888 г . Он обратил внимание, что пять поколений одной американской семьи страдали от эпизодически появляющихся отеков, которые рано или поздно заканчивались смертельным исходом. Многие врачи описывали клинику заболевания, но только в 1963 г . Dinkelaker доказал генетическую природу и конкретный механизм НАО [4, 6].
Существуют три клинически идентичных типа наследственного ангионевротического отека, определить которые можно лишь при исследовании компонентов комплемента в крови.
НАО 1-го типа (85–90 % случаев) связан с отсутствием гена, кодирующего ингибитор С1, или с различными его мутациями. При 2-м типе НАО (10–15 % пациентов) ген ингибитора имеет точковые мутации и молекулы ингибитора синтезируются, но имеют дефекты. НАО 3-го типа — это заболевание описано K.E. Binkley и A. Davis в 2000 г ., распространенность его неизвестна. Концентрация ингибитора С1 в плазме крови нормальная, механизм заболевания, вероятно, не связан с ингибитором С1. Этот тип наблюдается только у женщин, характер родословных предполагает Х-сцепленный доминантный тип наследования. Особенностью этой формы является развитие НАО во время беременности (через 2–3 нед.) или через 1–2 нед. на фоне приема экзогенных эстрогенов (контрацептивы, гормональная заместительная терапия) [3, 7, 8, 11].
Основными функциями С1 эстеразы являются: предотвращение спонтанной активации классического каскада комплемента; регулирование активации каскада свертывания крови при ингибировании факторов свертывания крови XIa и XIIa; ингибирование превращения плазминогена в плазмин в процессе фибринолиза; ингибирование активированного калликреина в реакциях калликреин-брадикининовой цепи [12]. Возникновение отека опосредовано двумя пептидами (брадикинин, кинин С2), образующимися в результате неингибируемой активации комплемента и связанных с ним систем. В результате действия этих пептидов на посткапиллярные венулы происходит сокращение эндотелиальных клеток с образованием между ними щелей, через которые плазма выходит в ткани [2, 5, 11].
К факторам, провоцирующим развитие отека, относятся: травмы (стоматологические вмешательства, эндотрахеальные манипуляции, тонзиллэктомии, случайные травмы); физическое перенапряжение; менструация; беременность; эмоциональный шок; тревога, стресс; прием лекарств и пищевых продуктов; инфекция, резкое изменение температуры [4, 6, 8–10].
Первые признаки НАО могут возникнуть уже в возрасте нескольких месяцев, но чаще после 1–2 лет жизни. У большинства больных НАО дебют заболевания отмечается до 20 лет (60 %), гораздо реже — в среднем и даже пожилом возрасте. В пубертатном периоде течение заболевания может утяжелиться в связи с гормональной перестройкой [3, 8].
Клинические проявления НАО характеризуются рецидивирующими отеками различной локализации: кожи лица, шеи, туловища, конечностей, слизистых оболочек верхних отделов дыхательных путей, желудочно-кишечного и урогенитального трактов без признаков воспаления [6, 7]. Особенностями отека кожи при НАО являются ограниченность по площади, плотная консистенция, беловатая окраска, отсутствие зуда, отсутствие крапивницы, относительная безболезненность при локализации в коже, а при отеке слизистой оболочки ЖКТ — боль, тошнота, рвота и диарея, может развиваться клиника «острого живота». При поражении урогенитального тракта появляется чувство тяжести в низу живота, дизурические явления [6, 8, 9]. Длительность развития отека, как правило, 24–48 часов, а рассасывания — до 3–4 суток [2, 6].
Зуд и крапивница для НАО не характерны, однако у некоторых пациентов в продромальном периоде отека отмечается сыпь, напоминающая мультиформную эритему. В редких случаях при локализации отека на лице могут вовлекаться менингеальные оболочки с проявлением менингеальных симптомов (ригидность затылочных мышц, резкая цефалгия, рвота, иногда судороги), при поражении лабиринтных систем развивается синдром Меньера, что выражается головокружением, тошнотой, рвотой. Все эти симптомы могут встречаться как одновременно, так и по отдельности. При атипичном течении заболевания отеки могут отсутствовать, возможны изолированные абдоминалгии, характерны полиартралгии. В очень редких случаях описаны эпилептический приступ, уртикарии, кожная пурпура, синдром Рейно [3, 7]. Отсутствие в семейном анамнезе сведений о НАО не исключает возможности постановки подобного диагноза [3, 6].
Диагноз НАО подтверждается определением комплемента в сыворотке крови. Регистрируется снижение содержания ингибитора С1 до 20–30 % по сравнению с нормой, а также общего уровня комплемента на 50 % и более вследствие постоянной спонтанной активации, уменьшение содержания или отсутствие С4 и С2 комплемента. Возможно снижение гемолитической активности комплемента [2, 8, 10]. В бессимптомной стадии болезни правильная диагностика основывается на низком содержании С4 компонента комплемента [8].
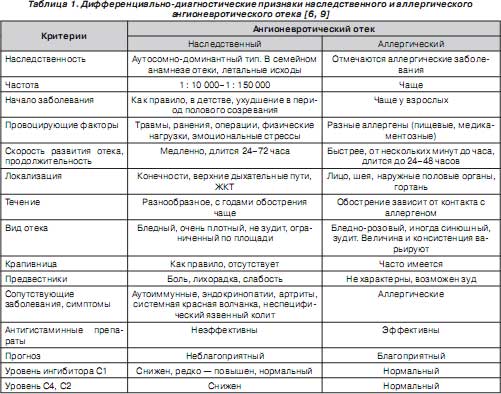
Важно провести дифференциальную диагностику с аллергическим ангионевротическим отеком или отеком Квинке (табл. 1), так как подходы к лечению этих двух заболеваний, несмотря на схожесть клиники, разные.
Терапию НАО можно разделить на лечение острого приступа НАО, профилактику развития обострений в результате оперативного вмешательства и базисную профилактическую терапию. Для лечения острой атаки используют переливание свежезамороженной плазмы как заместительную терапию (содержит ингибитор С1) и антифибринолитические препараты — аминокапроновую и транексаминовую кислоту как ингибиторы протеаз. При локализации отека в области шеи возможны эндотрахеальная интубация или трахеостомия. Для уменьшения сосудистой проницаемости вводят также стероиды [1–3, 6].
Ситуационная профилактика (перед оперативными вмешательствами): свежезамороженная плазма, аминокапроновая и транексамовая кислоты, оксиметалон, даназол [3, 6, 8]. Перманентная профилактика у больных с частыми, угрожающими жизни приступами — даназол, оксиметалон [1, 6].
1. Андросов В.Н., Порошина Ю.А., Лусс Л.В. Опыт лечения наследственного ангионевротического отека // Тер. арх. — 1988. — № 3.
2. Бурнашева Р.Х., Фассахов Р.С., Храмов В.В., Войцехович Г.С., Райзман С.М. Случай наследственного ангионевротического отека // Казанский медицинский журнал. — 1989. — Т. 70, № 1.
3. Викулов Г.Х., Феденко Е.С., Латышева Т.В. Дифференциальная диагностика и принципы терапии наследственного ангионевротического отека (анализ клинического наблюдения) // Лечащий врач. — 2004. — № 3.
4. Владимиров И., Стоянов В., Арнаудова Ж. Наследственный ангионевротический отек кожи и слизистой оболочки дыхательных путей // Журнал ушных, носовых и горловых болезней. — 1990. — № 4.
5. Дидковский Н.А., Пасхина Т.С., Рабинович С.Э., Нартикова В.Ф., Дворецкий Л.И., Решетова Н.В. Случай наследственного ангионевротического отека, обусловленного функциональной недостаточностью С1-инактиватора // Тер. арх. — 1989. — № 6.
6. Дранник Г.Н. Клиническая иммунология и аллергология. — К.: Полиграф плюс, 2006.
7. Забродская Л.В. Наследственный ангионевротический отек // Клінічна імунологія. Алергологія. Інфектологія. — 2006. — № 2(3).
8. Иванова М.В. К диагностике наследственного ангионевротического отека у детей // Педиатрия. — 1989. — № 4.
9. Протокол надання медичної допомоги хворим на алергічну кропив’янку та набряк Квінке: Наказ МОЗ України № 432 від 03.07.2006 р.
10. Lawlor G.J., Jr., Fisher T.J., Fdelman D.C. Manual of Allergy and Immunology. — London, 1995.
11. Roitt I., Brostoff J., Male D. Immunology. — London, 2000.
12. Lear S., Heelan B., Longhurst H. Наследственный ангионевротический отек: рациональная терапия улучшает качество жизни и может спасти жизнь пациента // Аллергология. — 2004. — № 1.
