Журнал «Здоровье ребенка» 4 (25) 2010
Вернуться к номеру
Профілактика та лікування ГРВІ в дітей шкільного віку з використанням ентерального рекомбінантного ліпосомального інтерферону альфа-2b
Авторы: Височина І.Л., Абатуров О.Є., Дніпропетровська державна медична академія
Рубрики: Педиатрия/Неонатология
Версия для печати
Доведена ефективність використання ліпосомальної форми рекомбінантного інтерферону альфа-2b (препарат Ліпоферон, розроблений ЗАТ «Вектор-Медика» на замовлення «Ядран» — Галенська Лабораторія д.д.») у схемах лікування та профілактики ГРВІ в дітей шкільного віку з організованих колективів за рахунок формування більш легкого перебігу гострого респіраторного захворювання та зменшення кратності епізодів ГРВІ у 1,6 раза протягом року після лікування.
Діти шкільного віку, організовані колективи, ентеральний ліпосомальний препарат Ліпоферон, лікування та профілактика ГРВІ
Протягом останніх десятиліть гострі респіраторні вірусні інфекції (ГРВІ) займають перше місце у структурі інфекційної захворюваності в дітей (близько 70 % від усієї інфекційної патології), характеризуються масовістю, сезонністю та багаторічною циклічністю, що обумовлює актуальність пошуку, розробки та впровадження нових засобів терапії і профілактики ГРВІ в дітей. При виборі заходів профілактики ГРВІ вирішальне значення має ймовірність інфікування людей, що є досить високою в епідемічних осередках та в організованих колективах, особливо в періоди загальних епідемій або сезонних підйомів захворюваності [10, 14–16, 18].
Одним із перспективних напрямків розвитку сучасної фармакології є розробка ліпосомальних форм препаратів, безперечними перевагами яких є доведені властивості ліпосом: захист лікарських речовин від деградації; завдяки селективному проникненню з крові в тканини ліпосоми сприяють прояву націленої специфічності; пролонгують дію введеного в організм лікарського засобу; змінюють фармакокінетику лікарських препаратів, підвищуючи їх фармакологічну ефективність; дозволяють створити водорозчинну форму ряду лікарських субстанцій, збільшуючи тим самим їх біодоступність тощо [8, 11, 13, 17, 19]. Основними фосфоліпідними компонентами мембрани ліпосом найчастіше бувають фосфатидилхолін або лецитин, яким властиві імуностимулююча, антиоксидантна й радіопротекторна дії, що дає певні переваги при розробці лікарських препаратів для профілактики та лікування ГРВІ [9, 10, 15, 18, 19]. Особливе значення в практиці лікарів-педіатрів має використання ліпосомального генно-інженерного інтерферону альфа-2b (Ліпоферон) для ентерального застосування, розробленого ЗАТ «Вектор-Медика» на замовлення «Ядран» — Галенська Лабораторія д.д.», у схемах лікування та профілактики ГРВІ в дітей. Доведено, що Ліпоферон має противірусні й імунокоригуючі властивості, стимулює продукцію власного інтерферону, а оптимальний режим внутрішньоклітинної доставки за рахунок включення рекомбінантного інтерферону альфа-2b у ліпосомальну капсулу підвищує його всмоктування в шлунково-кишковому тракті, захищає інтерферон від руйнування протеазами й удвічі збільшує час його циркуляції в крові [8, 9, 11]. Ліпоферон для перорального застосування легко дозується й не викликає ускладнень і побічних реакцій (гарячка, головний біль, міалгії, слабкість, лейкопенія, анемія), що реєструються при застосуванні ін''єкційної форми препаратів інтерферонів альфа-2b, що особливо важливо в педіатричній практиці [9]. Ефективність використання препарату Ліпоферон із метою профілактики та лікування ГРВІ підтверджена результатами порівняльних подвійних сліпих рандомізованих плацебо-контрольованих досліджень, які були проведені в ЦНДІ епідеміології МОЗ РФ, НДІ педіатрії і дитячої хірургії МОЗ РФ, ДНЦ «Інститут імунології» МОЗ РФ та Інституті грипу МОЗ РФ і засвідчили, що профілактичний прийом препарату Ліпоферон у дітей та дорослих сприяє вірогідному зниженню частоти ГРВІ у 2,2 раза з подальшим розвитком стійкого специфічного імунітету, а в разі розвинення гострого вірусного захворювання сприяє більш легкому перебігу та зменшенню ймовірності ускладнень ГРВІ [8–10, 12–15, 18].
Метою даного дослідження було вивчення клініко-імунологічної ефективності використання ліпосомального рекомбінантного інтерферону альфа-2b (Ліпоферон) у дітей шкільного віку з дитячих будинків для лікування та профілактики ГРВІ.
Матеріали та методи
За характером проведених нами лікувальних заходів були сформовані дві групи дітей. Діти першої групи спостереження напередодні очікуваного сезонного підвищення захворюваності на ГРВІ отримували профілактичний курс терапії з використанням ліпосомального рекомбінантного інтерферону альфа-2b (Ліпоферон). До першої групи спостереження випадковим методом нами були відібрані 18 дітей віком від 8 до 16 років, які на початку профілактичних заходів за результатами об''єктивного обстеження не мали будь-яких проявів ГРВІ або загострення хронічного захворювання.
Згідно з дизайном дослідження всім дітям першої групи проведені клініко-імунологічне обстеження в динаміці лікування Ліпофероном (до та після профілактичного курсу) та катамнестичне спостереження протягом року після закінчення профілактичних заходів. При вивченні імунологічного статусу в динаміці оцінювалися вміст лейкоцитів, лімфоцитів, CD25+, IgA, IgM, IgG, рівень TGF- b 1 (DRG ELISA, Німеччина), уміст цитокінів IL-10, IL-12р40+p70 (ELISA test kit, Diaclone, Франція) та IL-2 у сироватці крові (ELISA Kit, Ani Biotek Oy Orgenium Laboratories Business Unit, Фінляндія) і концентрація SIgA у ротоглотковому секреті (тест-система «Вектор-Бест», Росія). Забір крові та слини здійснювався вранці, натще, у присутності медичного працівника дитячого будинку. Усі імунологічні дослідження проводились у лабораторії діагностичного центру Дніпропетровської державної медичної академії.
Профілактичний курс препаратом Ліпоферон усім дітям першої групи проводився за схемою та в дозах, що відповідали інструкції виробника: перорально по 250 000 МО за 30 хвилин до прийому їжі 2 рази на тиждень протягом одного місяця.
Діти другої групи спостереження з діагнозом ГРВІ отримували лікування препаратом Ліпоферон. Терміни проведеного лікування збігалися з першою хвилею пандемічного грипу H1N1 в Україні (грудень 2009 року).
До другої групи спостереження включені всі діти, які перебували в одному з дитячих будинків нашого міста (n = 28, вік — 8–16 років) та мали ознаки ГРВІ легкого ступеня тяжкості, ознаки інтоксикаційного, гіпертермічного синдромів та прояви гострого ураження верхніх дихальних шляхів. Розвинення ознак ГРВІ в дітей шкільного віку з дитячого будинку реєструвалося з періодичністю 1–3 доби, що обумовило практично одночасне призначення лікувального курсу терапії препаратом Ліпоферон усім вихованцям дитячого будинку. Діти другої групи спостереження отримували лікування з першої доби захворювання на ГРВІ, препарат Ліпоферон призначали по 250 000 МО 2 рази на добу протягом трьох днів. Для відновлення ліпосомальної структури препарату безпосередньо перед використанням в ампули з Ліпофероном додавали по 2 мл дистильованої води, струшуючи 1–5 хвилин до утворення однорідної суспензії.
У дітей другої групи спостереження проводилася лише клінічна оцінка застосування Ліпоферону при лікуванні ГРВІ. Групу порівняння становили діти з інших організованих колективів, які за віком та статтю були порівнянними з дітьми другої групи, але не отримували лікування препаратом Ліпоферон. Усі діти другої групи спостереження та групи порівняння отримували симптоматичне лікування ГРВІ в повному обсязі: режимні заходи, дієтичне харчування, контролювався водний режим, із медикаментів використовували полівітаміни, жарознижувальні та при необхідності призначалися судинозвужувальні краплі в ніс, протикашльові й відхаркувальні препарати.
Проведене нами клініко-імунологічне дослідження ефективності використання Ліпоферону в схемах лікування та профілактики ГРВІ повністю відповідало вимогам біоетичного комітету та узгоджувалося з директорами, медичними працівниками та вихователями дитячих будинків.
Математична обробка результатів дослідження проводилася з використанням статистичних программ Statgraf, Matstat, Microsoft Excel для Windows, а при вивченні значущості розбіжностей статистичних виборок використовувалися пара- та непараметричні критерії [6, 7].
Обговорення отриманих результатів.
Проведений нами аналіз анамнестичних даних у 46 дітей першої та другої груп спостереження засвідчив, що за критеріями В.Ю. Альбицького, А.А. Баранова (1986) 26 дітей (56,5 % спостережень) часто хворіли на ГРВІ, інші хворіли на ГРВІ епізодично. За результатами оглядів ЛОР-лікаря хронічні вогнища інфекцій верхніх дихальних шляхів були зареєстровані в половини обстежених дітей за рахунок компенсованого хронічного тонзиліту; аденоїдні вегетації в анамнезі зареєстровані у 32,6 % випадків. За даними анамнезу в попередні роки на гострий бронхіт перехворіли 17 дітей (37 %).
Результати імунологічного обстеження в дітей першої групи спостереження у стані клінічного благополуччя напередодні початку профілактичного курсу препаратом Ліпоферон наведені на рис. 1.
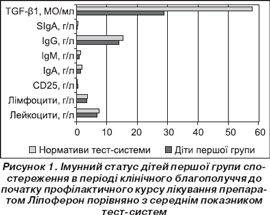
Згідно з результатами даного обстеження в імунологічному статусі дітей шкільного віку першої групи спостереження до початку профілактичного курсу терапії Ліпофероном лише показник концентрації TGF- b 1 був вірогідно нижчим за показник нормативу тест-системи (р Ј 0,05). Інші імунологічні показники, у тому числі й уміст цитокінів (IL-10, IL-12р40+p70, IL-2) та секреторного IgA у ротоглотковому секреті, вірогідно не відрізнялися від показників нормативів тест-систем.
Клінічна ефективність проведення профілактичних заходів у дітей шкільного віку з використанням препарату Ліпоферон підтверджена результатами катамнестичного спостереження протягом року за рахунок зменшення кратності зареєстрованих епізодів ГРВІ у 1,6 раза та зменшення тривалості ГРВІ в середньому на 2,2 дня. Також, за нашими даними, поряд зі зниженням рівня захворюваності в дітей першої групи спостереження зареєстровано більш легкий перебіг тих випадків ГРВІ, яких не вдалося запобігти, порівняно з тяжкістю перебігу ГРВІ в період до проведення профілактичного курсу препаратом Ліпоферон.
Зміни імунологічного статусу дітей першої групи в динаміці спостереження (до та після проведення профілактичного курсу лікування препаратом Ліпоферон) подані на рис. 2.
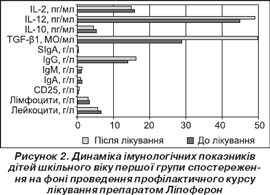
За нашими даними, у дітей першої групи спостереження (рис. 2) відразу після закінчення профілактичного курсу препаратом Ліпоферон (через місяць після початку терапії) реєструвалося вірогідне підвищення вмісту CD25+ клітин (р Ј 0,05) на фоні відносного зниження концентрації IL-2 у сироватці крові та збільшення концентрації TGF- b 1 (р Ј 0,05), що відбувалося при вихідному низькому значенні трансформуючого фактора росту, і цей приріст практично набував рівня нормативу тест-системи. Інші імунологічні показники дітей першої групи спостереження після закінчення профілактичного курсу лікування препаратом Ліпоферон мали лише характер тенденцій і не мали вірогідних розбіжностей з аналогічними показниками до лікування (р і 0,05) (рис. 2).
У регуляції стану імунітету особливу роль відіграють Т-регулюючі клітини, популяція яких гетерогенна і включає три субпопуляції. Перша — природні Т-регулюючі клітини, які експресують поверхневий маркер CD25+ і продукт транскрипційного гена-репресора Foxp3. Також існують дві індуцибельні субпопуляції — Т-reg1, які секретують високі рівні продукції IL-10, та Т 3 -хелперні, які секретують високі рівні трансформуючого фактора росту бета. Усі субпопуляції Т-регуляторних клітин мають виражену імуносупресуючу дію, що досягається по-різному: CD4+CD25+Foxp3 виконує контрибуцію метаболічно значимого для ефекторних клітин IL-2, сприяючи їх апоптозу; Т-reg1 завдяки продукції IL-10 пригнічують продукцію IL-12; Т 3 -хелпери через TGF- b пригнічують гемопоез, синтез запальних цитокінів, відповідь лімфоцитів на IL-2, IL-4, IL-7 та формування цитотоксичних NK- і Т-клітин. Трансформуючий фактор росту бета є елементом зворотної регуляції імунної відповіді, перш за все запальної реакції [1–5].
Дослідження, проведені eBioscience, Inc. 2000–2010, показали, що серед клітин, які будуть підтримувати фенотип Treg у культурі клітин, є Treg-ефекторні молекули IL-10 и TGF- b . Показано, що високі концентрації ключових цитокінів IL-2 и TGF- b , а також TCR-сигналізація є необхідними компонентами для утворення великої кількості Tregs людини або миші. При такому підході IL-2 и TCR-сигналізація антитіла викликають T-проліферації, додавання TGF- b спрямовує клітини до Tregs-фенотипу шляхом запобігання апоптозу й подальшого перетворення клітин CD4+T на Tregs переважно з високим рівнем експрессії Foxp3. Експерименти показали, що інтенсивність і стійкість індукованої Foxp3 прямо пропорційні кількості TGF- b що, у свою чергу, визначає ефективність пригнічення Treg [1–5].
Під впливом TGF- b адаптивні клітини Treg дозрівають у периферійних ділянках, у тому числі у слизових оболонках, пов''язаних із лімфоїдною тканиною (MALT), із CD4+ прекурсорами Treg, де вони набувають маркери, характерні Tregs, у тому числі CD25, CTLA4 і GITR/AITR. Пригнічуючий ефект Treg-клітин пов''язаний із виділенням цитокінів IL10 і TGF- b , які можуть викликати клітинний апоптоз ефекторних Т-клітин і блокування спільного стимулювання й дозрівання дендритних клітин [1–5].
З огляду на дані експериментальних досліджень та отримані нами результати підвищення концентрації CD25+ та TGF -b 1 (р Ј 0,05) у сироватці крові, що відбувається на фоні тенденційного (р і 0,05) зменшення IL-10 та IL-2 і збільшення продукції IL-12 у сироватці крові у межах нормальної реакції, на нашу думку, можна пояснити змінами внутрішніх популяційних відносин між Т-регуляторними клітинами і трактувати як перерозподіл субпопуляцій Т-лімфоцитів за рахунок активації Т-регулюючих клітин (CD4+CD25+Foxp3) та збільшення Т 3 -хелперів, які продукують трансформуючий фактор росту бета, що відбувається на фоні відносного пригнічення Т-reg1, яке проявляється зниженням продукції цитокіну IL-10. Відсутність підвищення вмісту IL-2 дозволяє констатувати відсутність будь-якого підвищення активації Т-клітин при використанні Ліпоферону з профілактичною метою в групі обстежених дітей.
Таким чином, проведення профілактичного курсу терапії препаратом рекомбінантного інтерферону Ліпоферон сприяє клінічному поліпшенню в дітей шкільного віку з організованих колективів, що супроводжується перерозподілом субпопуляцій Т-лімфоцитів.
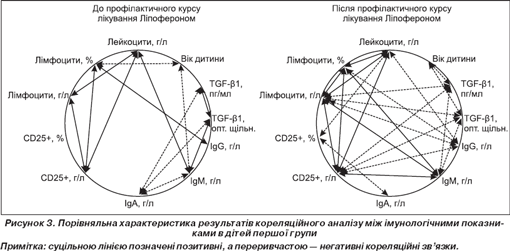
Проведений нами кореляційний аналіз імунологічних показників у дітей першої групи спостереження до та після профілактичного курсу лікування препаратом Ліпоферон дозволив виявити високовірогідні зв''язки між показниками, що вивчалися.
Узагальнюючи результати даного етапу дослідження, можна зробити висновок, що проведення протягом одного місяця профілактичного курсу лікування препаратом Ліпоферон у дітей шкільного віку з організованих колективів призводить до відновлення вмісту TGF- b 1 у периферійній крові, що відбувалося на фоні підвищення рівня ієрархічності імунологічних факторів та супроводжувалося появою більш стійкої системи взаємозв''язків між імунними показниками, що вивчалися (рис. 3).
У дітей другої групи спостереження з симптомами ГРВІ відзначалися підвищення температури в середньому до 38,8 °С та помірні або незначні прояви інтоксикаційного синдрому. На початку лікування в дітей другої групи у 28,6 % випадків тяжкість перебігу ГРВІ була розцінена як середня, в інших випадках діти мали ГРВІ легкого ступеня тяжкості. У групі порівняння (діти з інших організованих колективів) ГРВІ легкого ступеня тяжкості зареєстровано в 68 % спостережень, ГРВІ середнього ступеня тяжкості — у 20 %, а тяжкі форми — відповідно у 12 % випадків, що потребувало необхідності лікування дітей у стаціонарі. У жодної дитини другої групи спостереження не було зареєстровано ускладнень ГРВІ на відміну від дітей із групи порівняння (16 % спостережень), які також потребували госпіталізації до лікарні. Проведений нами аналіз тривалості проявів інтоксикаційного синдрому та гарячки в дітей другої групи з ГРВІ легкого та середнього ступеня тяжкості показав, що цей показник у середньому становив 2 доби, що майже вдвічі менше, ніж у групі порівняння — 3,8 доби. Середня тривалість епізоду ГРВІ у дітей другої групи спостереження становила в середньому 4,8 ± 0,5 дня, у групі порівняння — 6,7 ± 0,5 дня.
Таким чином, нами доведена клінічна ефективність використання Ліпоферону при лікуванні ГРВІ в дітей шкільного віку з організованих колективів. Так, застосування препарату в переважній більшості випадків сприяло тому, що ГРВІ перебігало легко й без ускладнень. На нашу думку, більш швидке одужання вихованців дитячого будинку з другої групи спостереження при симптоматичному лікуванні ГРВІ досягалося одночасним включенням в схему терапії ентерального ліпосомального рекомбінантного інтерферону альфа-2b у всіх дітей, які були під нашим наглядом.
Проведення профілактичного та лікувального курсів препаратом Ліпоферон показало, що переносимість препарату дітьми шкільного віку з організованих колективів була доброю, побічних та алергічних реакцій не зареєстровано в жодному випадку. Ще однією перевагою рекомбінантного інтерферону альфа-2b (Ліпоферон) є форма випуску — порошок для приготування суспензії у флаконах, що забезпечує фізіологічний шлях надходження препарату до організму дитини. Також ентеральне застосування Ліпоферону дозволяє уникнути психофізіологічних утруднень альтернативних шляхів введення препаратів: при ін''єкційному введенні — больові відчуття, порушення цілісності шкірних покривів; при ректальному введенні — психологічний бар''єр (соціально сформоване відчуття сорому у зв''язку із зазначеною ділянкою тіла) і можливі больові відчуття.
Висновки
1. Доведені безпечність та ефективність застосування ентерального ліпосомального рекомбінантного інтерферону альфа-2b за рахунок зменшення кратності та тривалості ГРВІ, що дозволяє рекомендувати використання Ліпоферону у схемах профілактики та лікування ГРВІ в дітей шкільного віку.
2. Проведення профілактичного курсу ентеральним ліпосомальним рекомбінантним інтерфероном
альфа‑2b призводить до підвищення концентрації CD25+ та TGF- b 1 у периферійній крові, що, на нашу
думку, можна пояснити перерозподілом субпопуляцій Т-регулюючих клітин за рахунок активації CD4+CD25+Foxp3 та збільшення популяції Т 3 -хелперів, які продукують трансформуючий фактор росту бета.
Проведений нами кореляційний аналіз імунологічних показників у дітей шкільного віку показав, що використання Ліпоферону з профілактичною метою сприяє підвищенню рівня ієрархічності імунологічних факторів, що призводить до появи більш стійкої системи взаємозв''язків між імунними показниками.
1. Hutton J.F., Gargett T., Sadlon T.J., Bresatz S., Brown C.Y., Zola H., Shannon M.F., D''Andrea R.J., Barry S.C. Development of CD4+CD25+FoxP3+ regulatory T cells from cord blood hematopoietic progenitor cells // J. Leukoc. Biol. — 2009 Mar. — 85(3). — 445-51.
2. Gregori S., Bacchetta R., Passerini L., Levings M.K., Roncarolo M.G. Isolation, expansion, and characterization of human natural and adaptive regulatory T cells. Review // Methods Mol. Biol. — 2007. — 380. — 83-105.
3. Takahashi T., Kuniyasu Y., Toda M., Sakaguchi N., Itoh M., Iwata M., Shimizu J., Sakaguchi S. Immunologic self-tolerance maintained by CD25+CD4+ naturally anergic and suppressive T cells: induction of autoimmune disease by breaking their anergic/suppressive state // Int. Immunol. — 1998 Dec. — 10(12). — 1969-80.
4. Shevach E.M. Regulatory T cells in autoimmmunity. Review // Ann. Rev. Immunol. — 2000. — 18. — 423-49.
5. Curotto de Lafaille M.A., Lafaille J.J. Natural and adaptive foxp3+ regulatory T cells: more of the same or a division of labor? Review // Immunity. — 2009 May. — 30(5). — 626-35.
6. Герасимов А.Н. Медицинская статистика. — М.: МИА, 2007. — 475 с.
7. Лапач С.Н., Чубенко А.В., Бабич П.Н. Статистические методы в медико-биологических исследованиях с использованием Excel. — К.: Морион, 2000. — 320 с.
8. Ершова И.Б., Косенко В.С., Осычнюк Л.М., Осипова Т.Ф., Мочалова А.А. Липосомные формы интерферонов в педиатрической практике при лечении ОРВИ у детей // Здоровье ребенка. — 2009. — № 2(17).
9. Липоферон ® в лечении вирусных и аллергических заболеваний // Внутрішня медицина. — 2007. — № 5(5).
10. Лобзин Ю.В., Львов Н.И., Колокольцов А.А. Клиническая эффективность препарата Липоферон в комплексной терапии больных гриппом и другими ОРЗ // Новости медицины и фармации. — 2007.— № 14(220).
11. Медикаментозное преодоление анатомических и клеточных барьеров с помощью липосом / Под ред. Л.М. Кузяковой, В.И. Ефременко. — Ставрополь, 2000. — 170 с.
12. Медуницына Е.Н. Влияние a -2 интерферона на клиническую эффективность аллергенспецифической иммунотерапии у больных атопической бронхиальной астмой и/или аллергическим риноконъюнктивитом // Клиническая иммунология. Аллергология. Инфектология. — 2007. — № 2(7).
13. Бажутин Н.Б., Золин В.В., Колокольцов А.А., Таргонский С.Н. Перспективы применения липосомальных препаратов в медицинской практике // Здоров''я України. — 2007. — № 3. — С. 71.
14. Петленко С.В., Романцов М.Г., Шульдякова О.Г., Коваленко А.Л. Снижение респираторной заболеваемости подростков в период неустойчивой эпидемической ситуации по ОРЗ и гриппу // Мат-лы IV Международной конф. «Клинические исследования лекарственных средств». — М., 2004. — С. 171-172.
15. Колокольцов А.А., Золин В.В., Таргонский С.Н., Бажутин Н.Б. Терапевтическая эффективность Липоферона — липосомированного препарата рекомбинантного альфа-2b интерферона при профилактике и лечении вирусных инфекций // Новости медицины и фармации. — 2009. — № 11–12. — С. 285-286.
16. Хаитов Р.М., Пинегин Б.В. Современные представления о защите организма от инфекции // Иммунология. — 2000. — № 1. — С. 61-64.
17. Швец В.И., Краснопольский Ю.М. Липосомы в фармации. Продукты нанобиотехнологии // Провизор. — 2008. — № 3.
18. Шульдякова О.Г. Респираторные инфекции у детей // Лекарственные средства, применяемые при вирусных заболеваниях / Под ред. М.Г. Романцова, Ф.И. Ершова. — М., 2007. — С. 233-277.
19. Юлиш Е.И., Абатуров А.Е. Липосомальная терапия: настоящее и будущее // Здоровье ребенка. — 2008. — № 1(10).
