Журнал «Здоровье ребенка» 6 (27) 2010
Вернуться к номеру
Вивчення рівня, структури та характеру бронхолегеневої патології в популяційній групі дітей раннього віку, яким у неонатальному періоді проводилася респіраторна терапія
Авторы: Беш Л.В.1, 2, Мацюра О.І.2, 1Львівський національний медичний університет імені Данила Галицького, 2Міська дитяча клінічна лікарня, м. Львів
Рубрики: Педиатрия/Неонатология
Версия для печати
У статті наведені літературні дані і власний досвід авторів, які доводять, що існує взаємозв’язок між проведеною респіраторною терапією та подальшим формуванням бронхолегеневої патології. Показані результати ретроспективного аналізу анкет 231 дитини раннього віку з перенесеними розладами дихання в неонатальному періоді.
Бронхолегенева патологія, респіраторна терапія, неонатальний період, діти раннього віку.
На сьогодні найгострішою проблемою в нашому суспільстві є стан здоров’я дитячого населення, оскільки саме здорові діти є основою для розвитку країни, визначають подальший її економічний, науковий, культурний потенціал та рівень здоров’я наступних поколінь [2].
Експертами Всесвітньої організації охорони здоров’я (ВООЗ) були визначені складові формування здоров’я, а саме:
— спосіб життя — до 50 %;
— вплив навколишнього середовища — до 20 %;
— генетична компонента (спадковість) — до 20 %;
— доступність і якість медичної допомоги — до 10 % [5].
Незважаючи на те що питома вага суто медичних проблем у формуванні здоров’я особи, за даними ВООЗ, становить не більше ніж 10 %, медичні аспекти збереження здоров’я в ранньому дитячому віці мають значно більший вплив, ніж у наступних вікових групах, оскільки дві третини причин, що формують стан здоров’я людини в майбутньому, зумовлені факторами, що впливають саме в період вагітності та протягом перших років життя дитини [5, 8].
За даними офіційної статистики, захворюваність дітей віком від 0 до 17 років включно за період 2003–2009 роки має позитивну тенденцію: у 2003 р. даний показник становив 1175,46 на 1000 дітей, у 2009 р. — 1393,9 на 1000 дітей. Найвищий рівень захворюваності спостерігається серед вікової групи 0–6 років (11,86 на 1000 відповідного населення), серед дітей 7–14 років (2,29) і 15–17 років (1,86). Структура захворюваності дітей 0–17 років за останні роки залишається незмінною: І місце стійко займають хвороби органів дихання — 63,9 % (2003) та 65,6 % (2009), ІІ місце — хвороби шкіри та підшкірної клітковини — 5,6 та 5,3 % відповідно, ІІІ місце — інфекційні та паразитарні хвороби — 4,2 та 3,8 % [5].
Аналіз статистичних результатів дозволяє зробити висновки, що хвороби органів дихання у дітей раннього віку є найбільшою проблемою сучасної педіатрії. Більше того, ця ситуація з часом буде лише загострюватися. Значно частіше почали виживати діти, які з різних причин потребують тривалої респіраторної підтримки: штучної вентиляції легень (ШВЛ), самостійного дихання під постійним позитивним тиском (СДППТ), оксигенотерапії, що, у свою чергу, нерідко призводить до формування рецидивної та хронічної бронхолегеневої патології [8]. У ранньому віці в кожної третьої дитини, яка перебувала на ШВЛ у неонатальному періоді, спостерігаються повторні та хронічні бронхолегеневі захворювання (бронхіальна астма (БА), бронхолегенева дисплазія, повторні пневмонії, рецидивні бронхіти), розвиток яких є в тісному взаємозв’язку з патологією неонатального періоду [1, 3, 7]. З переходом України на міжнародну систему обліку і статистики (1 січня 2007 р.) та впровадження порядку реєстрації новонароджених із масою 500 г і більше, виникає потреба розробки не лише нових схем лікування, а й профілактики хронічних захворювань у таких дітей. Зокрема, розвиток серйозної бронхолегеневої патології тягне за собою ряд проблем — високі показники смертності, висока вартість надання медичної допомоги, проблеми інвалідизації. Знання особливостей перебігу захворювань у різних популяційних групах дозволяє вчасно і грамотно організувати превентивні заходи та збільшити шанси дитини на одужання.
Саме така ситуація визначила актуальність і мету нашої роботи, яка полягала у вивченні рівня, структури та характеру бронхолегеневої патології у дітей, яким у неонатальному періоді проводилася респіраторна терапія.
Нами було проведено спрямований збір інформації шляхом викопіювання з «Медичних карт стаціонарного хворого» (о.ф. № 003/о) та «Статистичних карт хворого, що вибув із стаціонару» (о.ф. № 066/о) про дітей, які перебували на лікуванні у Львівській обласній клінічній лікарні (ЛОКЛ) (відділення патології недоношених новонароджених дітей) та Львівській міській дитячій клінічній лікарні (ЛМДКЛ) (відділення реанімації та інтенсивної терапії новонароджених, патології новонароджених та недоношених дітей) з приводу респіраторних розладів, і отримували відповідну респіраторну терапію (ШВЛ, СДППТ, оксигенотерапію).
Проаналізовано 485 історій хвороб дітей, які знаходилися на лікуванні у ЛОКЛ або ЛМДКЛ та виписані у терміні 1997–2006 рр. Відіслано 420 спеціальних анкет, розроблених таким чином, щоб отримати інформацію про стан здоров’я дитини від народження до досягнення 3-річного віку.
Отримано відповіді від 267 респондентів (63,6 % від загальної кількості розісланих анкет). У 231 анкеті (86,5 % від отриманих) були сформульовані чіткі відповіді на поставлені запитання, 36 (13,5 %) — відомості подані не в повному обсязі або помилково внесені дані іншої дитини (старшої, молодшої).
Для перевірки вірогідності отриманої статистичної інформації нами було розраховано мінімальне число спостережень, при яких би забезпечувався вірогідний результат. Відтак нами було використано формулу Паніотто:
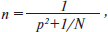
де n — необхідне число спостережень;
р — вірогідність помилки;
N — кількість одиниць у генеральній сукупності.
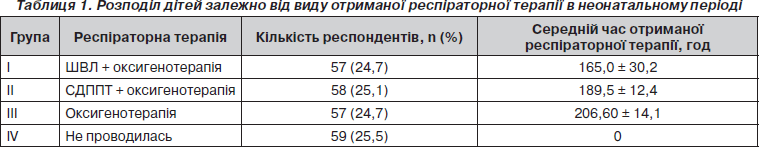
При підстановці даних у формулу (1) розраховано мінімальне число спостережень в одній групі, яке становить 48 осіб. Оскільки в нашому дослідженні планувалось проаналізувати 4 групи (яким проводилась: ШВЛ + оксигенотерапія, СДППТ + оксигенотерапія, винятково оксигенотерапія та група контролю), то мінімальне число спостережень мало би бути 192 особи. Отже, наявна кількість (231 анкета) дозволяє проводити медико-статистичний аналіз у всіх 4 групах з вірогідністю помилки менше ніж 5 % (p < 0,05). Розподіл дітей залежно від виду отриманої респіраторної терапії наведений у табл. 1.
У кожній групі аналізували такі показники: характер вигодовування немовлят; фізичний розвиток; особливості побуту і режиму фізичної активності; проведені профілактичні щеплення; обтяженість сімейного анамнезу (бронхолегенева патологія, атопія); прояви атопії в дитини (детальний опис виникнення та тривалості симптомів, провокуючих факторів); частота і характер респіраторної патології; обсяг лікування респіраторної патології; наявність проблем зі здоров’ям від народження до досягнення 3-річного віку.
Респонденти досліджуваних груп практично не відрізнялись за часткою недоношених дітей, що становила 72,1 % в основній групі та 71,2 % у контрольній (p > 0,05).
Особлива увага зверталася нами на причини розвитку респіраторної патології у дітей раннього віку, оскільки існують переконливі літературні дані про взаємозв’язок перенесених розладів дихання в неонатальному періоді з подальшим формуванням рецидивних чи хронічних захворювань бронхолегеневої системи [7, 10].
Саме тому при вивченні структури захворювань у досліджуваних дітей ми вирішили виділити дві основні групи:
1. Респіраторна патологія.
2. Інша патологія (захворювання травного каналу, ураження ЦНС тощо).
Рівень та структуру респіраторних захворювань у різних групах протягом 3-річного спостереження наведено на рис. 1.
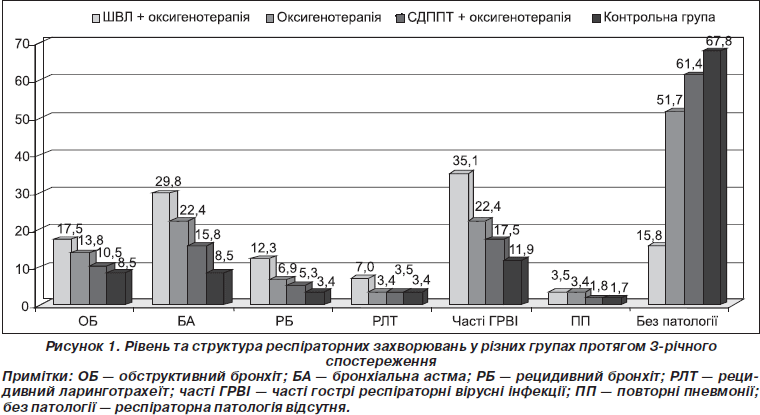
Аналізуючи рівень та структуру бронхолегеневої патології у дітей раннього віку, ми встановили, що частка рецидивного БОС (бронхіальна астма, обструктивний бронхіт) спостерігалася значно частіше в дітей, які отримували респіраторну терапію, зокрема ШВЛ + оксигенотерапію та СДППТ + оксигенотерапію (рис. 2).
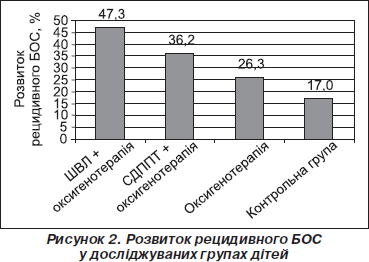
Таким чином, доведений корелятивний зв’язок між проведенням ШВЛ у неонатальному періоді й подальшим формуванням гіперреактивності дихальних шляхів, яка клінічно проявляється рецидивним бронхообструктивним синдромом (БОС) [7, 11]. Ситуацію можна пояснити впливом агресивної респіраторної терапії (тривала дія високих концентрацій кисню), формуванням запального процесу та морфологічних змін — фіброзу, що призводить до порушення архітектоніки бронхів та бронхіол. Анатомічні відхилення, у свою чергу, призводять до каскаду патофізіологічних змін [6].
Серед дітей, у яких спостерігався розвиток рецидивного БОС, було проаналізовано частоту повторних епізодів БОС, що відображено на рис. 3.
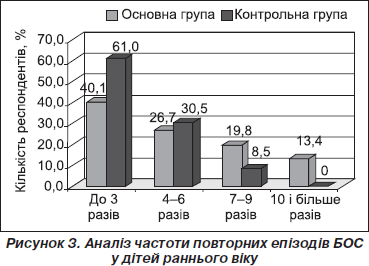
Як бачимо, серед досліджуваної когорти дітей, які отримували респіраторну терапію в неонатальному періоді (основна група) та мали БОС, кількість респондентів із частими загостреннями є суттєво більшою порівняно із контрольною групою. Зокрема, протягом перших трьох років життя загострення рецидивного БОС з частотою 7–9 разів було зареєстровано у 19,8 % дітей основної групи та 8,5 % контрольної, а загострення з частотою 10 і більше разів зафіксовані лише серед пацієнтів основної групи — 13,4 %.
Паралельно аналізу респіраторних захворювань ми вивчали також наявність іншої патології у респондентів (рис. 4). На думку батьків, 36,6 % дітей основної групи до досягнення 3-річного віку були здоровими. У структурі патології найпоширенішими (57 %) були респіраторні захворювання, гастроентерологічні (даний блок об’єднав проблеми шлунково-кишкового тракту, інфекційні та паразитарні: кишкові кольки, запори, гострі кишкові інфекції, дискінезії жовчевивідних шляхів, дисбіоз кишечника, гельмінтози) — 33,7 %, алергічні захворювання — 29,1 %, неврологічні (ДЦП, судоми, гіперзбудливість, гідроцефалія, часті головні болі, порушення мовлення) — 15,1 %. По 5,8 % становили захворювання ЛОР-органів та офтальмологічна патологія (хронічний тонзиліт, отит, аденоїдит, гайморит, сенсорна втрата слуху; зниження гостроти зору, косоокість, природжена вада зорового аналізатора, катаракта, астигматизм). Серед інших видів патології іноді реєструвалися нефрологічна та серцево-судинна.
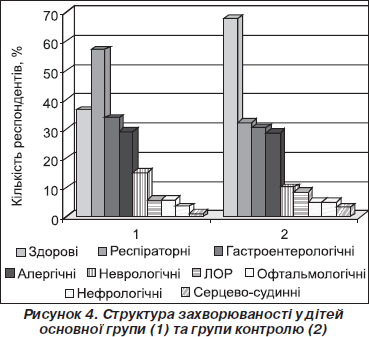
Водночас респонденти групи контролю були визнані здоровими у 67,8 %. У структурі патології найпоширенішими також були респіраторні захворювання, проте їхня частка була суттєво меншою порівняно з пацієнтами основної групи і становила 32,2 %. Гастроентерологічні захворювання становили 30,5 %, алергічні — 28,8 %. Неврологічні хвороби становили 10,2 %, ЛОР-патологія — 8,5 %. Серед інших патологій зареєстровано офтальмологічну, нефрологічну та серцево-судинну.
Наші дослідження показали, що у досліджуваних дітей частіше реєструвалася комбінована патологія (у 51,2 % респондентів основної групи та 23,8 % — групи контролю).
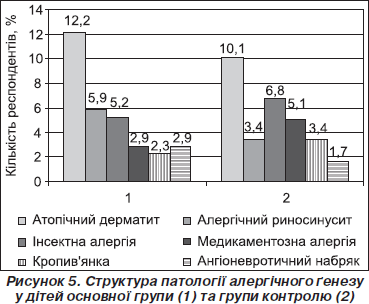
Цікавими виявилися результати, які дозволяють стверджувати, що у структурі захворюваності респондентів обох груп третю частину займали алергічні захворювання (29,1 та 28,8 % відповідно). Ці цифри не включають випадків бронхіальної астми, які реєструвалися в групі респіраторної патології. Отримані показники, безперечно, є високими, однак вони збігаються з літературними даними щодо поширеності алергічної патології в дитячій популяції [9]. Найпоширенішим алергічним захворюванням у дітей раннього віку в обох групах був алергічний дерматит, частка якого зафіксована у 12,2 % респондентів основної групи та 10,1 % — контрольної. Інсектна алергія найчастіше спричинялася комарами та бджолами. Медикаментозні реакції зафіксовані на антибіотики пеніцилінового та цефалоспоринового ряду, вітамінні та гомеопатичні препарати. У 7,4 % дітей основної та 5,9 % контрольної групи спостерігалися поєднання кількох нозологій алергічної природи. Структурний розподіл по нозологіях наведений на рис. 5.
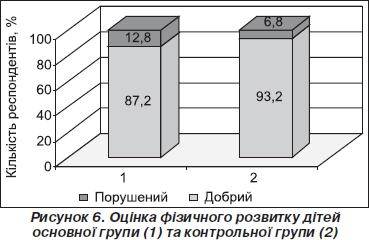
У процесі дослідження ми намагалися отримати дані стосовно фізичного розвитку дітей. Переважна більшість батьків оцінили фізичний розвиток своїх дітей як «добрий» (87,2 % респондентів основної групи та 93,2 % — контрольної) (рис. 6).
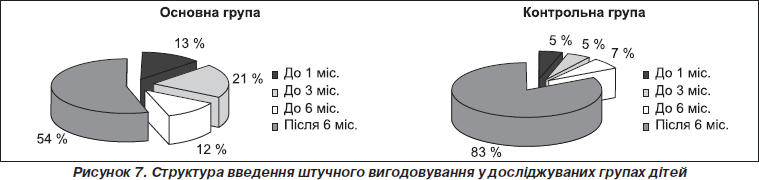
Аналіз характеру вигодовування дітей показав, що раннє штучне годування спостерігалося значно частіше серед дітей основної групи. Грудне годування після досягнення дитиною 6-місячного віку спостерігалося у 54,7 % респондентів основної групи, у той час як у групі контролю даний показник становив 83 % (рис. 7).
Проведення профілактичних щеплень, на думку респондентів, супроводжувалося патологічними реакціями у 12,8 % основної групи та 5,1 % групи контролю, що проявлялися вираженим неспокоєм малюка, підвищенням температури тіла до субфебрильних і фебрильних цифр, висипаннями на шкірі, розвитком БОС). Аналіз викладеної вище ситуації дозволяє нам стверджувати, що переважній більшості поствакцинальних реакцій можна було б запобігти за умови проведення профілактичних щеплень дітям з обтяженим анамнезом (недоношеність, алергічні, пульмонологічні, неврологічні захворювання) лише в умовах спеціалізованого стаціонару після відповідної підготовки.
Підсумовуючи отримані результати, ми мали можливість ще раз переконатися в тому, що перебіг неонатального періоду впливає на подальше здоров’я дитини. Внаслідок перенесених респіраторних розладів у немовлят спостерігається дисбаланс біологічно активних речовин, зниження функції захисних механізмів та досить часто формується гіперреактивність бронхів, що клінічно проявляється рецидивним БОС. Звичайно, вираженість запальної реакції і бронхоспазму в різних хворих є неоднаковою. Такі відмінності пояснюються індивідуальними особливостями та генетичними факторами, що впливають на здатність клітин до синтезу медіаторів, рівень резистентності чи ступінь порушення архітектоніки бронхів та бронхіол [7].
Висновки
1. Бронхолегеневі захворювання займають провідне місце у структурі захворювань дітей раннього віку.
2. Відзначений тісний кореляційний зв’язок між проведенням ШВЛ і частотою формування рецидивного БОС в катамнезі (p < 0,01).
3. Частота повторних епізодів БОС є вірогідно вищою серед дітей раннього віку, яким проводилася респіраторна терапія в неонатальному періоді (p < 0,01).
4. Взаємозв’язок «дихальні розлади — респіраторна терапія — подальше формування рецидивної або хронічної бронхолегеневої патології» існує та потребує подальшого активного вивчення.
1. Ласиця О.Л. Бронхообструктивний синдром у дітей та його диференційна діагностика, лікування // Алергологія дитячого віку. — К.: Книга плюс, 2004. — С. 106-120.
2. Ласиця О.І., Охотнікова О.М. Фактори ризику розвитку бронхіальної астми у дітей // Клінічна імунологія, алергологія, інфектологія. — 2006. — № 1. — С. 36-40.
3. Мачарадзе Д.Ш. Распространенность аллергических заболеваний у детей по данным литературы и ISAAC // Астма. — 2005. — Т. 6, № 1/2. — С. 11-17.
4. Методичні рекомендації до проведення епідеміологічного аналізу / Укладачі: М.Д. Чемич, Г.С. Зайцева, Н.І. Ільїна, В.В. Захлєбаєва. — Суми: Вид-во СумДУ, 2009. — 21 с.
5. Міністерство охорони здоров’я України. Стан здоров’я дітей в Україні. http://www.moz.gov.ua/ua/main/press/?docID=20987 (06.07.2010).
6. Сучасні підходи до діагностики, профілактики рецидивуючих і хронічних бронхітів у дітей / Ю.Г. Антипкін, Л.П. Арабська, О.А. Смірнова та ін. — К.: ЗАТ «ВІПОЛ», 2003. — 122 с.
7. Харченко М.В., Заблотских Т.В., Мизерницкий Ю.Л. Изменения вентиляционной функции легких у детей, находившихся на искусственной вентиляции легких в неонатальном периоде // Пульмонология детского возраста: проблемы и решения. — 2005. — Выпуск 5. — С. 57-60.
8. Шунько Є.Є. Національні медичні стандарти лікувально-профілактичної допомоги новонародженим // Матеріали укр. наук.-практ. конф. «Дихальна підтримка новонароджених та інші актуальні питання неонатології», м. Львів, 1–2 жовтня 2009 р. — С. 3-4.
9. Global Initiative for Asthma (GINA). Global Strategy for Asthma Management and Prevention. Revised 2007. http://www.ginasthma.org (last accessed January 12, 2010).
10. Halken S. Prevention of allergic disease in childhood:clinical and epidemiological aspects of primary and secondary allergy prevention // Pediatr. Allergy Immunol. — 2004. — Vol. 15, Suppl. 16. — Р. 9-32.
11. Skevaki C. Novel and Controversial Issues in Asthma // European Academy of Allergology and Clinical Immunology Newsletter. — 2008. — Issue 14. — P. 14.