Журнал «Медицина неотложных состояний» 1-2(32-33) 2011
Вернуться к номеру
Инсульт и кардиальная дисфункция
Авторы: Дубенко О.Е., Ракова И.А., Харьковская медицинская академия последипломного образования, кафедра невропатологии и нейрохирургии
Рубрики: Семейная медицина/Терапия, Медицина неотложных состояний
Версия для печати
С целью изучения влияния разных типов острого инсульта на развитие кардиальной дисфункции и повреждение миокарда обследовано 110 больных: 47 — с ишемическим инсультом, 40 — с геморрагическим, 23 — с субарахноидальным кровоизлиянием без заболеваний сердца в анамнезе. Результаты обследования показали, что изменения электрокардиограммы в виде удлинения интервала Q–T, депрессии сегмента S–T и отрицательного зубца Т чаще развиваются при кортикальных ишемических инфарктах и медиальной локализации гематомы, а также наличии межполушарных различий. Для больных с субарахноидальным кровоизлиянием в первые сутки было характерно наличие брадикардии и отрицательного зубца Т, а также более обратимый характер этих изменений по сравнению с ишемическим и геморрагическим инсультом. Изменения на электрокардиограмме сопровождались незначительным повышением уровня кардиального тропонина I, который был выше при геморрагическом инсульте и субарахноидальном кровоизлиянии и коррелировал с тяжестью инсульта, что свидетельствует о микроструктурном повреждении миокарда. Ведение больных с острым инсультом требует мероприятий по защите миокарда для предотвращения вторичных кардиальных осложнений.
Острый инсульт, электрокардиограмма, тропонин I.
В настоящее время констатировано огромное значение инсульта как всемирной пандемии [1]. Современный уровень понимания этой патологии позволяет рассматривать инсульт не только как неврологическую, но и как мультидисциплинарную проблему, в которой серце и мозг имеют два взаимосвязанных аспекта: с одной стороны, это инсульт, развивающийся в результате заболеваний сердца, с другой — кардиальная дисфункция при остром инсульте, которая способствует ранней смертности больных [2–4]. Взаимосвязь цереброваскулярной и кардиоваскулярной патологии обусловлена как общностью факторов риска острых нарушений мозгового кровообращения и ишемической болезни сердца (ИБС) (артериальная гипертония, курение, сахарный диабет, гиперхолестеринемия, избыточная масса тела), так и общностью физиологических и патофизиологических механизмов регуляции всей сердечно-сосудистой системы [5, 6]. Кардиальная дисфункция при остром инсульте описана около 60 лет назад и может проявляться в виде различных вариантов нарушения сердечного ритма, изменений на электрокардиограмме (ЭКГ), вплоть до развития острого инфаркта миокарда, что получило также название цереброкардиального синдрома. Установлено, что они коррелируют с ранней смертностью при инсульте. Вероятно, что целый ряд механизмов может участвовать в развитии кардиальной дисфункции при остром инсульте, среди которых повышение внутричерепного давления, нейрогуморальные сдвиги, центральный выброс симпатических медиаторов, повышение медиаторов воспаления, активация внутрисосудистого тромбообразования. Кроме того, сердце, как ни один другой орган, имеет многоуровневый невральный контроль, от премоторных и островковых отделов коры головного мозга до интрамуральных внутрисердечных ганглиев. Следовательно, инсульт как катастрофическое событие в центральной нервной системе может оказывать влияние на деятельность сердца. Высокочувствительными и высокоспецифичными маркерами миокардиального повреждения у больных с острым коронарным синдромом (ОКС) являются сердечные тропонины. В то же время за последние годы накопились клинические наблюдения, когда гипертропонинемия может обнаруживаться не только у больных с ОКС, но и при других заболеваниях, (внесердечного генеза), в том числе при остром инсульте [7]. Систематический обзор исследований, посвященных определению уровня тропонинов I (Тн I) и Т у больных с острым инсультом показал, что примерно у 1 из 5 госпитализированных больных с острым инсультом наблюдается повышение тропонинов, свидетельствующее об остром повреждении миокарда. Это ассоциируется с ишемическими изменениями на ЭКГ и возможно, что у значительной части этих больных имеется ИБС. Однако недостаточно ясно, связано ли увеличение смертности при повышении тропонинов с кардиальной патологией или обусловлено тяжестью инсульта [8]. Анализ прогностического значения при ишемическом инсульте (ИИ) различных биомаркеров крови показал статистически значимую связь с тяжестью инсульта для бета-тромбоглобулина, С-реактивного протеина, ферритина, глутамата, интерлейкина-6, тромбин-антитромбинового комплекса, тромбомодулина, матриксной металлопротеиназы-9 и тропонинов I и Т, при этом кардиальные маркеры показали наиболее тесную связь с плохим прогнозом [9].
Таким образом, кардиальные нарушения при остром инсульте могут осложнять его течение и влиять на прогноз. В связи с этим мы провели собственное исследование с целью изучения влияния разных типов инсульта на развитие кардиальной дисфункции и повреждение миокарда.
Материал и методы исследования
В исследование включены 110 больных с острым инсультом (мужчин — 59, женщин — 51, средний возраст 63,2 ± 9,6 года), из которых с ИИ — 47, с геморрагическим (ГИ) — 40, с субарахноидальным кровоизлиянием (САК) — 23. Характер и локализация инсульта у всех больных были подтверждены при магнитно-резонансной томографии (МРТ).
Тяжесть больных ИИ определяли по шкале NIHSS, тяжесть больных ГИ определялась по шкале комы Глазго и составляла от 5 до 14 баллов, в динамике — по шкале исходов Глазго, тяжесть больных с САК по шкале Ханта и Хесса — 2–4 балла [10]. Всем больным производилась 10-минутная запись ЭКГ с анализом вариабельности сердечного ритма при помощи компьютерного кардиографа Cardiolab+. Определение уровня Тн I в плазме крови производилось иммуноферментным методом с помощью набора реактивов «Хема-Медика» (Россия). Параметры нормы, установленные для используемого набора реагентов, составили 0–0,30 нг/мл. Обследование проводилось в динамике на 1-е — 3-и и 10–14-е сутки инсульта. Для исключения кардиогенных и метаболических влияний не включались больные с наличием в анамнезе заболеваний сердца (инфаркта миокарда, аритмий, пороков, застойной сердечной недостаточности), легких, почек, сахарного диабета, алкоголизма. Статистическая обработка полученных результатов проводилась на основе пакета программ Statistica 6,0. Результаты представлены в виде среднего значения (М) ± ошибка средней (m). Для сравнения полученных результатов использовали параметрический критерий Стьюдента и непараметрический критерий Вилкоксона. Для определения направления и силы связи между величинами использовали методы линейного и нелинейного корреляционного анализа. Различия считали достоверными при р < 0,05.
Результаты и их обсуждение
По данным МРТ, из 47 обследованных больных с ИИ у 33 очаги инфаркта мозга (70,2 %) локализовались в больших полушариях мозга, у 14 (29,8 %) — в субтенториальных структурах, у 16 (34,0 %) — в левом полушарии, у 17 (36,2 %) — в правом. У 16 (34,0 %) больных очаги охватывали кору и прилежащее белое вещество одной или нескольких долей мозга. У 17 (36,2%) больных очаги располагались в подкорковых структурах — базальных ганглиях и зрительном бугре. У 14 (29,8 %) из них очаги носили лакунарный характер — размерами не более 20 мм в диаметре. У остальных 3 (6,4 %) больных размеры субкортикальных инфарктов были более 20 мм и имели стриатокапсулярный характер. Размеры инфарктов в корковых отделах больших полушарий были больше, чем в подкорковых, и составляли от 27 ґ 30 мм до 120 ґ 82 мм. Тяжесть инсульта по шкале NIHSS была статистически значимо выше у больных с корковыми очагами — 11,5 ± 2,5 балла по сравнению с подкорковыми — 7,3 ± 2,1 балла (р < 0,05). Умерли 2 больных с обширными инфарктами, охватывающими лобно-теменно-височную область. Из 14 больных с субтенториальными очагами инфаркты визуализировались в области варолиева моста, в продолговатом мозге и в полушарии мозжечка. Тяжесть инсульта по шкале NIHSS у больных с субтенториальными очагами составила 6,0 ± 3,2 балла.
Анализ изменений ЭКГ у больных с ИИ показал, что при первом обследовании изменения деятельности сердца отсутствовали только у 4 (8,5 %) больных и заключались в развитии тахикардии у 17,0 % больных, реже наблюдалась брадикардия — у 6,3 % и наджелудочковая экстрасистолия — у 8,5 %. Нарушения функции проводимости регистрировались в виде замедления атриовентрикулярной (АV) проводимости (6,3 % больных) и удлинения интервала Q–T (12,8 % больных) больных. Наиболее часто регистрировались изменения сегмента S–T и зубца Т, называемые нарушениями процессов реполяризации. Изменения сегмента S–T чаще регистрировались в виде депрессии — у 9 (19,1 %) больных. Наиболее частым феноменом был отрицательный зубец Т — у 19 (40,4 %) больных. При оценке в динамике нами отмечено, что такие изменения, как тахикардия, экстрасистолия, удлинение интервала Q–T, имели тенденцию к регрессированию. Частота изменений со стороны сегмента S–T и зубца Т не снижалась, а частота депрессии сегмента S–T увеличилась до 26 %.
При сравнительной оценке изменений ЭКГ в зависимости от пораженного сосудистого бассейна выявлено, что развитие тахикардии и наджелудочковой экстрасистолии было характерно при поражении правого полушария. Локализация очагов в левом полушарии, а также в церебральных структурах, кровоснабжаемых сосудами вертебробазилярного бассейна, оказывала влияние на внутрижелудочковую проводимость и продолжительность интервала Q–T, вызывая его удлинение. Частота изменений сегмента S–T и зубца Т не различалась статистически значимо между очагами в различных сосудистых бассейнах. Однако динамика выявленных изменений показала, что при инфарктах левого полушария депрессия сегмента S–T и отрицательный зубец Т имели отчетливую тенденцию к регрессированию, тогда как при очагах в правом полушарии эти изменения были стойкими, частота их увеличивалась. Полученные данные свидетельствуют о том, что частота патологических изменений ЭКГ у больных с острым ИИ различается в зависимости от стороны локализации инфаркта мозга, что отражает функциональную асимметрию кардиоваскулярной иннервации. Правосторонняя локализация очага оказывает большее влияние на синоатриальный узел и продуцирует симпатические влияния на деятельность сердца. Левосторонние очаги оказывают влияние на атриовентрикулярный узел и внутрижелудочковую проводимость. При этом очаги в правом полушарии и субтенториальных структурах вызывают более стойкие и продолжительные влияния в виде изменений сегмента S–T и зубца Т.
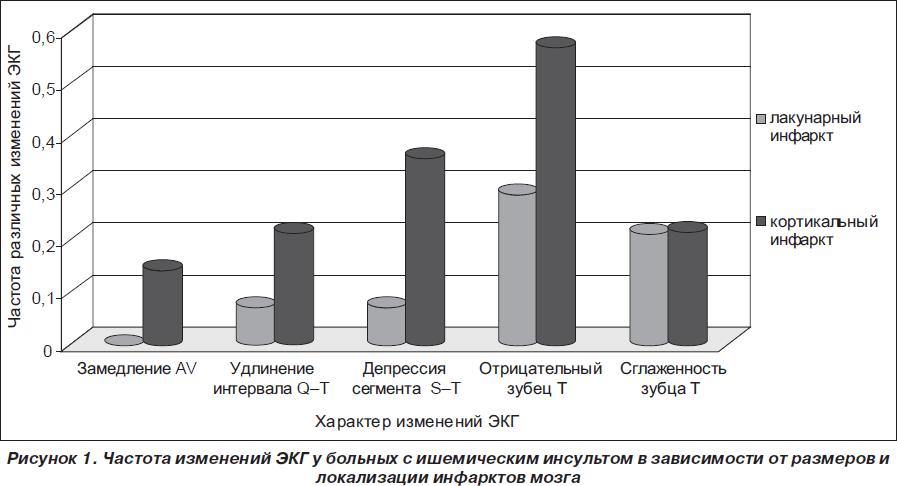
Была проведена сравнительная оценка частоты изменений ЭКГ у больных с кортикальными (n = 14) и лакунарными инфарктами (n = 14) мозга супратенториальной локализации. Существенные различия были выявлены со стороны как изменений функций проводимости, так и нарушений процессов реполяризации (рис. 1).
Так, у больных с лакунарными инфарктами не было выявлено замедления AV-проводимости, а удлинение интервала Q–T регистрировалось только у одного больного. Среди больных с кортикальными инфарктами замедление AV-проводимости наблюдалось у 2 (14,3 %), а удлинение интервала Q-T — у 3 (21,4 %) больных. Депрессия сегмента S–T регистрировалась в 5 раз, а отрицательный зубец Т — в 2 раза чаще при кортикальном инфаркте, чем при лакунарном. Сглаженность зубца Т регистрировалась с одинаковой частотой — в 21,4 % случаев в каждой подгруппе. Регистрация ЭКГ в динамике показала, что у больных с лакунарным инфарктом отрицательной динамики ЭКГ не наблюдалось ни в одном случае, у 5 (35,7 %) — положительная динамика в виде нормализации всех параметров ЭКГ, у 9 больных существенной динамики ЭКГ не отмечено. Среди больных с кортикальными инфарктами положительная динамика ЭКГ зарегистрирована у 3 (21,4 %) больных, отрицательная динамика в виде появления или усиления депрессии сегмента S–T — у 4 (28,6 %) , двое из которых умерли. Результаты полученных исследований позволяют предполагать, что на выраженность изменений ЭКГ и их динамику оказывают влияние размеры и локализация инфаркта мозга. Обширные инфаркты больших полушарий, охватывающие кору и прилежащее белое вещество лобно-теменно-височных долей, вероятно, с вовлечением островковой доли мозга, с наиболее тяжелым течением инсульта вызывают более выраженные изменения ЭКГ, что позволяет предполагать их нейрогенный характер.
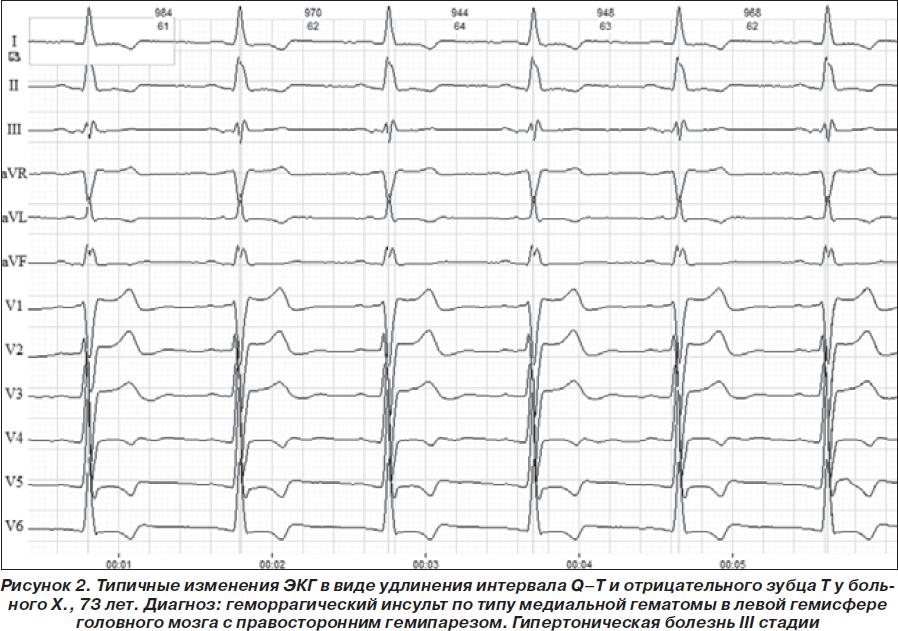
Среди 40 обследованных больных с ГИ кровоизлияния в левом полушарии наблюдались у 17 (42,5 %) больных, из них по типу латеральной гематомы — у 3, медиальной или смешанной — у 14. Кровоизлияния в правой гемисфере наблюдались у 19 (47,5 %) больных, из них по типу латеральной гематомы — у 6, медиальной и смешанной — у 13, кровоизлияние в мозжечок — у 4 (10 %). Состояние больных по шкале комы Глазго было тяжелее у больных с медиальной и смешанной локализацией гематомы — 11,8 ± 0,9 балла по сравнению с таковыми с латеральной локализацией — 13,9 ± 0,7 балла. Смертность была наиболее высокой среди больных со смешанными гематомами — умерли 7 больных. Оценка изменений сердечной деятельности по данным ЭКГ у больных с ГИ показала, что тахикардия и экстрасистолия наблюдались несколько чаще, чем у больных с ИИ. Нарушения проводимости в виде замедления AV-проводимости и удлинения интервала Q–T наблюдались более чем в 2 раза чаще, чем у больных с ИИ, — у 12,5 и 27,5 %. Депрессия сегмента S–T и отрицательный зубец Т при регистрации на 1-е — 3-и сутки наблюдались несколько реже, чем у больных с ИИ, — у 10,0 и 32,5 % больных, однако при повторной регистрации эти изменения не регрессировали, напротив, частота их увеличилась до 21,2 и 33,3 % соответственно (рис. 2).
Изменения на ЭКГ отсутствовали у 4 (10,0 %) больных. Сравнение изменений на ЭКГ в зависимости от пораженного полушария у больных с ГИ показало, что удлинение интервала Q–T также чаще было связано с поражением левого полушария. Частота изменений сегмента S–T и появление отрицательного зубца Т в первые 3 суток инсульта статистически значимо не отличались от таковых у больных с ИИ. При анализе ЭКГ в динамике были выявлены те же тенденции, что и при ИИ. При локализации очага в левом полушарии частота этих изменений уменьшалась, тогда как при поражении правого полушария изменения сохранялись и частота их увеличивалась. Сравнение частоты изменений ЭКГ в целом свидетельствует, что у выживших больных с ГИ при повторной регистрации количество нормальных ЭКГ увеличилось до 18,2 %, а у больных с ИИ — только до 13,0 %.
Мы провели также анализ частоты наиболее типичных изменений ЭКГ у больных с латеральной локализацией гематомы по сравнению с медиальной и смешанной гематомой. Отмечено, что такие изменения, как удлинение интервала Q–T и отрицательный зубец Т, статистически значимо чаще наблюдались у пациентов с медиальной и смешанной гематомой (р < 0,05) (рис. 3).
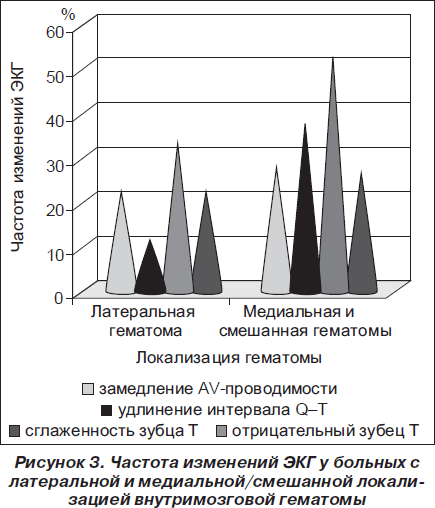
Вероятно, что большая частота изменений на ЭКГ при медиальной и смешанной локализации внутримозговой гематомы связана с тем, что такая локализация оказывает большее сдавление III желудочка, промежуточного и среднего мозга, вызывая повреждение центральных вегетативных аппаратов.
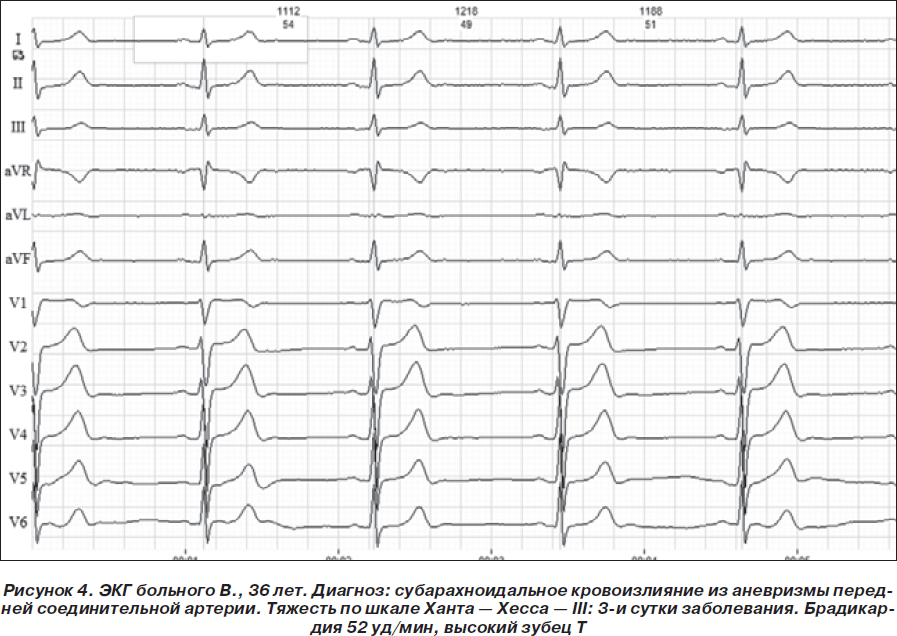
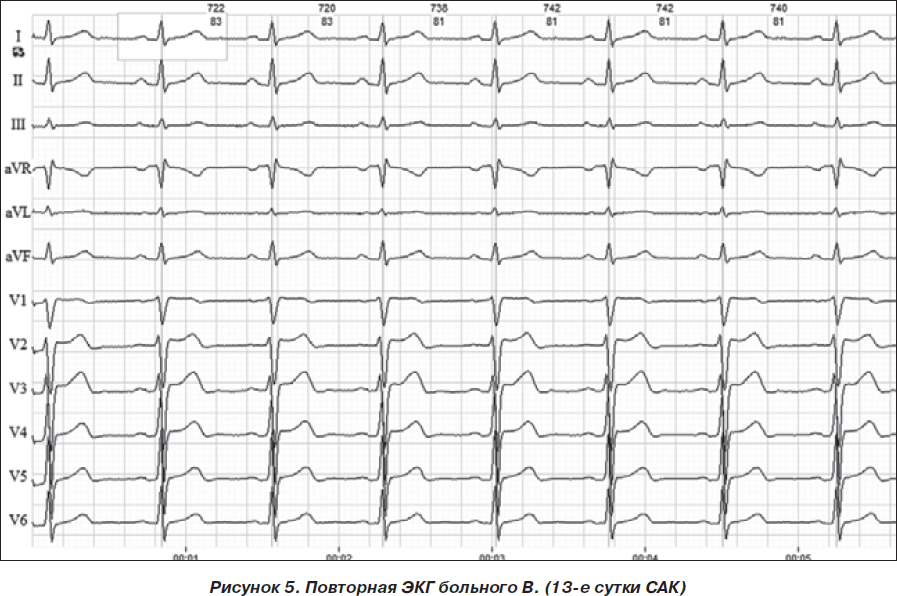
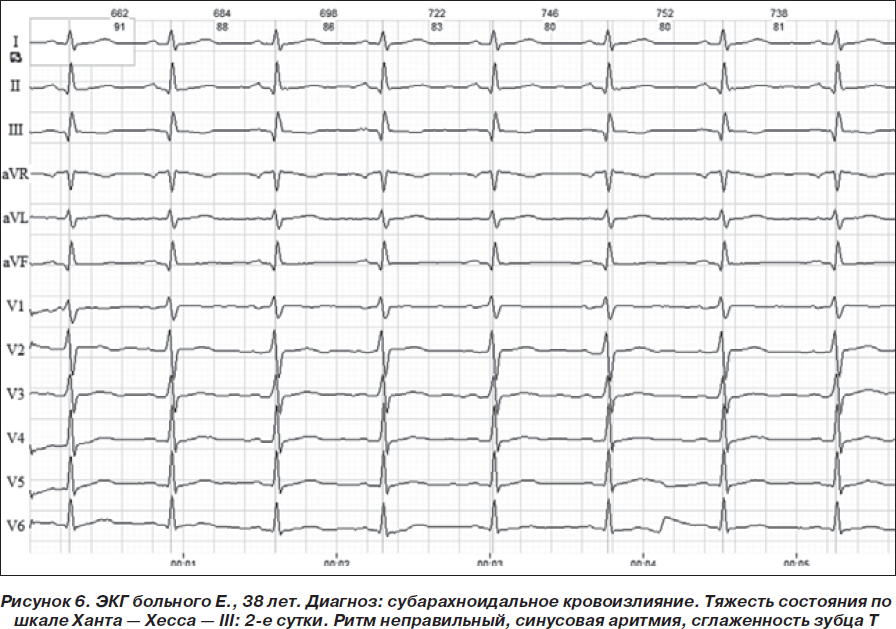
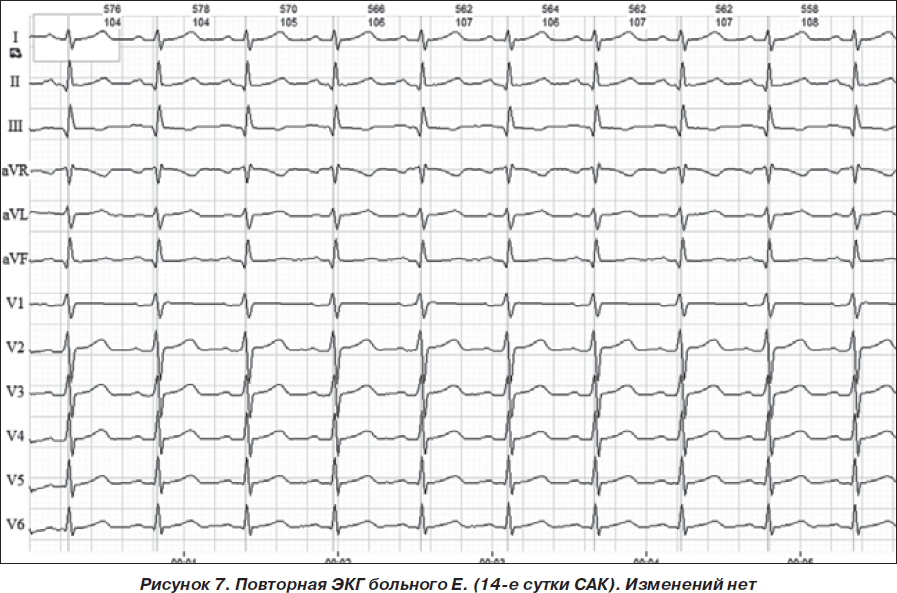
Среди 23 обследованных больных с САК ангиографическое обследование было выполнено 20 больным, у 12 из них обнаружена аневризма интрацеребральных артерий. У 4 больных субарахноидальное кровоизлияние сочеталось с вентрикулярным, у 2 — с кровоизлиянием в паренхиму лобных долей. У 5 больных САК осложнилось вторичным вазоспазмом и ишемическим повреждением мозга с развитием общемозговой и очаговой неврологической симптоматики. Изменения деятельности сердца были зарегистрированы у 22 из 23 больных: брадикардия в 1-е — 3-и сутки заболевания регистрировалась у 34,8 %, что в 3 раза чаще, чем у больных с ГИ, и в 5 раз чаще, чем у больных с ИИ. При этом замедление AV-проводимости не было зарегистрировано. Удлинение интервала Q–T зарегистрировано у 13,0 % больных, что не отличалось существенно от больных с ИИ, но было в 2 раза реже, чем при ГИ. Изменение сегмента S–T было регистрировалось более чем у трети больных. Изменения зубца Т наблюдались у большинства больных в виде высокого зубца Т, сглаженности или отрицательного зубца Т. Особенностью динамики ЭКГ у больных с САК был транзиторный характер этих изменений при благоприятном течении заболевания. Так, у 8 из 16 выживших больных к 10–14-м суткам изменения на ЭКГ отсутствовали (рис. 4–7).
Таким образом, в острой стадии инсульта изменения ЭКГ наблюдались у преобладающей части больных при всех видах инсульта. Изменения ЭКГ регистрировались в виде изменений сердечного ритма (тахикардия, брадикардия, экстрасистолия), функции проводимости и нарушений процессов реполяризации. Брадикардия была наиболее характерна для больных с САК в первые дни кровоизлияния — 34,8 %. Замедление AV-проводимости и удлинение интервала Q–T наиболее часто регистрировались у больных с ГИ — 12,5 и 27,5 %. Изменения сегмента S–T при всех видах инсульта наблюдались чаще в виде депрессии, реже — в виде незначительного подъема. Изменение зубца Т было наиболее частым феноменом при разных типах инсульта и проявлялось в виде сглаженности или инверсии, реже наблюдался высокий зубец Т. При этом депрессия сегмента S–T наиболее часто наблюдалась при САК, а отрицательный зубец Т — при ИИ. При сравнении изменений ЭКГ в зависимости от поражения правого или левого полушария была выявлена некоторая асимметрия. Удлинение интервала Q–T чаще развивалось при ИИ в левом полушарии. При ГИ отмечено преобладание замедления AV-проводимости, удлинения интервала Q–T и отрицательного зубца Т у больных с медиальной и смешанной локализацией внутримозговой гематомы, что сопровождалось более тяжелым состоянием этих больных. У больных с САК в первые несколько суток кровоизлияния кроме брадикардии наиболее часто наблюдались нарушения процессов реполяризации. Эти изменения носили более обратимый характер, чем у больных с ИИ и ГИ, что, возможно, связано с более молодым возрастом этой группы больных, меньшей частотой у них артериальной гипертонии и отсутствием атеросклеротического поражения артерий, в том числе коронарных.
Зависимость изменений ЭКГ и их динамики от размеров и локализации ишемического инфаркта мозга, локализации внутримозговой гематомы позволяет предположить их нейрогенный характер, обусловленный развитием нарушений центральной нейрогенной кардиоваскулярной регуляции в результате развития церебральной катастрофы.
Мы сочли необходимым выяснить, связаны ли выявленные изменения с повреждением сердечной мышцы. Определение уровня Tн I было проведено у 49 больных. Из них у 15 больных был ИИ, у 18 — ГИ и у 16 больных — САК. Определение проводилось в динамике двукратно — на 1-е — 3-и и 5–7-е сутки острого инсульта. Параметры нормы, установленные для используемого набора реагентов, составили 0– 0,30 нг/мл. Повышение Tн I выше контрольных значений в 1-е — 3-и сутки определялось у 10 (66,7 %) больных с ИИ. Однако повышение было незначительным и уровень Tн I колебался в пределах 0,4– 1,1 нг/мл. При повторном обследовании на 5– 7-е сутки был выше и колебался в пределах 0,4– 2,1 нг/мл. Средний уровень Tн I при первом обследовании составил 0,51 ± 0,07 нг/мл, при повторном — 0,86 ± ± 0,15 нг/мл, однако это повышение не было статистически значимым. При этом повышение Tн I выше 1,0 нг/мл отмечалось только при повторном исследовании у больных с крупными корково-подкорковыми инфарктами и у 1 больного с большим инфарктом в области варолиева моста и летальным исходом. В целом уровень Tн I был выше у больных с кортикальными инфарктами — 0,70 ± 0,02 (на 1-е — 3-и сутки) и 1,26 ± ± 0,06 при повторном исследовании по сравнению с большими и лакунарными инфарктами — 0,36 ± 0,02 (на 1-е — 3-и сутки) и 0,56 ± 0,03 (на 5–7-е сутки). Однако корреляционная связь между тяжестью состояния больных по шкале NIHSS и уровнем Tн I r = 0,47 была статистически незначимой (р = 0,073). Полученные данные свидетельствуют о том, что у большинства больных с ИИ имеется слабое увеличение в плазме крови уровня Tн I, которое незначительно повышается в динамике у больных с тяжелым инсультом. Среди больных с ГИ повышение Tн I выше контрольных значений на 1-е — 3-и сутки наблюдалось у 16 (88,9 %) больных, средний уровень был статистически значимо выше, чем у больных с ИИ, и составил 1,29 ± 0,36 нг/мл (р < 0,05). При повторном исследовании уровень Tн I на уровне контрольных значений выявлен у 3 больных, у 5 больных отмечалось снижение уровня Tн I, у 6 — незначительное повышение. В целом средний уровень снизился до 0,98 ± ± 0,16 нг/мл. Показатели находились в пределах 0,4– 6,8 нг/мл (на 1-е — 3-и сутки) и 0,5–2,4 нг/мл (на 5–7-е сутки). Однако это касалось только выживших больных. У всех умерших больных как с ГИ, так и с ИИ уровень Tн I был 2 нг/мл и выше. При сравнительном исследовании уровня Tн I при поражении правого и левого полушария различий не выявлено. У больных с ГИ отмечалась взаимосвязь между тяжестью состояния больных по шкале комы Глазго и уровнем Tн I, который возрастал в зависимости от количества баллов (рис. 8).
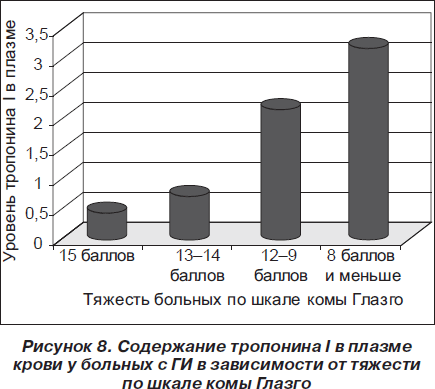
Корреляционная зависимость между тяжестью состояния больных в 1-е — 3-и сутки и уровнем Tн I была статистически значимой: r = –0,69 (р = 0,0012).
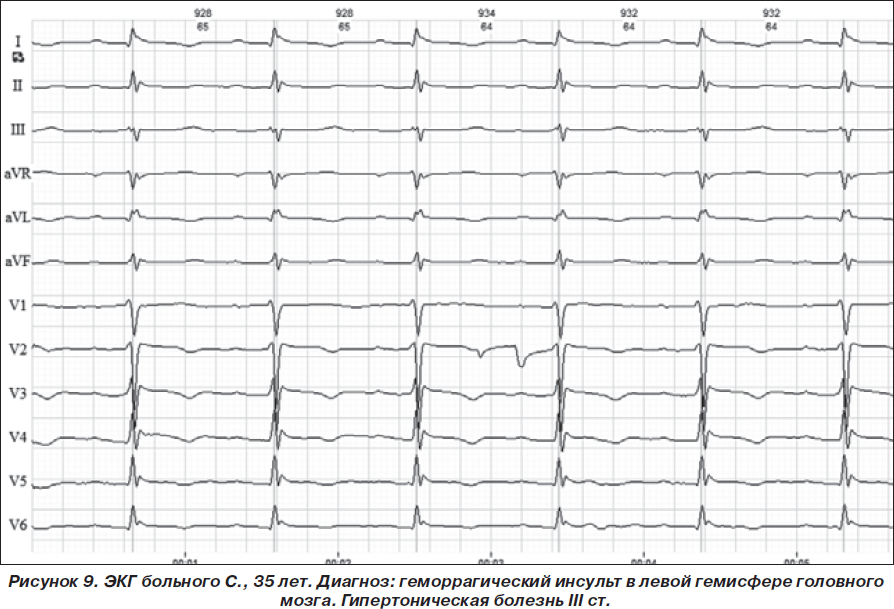
При сопоставлении уровня Tн I и ЭКГ отмечено, что изменения в виде удлинения интервала Q–T, депрессии сегмента S–T и отрицательного зубца Т наблюдались у больных с уровнем Tн I > 1,0 нг/мл. У одного умершего больного 32 лет с обширным кровоизлиянием в левой гемисфере с прорывом крови в желудочковую систему, отеком и дислокацией ствола мозга, отеком легких наблюдался наиболее высокий среди всех обследованных больных уровень Tн I — 6,8 нг/мл, при этом на ЭКГ регистрировались удлинение интервала Q–T, смещение сегмента S–T вверх в I, II, V2–V6-отведениях и отрицательный зубец Т. Однако инфаркт миокарда при патологоанатомическом обследовании не обнаружен, признаки атеросклероза коронарных артерий также отсутствовали (рис. 9).
Среди 16 обследованных больных с САК аневризматическая этиология была установлена у 10, 5 из них умерли в результате тяжелого кровоизлияния. Средний уровень Tн I на 1-е — 3-и сутки — 1,57 ± 0,27 нг/мл, что было статистически значимо выше, чем у больных с ИИ, и незначимо выше, чем у больных с ГИ. В динамике отмечалось снижение этого показателя до 1,02 ± 0,10 нг/мл, (р > 0,05). Повышение Tн I выше контрольных значений выявлено у 15 (93,75 %) больных, и его уровень колебался от 0,5 до 4,3 нг/мл в 1-е — 3-и сутки и от 0,5 до 1,5 нг/мл при повторном исследовании у выживших больных. У больных с САК также наблюдалась отчетливая тенденция к нарастанию уровня Tн I в зависимости от увеличения тяжести больных по шкале Ханта и Хесса. У всех больных с тяжестью состояния 8 баллов и меньше по шкале комы Глазго и 5 баллов по шкале Ханта и Хесса, что соответствовало коматозному состоянию и сопровождалось плохим прогнозом и летальным исходом, регистрировались наиболее высокие значения Tн I, которые колебались от 1,6 до 3,5 нг/мл. Однако корреляционная зависимость между тяжестью больных по шкале Ханта и Хесса и уровнем Tн I была статистически незначимой (r = 0,46; р = 0,072), возможно, из-за недостаточного количества наблюдений.
Проведенное исследование показало, что у большинства больных с острым инсультом при всех типах инсульта определяется повышенное содержание маркера миокардиального некроза Tн I без признаков ОКС. У больных с ИИ это повышение было незначительным, но у больных с ГИ и САК уровни Tн I были статистически значимо выше по сравнению с ИИ. Повышение Tн I > 1,0 нг/мл сопровождалось изменениями ЭКГ в виде удлинения интервала Q–T, депрессии сегмента S–T и отрицательного зубца Т, тогда как при уровне Tн I < 1,0 нг/мл эти изменения не наблюдались. Повышение уровня Tн I ассоциировалось с тяжестью состояния больных при всех типах инсульта, но статистически значимой была корреляционная зависимость между уровнем Tн I и тяжестью состояния больных с ГИ по шкале комы Глазго. У больных с ГИ и САК при нефатальном инсульте наблюдалось снижение уровня Tн I, тогда как у больных с ИИ — некоторое повышение. Признаки кардиальной дисфункции были наиболее выражены при ГИ и САК, однако при ИИ они более пролонгированы. Повышение Tн I > 2,0 нг/мл было связано с плохим прогнозом при всех типах инсульта. Таким образом, у больных с острым инсультом развивается повреждение миокарда, которое носит микроструктурный и субклинический характер, но сопровождается появлением в плазме крови низких уровней маркера миокардиального некроза. Вероятно, повреждение миокарда в острый период инсульта имело нейрогенный характер, хотя мы не могли точно исключить наличие асимптомной ИБС до развития инсульта. Так, в исследовании D. Calvet et al. [11] асимптомная ИБС с наличием минимум одного коронарного стеноза і 50 % при коронарографии была выявлена у 21 % больных, перенесших некардиоэмболический ИИ. Среди больных со стенозом внутренней сонной артерии с помощью МРТ сердца обнаружены миокардиальные рубцы у 41 %, свидетельствующие о перенесенном немом инфаркте миокарда [12]. Возможно, что с повреждением миокарда при остром инсульте связано увеличение риска смерти от ИБС у больных после перенесенного инсульта.
Очевидно, что ведение больных с острым инсультом требует мероприятий по защите миокарда с участием кардиологов и терапевтов, что еще раз подтверждает положение об инсульте как мультидисциплинарной проблеме.
1. Міщенко Т.С. Епідеміологія цереброваскулярних захворювань в Україні у 2007 р. // Судинні захворювання головного мозку. — 2008. — № 2. — С. 3-7.
2. Евтушенко С.К. От этиологии подвидов инсульта у лиц молодого возраста — к их эффективному лечению и профилактике // Матеріали ХІІ міжнародної конференції «Актуальні напрямки в неврології: сьогодення та майбутнє». — Судак, 2010. — С. 12-18.
3. Зозуля І.С., Мошенська О.П. Гострий період ішемічного інсульту: сучасний погляд на проблему // Український медичний часопис. — 2009. — № 4. — С. 67-73.
4. Никонов В.В., Савицкая И.Б. Старые и новые идеи церебропротекции ишемического инсульта // Медицина неотложных состояний. — 2007. — № 6(13). — С. 53-57.
5. Benerjee A., Silver L.E., HeneghanC. et al. Population-based comparison of risk factors for ischaemic stroke versus acute coronary syndromes: identical twins or distant relatives? // Cerebrovascular diseases / Abstracts of 17th European Stroke conference, Nice, France, 2008. — Vol. 25, Suppl. 2. — P. 16.
6. Hyvдrinen M., Qiao Q., Tuomilehto J. et al. The difference between acute coronary heart disease and ischaemic stroke risk with regard to gender and age in Finnish and Swedish population // International Journal of stroke. — 2010. — Vol. 5 (issue 3). — P. 152-156.
7. Higgins J.P. Elevation of cardiac troponin I indicates more than myocardial ischemia // Clin. Invest. Med. — 2003. — Vol. 26, № 3. — P. 133-146.
8. Kerr G., Ray G., Wu O., Stott D.J., Langhorne P. Elevated troponin after stroke — a systematic review // Cerebrovascular diseases / Abstracts of 17th European Stroke conference, Nice, France, 2008. — Vol. 25, Suppl. 2. — P. 59-60.
9. Whikeley W., Sengupta A., Chong W.L. Sandercock PAG. Blood markers for the prognosis of ischaemic stroke: a systematic review of 81 studies and 70 markers // International Journal of stroke / Abstracts of the 6th World stroke congress, Vienna, Austria, 2008. — Vol. 3, Suppl. 1. — P. 87.
10. Белова А.Н. Шкалы, тесты и опросники в неврологии и нейрохирургии. — М., 2004. — 432 с.
11. Calvet D., Touzй E., Varenne O. et al. Prevalence of asymptomatic coronary disease in ischemic stroke/TIA patient // Cerebrovascular diseases / Abstracts of 17th European Stroke conference, Nice, France, 2008. — Vol. 25, Suppl. 2. — P. 17.
12. Fierbach J.B., Goericke S., Hunold P. et al. Myocardial scars are an underestimated cardiovascular burden in patients with ICA stenosis // Cerebrovascular diseases / Abstracts of 17th European Stroke conference, Nice, France, 2008. — Vol. 25, Suppl. 2. — P. 16.