Журнал «Медицина неотложных состояний» 4(35) 2011
Вернуться к номеру
Гипергликемия при критических состояниях: возможные пути решения проблемы
Авторы: Обухова О.А., Кашия Ш.Р., Курмуков И.А., Салтанов А.И. ГУ «Российский онкологический научный центр РАМН», г. Москва
Рубрики: Семейная медицина/Терапия, Медицина неотложных состояний
Версия для печати
В последние годы отмечается повышенный интерес исследователей к проблеме спонтанной или стрессорной гипергликемии, возникающей в постагрессивный период у не страдающих диабетом лиц после перенесенного оперативного вмешательства, травмы, ожога или инфаркта миокарда. На сегодняшний день имеется достаточно фактов, доказывающих необходимость поддержания эугликемии в посттравматический период, однако эта задача остается до сих пор не решенной. Цель данной статьи — оценить теоретические предпосылки и современные клинические возможности коррекции гипергликемии у больного в критическом состоянии.
Метаболический ответ на системное повреждение. Одними из клинических проявлений метаболического ответа на системное повреждение являются гипергликемия и интолерантность к глюкозе, характерные для всех типов критических состояний, в том числе для больных, не страдающих диабетом. Этот феномен, возникающий после анестезии, операции, травмы [1–5] или ожога [6], описан еще в 30-е годы прошлого века как псевдодиабет больных с ожогами [7]. Подобные изменения отмечаются также при инфаркте миокарда и в сердечно-сосудистой хирургии [8, 9].
Метаболические изменения, возникающие после травмы, условно делятся на два периода или на две фазы [10, 11]. Первая фаза, возникающая непосредственно после травмы, так называемая ebb-фаза, характеризуется замедлением метаболической активности и снижением потребления кислорода. Как правило, сопровождается гипергликемией, повышенным гликолизом, замедленным окислением глюкозы, замедленным глюконеогенезом, низким окислением пирувата.
Обычно в течение нескольких часов (12–24 ч) ebb-фаза переходит в flow-фазу (со 2-х по 14–21-е сутки), когда скорость метаболических процессов повышается. Причем чем тяжелее травма, тем выше скорость метаболизма. Отмечается активация симпатоадреналовой системы, гипердинамия, повышается потребление кислорода, усиливается мышечный протеолиз и катаболизм белка, происходит увеличение экскреции калия. Эта фаза сопровождается задержкой жидкости, натрия, развитием интолерантности к глюкозе и гипергликемией, повышенным глюконеогенезом и гликолизом [12]. Аминокислоты, необходимые для синтеза протеинов и осуществления репарационных процессов в поврежденных тканях, образуются из мышечного белка. В то же время аминокислоты используются как субстрат для глюконеогенеза, что усиливает катаболизм протеинов и требует дополнительных затрат энергии [11, 13].
Секреция гормонов катаболизма. Известно, что после травмы повышается секреция кортикостероидов. Развивается так называемый общий адаптационный синдром, подразумевающий взаимосвязь между гормональными и метаболическими изменениями при стрессе. При возникновении неотложного (критического) состояния отмечается повышение секреции катехоламинов. Высокий уровень кортизола и катехоламинов может сохраняться в течение нескольких недель после травматического воздействия. Это зависит от тяжести повреждения и развивающихся осложнений [11, 13].
Секреция инсулина. Спонтанная гипергликемия при стрессе инициируется секрецией катаболических гормонов и является, по существу, следствием диссонанса между секрецией инсулина и развивающейся к нему резистентностью периферических тканей: скелетной мускулатуры, гепатоцитов, жировой ткани. Это обусловлено подавлением секреции инсулина на фоне адренергической стимуляции [14]. Параллельно развивается невосприимчивость периферических тканей к инсулину, в то время как продукция эндогенной глюкозы повышена. Это приводит к нарушению толерантности к глюкозе, изменению липидного обмена и, как следствие, к персистирующей гипергликемии и гиперлипидемии [15]. Этот феномен сформировался в результате патофизиологической адаптации и направлен на сохранение питательных субстратов для инсулинонезависимых жизненно важных органов, таких как мозг [16].
Резистентность к инсулину. Считается, что метаболические изменения после повреждения могут быть объяснены нарушением баланса между основными анаболическими (инсулином) и катаболическими гормонами (кортизолом, катехоламинами, глюкагоном). Эти процессы, сформировавшиеся в ходе эволюции, направлены на ускорение процесса заживления и активацию иммунной защиты в ущерб другим, заменимым процессам, например мышечной работе. Тем не менее эти компенсаторные реакции жизнеобеспечения могут привести к развитию тяжелых осложнений, нарушая метаболизм белков, жиров и углеводов. Возможно, терапевтическое применение инсулина способно нивелировать метаболический ответ на травму, позволяя использовать нутриенты по назначению [17, 18].
Резистентность к инсулину можно описать как невосприимчивость анаболических процессов к стандартным эффектам инсулина, и, вероятно, большинство метаболических нарушений, развивающихся на фоне критического состояния, обусловлены потерей чувствительности тканей к этому гормону [19, 20]. Клинические исследования последних лет доказывают, что у реанимационных больных хирургического профиля чувствительность к инсулину снижена на 50–70 % по сравнению со здоровыми добровольцами [21–23]. Тяжесть инсулиновой резистентности на фоне критического состояния коррелирует с тяжестью состояния, индексом массы тела и энергетическими потребностями и не зависит от уровня окисления питательных субстратов и причины, повлекшей за собой развитие критического состояния [21].
Анестезия и оперативное вмешательство влияют на водно-электролитный баланс, вызывая задержку натрия и воды и способствуя повышенной экскреции калия. Это происходит в результате специфического воздействия минералокортикоидов, катехоламинов и повышенной секреции антидиуретического гормона на фоне изменения и перераспределения объема циркулирующей крови. В ответ на системное повреждение почки начинают удерживать натрий и воду до тех пор, пока в результате интенсивной терапии общий натрий и общая вода тела не достигнут нормальных величин. Кроме того, из-за повреждения мембраны клетки натриевая помпа становится неэффективной, и поступление ионов натрия и хлора внутрь клетки значительно повышается. В то же время происходит повышенная экскреция почками калия, поступающего из разрушенных или поврежденных клеток, а также увеличивается выделение азота и гликогена. Эти изменения спонтанно исчезают на стадии выздоровления, однако при развитии осложнений патофизиологические механизмы продолжают действовать. Таких больных легко перегрузить натрием и водой, если они назначаются сверх потребностей [11, 24].
Терапевтическое применение инсулина. Многочисленные исследования доказывают, что инфузия глюкозы с добавлением необходимого количества калия и высоких доз инсулина способна уменьшить проявления отрицательного баланса азота у пациентов, находящихся в критическом состоянии. Например, у больных с ожогами, получавших растворы 50% глюкозы с добавлением высоких доз инсулина и необходимого количества калия, при достижении нормогликемии биохимические показатели сыворотки крови и мочи становились нормальными. В некоторых случаях при высокой резистентности к инсулину дозы препарата доходили до 1,2 ЕД на 1 грамм глюкозы. При достижении нормогликемии отмечалось быстрое снижение уровня мочевины и калия в сыворотке крови и в моче, что говорило о замедлении процессов катаболизма [25–27].
Общеизвестное влияние инсулина на водно-электролитный баланс объясняется воздействием инсулина на механизм Nа+-К+-помпы. Инсулин регулирует накопление гликогена и играет важную роль в поддержании гомеостаза К+. Благодаря инсулину увеличивается потребление калия периферическими тканями [28–30].
Эффекты инсулина на водно-электролитный обмен исследованы у больных с ожогами, имевших положительный водный и солевой баланс. Назначение глюкозы с инсулином привело к существенному увеличению диуреза, снижению концентрации калия в плазме крови и в моче и повышению плазменной концентрации натрия. Авторы объясняют этот феномен восстановлением K+-Na+-помпы, поврежденной в результате агрессивного воздействия, в результате чего возобновляется адекватная диффузия иона натрия и калия и таким образом стабилизируется водно-электролитный баланс [31].
Несмотря на нарушение утилизации энергетических и пластических субстратов в постагрессивном периоде, искусственное питание является одним из постулатов интенсивной терапии [62]. Основным углеводом и традиционном источником энергии в практике парентерального питания остается глюкоза. Long et al. на примере больных с ожогами показали, что при увеличении дозы вводимой глюкозы экскреция мочевины с мочой достоверно снижается. Это происходит до тех пор, пока поступление углеводов сопоставимо с энергетическими потребностями больного. Последующее увеличение доз глюкозы не снижает потерь азота, несмотря на введение инсулина [26, 32]. Считается, что гипералиментация на фоне стресса ничем не оправдана и не в состоянии повлиять на катаболические процессы [26, 34].
В 1999 г. опубликованы результаты исследования, целью которого явилась оценка возможности влияния высоких доз инсулина на усиление синтеза протеина в мышцах скелетной мускулатуры у больных, получивших тяжелые ожоги. Пациенты находились на энтеральном гиперкалорическом питании. На долю углеводов приходилось 82,3 % смеси, 15 % составляли белки и 2,7 % — жиры. Одна группа больных получала стандартную инсулиновую терапию, второй группе инсулин назначался в дозе 2,6 МЕ/кг в минуту. Концентрация глюкозы крови оценивалась каждый час. Исследование показало, что высокие дозы инсулина, назначаемые при тяжелой ожоговой травме, достоверно увеличивают анаболизм протеина в скелетных мышцах. Также было продемонстрировано, что применение низких доз инсулина на фоне гиперкалорийного питания ускоряет анаболизм в скелетной мускулатуре [25, 35, 63].
Имеются доказательства обоснованного применения интенсивной инсулинотерапии (ИИТ) в послеоперационном периоде при проведении полного парентерального питания у больных, перенесших абдоминальное хирургическое вмешательство. На фоне нормализации глюкозы крови удается редуцировать продукцию эндогенной глюкозы, стабилизировать утилизацию питательных субстратов, уменьшить потери азота. Это свидетельствует о влиянии инсулинотерапии на все звенья метаболизма [36–38].
ИИТ оказывает влияние на липидный профиль сыворотки крови. На фоне применения инсулинотерапии повышается уровень липопротеидов низкой плотности (ЛПНП) и высокой плотности (ЛПВП) и снижается концентрация холестерина. Известно, что ЛПВП и ЛПНП участвуют в процессах детоксикации. Авторами делается вывод, что увеличение этих липидных фракций положительно сказывается на выживаемости больных [39–41].
В 2001 г. были опубликованы данные рандомизированного, контролируемого исследования, целью которого являлась оценка клинических эффектов интенсивной инсулинотерапии в послеоперационном периоде. В исследование было включено 1548 больных отделений интенсивной терапии, находившихся на ИВЛ (62,7 % больных перенесли операции на сердце). Больные были разделены на две группы: группу, получавшую ИИТ (поддержание концентрации глюкозы крови около 6ммоль/л или ниже), и группу, находившуюся на стандартной инсулинотерапии (поддерживалась концентрация глюкозы крови от 10,5 до 11,5 ммоль/л, инфузия инсулина начиналась, если сахар крови был выше 12 ммоль/л). Было обнаружено, что на фоне ИИТ количество септических осложнений снижается на 46 %, частота развития острой почечной недостаточности, требующая проведения гемодиализа, уменьшалась на 41 %, а число случаев клинически значимой полинейропатии было редуцировано на 44 %. Среди больных, находившихся более 5 дней в ОРИТ и получавших ИИТ, было отмечено снижение смертности на 45 %. Исследователи объясняют этот факт предотвращением развития полиорганной недостаточности [42, 43].
Имеются сообщения о том, что назначение инсулина полезно и при проведении интрадиализного парентерального питания. Добавление инсулина к полному парентеральному питанию во время гемодиализа достоверно снижало элиминацию аминокислот (на 80 %) и замедляло подъем концентрации триглицеридов. Авторы делают вывод, что применение инсулина на фоне интрадиализного парентерального питания приводит к снижению протеолиза и ускорению белкового синтеза в скелетной мускулатуре [44, 45].
Интенсивная инсулинотерапия: «за» и «против». Алгоритм проведения ИИТ разработан еще в прошлом веке и заключается в проведении непрерывной инфузии инсулина с такой скоростью, которая необходима для достижения нормогликемии на фоне круглосуточного проведения питательной поддержки [46, 47].
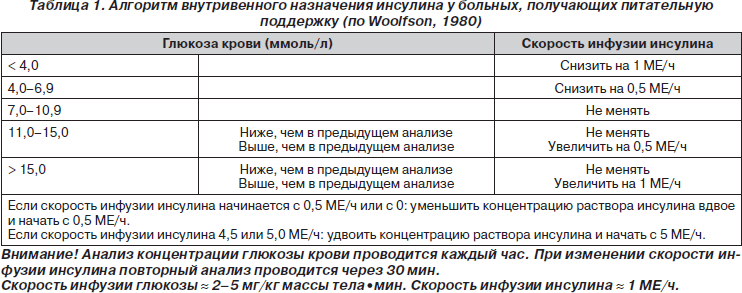
Техника проведения ИИТ достаточно проста. Для этого в 50 мл физиологического раствора растворяется 50 международных единиц инсулина (актрапид). Некоторые исследователи добавляют в раствор инсулина 2 мл крови больного. Кровь используется для предотвращения абсорбции инсулина пластиком шприца и системы для переливания [33]. Скорость инфузии инсулина меняется в зависимости от колебаний уровня глюкозы крови (табл. 1).
Одним из слагаемых успешного проведения парентерального питания у больного, находящегося в отделении интенсивной терапии, является оптимальная скорость введения питательных растворов. Многочисленными исследованиями доказано, что оптимальной скоростью введения глюкозы считается 2– 5 мг/кг•мин (200–500 г/сут для пациента весом 70 кг). Такая скорость обеспечивает адекватное подавление продукции эндогенной глюкозы, а также способствует оптимальной утилизации углеводов. При этой скорости инфузии отмечается подавление глюконеогенеза на 80 %. Если же скорость инфузии 1–3 мг/кг•мин (100– 300 г/сут при массе тела 70 кг), удается достигнуть максимального окисления глюкозы, однако глюконеогенез подавляется недостаточно. При более высокой скорости введения глюкозы, 7–8 мг/кг•мин или 700– 800 г/сут при массе тела 70 кг, утилизация глюкозы не адекватная, гипергликемия усиливается и значительно увеличивается выработка углекислого газа, что усугубляет дыхательную недостаточность [26, 48]. На сегодняшний день возможность использования ИИТ остается спорной. Во-первых, предполагаемые рамки эугликемии достаточно узкие, и даже небольшая передозировка инсулина может повлечь за собой серьезные последствия [49]. В различных открытых контролируемых исследованиях было показано, что на фоне ИИТ в 5–8 % случаев отмечается гипогликемия, требующая немедленной коррекции [42, 50]. Во-вторых, программа ИИТ должна осуществляться круглосуточно на фоне круглосуточного проведения искусственного питания. Это условие не всегда выполнимо. В-третьих, такая терапия требует скрупулезного лабораторного мониторинга, являющегося одним из слагаемых успешного лечения [53].
Существуют работы, оспаривающие положительный эффект ИИТ. Бельгийские исследователи опубликовали результаты мультицентрового проспективного рандомизированного исследования, в котором проводилось сравнение между группами реанимационных больных, получавших инсулин в высоких или в стандартных дозах. Исследование проведено у 1011 больных общей популяции, находившихся в 21 отделении интенсивной терапии 19 медицинских центров 7 стран. По результатам исследования авторы сделали вывод, что применение ИИТ не влияет на 28-дневную и общую выживаемость пациентов, находящихся в критическом состоянии [49].
Некоторые факторы, влияющие на степень гликемии. Кроме того, нельзя забывать о многочисленных факторах, влияющих на степень гликемии, таких как адекватность обезболивания, лекарственная полипрагмазия, сопутствующие заболевания (сахарный диабет не обсуждается!), органная недостаточность и т.д. Например, применение эпидурального обезболивания (местный анестетик или местный анестетик в комбинации с низкими дозами опиоидов) в послеоперационный период достоверно снижает уровень резистентности к инсулину в течение первых 48 часов после проведения оперативного вмешательства [51, 52].
Персистирующая гипергликемия может быть спровоцирована введением симпатомиметиков, стимулирующих a-адренорецепторы, а также назначением глюкокортикоидов и цитостатиков [53].
Сопутствующая патология также вносит свой вклад в развитие гипергликемии. Известно, что при циррозе печени развивается резистентность к инсулину, приводя к нарушению утилизации глюкозы в мышцах. Обнаружено, что даже после удачной пересадки печени резистентность к инсулину купируется лишь частично, и утилизация глюкозы в мышцах остается сниженной по сравнению с таковой у испытуемых волонтеров [54].
Известно, что у тучных пациентов толерантность к глюкозе снижена, и такие больные для поддержания нормогликемии требуют более высоких доз инсулина, чем нормостеники [55–57].
Ятрогенная гипер- и гипогликемия часто развивается на фоне искусственного питания. Избежать резкого колебания уровня глюкозы достаточно легко. Необходимо введение питательных субстратов с низкой постоянной скоростью при помощи инфузомата (перфузора) с периодическим контролем уровня глюкозы крови (интервал не более 4 часов). Рекомендуются современные технологии парентерального питания, в частности, введение трехкомпонентных смесей «три в одном» или «все в одном». В настоящее время готовые к использованию препараты «три в одном» в 3-камерном пакете считаются стандартом безопасного краткосрочного или длительного парентерального питания у взрослых пациентов. Они просты в эксплуатации, опасность контаминации раствора минимальная, а получаемая при смешивании трех компонентов питательная смесь сохраняет физическую стабильность в течение длительного времени и не нарушается при добавлении различных добавок: растворов электролитов, витаминов, микроэлементов и т.п. [58–60].
Одним из таких трехкомпонентных растворов является Оликлиномель, представляющий собой пакет, состоящий из 3 изолированных камер, разделенных перегородками. Одна из камер заполнена жировой эмульсией клинолеик, вторая — сбалансированной аминокислотной смесью синтамин, а третья — раствором глюкозы. При смешивании раствора концентрация глюкозы колеблется от 8 до 16 % в зависимости от инфузионной формы препарата (например, Оликлиномель N 4–550 (2000 мл) при совмещении питательных камер содержит 8% раствор глюкозы, а Оликлиномель N 7–1000 (1500 мл), соответственно, 16% раствор глюкозы). При этом общее количество глюкозы в пакетах (от 160 до 320 г) позволяет использовать препарат, выполняя современные рекомендации нутрициологов, касающихся общего объема глюкозы в сутки. При правильной скорости введения и точно подобранных дозах инсулина гипергликемия, как правило, не развивается [61]. Кроме того, благодаря закрытой системе контейнеров происходит асептическое растворение смеси; при этом сводится к минимуму риск инфицирования больного. После смешивания препарат может храниться и использоваться в течение двух суток при комнатной температуре или храниться при температуре 2–8 °С в течение недели. Простота в употреблении, сбалансированные формы для введения в периферические или центральные вены, с добавлением электролитов или без них — все это характеризует Оликлиномель как современный безопасный раствор для проведения парентерального питания в отделении интенсивной терапии и в стационаре общего профиля.
В заключение следует отметить, что история изучения взаимосвязи между метаболизмом углеводов, секрецией инсулина и резистентностью к нему началась более 150 лет назад. В последние 50 лет возобновился интерес к метаболическим, физиологическим и целлюлярным эффектам инсулина применительно к пациентам с различной патологией, находящихся в ОРИТ. Тем не менее лечебные возможности инсулина изучаются до сих пор. Сегодня инсулин по-прежнему занимает важное место в лекарственном арсенале врача анестезиолога-реаниматолога, позволяя решать многие трудные задачи, возникающие при лечении пациентов отделений реанимации и интенсивной терапии.
Впервые опубликовано в журнале «Вестник интенсивной терапии», 2008, № 3. Критические состояния
1. Weddell W.G. et al. Changes in the blood sugar level associated with surgical operations // Br. J. Surg. — 1934. — 22. — 80.
2. Cherke R.S.J. The hyperglycaemic response to different types of surgery and anaesthesia // Br. J. Anaesth. — 1970. — 42. — 45.
3. Thomsen V. Studies of trauma and carbohydrate metabolism with special reference to the existence of traumatic diabetes // Acta Med. Scand. — 1938. — (Suppl. 91). — 1.
4. Schreiber M.N. et al. Influence of laparoscopic-assisted hysterectomy vs vaginal hysterectomy on perioperative glucose metabolism // Cl. Nutr. — 1998 Aug. — Vol. 17, (Suppl. 1). — 6. — O.19.
5. Schricker Th. еt al. The catabolic response to surgery: how can it be modified by the anesthesiologist? // Canadian Journal of Anesthesia. — 2001. — 48. — R13.
6. Bayley B.N. Hyperglycaemia in burns // Br. Med. J. — 1960. — 2. — 1783.
7. Evans E.I. et al. The stress response in the severely burned // Ann. Surg. — 1951. — 134. — 588.
8. Dhatariya K. Hyperglycemia After Myocardial Infarction // Diabetes Care. — 2003. — 26. — 2222.
9. Longarela A.M. et al. Prevention of proteic catabolism and stress response after elective cardiac surgery // Cl. Nutr. — 2004 Aug. — Vol. 23 (4). — Р. 843(04-A-271-ESPEN).
10. Martnez-Riquelme A.E., Allison S.P. Insulin revisited // Cl. Nutr. Febr. — 2003. — Vol. 22, № 1. — Р. 7.
11. Попова Т.С. и соавт. Современные представления о метаболическом ответе на системное повреждение. Синдром гиперметаболизма-гиперкатаболизма // Нутритивная поддержка больных в критических состояниях. — М.: М-Вести, 2002. — С. 12-47.
12. Evans T.W. Hemodynamic and metabolic therapy in critically ill patients // N. Engl. J. Med. — 2001. — November 8, Vol. 345, № 19. — 1417.
13. Рябов Г.А., соавт. Энергетический метаболизм при неотложных состояниях // Искусственное питание в неотложной хирургии и травматологии / Под ред. Ермолова А.С. — М.: НИИ СП им. Н.В. Склифосовского, 2001. — С. 21-82.
14. Porte D. et al. the effect of epinephrine on immunoreactive insulin levels in man // J. Clin. Invest. — 1966. — 45. — 228.
15. Martnez-Riquelme A.E. et al. Insulin revisited // Cl. Nutr. Febr. — 2003. — Vol. 22, № 1. — Р. 7-15.
16. Sobotka L. Basics in clinical nutriron. — Prague, Czech Republic, «Galen», 2004. — 500 p.
17. Carlson G.L. Insulin resistance and glucose-induced thermogenesis in critical illness // Proc. Nutr. Soc. — 2001. — 60. — 381-8.
18. Schricker Th. et al. Strategies to attenuate the catabolic response to surgery and improve perioperative outcomes // Can. J. Anesth. — 2007 June. — 54, 6. — Р. 414-419.
19. Hunter S.J., Garvey W.T. Insulin action and insulin resistance: diseases involving defects in insulin receptors, signal transduction, and the glucose transport effector system // Am. J. Med. — 1998. — 105. — 331-45.
20. Carlson G.L. Insulin resistance and glucose-induced thermogenesis in critical illness // Proc. Nutr. Soc. — 2001. — 60. — 381-8.
21. Zaunera A. et al. Severity of insulin resistance in critically ill medical patients // Metabolism Clinical and Experimental. — 2007. — 56. — 1-5.
22. Black P.R., Brooks D.C. et al. Mechanism of insulin resistance following injury // Ann. Surg. — 1982. — 196. — 420-35.
23. Saeed M., Carlson G.L. et al. Selective impairment of glucose storage in human sepsis // Br. J. Surg. — 1999. — 86. — 813-21.
24. Kraft M.D. еt al. Treatment of electrolyte disorders in adult patients in the intensive care unit // Am. J. Health-Syst. Pharm. — 2005 Aug 15. — Vol. 62. — 1663.
25. Ferrando A.A. et al. A submaximal dose of insulin promotes net skeletal muscle protein synthesis in patients with severe burns // Ann. Surg. — 1999. — 229. — 11-18.
26. Frank B. et al. Applied Nutrition in ICU Patients. A Consensus Statement of the American College of Chest Physicians // CHEST. — 1997. — 111. — 769-78.
27. Hoffer L.J. Protein and energy provision in critical illness // American Journal of Clinical Nutrition. — 2003 Nov. — Vol. 78, № 5. — 906-911.
28. Sweeney G., Klip A. Regulation of the Na+/K+-ATPase by insulin: why and how? // Mol. Cell. Biochem. — 1998. — 182. — 121-133.
29. Sahir S. Rassam et al. Perioperative electrolyte and fluid balance // Critical Care & Pain. — 2005. — 5(5). — 157-160.
30. Alex G. Therien and Rhoda Blostein. Mechanisms of sodium pump regulation // Am. J. Physiol. Cell Physiol. — 2000 Sep. — 279, Vol. 279, Issue 3. — C541-C566.
31. Hinton P. et al. Electrolyte chages after burn ijury and effect of treatment // Lancet. — 1973. — 2 (7823). — 218.
32. Long J.M. et al. Effect of carbohydrate and fat intake on nitrogen excretion during total intravenous feeding // Ann. Surg. — 1977. — 185(4). — 417.
33. DeFronzo et al. Glucose clamp technique: a method for quantifying insulin secretion and resistance // Am. J. Physiol. — 1979. — 237(3). — E214-E223 (or Am. J. Physiol.: Endocrinol. Metab. Gastrointest. Physiol. — 1979. — 6(3). — E214-E223).
34. Hoffer L.J. Protein and energy provision in critical illness // American Journal of Clinical Nutrition. — 2003 Nov. — Vol. 78, № 5. — 906-911.
35. Schricker Th. et al. Parenteral nutrition and protein sparing after surgery: do we need glucose? // Metabolism Clinical and Experimental. — 2007. — 56. — 1044-1050.
36. Brandi L.S. et al. Insulin resistance after surgery: normalization by insulin treatment // Clin. Sci. (Lond). — 1990. — 79. — 443-450.
37. Thorell A. et al. Intensive Insulin Treatment in Critically Ill Trauma Patients Normalizes Glucose by Reducing Endogenous Glucose Production // The Journal of Clinical Endocrinology & Metabolism. — 2004. — Vol. 89, № 11. — Р. 5382-5386.
38. Soop M. et al. Postoperative changes in endogenous glucose release are related to changes in whole-body net protein breakdown // Cl. Nutr. — 2004 Aug. — Vol. 23(4). — Р. 786 (04-A-640ESPEN).
39. Mesotten D. et al. Contribution of Circulating Lipids to the Improved Outcome of Critical Illness by Glycemic Control with Intensive Insulin Therapy // The Journal of Clinical Endocrinology & Metabolism. —2004 Jan. — Vol. 89, № 1. — 219-226.
40. Brian J. Van Lenten et al. The role of lipoproteins and receptor-mediated endocytosis in the transport of bacterial lipopolysaccharide (endotoxin/atherosclerosis) // Proc. Natl. Acad. Sci. USA. — 1986 April. — Vol. 83. — Р. 2704-2708.
41. Harris H.W., Johnson J.A., Wigmore S.J. Endogenous lipoproteins impact the response to endotoxin in humans // Crit. Care Med. — 30. — 23-31.
42. Van den Berghe G. et al. Intensive Insulin Therapy in Critically Ill Patients // NEJM. — 2001 Nov. 8. — V. 345, № 19. — 1359-1367.
43. Van den Berghe G. Intensive Insulin Therapy in the Medical ICU // NEJM. — 2006 Febr. 2. — V. 354, № 5. — 449-461.
44. Dobere E. et al. Insulin improves the efficiency of intradialytic parenteral nutrition (IDPN) // Cl. Nutr. Suppl. — 2007. — Vol. 2, Suppl. 2, 13 (O024).
45. Lim V.S. et al. Insulin Is Protein-Anabolic in Chronic Renal Failure Patients // J. Am. Soc. Nephrol. — 2003. — 14. — 2297-2304.
46. Woolfson M.J. Control of bllod glucose during nutritional support in ill patients // Intensive Care. — 1980. — 7. — 11.
47. Woolfson M.J. An improve method for blood glucose control during nutritional support // J. Parenter. Enteral. Nutr. — 1981. — 5. — 436.
48. Schricker Th. et al. Strategies to attenuate the catabolic response to surgery and improve perioperative outcomes // Can. J. Anesth. — 2007. — 54, 6. — Р. 414-419.
49. Devos P. et al. Effects of intensive insulin therapy in critically ill patients on long-term outcome variables: data from the glucontrol study // Cl. Nutr. Suppl. — 2007. — Vol. 2, Suppl. 2. — 93(Р175).
50. Zauner A.l. et al. Severity of insulin resistance in critically ill medical patients // Metabolism Clinical and Experimental. — 2007. — 56. — 1-5.
51. Donatelli F. et al. Epidural Anesthesia and Analgesia Decrease the Postoperative Incidence of Insulin Resistance in Preoperative Insulin-Resistant Subjects Only // Anesth. Analg. — 2007. — 104. — 1587-1593.
52. Uchida I. et al. Effect of epidural analgesia on postoperative insulin resistance as evaluated insulin clamp technique // Br. J. Surg. — 1988. — 75(6). — 557-562.
53. Руднов В.А. Клиническая значимость и возможные пути коррекции гипергликемии при критических состояниях // Cons. Med. — 2006. — Том 08, № 7. — 23.
54. Selberg O. et al. A pet scan analysis of skeletal muscle glucose metabolism in patients after liver transplantation // Cl. Nutr. Aug. — 2001. — Vol. 20, Suppl. 3. — Р. 5(26).
55. Felber J.P. et al. Glucose storage and oxidation in different degress of human obesity measured by continuous indirect calorimertry // Diabetologia. — 1981. — 2. — 39.
56. Greco A.V. et al. Insulin Resistance in Morbid Obesity: Reversal With Intramyocellular // Fat. Depletion. Diabetes. — 2002. — 51. — 144-151.
57. Kern Ph.A. et al. Adipose tissue tumor necrosis factor and interleukin-6 expression in human obesity and insulin resistance // Am. J. Physiol. Endocrinol. Metab. — 2001 May. — Vol. 280, Issue 5. — E745-E751.
58. Dupertuis Y.M. et al. Assessment of Ascorbic Acid Stability in Different Multilayered Parenteral Nutrition Bags: Critical Influence of the Bag Wall Material // JPEN. — 2005. — 29(2). — 125.
59. Dupertuis Y.M., Morch A. et al. Physical characteristics of total parenteral nutrition bags significantly affect the stability of vitamins C and B1: a controlled prospective study // JPEN. — 2002. — 26. — 310.
60. Ferreyra M.E. et al. Lipid Peroxidation in Total Parenteral Nutrition Bags // Nutr. in Cl. Pract. — 2008 April/May. — Vol. 23, № 2. — 240 (78-671).
61. Lerebours E. et al. Utilisation de ClinOlйic® en pathologie digestive // Nutr. Clin. Mйtabol. — 1996. — V. 10(4), Suppl. 1. — Р. 25S-27S.
62. Лейдерман И.Н. Современная концепция нутритивной поддержки при критических состояниях. 5 ключевых проблем. Клиническое питание. — С. 44.
63. Vary T.C. et al. Mechanisms regulating skeletal muscle glucose metabolism in sepsis // Shock. — 1995.