Журнал «Боль. Суставы. Позвоночник» 2 (02) 2011
Вернуться к номеру
Інструментальна візуалізація в ревматології Частина І. Радіоізотопна сцинтиграфія, термографія, позитронно-емісійна томографія, магнітно-резонансна томографія
Авторы: Коваленко В.М.1, Борткевич О.П.1, Проценко Г.О.1, Поворознюк В.В.2, Григор’єва Н.В.2, Дзерович Н.І.2, Шуба Н.М.3, Дубкова А.Г.3
1Національний науковий центр «Інститут кардіології ім. академіка М.Д. Стражеска» НАМН України, 2ДУ «Інститут геронтології НАМН України»
3Національна медична академія післядипломної освіти ім. П.Л. Шупика МОЗ України, м. Київ
Рубрики: Семейная медицина/Терапия, Ревматология, Травматология и ортопедия, Неврология
Версия для печати
Радіоізотопна сцинтиграфія (РС)
Радіоізотопна сцинтиграфія суглобів проводиться за допомогою остеотропних радіологічних фармацевтичних препаратів (пірофосфат, фосфон), мічених 99mTc. Зазначені препарати активно накопичуються в місцях активного кісткового й колагенового метаболізму, особливо інтенсивно — в збуджених тканинах суглобів, що відображається на сцинтиграмі суглобів.
Метод РС сьогодні використовується для ранньої діагностики артритів, виявлення субклінічних фаз ураження суглобів, диференційної діагностики запальних і дегенеративно-дистрофічних уражень суглобів при ревматичних захворюваннях суглобів (РЗС).
Для ранньої діагностики патологічних змін у суглобах, виявлення реактивного запалення може бути використана сцинтиграфія скелета з радіоактивним пірофосфатом технецію. Гіперфіксація з дифузійним розподілом радіонукліда відзначається за наявності реактивного синовіту. У гіповаскулярних ділянках епіфізів кісток на сцинтиграмах у зонах ішемії визначається зниження накопичення радіофармпрепарату, тоді як у місцях посиленого кровопостачання, що відповідає ділянкам перебудови кістки, накопичення його рівномірно підвищується.
При порівнянні даних РС із результатами внутрішньокісткової флебографії та виміру внутрішньокісткового тиску відзначено, що венозний стаз і підвищений тиск у кістково-мозковому каналі поєднуються з аномально високим поглинанням радіофармпрепарату, при цьому ступінь поглинання останнього прямо пропорційний стадії процесу. Наприклад, аналіз розподілу радіонукліду при коксартрозі виявив підвищене накопичення міченого з’єднання в зонах посиленого навантаження, в основ- ному в кістозних стінках та остеофітах, а також у зонах кісткоутворення.
Термографія (ТГ)
У широкому змісті слова ТГ є створеною різними способами графічною реєстрацією теплового поля об’єктів (поля їх інфрачервоного випромінювання). Термограмою називають фіксоване двовимірне зображення температурного поля частини або всього тіла обстежуваного.
ТГ є допоміжним діагностичним тестом, що повинен бути розшифрований у єдиному зв’язку з клінічними, лабораторними, анамнестичними даними, що отримані відповідно до діагностичного алгоритму. На думку Л.Г. Розенфельда й співавт. (1988), основними перевагами термографії є:
— Абсолютна нешкідливість. Організм людини не піддається ні опроміненню, ні ушкодженню. Можливе багаторазове дослідження у того самого суб’єкта.
— Висока швидкість дослідження. Залежно від типу термографа потрібно від 1/16 до 4 хв. Час, необхідний для врівноваження температури шкіри обстежуваного пацієнта й навколишнього повітря (орієнтовно 15 хв) можна істотно зменшити при відповідній організації кабінету термографії.
— Підвищена точність. Мінімальний градієнт температури, що реєструється між двома точками на відстані одного міліметра, становить 0,1 °С. Така точність дозволяє здійснити попередню топічну діагностику вогнища ураження.
— Можливість вибору послідовності нешкідливих дослідницьких процедур для вагітних жінок і дітей.
— Можливість одночасної оцінки функціонального стану великої кількості різних систем організму (при оглядовій термографії).
Важливими умовами коректного виконання термографії є грамотна організація кабінету, а також підготовка пацієнта до дослідження. У приміщеннях кабінету необхідно вжити заходи для стабілізації впливу факторів зовнішнього середовища на термодіагностичну апаратуру та пацієнта. З цією метою на двері й вікна навішують щільні світлозахисні штори. Можливі джерела інфрачервоного опромінення (батареї центрального опалення) екранують. Для підтримки стабільного мікроклімату ефективне використання кондиціонерів тощо. Рекомендується підтримувати в оглядовому приміщенні температуру 22 ± ± 1 °С, тому що при більш високій спостерігається зниження контрастності термограм, а при більш низькій — у пацієнтів розвивається вазоконстрикція, що різко знижує інформативність методу. Відносна вологість повітря у приміщеннях кабінету — 40–70 %, швидкість руху повітряних потоків не повинна перевищувати 0,15–0,2 м/с. Цим вимогам відповідає закрите приміщення, обладнане кондиціонером.
При РЗС варто дотримуватися таких загальних правил підготовки пацієнта до ТГ:
А. Верхні кінцівки:
— Руки повинні бути чистими, лак із нігтів зняти.
— За добу до ТГ-обстеження не застосовувати креми, не приймати фізіопроцедури, судинорозширюючі або судинозвужуючі фармпрепарати.
— При обстеженні верхні кінцівки звільняють від одягу й укладають на столик-підставку.
Б. Нижні кінцівки:
— Нижні кінцівки звільняють від будь-яких пов’язок, компресів та оголюють для адаптації шкіри до температури приміщення.
— За добу до обстеження не вживати лікарські речовини та не приймати фізіотерапевтичні процедури.
— Напередодні ввечері необхідно зробити ніжну ванну для зняття жирового покриву та відшаровувань епідермісу. Лак із нігтів зняти.
— Обстеження пацієнта проводять лежачи на спині чи в положенні стоячи.
Перед дослідженням повинен бути період температурної адаптації (у дорослого 10–15 хв). У зв’язку з тим, що температурні показники організму людини змінюються протягом доби кожні 3–4 години з коливаннями 0,2–0,4 °С, порівняльні (динамічні) дослідження рекомендується здійснювати в той самий час. Також необхідно враховувати, що максимальна температура в здорових людей спостерігається в період з 15-ї до 16-ї години дня.
Правильна інтерпретація термограм вимагає знання загальної фізіології, анатомії та спеціальних галузей медицини. У нормі в здорової людини існують зони гіпер- і гіпотермії, що обумовлено рядом причин. Поява зон гіпертермії може бути викликана:
— Підвищеним обміном речовин у даному органі або тканині в певний проміжок часу (наприклад, молочні залози в період лактації).
— «Порожнинним ефектом» (ділянки орбіт, пупка, міжсідничних складок, піхвова та пахвова ділянки, міжпальцьові проміжки, медіальні поверхні зведених разом нижніх або верхніх кінцівок, які щільно притиснуті до тіла).
Деякі топографічні особливості нормальних термограм
Спина та хребет на термограмах представлені гомогенною термотопографією за наявності незначної гіпертермії в серединній ділянці поперекової ділянки. Іноді спостерігається помірна гіпертермія міжлопаткового простору.
На термограмі спини можна виділити 4 постійні зони гіпертермії:
— у проекції остистих відростків, починаючи з рівня середньогрудного відділу хребта; ширина першої зони трохи більша в нижньогрудному й верхньопоперековому відділах порівняно з нижньопоперековим;
— у проекції міжсідничної складки;
— дві симетричні зони в проекції крижово-клубових зчленувань (латеральніше та трохи вище міжсідничної складки);
— у проекції нирок (симетрично розташовані ділянки гіпертермії нерівномірної інтенсивності).
Виникнення крижового чи попереково-крижового корінцевого синдрому призводить до зниження температури шкіри нижньої кінцівки в зоні іннервації даного корінця на 0,7–0,9 °С з одночасною легкою гіпертермією сегмента на рівні відповідних сегментів симпатичного стовбура. Новокаїнова блокада ураженого корінця нормалізує температуру поверхні відповідного дерматому кінцівки та знижує температуру сегмента в попереково-крижовій ділянці на 0,2–0,3 °С. Через 10–12 хв після завершення новокаїнової або тримекаїнової блокади поперекових симпатичних вузлів підвищується температура шкіри ступні й гомілки відповідної сторони на 0,7–0,9 °С, що зберігається протягом 2–3 хв. Середня температура шкіри в ділянці спини й хребта — 33,5–34,2 °С (Розенфельд Л.Г., 1988).
Верхні кінцівки. Термографічне зображення обох верхніх кінцівок характеризується симетричністю, хоча за даними Г.М. Фролова й співавт. (1979), відзначається незначна термоасиметрія верхніх кінцівок, пов’язана з переважним розвитком правої або лівої кінцівки або різницею артеріального тиску в них.
Зони гіпертермії на термограмах верхніх кінцівок у нормі визначаються в проекції проходження судинних пучків — внутрішня поверхня плеча, ліктьового суглоба, передпліччя, пахвова ділянка. Відносною гіпотермією характеризуються зовнішня поверхня плеча й передпліччя, пальці (порівняно з долонями). У ділянці І пальця кисті, міжпальцьових проміжків, за ходом великих вен на тильній стороні кисті відзначається помірна гіпертермія (Лихтерман Л.Б., 1983). Середня температура шкіри в ділянці верхніх кінцівок (крім пальців) — 31,2–32,6 °С, пальців кистей — 27,2–28,6 °С (Розенфельд Л.Г., 1988).
Нижні кінцівки. Термографічне зображення обох нижніх кінцівок також є симетричним. У верхній і середній третинах гомілок визначаються зони вираженої гіпертермії, тоді як у ділянці колінного суглоба, нижньої третини гомілки й ступні мають місце ділянки гіпотермії.
На термограмах тильної поверхні ступні реєструється гетерогенна картина з тенденцією до зменшення гіпертермії зверху вниз — в ділянці пальців визначається зона гіпотермії. На підошовній поверхні ступні інтенсивність гіпертермії більше виражена вздовж медіального краю, особливо в проекції склепіння ступні. По латеральному краю та в ділянці пальців реєструються зони гіпотермії.
На задній поверхні стегон визначається зона вираженої гіпотермії в проекції сідниць і зона гіпертермії у верхній третині стегон, підколінній ямці, верхній третині гомілок. Для гомілок характерна тенденція до зменшення інтенсивності гіпертермії в дистальному напрямку. Над ахіловим сухожиллям визначається зона гіпотермії. Середнє значення температури шкірного покриву в ділянці нижніх кінцівок (крім пальців ступні) — 32,1–32,4 °С, пальців ступні — 23,3–23,9 °С (Розенфельд Л.Г., 1988).
Аналіз і обробка термограм проводиться за такими термографічними ознаками (Розенфельд Л.Г., 1988):
— виявлення термоасиметрії;
— вивчення площі асиметричної ділянки (зони гіпо- або гіпертермії): розміри, ступінь однорідності, характеристика границь тощо;
— визначення температурного градієнта та обчислення його коефіцієнта, що виражає відношення різниці температури між точками й відстані між ними;
— визначення максимальної, мінімальної й середньої абсолютної температури симетричних ділянок;
— визначення термографічного індексу (ТІ), що являє собою відношення суми температур, що відповідають кожному ізотермічному полю, до загальної площі зони патологічної термоасиметрії:
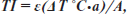
де ε — сума температур, що відповідають кожному ізотермічному полю; ΔТ — різниця між температурою кожного температурного градієнта й стандартом, що відповідає середній температурі даної ділянки поверхні тіла людини; а — виявлена температура кожного градієнта; А — загальна площа зони патологічної термоасиметрії.
У нормі термографічний індекс знаходиться в межах від 4,62 до 4,94 і становить у середньому 4,87 (Collins A. et al., 1974).
За даними Н.К. Тернового та співавт. (1988), при остеоартрозі (ОА) І рентгенологічної стадії за Н.С. Косинською спостерігаються термоасиметрія суглобів, зона гіпотермії над ділянкою суглоба, що поступово переходить у зону гіпертермії вище й нижче розташованих сегментів кінцівки. Градієнт температур у зоні гіпотермії становить 0,6 ± 0,2 °С.
На термограмах хворих ОА ІІ–ІІІ стадій спостерігаються термоасиметрія, зона гіпертермії над ураженим суглобом різного рельєфу та ступеня вираженості, що вказує на гіперваскуляризацію суглоба й асептичне запалення в його синовіальній оболонці (СО) та параартикулярній клітковині. Градієнт температур патологічно зміненого суглоба становить 1,0 ± 0,2 °С.
У випадку ефективного лікування термограма характеризується зменшенням температурної асиметрії, зниженням інтенсивності гіпертермії, градієнт температур знижується до 0,4–0,8 °С.
Позитронно-емісійна томографія (ПЕТ)
Позитронно-емісійна томографія — новітній метод радіоізотопної діагностики.
Головна перевага ПЕТ — можливість не тільки одержувати зображення внутрішніх органів, але й оцінювати їх функцію та метаболізм, таким чином, за допомогою ПЕТ вдається діагностувати хворобу на самому ранньому етапі, ще до прояву клінічних симптомів.
Радіоактивна речовина вводиться внутрішньовенно або інгалюється у вигляді газу до початку ПЕТ. Потім протягом 30–90 хв пацієнта просять спокійно лежати й не розмовляти, тому що фізична активність може вплинути на поширення речовини в організмі. Після потрібного розподілу радіоактивної речовини починають сканування, яке може тривати 30–45 хвилин. Іноді при дослідженні серця під час ПЕТ пацієнту дають дозоване фізичне навантаження для оцінки кровопостачання й функціонування серця.
Після закінчення ПЕТ рекомендується пити багато рідини, щоб швидше вивести радіоактивну речовину з організму.
Мінімум за 4 години до ПЕТ варто утримуватися від прийому їжі. Пацієнтам з діабетом даються додаткові інструкції, оскільки рівень глюкози в крові впливає на результати ПЕТ.
Доза радіаційного опромінення при ПЕТ досить мала — близько 7 мЗв (при комп’ютерній томографії (КТ) вона становить приблизно 8 мЗв). Період напіврозпаду радіоактивних речовин, що використовуються, дуже малий (від 10 хв до 2 год), тому всі вони швидко виводяться з організму. ПЕТ протипоказана вагітним.
Магнітно-резонансна томографія (МРТ)
МРТ за останні роки стала одним із провідних методів неінвазивної діагностики. З 70-х років, коли принципи магнітного резонансу (МР) уперше стали використовуватися для дослідження людського тіла, до сьогодні цей метод медичної візуалізації невпізнанно змінився й продовжує швидко розвиватися. Удосконалюються технічне оснащення, програмне забезпечення, розвиваються методики одержання зображень, розробляються МР-контрастні препарати. Це дозволяє постійно знаходити нові сфери застосування МРТ. Якщо спочатку її застосування обмежувалося лише дослідженнями центральної нервової системи, то зараз МРТ із успіхом застосовується практично в усіх галузях медицини, в тому числі для дослідження опорно-рухового апарату.
Процес переходу електронів ядра зі збудженого стану в рівноважне називається спін-решітковим релаксаційним процесом або поздовжньою релаксацією. Він характеризується Т1 — спін-решітковим часом релаксації, необхідним для переходу 63 % ядер у стан рівноваги після їх порушення 90° імпульсом. Виділяють також Т2 — спін-спіновий час релаксації.
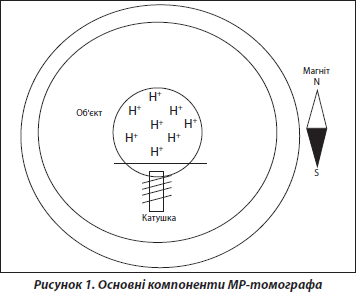
Існує ряд способів одержання МР-томограм, що відрізняються порядком і характером генерації радіочастотних імпульсів, методами аналізу МР-сигналів. Найбільше поширення мають два способи: спін-решітковий та спін-еховий. При спін-решітковому аналізують переважно час релаксації T1. Різні тканини (сіра й біла речовина головного мозку, спинномозкова рідина, пухлинна тканина, хрящ, м’язи тощо) мають у своєму складі протони з різним часом релаксації T1. Із тривалістю T1 пов’язана інтенсивність МР-сигналу: чим коротше T1, тим інтенсивніше МР-сигнал і тим світліше виглядає дане місце зображення на телемоніторі. Жирова тканина на МР-томограмах — біла, слідом за нею за інтенсивністю МР-сигналу в порядку зменшення йдуть головний і спинний мозок, щільні внутрішні органи, судинні стінки та м’язи. Повітря, кістки й кальцифікати практично не дають МР-сигналу й тому відображаються чорним кольором. Зазначені взаємини часу релаксації T1 створюють передумови для візуалізації нормальних і змінених тканин на МР-томограмах.
При іншому способі МР-томографії, що має назву спін-ехового, на пацієнта направляють серію радіочастотних імпульсів, що повертають прецесуючі протони на 90°. Слідом за припиненням подачі імпульсів реєструють відповідні МР-сигнали. Проте інтенсивність відповідного сигналу по-іншому пов’язана з тривалістю Т2: чим коротший Т2, тим слабший сигнал і, отже, нижча яскравість світіння екрану телемонітору. Таким чином, підсумкова картина МРТ за способом Т2 протилежна МРТ за T1 (як негатив позитиву).
На МР-томограмах краще, ніж на комп’ютерних томограмах, відображаються м’які тканини: м’язи, жирові прошарки, хрящі, судини. На деяких апаратах можна одержати зображення судин, не вводячи в них контрастний засіб (МР-ангіографія). Внаслідок невеликого вмісту води в кістковій тканині остання не створює ефекту, що екранує, як при рентгенівській комп’ютерній томографії, тобто не заважає зображенню, наприклад, спинного мозку, міжхребцевих дисків тощо. Звичайно, ядра водню утримуються не тільки у воді, але і в кістковій тканині фіксовані в дуже великих молекулах і щільних структурах і не є перешкодою для МР-томографії.
Переваги й недоліки методу
Основні переваги МРТ: неінвазивність, нешкідливість (відсутність променевого навантаження), тривимірний характер одержання зображень, природний контраст від крові, що рухається, відсутність артефактів від кісткової тканини, висока диференціація м’яких тканин, можливість виконання МР-спектроскопії для прижиттєвого вивчення метаболізму тканин in vivo. МРТ дозволяє отримувати зображення тонких шарів тіла людини в будь-якому перетині — у фронтальній, сагітальній, аксіальній і косій площинах. Можна реконструювати об’ємні зображення органів, синхронізувати одержані томограми із зубцями електрокардіограми.
До основних недоліків звичайно зараховують досить великий час, необхідний для отримання зображень (звичайно хвилини), що призводить до появи артефактів від дихальних рухів (що особливо знижує ефективність дослідження легень), аритмій (при дослідженні серця); неможливість надійного виявлення кальцифікатів, деяких видів патології кісткових структур; досить високу вартість устаткування та його експлуатації; спеціальні вимоги до приміщень, у яких перебувають прилади (екранування від перешкод); неможливість обстеження хворих із клаустрофобією, штучними водіями ритму, великими металевими імплантатами з немедичних металів.
Протипоказання до проведення МРТ (табл. 1)
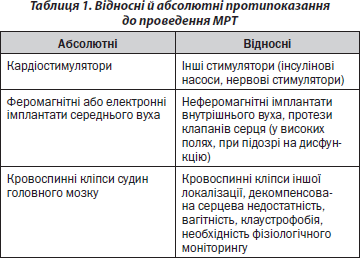
До абсолютних протипоказань зараховують стани пацієнтів, при яких проведення дослідження створює загрозу для їхнього життя. Наприклад, наявність імплантатів, які активуються електронним, магнітним або механічним шляхами, — у першу чергу штучних водіїв ритму. Вплив радіочастотного випромінювання МР-томографа може порушити функціонування стимулятора, що працює в системі запиту, тому що зміни магнітних полів можуть імітувати серцеву діяльність. Магнітне притягання може викликати також зсув стимулятора в гнізді та зрушити електроди. Крім того, магнітне поле створює перешкоди для роботи феромагнітних або електронних імплантатів середнього вуха. Наявність штучних клапанів серця також становить небезпеку і є абсолютним протипоказанням тільки при дослідженні на МР-томографах із високими полями, а також якщо клінічно запідозрено ушкодження клапана. До абсолютних протипоказань до дослідження зараховують також наявність невеликих металевих хірургічних імплантатів (гемостатичні кліпси) у центральній нервовій системі, тому що зсув їх унаслідок магнітного притягання загрожує кровотечею. Крім потенційної небезпеки, наявність металевих імплантатів з магнітними властивостями викликає артефакти, що ускладнюють інтерпретацію результатів дослідження.
Відносними протипоказаннями, крім перерахованих вище, є також декомпенсована серцева недостатність, необхідність фізіологічного моніторингу (механічна вентиляція легень, електричні інфузійні насоси). Клаустрофобія є перешкодою для проведення дослідження в 1–4 % випадків. Перебороти її можна, з одного боку, використанням приладів із відкритими магнітами, з іншого боку — докладним поясненням пристрою апаратури та процедури обстеження. Що стосується обстеження вагітних жінок, свідчень негативної дії МРТ на ембріон або плід не отримано, проте рекомендується уникати МРТ у перші 3 міс. вагітності. Застосування МРТ при вагітності показано у випадках, коли інші неіонізуючі методи візуалізації не дають задовільної інформації. МРТ-дослідження вимагає більшої участі в ньому хворого, ніж КТ, оскільки рухи хворого під час дослідження сильніше впливають на якість зображень, тому дослідження хворих із гострою патологією, порушенням свідомості, спастичними станами, деменцією та дітей нерідко є складним.
Різниця сигналів від різних тканин, тобто контрастність MР-зображення може бути істотно поліпшена МР-контрастними агентами (МР-КА). Суть їх застосування полягає у зміні магнітних параметрів протонів тканин/органів, тобто зміні часу релаксації Т1 і Т2 протонів.
На сьогодні існує кілька класифікацій МР-контрастних агентів. За переважним впливом на час релаксації МР-КА поділяють на Т1-КА (укорочують Т1, збільшують інтенсивність МР-сигналу тканин — позитивні) і Т2-КА (укорочують Т2, зменшують інтенсивність МР-сигналу — негативні). Залежно від магнітних властивостей МР-КА розподіляють на парамагнітні та суперпарамагнітні.
Парамагнітні КА. Парамагнітні властивості мають атоми з одним або декількома неспареними електронами — магнітні іони гадолінію (Gd), хрому, нікелю, заліза, марганця. Найбільш широке клінічне застосування одержали сполучення гадолінію. Парамагнетики зараз найбільш широко використовуються в ревматологічній практиці.
Суперпарамагнітні КА. Суперпарамагнітний оксид заліза, феромагнітні КА, до складу яких входять феромагнітні оксиди заліза, структурно подібні до ферриту магнетиту (Fe2 + OFe23 + O3).
Ще одна класифікація заснована на фармакокінетиці КА (Сергєєв П.В. та ін., 1995): позаклітинні (тканинонеспецифічні); шлунково-кишкові; органотропні (тканиноспецифічні); макромолекулярні (використовують для визначення отвору судин).
В Україні відомі чотири МР-КА — позаклітинні водорозчинні парамагнітні КА (табл. 2), з них широко використовуються Омніскан і Магневіст. Позаклітинні КА вводять внутрішньовенно, на 98 % виділяються нирками, не проникають через гематоенцефалічний бар’єр, мають низьку токсичність і належать до групи парамагнетиків.
МРТ суглобового хряща
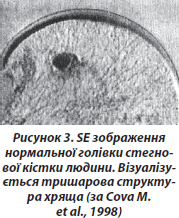
МР-картина суглобового хряща (СХ) відтворює сукупність його гістологічної будови й біохімічного складу. СХ є гіаліновим, не має власного кровопостачання, лімфатичного дренажу й іннервації. СХ складається з води й іонів, волокон колагену ІІ типу, хондроцитів, агрегованих протеогліканів й інших глікопротеїнів.
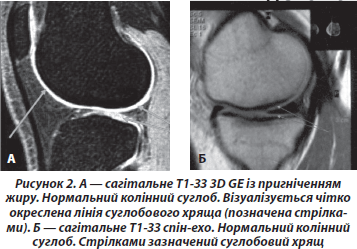
На сьогодні МРТ та УЗД — основні способи візуалізації гіалінового СХ. МРТ здійснюється в основному з використанням градієнт-ехопослідовностей та характеризує вміст води в СХ. Вміст і розподіл гідрофільних молекул протеогліканів та анізотропна організація колагенових фібрил впливає не тільки на сумарну кількість води (протонну щільність у СХ), але й на стан релаксаційних властивостей, тобто Т2 цієї води, даючи хрящу характерні «зональні» або «розшаровуючі» зображення на МРТ, що відповідають гістологічним шарам СХ.
На дуже коротких Т-зображеннях (< 5 мс) СХ у типовому випадку має двошаровий вигляд: глибокий шар — розташований ближче до кістки — має низький сигнал, оскільки присутність кальцію значно скорочує ТR і не дає зображення; поверхневий шар — дає середньоінтенсивний/високоінтенсивний МР-сигнал.
На проміжних Т-зображеннях (5–40 мс) СХ має тришаровий вигляд: поверхневий шар з низьким сигналом, перехідний шар і глибокий шар, що має низький МР-сигнал. При Т2-зважуванні сигнал не включає проміжний шар, інтенсивність зображення СХ є гомогенно низькою.
МРТ кісток та кісткового мозку
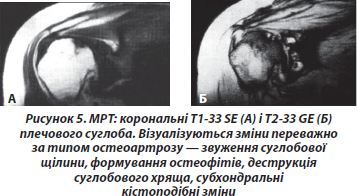
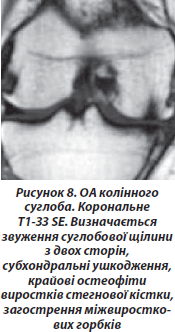
Корковий шар і трабекули кісткової тканини містять мало протонів водню й багато кальцію, що сильно скорочує TR і тому не дає певного МР-сигналу. На МР-томограмах вони мають зображення кривих ліній з відсутністю сигналу (темних смуг), окреслюють середньоінтенсивні та високоінтенсивні тканини (кістковий мозок, жирову тканину тощо). Завдяки багатоплощинним томографічним можливостям МРТ є більш чутливою, ніж рентгенографія або КТ, для візуалізації більшості змін цих структур. Остеофіти, особливо центральні, характерні для ОА, краще візуалізуються МРТ, ніж звичайною рентгенографією. Кістковий склероз також добре виявляється при МРТ і має низьку інтенсивність сигналу в усіх імпульсних послідовностях, що обумовлено кальцифікацією та фіброзом. При МРТ також можна виявити запалення ентезисів і періостит. Цей метод може використовуватися також для вивчення трабекулярної мікроархітектоніки кісток, що актуально для моніторингу трабекулярних змін субхондральної кістки при розвитку й прогресуванні РЗС, у тому числі ревматоїдний артрит (РА), остеоартроз (ОА), анкілозуючий спондиліт (АС) тощо.
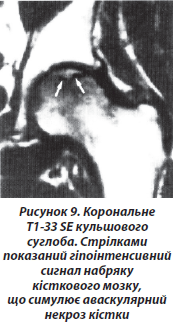
МРТ є унікальною методикою для одержання зображення кісткового мозку та звичайно дуже чутливою, хоча не дуже специфічною для діагностики остеонекрозу, остеомієліту, первинної інфільтрації та травм, особливо кісткової контузії й переломів без зміщення. Ознаки цих захворювань на рентгенограмах не виявляються до тих пір, поки кортикальний і/або трабекулярний відділи кістки не будуть уражені. У кожному з перерахованих випадків збільшується вміст вільної води, що має вигляд сигналу низької інтенсивності на Т1-ЗЗ й сигналу високої інтенсивності на Т2-ЗЗ, які показують високий контраст із нормальним кістковим жиром, що має сигнал високої інтенсивності на Т1-ЗЗ та низький сигнал на Т2-ЗЗ. Винятком є Т2-ЗЗ FSE (швидкий спін-ехо), на якому зображення жиру й води мають сигнал високої інтенсивності. Послідовності градієнт-ехо, принаймні, з великою силою поля є в основному не чутливими до патології кісткового мозку, тому що магнітні ефекти гасить кісткова тканина. Ділянки набряку субхондрального кісткового мозку часто виявляють у суглобах хворих з прогресуючим АС та ОА. Звичайно ці ділянки локального набряку кісткового мозку локалізуються в місцях запального процесу (наприклад, крижово-клубові зчленування при АС) або втрати суглобового хряща/хондромаляції при ОА. Іноді епіфізарний набряк кісткового мозку видно на деякій відстані від суглобової поверхні або ентезису. Залишається невідомим, яка величина й поширеність цих кістково-мозкових змін сприяє виникненню локального болю й нестабільності суглоба, а також коли вони є предикторами прогресування РЗС.
МРТ синовіальної оболонки й синовіальної рідини (СР)
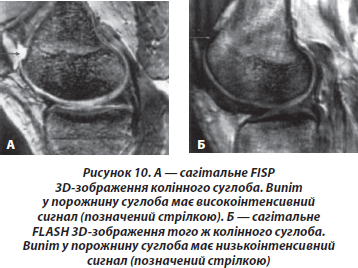
Нормальна СО є занадто тонкою для візуалізації при звичайних послідовностях МРТ, її складно відрізнити від поруч розташованої СР або СХ. У нормі в суглобах утримується невелика кількість СР, об’єм якої в різних суглобах варіює. У гомілковоступневому суглобі, наприклад, може утримуватися відносно велика кількість СР в нормі. Усе ще невідомо, яку ж кількість СР варто розцінювати як патологічну. За допомогою 3D-реконструкції при МРТ можливий підрахунок об’єму вільної СР в суглобах. Для моніторингу відповіді на лікування в пацієнтів з РЗС або вивчення нормального фізіологічного функціонування СР в суглобі in vivo ця методика може бути дуже корисною. МР-сигнал негеморагічної СР має низьку інтенсивність на Т1-ЗЗ і високу на Т2-ЗЗ завдяки наявності вільної рідини. Геморагічна СР може містити метгемоглобін, що має короткий Т1 і дає високоінтенсивний сигнал на Т1-ЗЗ, і/або дезоксигемоглобін, що має вигляд низькоінтенсивного сигналу на Т2-ЗЗ. При хронічному рецидивуючому гемартрозі в СО відкладається гемосидерин, що дає низькоінтенсивний сигнал на Т1-ЗЗ і Т2-ЗЗ. Геморагії часто розвиваються в підколінних кістах (розташовуються переважно в м’яких тканинах задньої поверхні гомілки). Витікання СР з ушкодженої кісти Бейкера може нагадувати форму пера при посиленні КА, що містить гадоліній. При внутрішньовенному введенні КА він локалізується уздовж поверхні фасції між м’язами позаду від суглобової капсули колінного суглоба.
 Збуджена, набрякла СО звичайно має повільний Т2, характеризуючи високий вміст інтерстиціальної рідини (МР-сигнал високої інтенсивності на Т2-ЗЗ). На Т1-ЗЗ стовщення СО має низько- або середньоінтенсивний МР-сигнал, проте стовщену СО складно відрізнити від прилеглих м’яких тканин, наприклад, СО чи СХ. Відкладення гемосидерину або хронічний фіброз можуть знижувати інтенсивність сигналу гіперплазованої СО на Т2-ЗЗ, а іноді навіть на Т1-ЗЗ, що зважені за щільністю протонів, у всіх градієнт-ехопослідовностях.
Збуджена, набрякла СО звичайно має повільний Т2, характеризуючи високий вміст інтерстиціальної рідини (МР-сигнал високої інтенсивності на Т2-ЗЗ). На Т1-ЗЗ стовщення СО має низько- або середньоінтенсивний МР-сигнал, проте стовщену СО складно відрізнити від прилеглих м’яких тканин, наприклад, СО чи СХ. Відкладення гемосидерину або хронічний фіброз можуть знижувати інтенсивність сигналу гіперплазованої СО на Т2-ЗЗ, а іноді навіть на Т1-ЗЗ, що зважені за щільністю протонів, у всіх градієнт-ехопослідовностях.
При внутрішньовенному введенні КА швидко розподіляється по гіпервaскуляризованих тканинах, наприклад СО. Хелатний комплекс гадолінію має відносно малі молекули, що швидко дифундують усередину навіть через нормальні капіляри та, як недолік, із часом у СР. Безпосередньо після болюсного в/в введення КА СО може візуалізовуватися окремо від інших структур. Контрастне відображення СО та жирової тканини може бути посилене методикою пригнічення жиру. Швидкість, з якою відбувається контрастне посилення СО, залежить від багатьох факторів: швидкості крові в СО, об’єму гіперплазованої синовіальної тканини та свідчить про активність процесу при РЗС. Крім того, визначення кількості й розподілу збудженої СО та СР в суглобах при РЗС надає можливість встановлення ступеня вираженості синовіту шляхом моніторингу швидкості синовіального посилення з Gd-утримуючим КА в період спостереження за хворим. Висока швидкість синовіального посилення та швидке досягнення піка посилення при болюсному введенні КА свідчить про активне запалення або гіперплазію, у той час як повільне посилення відповідає хронічному фіброзу СО. Хоча складно контролювати тонкі відмінності у фармакокінетиці Gd-утримуючого КА при МР-дослідженнях у різні періоди хвороби в одного й того ж хворого, швидкість і пік синовіального посилення можуть служити критеріями для призначення або скасування відповідної протизапальної терапії, у тому числі з використанням базисних чинників. Високі показники цих параметрів є ознаками гістологічно активного синовіту.
МРТ інших компонентів суглоба
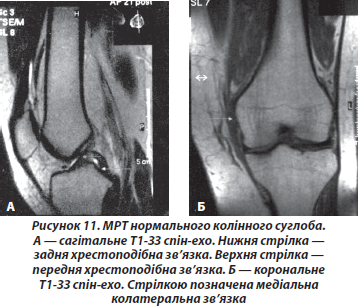
Допоміжний апарат суглоба, тобто зв’язки, меніски, сухожилки та суглобова губа є важливими для підтримки статичної та динамічної стабільності, розподілі механічного навантаження й функціональної цілісності суглобів. Втрата цих функцій підвищує біомеханічне зношування і є причиною ушкодження суглоба. Неушкоджені зв’язки мають вигляд темних смуг, переривання їх є прямою ознакою їх розриву. Проте необхідно враховувати, що імітація розриву зв’язкового апарата може візуалізуватись при одержанні косої площини зрізу через інтактну зв’язку, тому для отримання зображення деяких зв’язок може бути необхідний вибір спеціальної площини. Наприклад, передня хресто- подібна зв’язка колінного суглоба найкраще видна на косих сагітальних зображеннях колінного суглоба в нейтральній позиції чи прямих сагітальних зображеннях із невеликим відведенням гомілки.
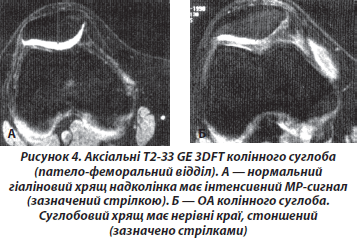
Меніски складаються з фіброзного хряща й містять велику кількість колагенових волокон, просторово розташованих так, щоб протистояти силі натягу при впливі вагових навантажень. Волокна орієнтовані переважно циркулярно, особливо в периферичній частині меніска, що пояснює схильність до поздовжніх розривів. Коли відбувається локальна втрата колагена, наприклад, при міксоїдній або еозинофільній дегенерації, що звичайно теж супроводжується локальним збільшенням вмісту води, зменшується ефект укорочення Т2, а сигнал від води не маскується й проявляється у вигляді округлої або лінійної ділянки з середньоінтенсивним сигналом усередині меніска на коротких Т-зображеннях (Т1-зважених за протонною щільністю спін-ехо або градієнт-ехо) і має схильність поступово зникати при довгому Т1. Ці патологічні сигнали не є розривами на відміну від порушення цілісності меніска, розрив меніска може бути пов’язаний із грубою деформацією поверхні меніска. Іноді велика кількість суглобової рідини окреслює контур розриву меніска, причому він візуалізується на Т2-ЗЗ. Таким чином, короткі Т-зображення є високочутливими (> 90 %), але часто неспецифічними для розривів меніска, тоді як довгі Т-зображення є нечутливими, хоча високоспецифічними.


МРТ є чутливим методом оцінки всього спектра патології сухожилків і виявляє тендиніти та розриви сухожилків у більшості випадків із більшою точністю, ніж клінічне обстеження, і майже не поступається УЗД. Нормальні сухожилки мають рівні краї та гомогенний сигнал низької інтенсивності при Т2-ЗЗ. Розрив сухожилка може бути частковим або повним, зображується різними ступенями переривання сухожилля (високоінтенсивним сигналом усередині сухожилля на Т2-ЗЗ). При теносиновіті рідина може бути видна під оболонкою сухожилка, але саме сухожилля має звичайний вигляд. Тендиніт звичайно є результатом потовщення й нерівності сухожилля, але більш надійний симптом — збільшення інтенсивності сигналу всередині сухожилка на Т2-ЗЗ. Розрив сухожилля при РЗС може бути результатом механічного зношування, що виникає через тертя об зазубрені остеофіти й гострі краї ерозій або первинного запалення в самому сухожиллі. Відрив сухожилля від місця прикріплення може бути гострим чи виникати внаслідок постійної мікротравматизації/запалення. Частіше розриваються сухожилля екстензорів зап’ястя або кисті, ротаторної манжети плеча, сухожилля заднього великогомілкового м’яза в гомілковостопному суглобі. Тендиніт і розрив ротаторної манжети плеча й сухожилля довгої голівки біцепса в більшості випадків проявляється болем і нестабільністю в плечовому суглобі. Повний розрив ротаторної манжети плеча — результат переднього підвивиху голівки плечової кістки й часто є супутнім при РЗС.
М’язи містять менше колагену, тому мають сигнал середньої інтенсивності на Т1-ЗЗ і Т2-ЗЗ. Запалення м’язів іноді видно поряд із запальним артритом, воно має сигнал високої інтенсивності на Т2-ЗЗ, тому що в обох випадках з інтерстиціальним набряком підвищується вміст води, а подовження Т2 пов’язане із втратою колагену. І навпаки, фіброз, як наслідок запалення, веде до зниження інтенсивності сигналу на Т2-ЗЗ, у той час як мармурова жирова атрофія м’язів має високоінтенсивний сигнал жиру на Т1-ЗЗ.
На основі отриманих даних групою OMERACT 2002 RAMRIS (Outcome Measures in Rheumatology Clinical Trials RA MRI scoring system) запропоновані стандартні протоколи дослідження хворих на РА за допомогою МРТ.
Зразки протоколів та рекомендації групи OMERACT 2002 RAMRIS для оцінки ураження суглобів кистей при РА за допомогою MPT (EULAR, 2005)
Зразки протоколів, які можуть бути застосовані для оцінки п’ястковофалангових (А) та зап’ястних (Б) суглобів за допомогою OMERACT 2002 RAMRIS (Outcome Measures in Rheumatology Clinical Trials RA MRI scoring system).
Протокол OMERACT RAMRIS (із застосуванням атласу MPT для PA, EULAR-OMERACT)
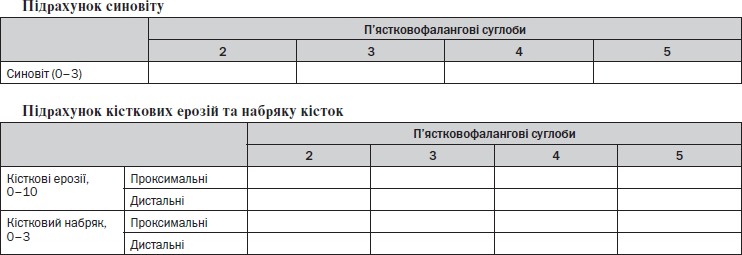
(А) П’ястковофалангові суглоби
Ідентифікаційні дані пацієнта__________________________
Центр, де проводилося дослідження_____________________
Прилад, за допомогою якого проведена МРТ______________
Послідовності, що оцінені_____________________________
______________Лікар
— Кісткові ерозії підраховують від 0 до 10 відповідно до частки залученої кістки (за приростом на 10 %): 0: 0 %, 1: 1–10 %, 2: 11–20 % ... 10: 91–100 %.
— Кістковий набряк підраховують від 0 до 3 відповідно до частки залученої кістки (за приростом на 33 %): 0: 0 %, 1: 1–33 %, 2: 34–66 %, 3: 67–100 %.
— Підрахунок здійснюють від хрящової поверхні (за відсутності її — від місця кращої візуалізації) на глибину 1 см.
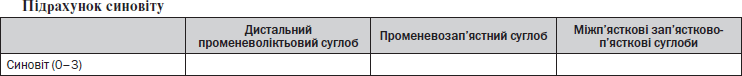
(Б) Зап’ясткові суглоби
Ідентифікаційні дані пацієнта__________________________
Центр, де проводилося дослідження_____________________
Прилад, за допомогою якого проведена МРТ______________
Послідовності, що оцінені_____________________________
______________Лікар
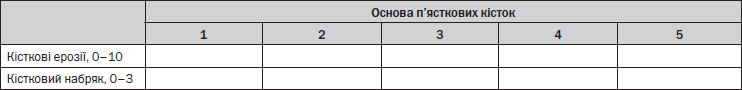
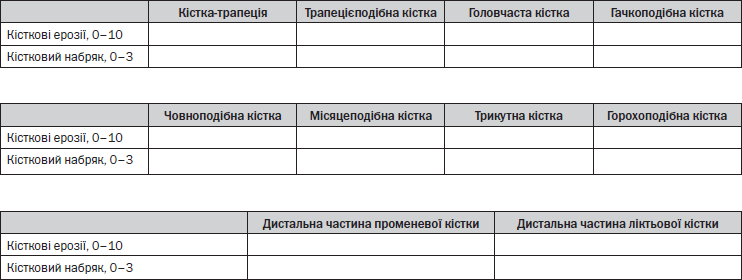
Підрахунок кісткових ерозій та набряку кісток
— Кісткові ерозії підраховують від 0 до 10 відповідно до частки залученої кістки (за приростом на 10 %): 0: 0 %, 1: 1–10 %, 2: 11–20 % ... 10: 91–100 %.
— Кістковий набряк підраховують від 0 до 3 відповідно до частки залученої кістки (за приростом на 33 %): 0: 0 %, 1: 1–33 %, 2: 34–66 %, 3: 67–100 %.
— Для зап’ястних кісток підрахунок здійснюють по всій кістці. Для довгих кісток підраховують від хрящової поверхні (а за її відсутності — від місця кращої візуалізації) на глибину 1 см.
Рекомендації групи OMERACT з РА щодо базисних МРТ-послідовностей, визначень можливих патологічних МРТ-змін суглобів у разі РА та їх підрахунку (OMERACT 2002 RAMRIS)
A. Базисні МРТ-послідовності
Передбачається, що наступні МРТ-дослідження, метою яких буде оцінка запальних та деструктивних змін при РА, будуть включати принаймні:
1) візуалізацію у двох площинах Т1-зважених зображень1 до та після в/в введення контрасту гадолінію2; 2) Т2-зважену послідовність чи, в разі неможливості її отримання, STIR-послідовність.
Б. Визначення важливих патологічних МРТ-змін суглобів
— Синовіт: ділянка синовіальної оболонки, товщина якої збільшується3 після введення гадолінію порівняно з нормальною синовією.
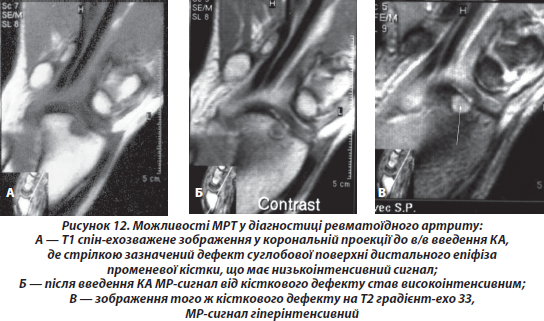
— МРТ-кісткова ерозія: кісткове ушкодження з гострими краями, з чіткою юкста-артикулярною локалізацією та типовими характеристиками сигналу4, що візуалізується в двох площинах з обривом кортикального шару, що видно принаймні в одній площині5.
— МРТ-кістковий набряк: ушкодження6 у трабекулярній кістці з нечітко визначеними краями та характеристиками сигналу, які відповідають підвищеному вмісту води7.
B. Підрахункова система (OMERACT 2002 RAMRIS).
— Синовіт оцінюють у трьох локусах зап’ястка (дистальний променеволіктьовий суглоб, променево- зап’ястний суглоб, міжп’ясткові та зап’ястково- п’ясткові суглоби) та в кожному п’ястково- фаланговому суглобі. Не оцінюють І зап’ястково-п’ястковий та І п’ястковофаланговий суглоби. Шкала 0–3 бали: 0 — норма; 1–3 — синовіт (слабкий, помірний, виражений) — за 1/3 припущеного максимального об’єму потовщеної синовіальної оболонки.
— Кісткові ерозії: оцінюють окремо кожну кістку (зап’ясток — зап’ясткові кістки, дистальний відділ променевої та дистальний відділ ліктьової кістки, основи п’ясткових кісток; п’ястковофалангові суглоби — головки п’ясткових кісток та основи фаланг). Шкала 0–10 балів, градуйована за часткою ерозованої кістки в «оціненому обсязі кістки» на всіх доступних зображеннях: 0 — ерозій немає; 1 — 1–10 % кістки ерозовані; 2 — 11–20 % і т.д. Для довгої кістки «оцінений обсяг кістки» — від хрящової поверхні (за її відсутності — від місця кращої візуалізації) на глибину 1 см. Щодо зап’ясткової кістки, то оцінюють її всю.
— Кістковий набряк підраховують для кожної кістки окремо (як для ерозій). Шкала 0–3, градуйована за часткою кістки з набряком, наприклад: 0 — набряку немає; 1 — набряклі 1–33 % кістки; 2 — 34–66 %; 3 — 67–100 %.
Таким чином, МРТ є високоефективним діагностичним, неінвазивним методом, що відображає всі складові частини суглоба одночасно та сприяє вивченню структурних і функціональних параметрів при захворюваннях суглобів.
МРТ може виявляти дуже ранні зміни, пов’язані з дегенерацією СХ, коли клінічні симптоми РЗС мінімальні або відсутні. Раннє виявлення пацієнтів, у яких є ризик прогресування захворювання, виявлений при МРТ, дозволяє призначити відповідне лікування набагато раніше, ніж їх виявлення при інших клінічних, лабораторних і радіологічних методах.
Застосування МР-КА дозволяє значно підвищити інформативність методу при РЗС, оскільки може забезпечувати об’єктивні й кількісні виміри тонких, незначних морфологічних і структурних змін різних тканин суглоба протягом часу, і тому більш надійно відображає прогресування захворювання, а також дозволяє проводити моніторинг відповіді на лікування пацієнтів з РЗС. Це полегшує оцінку нових препаратів для лікування РЗС й може дозволяти швидше проводити дослідження в деяких пацієнтів.
Подальша робота є необхідною для оптимізації МРТ, оскільки вона може бути застосована як потужний об’єктивний метод дослідження РЗ, а також потенційно нових препаратів для їх лікування.
1 Можуть бути отримані як послідовність у двох вимірах у двох площинах або як послідовність у трьох вимірах з ізометричними елементами об’ємного зображення в одній площині, що дозволяє реконструкцію в інших площинах.
2 Ймовірно, в/в введення гадолінію не є обов’язковим, якщо немає необхідності оцінити деструктивні зміни (ерозії).
3 Збільшення (посилення) визначають при порівнянні Т1-зважених зображень, отриманих до та після в/в введення гадолінію.
4 Т1-зважене зображення — це втрата нормальної низької інтенсивності сигналу від кортикальної кістки та втрата нормальної високої інтенсивності сигналу від трабекулярної кістки.
5 Швидке постгадолінієве посилення означає наявність активного гіперваскуляризованого панусу в ерозії. Необхідно розглядати також інші фокусні кісткові ушкодження, у тому числі метастази, але зазвичай їх відрізняють за допомогою додаткових зображень та клінічних проявів.
6 Можуть бути ізольованими або оточеними ерозіями чи іншими аномаліями кісток.
7 Висока інтенсивність сигналу на Т2-зважених та STIR-зображеннях та низька інтенсивність сигналу на Т1-зважених зображеннях.
1. Агабабова Э.Р. Спондилоартриты как объект перспективных научных исследований в ревматологии // Избранные лекции по клинической ревматологии. В.А. Насонова, Н.В. Бунчук (ред.). — М.: Медицина, 2001. — С. 74-82.
2. Коваленко В.М., Шуба Н.М. Номенклатура, класифікація, критерії діагностики та програми лікування ревматичних хвороб. — К.: Зовнішторгвидав України, 2004. — 156 с.
3. Коваленко В.Н., Борткевич О.П. Остеоартроз: Практическое руководство. — 2-е изд., перераб. и доп. — К.: Морион, 2005. — 592 с.
4. Alasaarela E., Takalo R., Tervonen O. et al. Sonography and MRI in the evaluation of painful arthritic shoulder // Br. J. Rheumatol. — 1997. — 36. — 996-1000.
5. Alassaarela E., Suramo I., Tervonen O. et al. Evaluation of humeral head erosions in rheumatoid arthritis: a comparison of ultrasonography, magnetic resonance imaging, computed tomography anв plain radiography // Br. J. Rheumatol. — 1998. — 37. — 1152-1156.
6. Beltran J., Caudil J.L., Herman L.A. et al. Rheumatoid arthritis: MR imaging manifestations // Radiology. — 1987. — 165. — 153-157.
7. Boers M., Kostense P.J., Verhoeven A.C., van der Linden S. Inflammation and damage in an individual joint predict futher da- mage in that joints in patients with early rheumatoid arthritis // Arthritis Rheum. — 2001. — 44. — 2242-2246.
8. EULAR: Working Party on Imaging in Rheumatology (2005) http://www.doctor33.it/eular/fr_references.asp
9. Kellgren J.H., Lawrence J.S. Radiological assessment of rheumatoid arthritis // Ann. Rheum. Dis. — 1957. — 16. — 485-493.