Журнал «Травма» Том 11, №1, 2010
Вернуться к номеру
Применение биокомпозиционного наноструктурированного препарата «Коллапан» и обогащённой тромбоцитами аутоплазмы в инжиниринге костной ткани
Авторы: Г.Н. Берченко, Г.А. Кесян, Д.С. Микелаишвили - ФГУ «ЦИТО им. Н.Н. Приорова Росмедтехнологии», Москва, Россия
Рубрики: Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
На 60 кроликах проведено сравнительное изучение влияния обогащённой тромбоцитами аутоплазмы (PRP), препарата «Коллапан» и их сочетанного применения на заживление сегментарного дефекта (0,6-0,7 см) лучевой кости у кроликов. Использование в инжиниринге костной ткани сочетанного применения PRP и «Коллапана» способствует значительной активизации репаративной регенерации кости, что проявляется в ускорении образования, созревания и ремоделирования костной мозоли, сокращению сроков заживления костного дефекта.
На 60 кроликах проведене порівняльне вивчення впливу збагаченої тромбоцитами аутоплазмм (PRP), препарату «Коллапан» та їхнього поєднаного застосування на загоєння сегментарного дефекту (0,6-0,7 см) променевої кістки у кроликів. Використання в інжинірингу кісткової тканини поєднаного застосування PRP і «Коллапана» сприяє значній активізації репаративної регенерації кістки, що проявляється в прискоренні утворення, дозрівання й ремоделювання кісткової мозолі, скороченню строків загоєння кісткового дефекту.
Comparable studies of influence of platelet-rich plasma (PRP), preparatus Collapan and their both implementation in heeling of segmental defects of 60 rabbit’s radiuses were done. Combined application of PRP and Collapan in engineering of bone tissue promotes valuable activation of bone reperetive regeneration, which can be presented by acceleration of formation, maturation and remodeling of bone regenerate, decrease of bone defect’s healing period.
инжиниринг кости, гидроксиапатит, «Коллапан»
інжиніринг кістки, гидроксиапатит, «Коллапан»
engineering of bone tissue, hydroxyapatite, Collapan
Несмотря на значительные успехи в хирургической технике, лечение переломов кости может сопровождаться развитием осложнений. Замедленное или полное несращение переломов кости развивается в 5% случаев всех переломов и до 20% случаев высокоэнергитичных переломов [9]. Предотвращение развития подобных осложнений, стимуляция процессов репаративной регенерации кости, а также лечение больших костных дефектов, формирующихся после тяжелых травм или различных заболеваний, требуют новых подходов с использованием биологически активных материалов и тканевого инжиниринга. В настоящее время в клинической практике с целью замещения костных дефектов используют кальций-фосфатные материалы [13], для активизации остеогенеза применяют обогащенную тромбоцитами аутоплазму (Platelet-Rich Plasma – PRP) [14,15].
В данной работе изучены особенности заживления сегментарных дефектов лучевой кости "кроликов при имплантации PRP и «Коллапана».
Материал и методы
Экспериментально-морфологическое исследование проведено на 60 кроликах породы шиншилла (разделены на 4 группы, в каждой по 15 животных), массой 4 ± 0,5 кг. Под наркозом животным формировали дефект лучевой кости 0,6-0,7 см. с обнажением костномозгового канала. В 1-й группе животных производилось послойное ушивание раны (контрольная группа); во 2-й группе в полость костного дефекта вводилась обогащённая тромбоцитами аутоплазма (PRP); в 3-й группе – «Коллапан»; в 4-ой группе – смесь PRP и «Коллапана». Животные выводились из опыта через 30, 60 и 90 дней (по 5 животных на срок) после операции. Гистологические срезы исследуемого материала окрашивали гематоксилином и эозином, а также пикрофуксином по Ван Гизону и изучали в светооптическом микроскопе.
Для получения аутологичной PRP производили забор крови из сердца животного (примерно 20-30 мл), с последующим её двукратным центрифугированием. Первым этапом кровь центрифугировалась 10 мин. при g=1000, вторым этапом остаток тромболейкоцитарной массы центрифугировался в течение 20 мин. при g= 3000 с последующим удалением надосадочной жидкости после каждого центифугирования. Коллапан – биокомпозиционный материал на основе наноструктурированного синтетического гидроксиапатита (размер частиц гидроксиапатита 20 нанометров), коллагена и антибиотика. Производится фирмой «Интермедапатит», Россия (фирма прошла сертификацию по европейскому стандарту ИСО 13485-2003); регистрационный номер «Коллапана» в РФ - ФС 01034437/4437-06.
Результаты и обсуждение
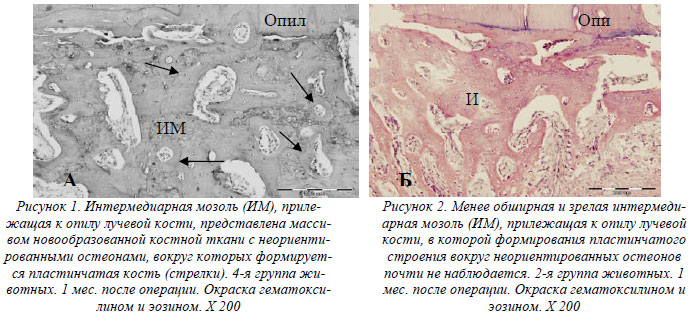
Морфологическое исследование показало, что через 1 месяц после операции во всех группах животных наблюдалось формирование первичной костно-хрящевой мозоли. В наименее зрелых участках мозоли – в центре костного дефекта во 2-й и особенно 1-й группах животных - признаки остеогенеза выражены слабо, в то же время в 3-й и, особенно, в 4-й группах видно активное формирование остеоида непосредственно на поверхности имплантированных гранул «Коллапана» без формирования между ними прослоек рыхлой соединительной ткани. Имплантированный «Коллапан» не вызывал воспалительной реакции в виде какой-либо клеточной инфильтрации ткани. Наиболее развитая интермедиарная мозоль располагалась вблизи опила кортикальной пластинки, причем по степени зрелости она убывала от 4-й к 1-й группе животных. Наибольший объем новообразованной костной массы и более развитое пластинчатое строение формирующихся остеонов определялось в 4-й группе животных (рис.1). В наиболее зрелых участках мозоли (вблизи опила) элементы имплантированного Коллапана резорбировались и не выявлялись. В 3-й и, особенно, 2-й группах животных, по сравнению с 4-й, новообразованная костная масса интемедиарной мозоли менее обширна, пластинчатое строение формирующихся в ней остеонов слабо выражено (рис.2). В 1-й группе животных к данному сроку интермедиарная мозоль представлена лишь немногочисленными остеоидными костными трабекулами.
Ко 2-3-у месяцу после операции признаки созревания и ремоделирования костной мозоли в виде увеличения костной массы, перестройки грубоволокнистых незрелых костных структур в пластинчатую кость и постепенной ориентации остеонов вдоль оси кости прогрессировали, что в наибольшей степени выражено в 4-й группе животных. В центральных отделах костного дефекта 3-й группы животных в костном массиве интемедиарной мозоли и некоторых трабекулах эндостальной мозоли выявлялись отдельные частицы «Коллапана», тогда как в 4-й группе они полностью резорбировались. Формирование новообразованной костной массы, её ремоделирование с образованием пластинчатых структур и ориентированных остеонов более активно происходило в 3-й группе животных по сравнению со 2-й. Наименее зрелая костная мозоль определялась в 1-й группе животных, где интермедиарная мозоль была представлена преимущественно тканью в виде губчатой кости.
Полное сращение дефекта лучевой кости у животных происходило: в 1-й группе - на 75±4,6, во 2-й – на 69±3,7, в 3-й – на 66±3,4, в 4-й – на 55±3,5 сутки после операции.
На моделях различных животных показано, что некоторые кальций-фосфатные материалы, такие как синтетический гидроксиапатит, бетатрикальций фосфат, бифазная трикальцийфосфатная керамика, индуцируют эктопический (внекостный) остеогенез, то есть обладают остеоиндуктивными свойствами [10,16]. В культуре клеток определённые кальций-фосфатные материалы способствуют дифференцировке стволовых мезенхимальных клеток костного мозга человека в остеобласты в условиях отсутствия в культуральной среде остеогенных стимулирующих факторов, что свидетельствует о важнейшей роли клеточно-матриксного взаимодействия в направлении дифференцировки плюрипотентных малодифференцированных клеток [12].
В многочисленных экспериментально- и клинико-морфологических исследованиях нами обнаружено, что материал «Коллапан», обладая антимикробными, остеокондуктивными и остеоиндуктивными свойствами, является постепенно резорбируемой матрицей, на поверхности которой в условиях условно асептических и инфицированных костных дефектов формируется новообразованная кость [1-6,8]. При этом вокруг частиц «Коллапана» при различных сроках исследования признаков воспалительной реакции не выявляется, между имплантируемым материалом и новообразованной костью прослоек фиброзной ткани не формируется. Использование «Коллапана» в клинике у больных с открытыми и закрытыми переломами, с несросшимися переломами и ложными суставами длинных трубчатых костей (313 больных), при комплексном лечении хронического остеомиелита (92 пациента) способствовало сокращению сроков пребывания больных в стационаре, предотвращению рецидивов хронического воспалительного процесса и повторной госпитализации в связи с отсутствием осложнений [6,8].
В настоящее время в клинической практике с целью активизации остеогенеза находит метод использования обогащенной тромбоцитами аутоплазмы (PRP) [14,15]. Аутологичная PRP представляет собой концентрированную суспензию тромбоцитов в ограниченном объеме плазмы. Метод основан на применении аутологичных тромбоцитов, в которых содержатся многочисленные факторы роста и цитокины, способствующие регенерации повреждённой кости. В ά-гранулах тромбоцитов выявлено свыше 30 ростовых факторов, среди которых наиболее важное значение для регенерации кости имеют тромбоцитопроизводный фактор роста (PDG F), фактор роста эндотелия сосудов (VEG F) и трансформирующий фактор роста (TGF-β). Последний представляет собой большую группу белков, среди которых TGF-β1 и морфогенетические белки кости модулируют клеточную пролиферацию и дифференцировку малодифференцированных клеток в остеобласты, увеличивают синтез внеклеточного матрикса кости и ингибируют его деградацию.
Тканевой инжиниринг является альтернативой для использования аутотрансплантатов и костных аллоимплантатов. Инжиниринг тканей – это создание в лабораторных условиях живых функциональных компонентов, которые могут быть использованы для регенерации неправильно функционирующих тканей [11]. В инжиниринге кости используется три компонента: 1) живые клетки (обычно мезенхимальные стволовые клетки, полученные из костного мозга и способные дифференцироваться в остеобласты или хондробласты); 2) матрица, обладающая остеокондуктивными свойствами, к которой могут прикрепляться предшественники остеобластов с последующим ростом и формированием кости; 3) факторы роста, стимулирующие клеточную активность и дифференцировку с развитием остео- или хондрогенеза. Исходя из основных принципов тканевого инжиниринга, с целью активизации регенерации костной ткани сотрудниками ЦИТО разработан метод сочетанного применения «Коллапана» и обогащённой тромбоцитами аутоплазмы в травматолого-ортопедической практике. В данном случае в качестве живых клеток используется концентрат собственных тромбоцитов, которые, разрушаясь в костном дефекте, выделяют многочисленные факторы роста, запускающие и активирующие процессы остеогенеза, тогда как «Коллапан» выполняет роль постепенно лизирующейся матрицы, обладающей не только остеокондуктивными, антибактериальными, но и остеоиндуктивными свойствами.
Как показало данное исследование, сочетанное применение «Коллапана» с аутологичной PRP, по-видимому, за счёт синергизма их действия, вызывает значительную активизацию репаративной регенерации кости, выраженную в большей степени, чем при использовании «Коллапана» или аутологичной PRP в отдельности. В данном случае «Коллапан», кроме всего прочего, служит средством локальной доставки выделяющихся из тромбоцитов аутологичных факторов роста. Не исключено, что факторы роста могут связываться физическими или ковалентными связями с элементами «Коллапана» с последующим пролонгированным выделением в костном дефекте. Локально выделяющиеся аутологичные факторы роста, стимулируя адгезию, пролиферацию, дифференцировку клеток-предшественников остеобластов, функциональную активность остеобластов и синтез этими клетками внеклеточного матрикса кости, значительно усиливают остеоиндуктивные свойства биокомпозиционного материала «Коллапан», ускоряют этапы репаративной регенерации кости. Использование данного метода в клинике способствовало у 30-и больных с замедленно консолидирующимися переломмами сокращению сроков сращения на 7±3,2 дня, а у 42 больных с несросшимися переломами и ложными суставами – на 12±4,8 дня [7].
Выводы
Использование в инжиниринге костной ткани биокомпозиционного наноструктурированного препарата «Коллапан» в сочетании с факторами роста обогащённой тромбоцитами аутоплазмы (PRP) является безопасным и эффективным методом активизации репаративной регенерации кости, который может быть рекомендован для широкого внедрения в клиническую практику.
1. Арсеньев И.Г. Экспериментально-морфологическое обоснование клинического применения деградируемых биоимплантатов в комплексном лечении переломов и ложных суставов длинных трубчатых костей: Автореф. дис. ... кандидата мед. наук. – М., 2007. – 25 с.
2. Берченко Г.Н., Кесян Г.А., Уразгильдеев Р.З. и др. Сравнительное экспериментально-морфологическое исследование влияния некоторых используемых в травматолого-ортопедической практике кальций-фосфатных материалов на активизацию репаративного остеогенеза // «Бюллетень Восточно-сибирского научного центра Сибирского отделения РАМН».- №4.- 2006. - С.327-332.
3. Берченко Г.Н., Кесян Г.А. Активизация репаративного остеогенеза при заполнении сегментарного дефекта длинной трубчатой кости композиционным препаратом Коллапан. // «Травма».- 2008.-Т.9,№ 3.-С.282-286.
4. Берченко Г.Н. Биокомпозиционный наноструктурированный препарат Коллапан в инжиниринге костной ткани. / Искусственные материалы в травматологии и ортопедии.- М,, 2009.-С.7-13.
5. Жердев К.В. Применение имплантата Коллапан-гель в детской костной патологии. Автореф. дис. . кандидата мед. наук. – М., 2007. – 22 с.
6. Кесян Г.А., Берченко Г.Н., Уразгильдеев Р.З и др. Обоснование использования отечественного биокомпозиционного препарата Коллапан в комплексном лечении переломов и ложных суставов длинных трубчатых костей // Вестник Российской академии медицинских наук.-2008.- № 9.-С.24-32.
7. Кесян Г.А., Берченко Г.Н., Уразгильдеев Р.З. и др. Применение Коллапана и факторов роста в лечении травматолого-ортопедических больных / «Искусственные материалы в травматологии и ортопедии».- М, 2009.-С.45-48.
8. Уразгильдеев З.И., Бушуев О.М., Берченко Г.Н. Применение Коллапана для пластики остеомиелитических дефектов кости // Вестник травматологии и ортопедии им. Н.Н. Приорова. – 1998.- № 2. – С.31 -35.
9. Dickson G., Buchanan F., Marsh D et al. Orthopaedic tissue engineering and bone regeneration. Technology Health Care. 2007. V. 15. P. 57-67.
10. Habibovic P., Sees T.M., van den Doel M.F., et al. Osteoinduction by biomaterials – physicochemical and structural influences. J. Biomed. Mater. Res. 2006. V. 77A. P. 747-762.
11. Hench L.L., Jones J.R., Biomaterials, artificial organs and tissue engineering. Woodhead Publishing Limited, 2005. 287 p.
12. Muller P., Bulnheim U., Diener A., et al. Calcium phosphate surfaces promote osteogenic differentiation of mesenchymal stem cells. J. Cellular Molec. Medicine. 2007. V.12. Issue 1. P. 281-291.
13. Ransford A.O., Morley T., Edgar M.A., et al. Synthetic porous ceramic compared with autograft in scoliosis surgery. A prospective, randomized study of 341 patients. J Bone Joint Surg [Br]. 1998. V. 80-B. P. 13-18.
14. Simman R., Hoffmann A., Bohinc J. et al. Role of platelet-rich plasma in acceleration of bone fracture healing. Ann. Plast. Surg. 2008. V. 61. P. 337-344.
15. Wrotniak M., Bielecki T., Gazdzik T.S. Current opinion about using the platelet-rich gel in orthopaedics and trauma surgery. Ortopedia Traumatologia Rehabilitacja. 2007. V. 9 № 3. P. 227-238.
16. Yuan H., van Blitterswijk CA., de Groot K. et al. Cross-species comparison of ectopic bone formation in biphasic calcium phosphate (BCP) and hydroxyapatite (HA) scaffolds. Tissue Eng. 2006. V. 12. P. 1607-1615.