Журнал «Здоровье ребенка» 5 (40) 2012
Вернуться к номеру
Деласкин — новые возможности терапии атопического дерматита у детей в Украине
Авторы: Клименко В.А., Кожемяка А.И., Адарюкова Л.М., Карпушенко Ю.В., Давиденко Е.В., Котовщикова Т.С. - Харьковский национальный медицинский университет, Харьковский областной детский аллергоцентр при КУЗ ОДКБ № 1
Рубрики: Педиатрия/Неонатология
Разделы: Справочник специалиста
Версия для печати
В статье проанализированы научные данные о механизмах действия синтетических танинов. Представлено место препаратов данной группы в алгоритме терапии атопического дерматита у детей. Приведены собственные данные об эффективности крема Деласкин в лечении обострения атопического дерматита легкой степени у детей.
У статті проаналізовані наукові дані про механізми дії синтетичних танінів. Наведено місце препаратів даної групи в алгоритмі терапії атопічного дерматиту в дітей. Наведено власні дані про ефективність крему Деласкін у лікуванні загострення атопічного дерматиту легкого ступеня в дітей.
There had been analyzed scientific data on mechanisms of synthetic tannins action. The place of these agents in therapy algorithm for atopic dermatitis is presented. Own data on efficacy of Dermaskin cream in treatment of atopic dermatitis mild exacerbations in children are given.
атопический дерматит, лечение, синтетические танины, Деласкин.
атопічний дерматит, лікування, синтетичні таніни, Деласкін.
atopic dermatitis, treatment, synthetic tannins, Delaskin.
Предпосылки появления в Украине нового нестероидного препарата для лечения атопического дерматита (АД)
1. АД известен давно — впервые описан van Helment в 1607 г. За последующие 400 лет достигнут значительный прогресс в понимании механизмов заболевания: открыты гены, ответственные за развитие АД, определена их локализация на хромосомах, предложено множество теорий патогенеза, разработаны эффективные походы к лечению обострений. Но реальность такова, что в то время «когда наши космические корабли бороздят просторы вселенной», мы не можем вылечить больного от АД — аллергия, начавшись в колыбели, преследует человека всю жизнь. При наблюдении такого пациента задача врача — обеспечить контроль заболевания путем предупреждения рецидивов и снижения их тяжести, раннего быстрого безопасного купирования обострений, предотвращения осложнений. Такая тактика предполагает длительное (годами!) применение определенных препаратов. Следовательно, и требования к этим лекарственным средствам возрастают: они должны быть не только эффективными, но и максимально безопасными, ибо при многолетнем применении побочные эффекты (если таковые имеются) обязательно проявятся клинически и будут оказывать влияние на прогноз заболевания. Таким образом, существует потребность в препарате безопасном, без побочных эффектов для длительного применения при АД.
2. Следующая проблема, связанная с ведением больных с АД, — как контролировать заболевание и какие препараты (местного или системного действия) являются средствами первой линии терапии? Этот вопрос длительное время был причиной дискуссий. До 80-х годов прошлого века признавалась главенствующая роль препаратов системного действия, применяемых внутрь, перорально. Считалось, что «кожа — зеркало атопии» и на ней отражаются те патологические изменения, которые первично произошли во внутренних органах — прежде всего в печени или в нервной системе. Кератиноциты презрительно именовали «молчащим большинством», а некоторые исследователи (Н.А. Мануилова, 1973) даже рассматривали эпидермис как гигантскую открытую голокриновую железу, секретом которой является роговой слой. Открытия последних лет кардинально изменили наше представление о значении кожи в формировании АД. Первым концепцию лимфоидной ткани, ассоциированной с кожей (SALT — skin associated lymphoid tissue) сформулировал J. Streilin в 1978 г. Этим термином были объединены антигенпрезентирующие клетки эпидермиса, тропные к эпидермису Т-клетки, кератиноциты и региональные лимфоузлы. Позднее понятие об иммунной системе кожи расширилось за счет включения клеток, размещенных главным образом в дерме, — тучных клеток, макрофагов, В-лимфоцитов, эндотелия кровеносных и лимфатических сосудов. Сегодня доказано, что клетки эпидермиса выполняют важную иммунологическую функцию — они формируют микроокружение путем синтеза множества цитокинов и ответственны за развитие воспалительного процесса в коже [1]. В последние годы показана ключевая роль генетического дефекта в синтезе белка кожи — филаггрина (вызывает агрегацию кератиновых филаментов и регулирует проницаемость эпидермального барьера) в патогенезе АД [2]. За изучение роли филаггрина и новых подходов к терапии дерматита доктору С. Молин из Мюнхена в 2010 году была присуждена престижная премия Хайнца Маурера (основателя компании «Себафарма») за исследование в области дерматологии [3].
Более того, через кожу происходит не только формирование местного воспалительного процесса (дерматит), но и сенсибилизация всего организма с формированием системного аллергического ответа (аллергический ринит, астма) [4, 5]. Таким образом, современный слоган, характеризующий роль кожи в формировании АД, следующий: «кожа — входные ворота (entry point) атопии». Учитывая современные данные о значении кожи и SALT в патогенезе АД, ведущее место в лечении уделяется наружной терапии [6]. «Наружной» она называется только исторически, традиционно — по способу нанесения препарата. По механизму действия эти препараты имеют патогенетическое значение, поскольку действуют на иммунокомпетентные клетки кожи, не только изменяя течение болезни, но и влияя на системные проявления аллергии, на прогноз заболевания. Системным средствам, традиционно использовавшимся педиатрами при лечении АД, сегодня отводится вспомогательная роль. Таким образом, препарат для лечения АД должен быть топического применения.
3. Следующий аспект проблемы — эффективность купирования обострения будет тем выше, чем раньше начата терапия: легче ликвидировать воспалительные изменения в самом начале. Именно в этот момент терапевтические меры будут наиболее успешны и позволят предупредить не только дальнейшее прогрессирование поражений на коже, но и вторичные (чаще — инфекционные) осложнения. Таким образом, существует потребность в препарате для применения при первых клинических признаках дерматита.
4. Стандартом терапии АД сегодня являются топические глюкокортикостероиды (ТГКС). Но данная группа препаратов имеет ряд побочных эффектов, ограничивающих их применение, как по длительности, так и по площади нанесения. Для снижения риска осложнений разработаны современные технологии аппликаций ТГКС:
— тандем-терапия — нанесение один раз в сутки стероидного препарата, второй раз — безопасного противовоспалительного и противозудного препарата;
— ступенчатое лечение — нанесение ТГКС по очереди на разные пораженные участки кожи, на другие участки — безопасный противовоспалительный препарат;
— штриховой метод — используется при генерализованном поражении.
Таким образом, существует потребность в безопасном топическом противовоспалительном препарате для сочетанного применения с ТГКС при обострениях АД тяжелой степени или при генерализованном поражении кожных покровов.
Всем вышеперечисленным требованиям соответствуют препараты на основе синтетических танинов.
Значение синтетических танинов в терапии АД
Танины (дубильные, вяжущие вещества) традиционно используются в народной медицине — именно свойствами этих веществ обусловлено лечебное действие примочек и ванн с корой дуба, чаем при АД. Танины также содержатся в зверобое, змеином горце, шалфее, цветках ромашки и других лечебных растениях. Синтетический танин (на сегодняшний день доступен только один — сульфированная натриевая соль фенол-метаналь-мочевины поликонденсата) был разработан в середине прошлого столетия. Он имеет существенные преимущества перед природными аналогами благодаря очистке действующего вещества от примесей, точности дозирования, контролю качества на всех этапах производства, более длительному сроку годности и отсутствию красящих компонентов. Основные свойства танинов — вяжущее, противовоспалительное, противозудное, антимикробное.
Вяжущее действие. Танины, образуя химические связи между протеинами кожи и экссудата, создают коагуляционную пленку в верхних слоях эпидермиса, которая препятствует трансэпидермальной потере воды. Преципитация протеинов также определяет уплотнение и стабилизацию клеточных мембран, уменьшая, таким образом, экссудацию тканевой жидкости и местный воспалительный процесс.
Противовоспалительный эффект танинов связан не только с их вяжущим действием, но и с непосредственным угнетением целого ряда провоспалительных энзимов, имеющих значение в патогенезе АД — в частности, в эксперименте in vitro доказано, что синтетические танины угнетают активность нейтрофильной эластазы (Mrowietz et al.) [7], химазы тучных клеток и плазмина (Wiedow et al.) [8]. Исследованиями Zuberbier et al. доказано, что синтетические танины угнетают анти-IgE-индуцированное выделение гистамина [9]. Данный эффект — дозозависимый; им объясняется и противовоспалительная эффективность танинов при лечении аллергических реакций 1-го типа, и противозудные свойства препарата.
Противомикробный эффект танинов обусловлен образованием коагуляционной пленки, препятствующей проникновению микроорганизмов в кожу; уменьшением экссудации, что способствует устранению питательного субстрата для бактерий и грибков. Исследователями (Regina Fölster-Holst и другие) была высказана гипотеза, что противомикробный эффект танинов связан со связыванием белков фибриногена и фибронектина, которые задействованы в адгезии золотистого стафилококка в кожу [10].
Противозудные свойства синтетических танинов непосредственно связаны с вяжущим, противовоспалительным, противомикробным эффектами, следствием которых является снижение стимуляции нервных рецепторов в коже. Также противозудный эффект обусловлен снижением IgE-зависимой продукции гистамина и непосредственно местноанестезирующим действием, которое ощущал каждый из нас при полоскании ротовой полости отваром коры дуба.
Препараты на основе синтетических танинов широко применяются в Европе для лечения многих воспалительных заболеваний кожи (в том числе и АД), но в Украине первый препарат этой группы — Деласкин производства фармацевтической компании Dermapharm AG (Грюнвальд, Германия) — появился только в 2010 году.
В 2011 году сотрудниками кафедры пропедевтики педиатрии № 2 ХНМУ и Харьковского областного аллергоцентра (заведующая — Л.М. Адарюкова) при КУЗ ОДКБ № 1 (главврач — О.В. Пионтковская) проведена апробация препарата Деласкин, представленного двумя лекарственными формами — крем и порошок. Препарат получали 50 детей в возрасте от 3 мес. до 17 лет. Все пациенты были разделены на 3 группы:
1) крем Деласкин применялся в качестве наружной монотерапии при обострении АД легкой степени тяжести — 20 детей;
2) крем Деласкин применялся в сочетании с ТГКС:
— при обострении АД средней тяжести — 12 детей;
— при обострении АД тяжелой степени в режиме тандем-терапии (Деласкин — утром и днем, а препарат ТГКС — вечером) — 7 детей;
— при обострении АД тяжелой степени с генерализованным поражением кожи согласно алгоритму: Деласкин — 3 раза в день на всю пораженную поверхность кожи, а ТГКС — штриховым методом 1 раз в сутки — 5 детей. Больные данной группы дополнительно применяли порошок Деласкин 2 раза в неделю в виде прохладной ванны (t = 33–34 °С) из расчета 1 саше (10 г) на 50 л воды;
3) крем Деласкин применялся для лечения опрелостей у детей грудного возраста с АД — 6 детей.
У всех детей достигнута ремиссия АД. Не было зарегистрировано побочных реакций на препарат.
По результатам апробации препарата выполнено научное исследование, задачей которого явилась оценка эффективности крема Деласкин в терапии обострений АД легкой степени (больные 1-й группы).
Методика работы
Под наблюдением находилось 20 детей в возрасте от 3 мес. до 17 лет, страдающих АД. Верификация диагноза проводилась в соответствии с критериями Hanifin, Rajka, 1980. Критерии включения: наличие обострения АД легкой степени (индекс SCORAD менее 23); эритематозная или эритематосквамозная клинико-морфологическая форма дерматита. Крем Деласкин наносился 3 раза в день. Также всем детям были назначены элиминационные мероприятия, антигистаминные препараты и базисная наружная терапия. Оценка лечения проводилась на 3, 5 и 7-й дни. Критерии эффективности — переносимость препарата, динамика индекса SCORAD, субъективная оценка пациентов. Статистическая обработка проведена на персональном компьютере с использованием программы Excel 2003.
Результаты
Непереносимости крема Деласкин не зарегистрировано ни у одного пациента. Субъективная оценка препарата пациентами и их родителями — позитивная. Основные аргументы: не оказывает раздражающего действия; успокаивает зуд; не пачкает одежду и постельные принадлежности; доступный, недорогой по цене. Динамика интегрального показателя тяжести обострения АД (SCORAD) представлена на рис. 1.
/77/77.jpg)
На 7-й день терапии у всех пациентов отмечена положительная клиническая динамика: у 17 (85 %) детей — полная ликвидация воспалительных изменений на коже, у 3 больных сохранялись воспалительные морфологические элементы — им был назначен ТГКС коротким курсом.
Выводы
Крем Деласкин эффективен в лечении обострений АД легкой степени у детей, что позволяет рассматривать его в качестве препарата выбора при первых клинических признаках дерматита.
Клиническая оценка эффективности Деласкина у пациентов 2-й группы требует дальнейшего изучения, так как препарат применялся в комплексной терапии с ТГКС.
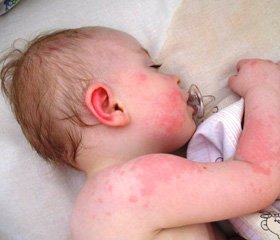
Клиническая эффективность крема Деласкин в терапии опрелостей у детей с АД (3-я группа больных) представлена на рис. 2. Опрелости у детей с АД — проблема, требующая особого подхода. Поражения кожи у этих детей возникают даже при наличии хорошего ухода, характеризуются торпидностью к терапии и частыми осложнениями, чаще — грибковой этиологии. У всех детей (6 чел.) отмечена положительная клиническая динамика с 3-го дня терапии и ликвидация воспалительных изменений — к 6,3 ± 0,7 дню.
Появление в Украине противовоспалительного нестероидного препарата новой группы — синтетических танинов (Деласкин) позволит повысить эффективность и безопасность лечения АД у детей.
1. Novak N., Bieber T., Leung D.Y.M. Immune mechanisms leading to atopic dermatitis // J. Allergy Clin Immunol. — 2003. — Vol. 112, № 6. — P. 128-139.
2. Кожные и венерические болезни. Олег Иванов // http://readr.ru/oleg-ivanov-koghnie-i-venericheskie-bolezni.html
3. Премия Heinz Maurer за научные исследования в области дерматологии // http://www.sebamedrussia.ru/news/777/
4. Spergel J.M., Mizoguchi E., Brewer J.P. et al. Epicutaneuos sensitization with protein antigen induces localized allergic dermatitis and hyperresponsiveness to methaholine after single exposure to aerosolized antigen in mice // J. Clin. Invest. — 1998. — Vol. 101. — P. 1614-22.
5. Spergel J.M., Paller A.S.S. Atopic dermatitis and the atopic march // J. Allergy Clin. Immunol. — 2003. — Vol. 112, № 6 (suppl). — P. 118-127.
6. Ellis C., Luger T., Abeck D. et al. International Consensus Conference on Atopic Dermatitis II (ICCAD II): clinical update and current treatment strategies // Brit. J. Dermatol. — 2003 May. — Vol. 148, Suppl. 63. — P. 3-10.
7. Mrowietz U., Ternowitz T., Wiedow O. Selective inactivation of human neutrophil elastase by synthetic tannin // J. Invest. Dermatol. — 1991. — 97. — 529-533.
8. Wiedow O., Weindler F., Mrowietz U. The effect of tamol on humanmast cell chymase and plasmin // Skin. Pharmacol. — 1997. — 10. — 90-96.
9. Zuberbier T., Khreis I., Guhl S. et al. Tannin inhibits histamine release // Allergy. — 1999. — 54. — 898-900.
10. Cho S.H., Strickland I., Boguniewicz M. et al. Fibronectin and fibrinogen contribute to the enhanced binding of Staphylococcus aureus to atopic skin // J. Allergy Clin. Immunol. — 2001. — 108. — 269-274.

/78/78.jpg)