Газета «Новости медицины и фармации» Кардиология (447) 2013 (тематический номер)
Вернуться к номеру
Как повысить безопасность длительной терапии ацетилсалициловой кислотой: мифы и реальность
Авторы: Долженко М.Н., д.м.н., профессор, Национальная медицинская академия последипломного образования им. П.Л. Шупика, г. Киев
Рубрики: Кардиология
Разделы: Справочник специалиста
Версия для печати
Целесообразность применения ацетилсалициловой кислоты (АСК) в профилактике кардио и цереброваскулярных событий доказана многократно. Еще в 70х годах были высказаны предположения, что регулярный прием аспирина может снизить риск развития инфаркта миокарда (ИМ) и коронарной смерти [1–4]. Было проведено пять наиболее крупных исследований по применению аспирина с целью первичной кардиоваскулярной и цереброваскулярной профилактики: Physicians Health Study, British Doctors Study, Thrombosis Prevention Trial (TPT), Hypertension Optimal Treatment Study (HOT) и Primary Prevention Project (РРР) [5–9].
В целевом анализе Antithrombotic Trialists’ Collaboration (2002) обобщены данные относительно лечения 18 788 пациентов с ИМ в анамнезе, полученные в 12 важнейших рандомизированных клинических исследованиях эффективности антитромбоцитарных средств. Применение преимущественно АСК уменьшило относительный риск нефатального ИМ на 28 % (p < 0,0001), сосудистой смерти — на 15 % (p < 0,0006), смерти в целом — на 11 % (p = 0,02). Суточные дозы препарата 80–325 мг уменьшали риск сердечнососудистых событий.
Однако при длительном применении АСК возникают побочные реакции, из которых наиболее выражены поражения желудочнокишечного тракта (ЖКТ). Какие возможны варианты для протекции ЖКТ у больных с кардио и цереброваскулярной патологией?
Как повысить безопасность антитромбоцитарной терапии у пациентов с язвенной болезнью в анамнезе?
В 2008 году в JACC [10] был опубликован Консенсус экспертов ACCF/ACG/AHA по снижению гастроинтестинальных рисков при применении антитромбоцитарной терапии и нестероидных противовоспалительных препаратов, который дает ответ на данный вопрос.
В данном документе подчеркивается, что использование низких доз АСК для кардио и церебропрофилактики связано с 2 и 4кратным повышением риска развития язвенной болезни. Сразу декларируется информация, что ни кишечнорастворимая (КР) форма, ни добавление буферных препаратов (тем более, например, гидроокиси магния в неадекватной дозировке) не снижают риск кровотечения [11–13]. Пациентам с риском развития язвенной болезни должна быть назначена гастропротекторная терапия, кроме того, АСК должна применяться в дозе, не превышающей 81 мг, при длительной терапии.
Американская ассоциация сердца рекомендует применение низких доз АСК у пациентов с 10летним кардиоваскулярным риском, который больше или равен 10 % [15], а Рабочая группа по профилактике США — применение АСК для пациентов с 5летним риском, больше или равным 3 % [16]. Среди пациентов пожилого возраста отношение шансов кровотечения при суточной дозе АСК 75, 150 и 300 мг составляет 2,3; 3,2 и 3,9 соответственно. Снижение дозы не влияет на антитромботическую эффективность, однако увеличение дозы повышает риск кровотечений [17].
Таким образом, в Рекомендациях ACC/AHA подчеркивается целесообразность снижения дозы АСК от 325 до 81 мг у лиц с высоким риском язвенной болезни [18]. Язвенная болезнь в анамнезе, особенно сопровождающаяся кровотечениями, представляется наиболее важным фактором риска. Важным фактором риска является увеличение возраста начиная с 60 лет. Пол является менее важным фактором, хотя риск кровотечений у мужчин несколько выше, чем у женщин [19].
Особо подчеркивается роль H.pylori. В рекомендациях предлагается проводить обязательное тестирование и лечение H.pylori у пациентов с язвенной болезнью в анамнезе перед началом длительной антиагрегантной терапии.
Как повысить безопасностьантитромбоцитарной терапии у пациентов без заболеваний ЖКТ в анамнезе?
Для решения данной задачи следует остановиться на противопоказаниях для приема АСК. Прежде всего это гиперчувствительность к АСК. Кроме того, как было представлено ранее, необходимо избегать назначения аспирина у больных с эрозивноязвенными поражениями ЖКТ (в фазе обострения), а также желудочнокишечными кровотечениями. Не следует назначать АСК больным с аспириновой астмой, заболеваниями крови, такими как геморрагические диатезы (гемофилии, болезнь Виллебранда, телеангиэктазии, гипопротромбинемия, тромбоцитопения, тромбоцитопеническая пурпура), расслаивающей аневризмой аорты, портальной гипертензией; противопоказаниями также являются дефицит витамина K, печеночная/почечная недостаточность; беременность (I и III триместры), кормление грудью; дефицит глюкозо6фосфатдегидрогеназы; детский возраст (до 15 лет с гипертермией на фоне вирусных заболеваний — риск развития синдрома Рея). С осторожностью назначать больным с гиперурикемией, нефролитиазом, тяжелыми заболеваниями печени.
Как соотносятся риск и польза от применения АСК?
При назначении больному длительной терапии АСК, часто пожизненной, нужно правильно оценить риск/пользу: все преимущества антитромбоцитарной эффективности и риск развития патологии ЖКТ [20]. В соответствии с концепцией С. Patrono во взрослой популяции людей, считающихся здоровыми, возникает 1 случай желудочнокишечного кровотечения на 1 тыс. человек в год. Использование АСК риск этого кровотечения удваивает как у здоровых лиц, так и при развитии атеросклероза.
Решение о возможности применения АСК с профилактической целью определяется риском осложнений ишемии миокарда. Там, где риск этих осложнений сравнительно низок (здоровые люди с факторами риска, больные артериальной гипертонией), положительный эффект АСК (снижение риска ишемических событий) оказывается сопоставимым с риском кровотечения. В случае более высокого риска (стабильная стенокардия и острый коронарный синдром, а также ИМ в анамнезе) 1–2 новых случая кровотечения у 1 тыс. больных, принимающих АСК, оказываются вполне приемлемой платой за предотвращение десятков новых сосудистых событий. Следует отметить, что в случае применения относительно низких доз АСК ≤ 325 мг/сут, увеличение риска кровотечений и побочных действий, требующих отмены препарата, оказывается приемлемым для большинства клинических состояний. Как в исследовании CURE, так и в метаанализе АТТ было доказано, что оптимальная доза АСК, способная обеспечить приемлемое соотношение пользы и риска, находится в пределах 75–150 мг/сут и может считаться вполне безопасной.
Возможные фармацевтические формы выпуска АСК. Их целесообразность
С целью гастропротекции были созданы новые фармацевтические формы АСК для длительной антитромбоцитарной терапии: растворимые формы, формы с контролируемым высвобождением [21], АСК в энтеросолюбильной оболочке для растворения в кишечнике, накожные формы [22], буферные формы. Кроме того, были предложены комбинированные препараты, сочетающие в себе АСК и антациды (например, гидроокись магния). Ряд изменений (контролируемое высвобождение и накожные формы) призван уменьшить гастротоксическое действие АСК за счет относительно избирательной блокады синтеза тромбоксана А2 тромбоцитами и минимального влияния на образование сосудистых и желудочных простаноидов. Считается, что препараты АСК, покрытые кишечнорастворимой оболочкой, могут быть менее гастротоксичны изза ослабления прямого раздражающего действия кислоты на слизистую оболочку желудка. Сходный механизм уменьшения негативного действия АСК на желудочнокишечный тракт предложен для обоснования использования комбинации препарата с гидроокисью магния.
Какая имеется доказательная база по безопасному применению АСК?
На сегодняшний день проведено несколько исследований с АСК, покрытых КРоболочкой. Одно из них опубликовано в 2007 году в американском журнале Thoracic Surgery. У бессимптомных больных, длительно принимавших АСК, при исследовании слизистой желудка был диагностирован эрозивный гастрит: у 90 % больных, получавших обычную АСК, и у 60 %, принимавших препарат в виде КРформы [23]. При эндоскопической оценке краткосрочных эффектов обычных и КРформ АСК преимущество последней продемонстрировано в 5 исследованиях [24, 25].
В случае, когда желудочнокишечное кровотечение всетаки произошло, при применении КРформы АСК (325 мг) наблюдается меньшая кровопотеря, чем при приеме обычной формы АСК (325 мг) [26].
Следует отметить позитивный комплайенс КРформы АСК по сравнению с другими формами. Так, результаты крупного проспективного эпидемиологического исследования с участием 577 немецких врачей [27] показали, что у 1156 кардиологических больных, изначально получавших КРформу АСК, и 1570 больных, у которых АСК в обычной форме была заменена на АСК в КРформе, в ходе наблюдения выявлено существенное снижение частоты симптомов диспепсии после замены обычной АСК на КРформу. В начале исследования среди больных, принимавших желудочнорастворимую форму АСК, на изжогу жаловались 37,6 % больных, а в дальнейшем, на фоне приема КРформы АСК, число таких больных уменьшилось до 19,1 % через 3 мес. и до 10,5 % через 2 года лечения.
Какова эффективность кишечнорастворимой формы АСК в плане выживаемости больных после ИМ?
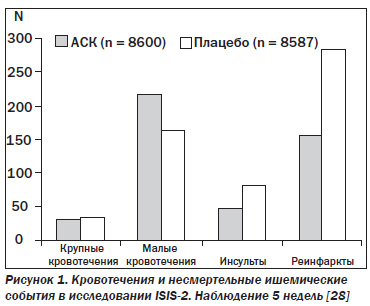
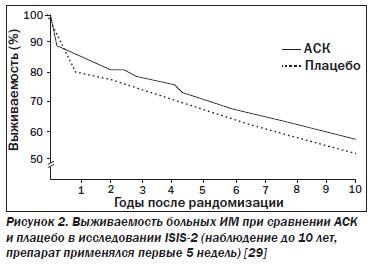
У больных с подозрением на ИМ в исследовании ISIS 2 (Second International Study of Infarct Survival) [28] применялась КРформа АСК в дозе 162 мг/сут в течение 5 недель. У 4300 больных удалось предотвратить более 100 смертельных исходов. Для предотвращения одного смертельного исхода оказалось необходимым подвергнуть лечению АСК всего 40 больных. Применение препарата сопровождалось почти двукратным снижением частоты нефатальных рецидивов ИМ и ишемического инсульта (рис. 1). По способности снижать риск смерти при ИМ применение этого средства оказалось сопоставимым с тромболитической терапией стрептокиназой, а их сочетанное использование дополнительно влияло на смертность. Более того, 5недельное применение КР АСК не привело к статистически значимому увеличению риска крупных кровотечений (рис. 1) и геморрагического инсульта даже тогда, когда АСК применяли одновременно со стрептокиназой. Разница в смертности в пользу АСК в виде КРформы по сравнению с плацебо сохранялась и при 10летнем наблюдении за больными, участвовавшими в ISIS2 (рис. 2) [29]. Следует отметить, что КРформа АСК не применяется в ургентной ситуации, когда нужна быстрая абсорбция препарата, хотя при разжевывании таблетки и всасывании ее во рту достигается одинаковая с обычной формой абсорбция.
Следует отметить, что в журнале Lancet в 2001 году было опубликовано исследование, в котором было зарегистрировано положительное влияние препарата на смертность [30]. В этом исследовании использовалась КРформа АСК у 4495 человек с хотя бы одним из традиционных факторов риска ИБС (возраст > 65 лет, артериальная гипертония, гиперхолестеринемия, сахарный диабет, ожирение, преждевременное развитие ИМ у ближайших родственников), которые были рандомизированы к приему 100 мг КР АСК или в группу сравнения. За 3,5 года вмешательства среди 2226 пациентов, принимавших АСК, от сердечнососудистых причин умерли 17 человек, а среди 2269 в группе контроля от этих причин умер 31 пациент — снижение риска на 44 % (p < 0,05). Статистически незначимое преимущество в группе АСК было отмечено и по частоте инсультов и транзиторных ишемических атак, ИМ, новых случаев развития стенокардии и периферического атеросклероза. Достигалось это преимущество ценой большей вероятности развития кровотечений, в основном желудочнокишечных: 17 в группе вмешательства и 5 в группе контроля.
В отношении других форм АСК, таких как буферные, растворимые и комбинированные с антацидом, отсутствуют доказательства выживаемости пациентов, которые представлены в отношении КРформы АСК в исследовании ISIS2 и PPP. Почему же не кишечнорастворимые формы применяются в нашей практике? Человечество всегда будет стремиться предложить чтото новое в попытках уменьшить поражение ЖКТ, хотя зачастую данный путь не может увенчаться успехом. В частности, ошибочно утверждение, что добавленный в таблетку гидроксид магния «гасит» соляную кислоту желудка и препятствует местному повреждающему действию АСК. К сожалению, содержание гидроксида магния в подобной таблетке всего 15,2 мг, а известно, что минимальная терапевтическая доза гидроксида магния — 300 мг на прием. Следует добавить также, что комбинация «АСК + антацид» пока еще не была одобрена FDA (Food and Drug Administration).
С какими препаратами у АСК возможно взаимодействие?
— Нестероидные противовоспалительные препараты — повышение риска развития тяжелых желудочнокишечных и нежелудочнокишечных кровотечений и других побочных эффектов.
— Препараты, подщелачивающие мочу (ингибиторы карбоангидразы, цитраты, натрия бикарбонат, антациды, особеннно кальций и/или магнийсодержащие), при длительном использовании — ускорение выведения и снижение эффективности ацетилсалициловой кислоты.
— Антикоагулянты, производные кумарина и индандиона, гепарин, тромболитические препараты (альтеплаза, анистреплаза, стрептокиназа, урокиназа), ингибиторы агрегации тромбоцитов — повышение риска развития кровотечений.
— Цефамандол, цефоперазон, цефотетан, пликамицин, вальпроевая кислота — повышение риска развития кровотечений, токсичности вальпроевой кислоты.
— Метотрексат — усиление токсичности метотрексата.
— Ванкомицин — повышение риска развития ототоксичности.
— Пробенецид, сульфинпиразон — повышение токсичности ацетилсалициловой кислоты.
— Ципрофлоксацин, ломефлоксацин, норфлоксацин, офлоксацин, эноксацин, итраконазол, кетоконазол, тетрациклин — забуференные формы ацетилсалициловой кислоты снижают их всасывание и эффективность. Необходимо разобщить прием во времени.
Таким образом, если мы хотим уменьшить риск развития кровотечения у больного с язвенной болезнью в анамнезе, то сначала необходимо провести тест на Н.pilory, лечение язвенной болезни и назначать АСК совместно с гастропротекторами.
В случае, когда нужно назначить длительную терапию АСК больному без язвенной болезни в анамнезе, препаратом выбора является кишечнорастворимая форма АСК.
В Украине наилучшим фармэкономическим профилем обладает Полокард, который производится и применяется в Европе уже более 70 лет.
1. Expert Consensus Document on the use of antiplatelet agents. The Task Force on the use of antiplatelet agents in patients with atherosclerotic cardiovascular disease of the European Society of Cardiology // Eur. Heart J. — 2004. — 25. — 16681.
2. Hennekens C.H., Karlson L.K., Rosner B. A casecontrol study of regular aspirin use and coronary deaths // Circulation. — 1978. — 58. — 358.
3. Hammond E.C., Garfinkel L. Aspirin and coronary heart disease: findings of a prospective study // Br. Med. J. — 1975. — 2. — 26971.
4. Jick H., Miettinen O.S. Regular aspirin use and myocardial infarction // Br. Med. J. — 1976 May 1. — 1(6017). — 1057.
5. Final report on the aspirin component of the ongoing Physicians’ Health Study. Steering Commitee of the Physicians’ Health Study Research Group // N. Engl. J. Med. — 1989. — 321. — 12935.
6. Peto R., Gray R., Collins R. et al. Randomized trial of prophylactic daily aspirin in British male doctors // Br. Med. J. — 1988. — 296. — 3136.
7. Thrombosis prevention trial: randomised trial of lowintensity oral anticoagulation with warfarin and lowdose aspirin in the primary prevention of ischaemic heart disease in men at increased risk. The Medical Research Council’s General Practice Research Framework // Lancet. — 1998. — 351. — 23341.
8. Hansson L., Zanchetti A., Carruthers S.G. et al. Effects of intensive bloodpressure lowering and low dose aspirin in patients with hypertension: principal results of Hypertension Optimal Treatment (HOT) randomized trial // Lancet. — 1988. — 351. — 176672.
9. Collaborative Group of the Primary Prevention Project. Lowdose aspirin and vitamin E in people at cardiovascular risk: a randomised trial in general practice // Lancet. — 2001. — 357. — 8995.
10. Deepak L. Bhatt et al. ACCF/ACG/AHA 2008 Expert Consensus Document on Reducing the Gastrointestinal Risks of Antiplatelet Therapy and NSAID Use // J. Am. Coll. Cardiol. — 2008. — 52. — 15021517.
11. De Abajo F.J., Garcia Rodriguez L.A. Risk of upper gastrointestinal bleeding and perforation associated with lowdose aspirin as plain and entericcoated formulations // BMC Clin. Pharmacol. — 2001. — 1; 1. — 20.
12. Kelly J.P., Kaufman D.W., Jurgelon J.M., Sheehan J., Koff R.S., Shapiro S. Risk of aspirinassociated major uppergastrointestinal bleeding with entericcoated or buffered product // Lancet. — 1996. — 348. — 1413 1416.
13. Pearson T.A., Blair S.N., Daniels S.R. et al. AHA guidelines for primary prevention of cardiovascular disease and stroke: 2002 update: Consensus Panel Guide to Comprehensive Risk Reduction for Adult Patients Without Coronary or Other Atherosclerotic Vascular Diseases. American Heart Association Science Advisory and Coordinating Committee // Circulation. — 2002. — 106. — 388391
14. Garcia Rodriguez L.A., HernandezDiaz S., de Аbajo F.J. Association between aspirin and upper gastrointestinal complications: systematic review of epidemiologic studies // Br. J. Clin. Pharmacol. — 2001. — 52. — 563571.
15. Mosca L., Banka C.L., Benjamin E.J. et al. Evidencebased guidelines for cardiovascular disease prevention in women: 2007 update // Circulation. —2007. — 115. — 14811501.
16. Hayden M., Pignone M., Phillips C., Mulrow C. Aspirin for the primary prevention of cardiovascular events: a summary of the evidence for the U.S. Preventive Services Task Force // Ann. Intern. Med. — 2002. — 136. — 161172.
17. Sorensen H.T., Mellemkjaer L., Blot W.J. et al. Risk of upper gastrointestinal bleeding associated with use of lowdose aspirin // Am. J. Gastroenterol. — 2000. — 95. — 22182224.
18. Anderson J.L., Adams C.D., Antman E.M. et al. ACC/AHA 2007 guidelines for the management of patients with unstable angina/nonSTelevation myocardial infarction: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the 2002 Guidelines for the Management of Patients With Unstable Angina/NonSTElevation Myocardial Infarction): developed in collaboration with the American College of Emergency Physicians, the Society for Cardiovascular Angiography and Interventions, and the Society of Thoracic Surgeons endorsed by the American Association of Cardiovascular and Pulmonary Rehabilitation and the Society for Academic Emergency Medicine // J. Am. Coll. Cardiol. — 2007. — 50. — e1e157.
19. HernandezDiaz S., Garcia Rodriguez L.A. Cardioprotective aspirin users and their excess risk of upper gastrointestinal complications // BMC Med. — 2006. — 4. — 22.
20. Patrono C., Coller B., Fitzgerald G.A. et al. Platelet — Active Drugs: The Relationships among dose, effective ness, and side effects // The Seventh ACCP Conference of Antithrombotic and Thrombolytic Therapy // Chest. — 2004. — Vol. 126. — 234S264S.
21. Clarke R.J., Mayo G., Price P., Fitzgerald G.A. Suppresion of thromboxane A2 but not systemic prostacyclin by controlledreleased aspirin // N. Engl. J. Med. — 1991. — 325. — 113741.
22. Keimowitz R.M., Pulvermacher G., Mayo G., Fitzgerald D.J. Aspirin and platelets: transdermal modification of platelet function: a dermal aspirin preparation selectively inhibits platelet function; a dermal aspirin preparation selectively inhibits platelet cyclooxygenase and preserve prostacyclin biosynthesis // Circulation. — 1993. — 88. — 55661.
23. Jaszewsky R. Frequency of gastroduodenal lesions in asymptomatic patients on chronic aspirin or nonsteroidal antiinflammatory drug therapy // J. Clin. Gastroenterol. — 1990. — 12. — 103.
24. Walker J., Robinson J., Stewart J. et al. Does entericcoated aspirin result in a lower incidence of gastrointestinal complications compared to normal aspirin? // Interact. Cardiovasc Thorac. Surg. — 2007. — 6(4). — 51922.
25. Cole A.T., Hudson N., Liew L.C. et al. Protection of human gastric mucosa against aspirinenteric coating or dose reduction? // Aliment. Pharmacol. Ther. — 1999. — 13(2). — 18793.
26. Savon J., Allen M.L., Di Marino A.J. Jr et al. Gastrointestinal blood loss with low–dose (325 mg) plain and entericcoated aspirin administration // Am. J. Gastrointerol. — 1995. — 90. — 581.
27. Dietz R., Rauch B. Leitlinie zur Diagnose und Behandlung der chronischen koronaren Herzerkrankung der Deutschen Gesellschaft fr Kardiologie — Herz und Kreislaufforschung (DGK) // Z. Kardiol. — 2003. — 92. — 50121.
28. ISIS2 (Second International Study of Infarct Survival) Collaborative Group: Randomised trial of intravenous streptokinase, oral aspirin, both, or neither among 17,187 cases of suspected acute myocardial infarction: ISIS2 // Lancet. — 1988. — 2. — 34960.
29. Baigent C., Collins R., Appleby P. et al. ISIS2: 10 year survival among patients with suspected acute myocardial infarction in randomized comparision of intravenous streptokinase, oral aspirin, both, or neither // BMJ. — 1998. — 316. — 133743.
30. Collaborative Group of the Primary Prevention Project. Lowdose aspirin and vitamin E in people at cardiovascular risk: a randomised trial in general practice // Lancet. — 2001. — 357. — 8995.

