Газета «Новости медицины и фармации» 4 (445) 2013
Вернуться к номеру
Эпидемиология искусственных эпидемических процессов как третий раздел эпидемиологии
Авторы: Супотницкий М.В., к.б.н., микробиолог, Федеральное государственное бюджетное учреждение «Научный центр экспертизы средств медицинского применения» Министерства здравоохранения Российской Федерации, г. Москва
Рубрики: Инфекционные заболевания
Разделы: Справочник специалиста
Версия для печати
 Цель данной работы — обоснование третьего раздела эпидемиологии — эпидемиологии искусственных эпидемических процессов и других умышленно вызванных биологических поражений (неправильной эпидемиологии). В статье приведены доказательства того, что эпидемиология, этиология и клиника естественных и искусственно вызванных эпидемий (вспышек) и других массовых искусственных поражений населения биологической природы имеют принципиальные отличия. И если не будет своевременно выявлен искусственный характер эпидемии (вспышки) инфекционной болезни, то попытки ее прерывания за счет воздействия на звенья классической триады эпидемического процесса окажутся неэффективными. Поэтому искусственные эпидемические процессы и другие умышленно вызванные биологические поражения должны рассматриваться как самостоятельные объекты эпидемиологического исследования. Неправильная эпидемиология — это система научных знаний, обосновывающих распознание искусственно вызванных вспышек (эпидемий) инфекционных болезней, поражений биологическими токсинами, искусственными генетическими конструкциями и наночастицами, а также устранение (минимизацию) их последствий и оказание содействия правоохранительным органам в выявлении организаций и преступников, осуществивших применение биологических агентов для поражения людей. В отличие от общей и частной эпидемиологии в компетенцию неправильной эпидемиологии не входит предотвращение вспышек (эпидемий) инфекционных болезней и поражений другими биологическими агентами. Их предотвращение является задачей правоохранительных органов.
Цель данной работы — обоснование третьего раздела эпидемиологии — эпидемиологии искусственных эпидемических процессов и других умышленно вызванных биологических поражений (неправильной эпидемиологии). В статье приведены доказательства того, что эпидемиология, этиология и клиника естественных и искусственно вызванных эпидемий (вспышек) и других массовых искусственных поражений населения биологической природы имеют принципиальные отличия. И если не будет своевременно выявлен искусственный характер эпидемии (вспышки) инфекционной болезни, то попытки ее прерывания за счет воздействия на звенья классической триады эпидемического процесса окажутся неэффективными. Поэтому искусственные эпидемические процессы и другие умышленно вызванные биологические поражения должны рассматриваться как самостоятельные объекты эпидемиологического исследования. Неправильная эпидемиология — это система научных знаний, обосновывающих распознание искусственно вызванных вспышек (эпидемий) инфекционных болезней, поражений биологическими токсинами, искусственными генетическими конструкциями и наночастицами, а также устранение (минимизацию) их последствий и оказание содействия правоохранительным органам в выявлении организаций и преступников, осуществивших применение биологических агентов для поражения людей. В отличие от общей и частной эпидемиологии в компетенцию неправильной эпидемиологии не входит предотвращение вспышек (эпидемий) инфекционных болезней и поражений другими биологическими агентами. Их предотвращение является задачей правоохранительных органов.
Современное деление эпидемиологии на общий и частный разделы сложилось более чем 100 лет назад, когда была установлена роль микроорганизмов в развитии эпидемических процессов и еще не существовало угрозы искусственных эпидемий, вызванных применением биологического оружия (БО) или актами биотеррора. Однако за прошедшие годы эпидемические угрозы качественно изменились. Вопервых, начавшаяся в 1930х гг. гонка биологических вооружений дала возможность ряду развитых стран накопить опыт по созданию и применению БО. Вовторых, так называемая «почтовая эпидемия» сибирской язвы, вспыхнувшая осенью 2001 г. в США, показала, что в мире имеются силы, способные профессионально осуществлять биотеррористические акты в рамках стратегий непрямых действий, оставаясь при этом неустановленными1. Втретьих, в настоящее время способы и средства биологического поражения людей по своим возможностям вышли далеко за пределы эпидемических процессов, которые являются объектами изучения общей и частной эпидемиологии. Поэтому цель данной работы состоит в обосновании нового раздела эпидемиологии — эпидемиологии искусственных эпидемических процессов и других умышленно вызванных биологических поражений (неправильной эпидемиологии)2, способного разрабатывать подходы к их распознанию и устранению последствий.
Ограниченность общей и частной эпидемиологии при описании новых средств биологического поражения людей
Биологические поражающие агенты — это кантовская «вещь в себе» (Ding an sich). Обычно специалисты, пишущие на темы биологических угроз, перечисляют в табличной форме десятки микроорганизмов и токсинов, способных вызывать поражения людей (см. работу [7]). Но оценить по формальным признакам потенциальную опасность какогото конкретного из них и сказать, что биологический агент, прописанный под № 5, опасней того, что прописан под № 10, будет серьезным упрощением проблемы противодействия актам биотеррора и биодиверсий. Основное преимущество преступников перед системой здравоохранения и правоохранительными органами государства — фактор внезапности. Именно преступники, сообразуясь с обстоятельствами, будут выбирать время и место совершения преступления. Например, секта раджинишистов, умело используя отсутствие контроля за продуктами в салатбарах города Даллас (штат Орегон, США), добилась инкапситации 751 человека возбудителем сальмонеллеза, не рассматриваемого в качестве потенциального агента БО изза низкой летальности среди заболевших [66]. Возбудитель сибирской язвы вызвал панику в 2001 г. в США не количеством жертв, а уже своим появлением в почтовых рассылках известным политикам и журналистам [25, 41].
На момент подписания ведущими государствами в 1972 г. Конвенции о запрещении разработки, производства и накопления запасов бактериологического (биологического) и токсинного оружия и их уничтожении в качестве биологических поражающих агентов рассматривались только микроорганизмы и бактериальные токсины. Вызываемые ими эпидемические процессы и поражения (токсины) формально попадали в компетенцию общей и частной эпидемиологии. Но за сорок лет ситуация в военной биологии сильно изменилась. К уже имевшимся биологическим агентам добавились принципиально новые, не вызывающие инфекционный процесс (т.е. репликации микроорганизма в организме человека) у человека. Их применение не проявляет себя эпидемиями в их традиционном понимании. К таким биологическим агентам L. Black [16]3 относит искусственные (химерные) генетические конструкции, разрабатывающиеся в рамках технологии соматической генной терапии наследственных и инфекционных болезней, а D.M. Goncalves с соавт. [32] — нанообъекты. Последние авторы заявляют о необходимости формирования новой ветви токсикологии — нанотоксикологии, т.е. науки, изучающей потенциальную опасность наноструктур и наномеханизмов4. Искусственные генетические конструкции и нанообъекты воздействуют на клетку через специфические рецепторы, т.е. обладают биологической специфичностью. Поэтому к биологическим поражающим агентам в настоящее время следует относить не только специально отобранные возбудители инфекционных болезней и вещества биологического происхождения, но и вещества, действующие как молекулы биологического происхождения, способные при умышленном применении вызывать массовые поражения людей, животных и растений.
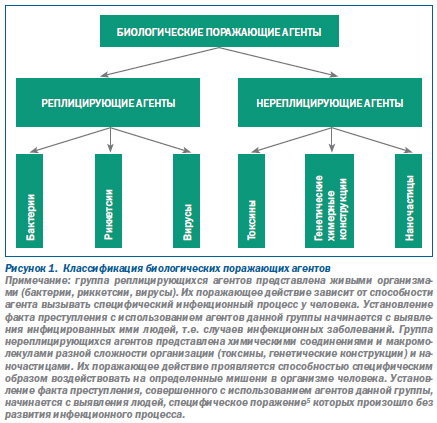
Вследствие этого, как первый шаг к созданию современной классификации биологических поражающих агентов для третьего раздела эпидемиологии, их целесообразно разделить по способности к репликации в организме человека на две группы: реплицирующиеся и нереплицирующиеся агенты. Такая классификация не учитывает «рейтинги» предыдущих, но является удобной для медицинских работников и сотрудников правоохранительных органов при установлении факта совершенного преступления (рис. 1).
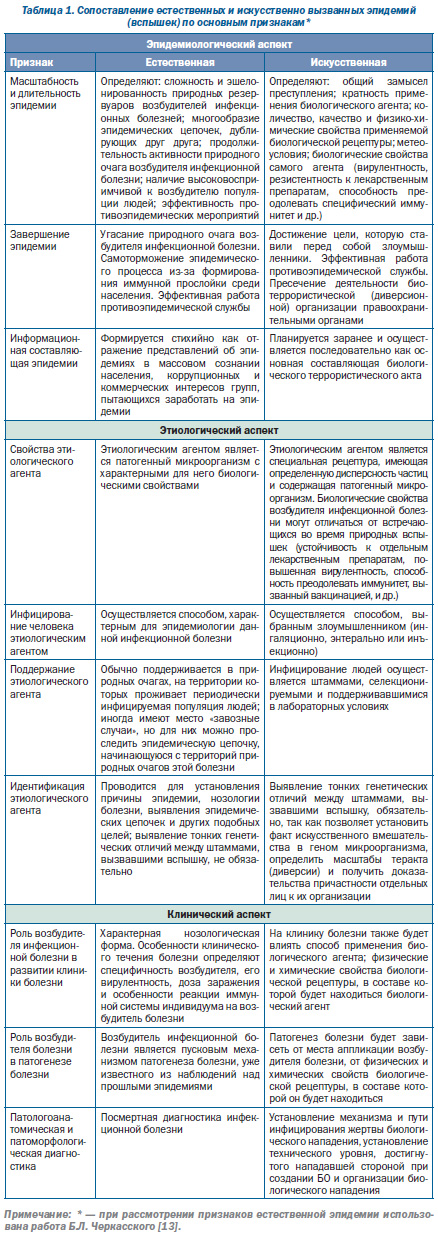
Для понимания объекта, цели и задач неправильной эпидемиологии сопоставим эпидемиологический, этиологический и клинический аспекты искусственных и естественных эпидемий (вспышек) инфекционных болезней (табл. 1).
Эпидемиология искусственных эпидемий (вспышек) и поражений токсинами
Внешнее сходство между естественными и искусственными эпидемическими процессами обнаруживается без особого труда — появление на определенной территории за определенный период времени людей с одним и тем же инфекционным заболеванием, однако единой внутренней логики у них нет. Масштабность и длительность этих процессов зависят от различных факторов. Классическая триада эпидемического процесса предполагает наличие: источника возбудителя инфекции (например, эпизоотии среди диких животных), механизма передачи возбудителя инфекции (наличие инфицированных насекомых, способных паразитировать на людях и животных, например блох, как переносчиков возбудителя чумы от больных чумой крыс к людям) и восприимчивости населения к данной инфекции. Сложная и эшелонированная организация природных резервуаров возбудителей инфекционных болезней, многообразие эпидемических цепочек, дублирующих друг друга, продолжительная активность природного очага возбудителя инфекционной болезни могут превратить естественно возникшую эпидемию в катастрофу. Но выключение (искоренение) любого из факторов эпидемического процесса приводит к его остановке [13]. Уже по этим причинам о механизмах развития искусственного эпидемического процесса, о его структуре, движущих силах, проявлениях и типах нельзя судить на основе представлений о естественном эпидемическом процессе.
Триада при искусственных эпидемических процессах иная. Источником возбудителя инфекционной болезни при применении БО и осуществлении биологических убийств или терактов становятся специальные устройства, разработанные для ведения биологической войны, осуществления биологических убийств и терактов (рис. 2).
При воздушнокапельном инфицировании возбудителем инфекционной болезни в природном очаге, источником инфекции является больной человек. Дисперсность капелек мокроты (200–50 мкм), образующихся при кашле или чихании, не позволяет им распространяться на значительное расстояние от источника. Капли такого размера движутся через воздух (газовую фазу) и быстро оседают. Как правило, заболевают люди, находящиеся в непосредственной близости от больного. Масштабируют вспышки воздушнокапельных инфекций любые факторы внешней среды и санитарного состояния территорий, которые приводят к скученности людей. При применении биологического агента террористами его источником является техническое устройство. Это устройство формирует механизм передачи возбудителя инфекционной болезни — облако частиц мелкодисперсного биологического аэрозоля. Такие частицы движутся вместе с воздухом (газовой фазой), т.е. ведут себя как газ и могут распространяться на значительно большие расстояния, чем капельки мокроты больного человека. Критическую роль в масштабировании вспышки болезни играют совершенно иные факторы, чем при воздушнокапельной инфекции. Прежде всего это: 1) физическая и биологическая устойчивость аэрозоля; 2) дисперсность вдыхаемого человеком аэрозоля (см. ниже); 3) масштабность и кратность биологических атак [8] (рис. 3).
При распространении возбудителя инфекционной болезни или токсина с пищей механизм передачи будет сформирован преступниками в технологической цепочке приготовления продукта. Масштаб и длительность искусственной вспышки инфекционной болезни определяются не только техническими характеристиками источника возбудителя инфекции, но и замыслом самого преступления (рис. 4).
Следовательно, основной особенностью искусственных эпидемических процессов, позволяющей отличать их от природных эпидемических процессов, является их неправильная эпидемиология, т.е. обнаружение случаев инфекционных болезней среди людей при отсутствии в природе условий для их появления [9].
Выявление источника возбудителя инфекции, путей и факторов его передачи начинается с эпидемиологического обследования эпидемического очага. Но понятие «эпидемический очаг» как место пребывания источника возбудителя инфекции (больной человек при кори; больной человек и вши при сыпном тифе; суслики, сурки и мышевидные грызуны, вовлекающиеся в эпизоотии чумы, и блохи, передающие чумную палочку от них в популяции людей) и прилегающая территория, в пределах которой возбудитель инфекции передается к людям (подробно см. [3]), не может быть применено при эпидемиологическом обследовании очагов инфекционных болезней, образовавшихся в результате биологического нападения. В этом случае протяженность очага, его границы будут определяться не особенностями поддержания в природе возбудителя инфекционной болезни и условиями социальнобытовой обстановки в очаге, а техническими возможностями преступников по применению биологических агентов; выбранным ими объектом преступления; моделью территории, на которой совершено биологическое нападение; метеоусловиями в момент применения биологического агента и другими подобными факторами (рис. 5).
Искусственный эпидемический очаг будет локализован с подветренной стороны от возможной точки атаки аэрозолем. Это важная характерная особенность искусственного эпидемического процесса, вызванного однократным ингаляционным применением биологического агента. Полоса поражения6 будет зависеть от способа рассеивания биологических агентов и высоты источника аэрозоля над местностью.
Известны три способа рассеивания биологических агентов [67].
1. Рассеивание точечным источником — предполагает рассеивание аэрозоля стационарным генератором из одной точки.
2. Рассеивание линейным источником — аэрозоль возбудителя инфекционной болезни рассеивается по одной линии либо по множеству линий, «прочерченных» поперек направлению ветра. Например, такими линейными источниками будут установленные или сброшенные с одного или нескольких самолетов (других транспортных средств) источники аэрозоля (бомбы малого калибра или другие диспергирующие устройства). В последнем случае формируется линия небольших точечных источников, которые дают широкую полосу аэрозоля по поверхности земли. Распределение людей, получивших ингаляционное поражение, будет зависеть от высоты линейного источника аэрозоля (рис. 6).
3. Рассеивание многоточечным источником — источники аэрозоля расположены на местности (или над местностью) в произвольном порядке. Каждый из них представляет собой небольшой точечный источник, зона поражения одного источника перекрывается другим.
Эпидемический очаг в общей эпидемиологии считается ликвидированным тогда, когда обезврежен или блокирован источник возбудителя инфекции (обсервация, изоляция, госпитализация заболевших людей); окружающие проверены на носительство возбудителя болезни и свободны от него; в очаге проведены мероприятия по уничтожению возбудителя болезни или переносчиков инфекции (дезинфекция, дезинсекция, дератизация); когда истекает максимальный срок инкубации при данной болезни и среди лиц, общавшихся с больным, нет больше случаев болезни. Для ликвидации же искусственного эпидемического очага этих мер недостаточно. Искусственный эпидемический очаг может возникнуть вновь без всякой связи с природными очагами возбудителя болезни. Появление таких очагов будет продолжаться либо до ликвидации террористической (диверсионной) организации, либо до достижения террористами поставленной цели (рис. 4). Прекращение искусственно вызванной эпидемии (вспышки) или серии убийств с помощью биологического токсина зависит уже не от действий эпидемиологов, а от способности правоохранительных органов обнаружить и ликвидировать террористическую (диверсионную) организацию.
Этиология искусственных эпидемий и поражений токсинами
Даже при одной нозологической форме болезни ее этиология при искусственных и естественных эпидемиях может различаться. Инфицирование людей возбудителем инфекционной болезни при естественно развившихся эпидемиях происходит: трансмиссивно — посредством переносчиков (блохи для возбудителя чумы); контактно — через повреждения кожи и слизистых поверхностей, например при разделке туш животных, погибших от сибирской язвы; алиментарным путем — употребление в пищу продуктов и воды, контаминированных возбудителями кишечных инфекций; воздушнокапельным путем — первичная легочная чума. При любом из перечисленных способов инфицирования человека способность микроорганизма вызывать инфекционный процесс и его летальная доза зависят от его биологических свойств (вирулентность, токсигенность и др.), биологии переносчика, если он присутствует в эпидемической цепочке, и восприимчивости к возбудителю инфекции человека, замкнувшего эпидемическую цепочку.
При ингаляционном применении того же микроорганизма (токсина) его способность вызывать поражение людей будет зависеть прежде всего от физикохимических свойств биологической рецептуры7 и способа ее применения. Именно эти два фактора определяют «полосу свободы» в действиях террористов. Поражение людей сибирской язвой во время «почтовой эпидемии» 2001 г. в США стало возможным благодаря использованию террористами биологической рецептуры, предназначенной для снаряжения кассетных биологических боеприпасов американской армии. После вскрытия конверта рецептура распространялась воздушными потоками по помещениям. Никаким иным способом в условиях существовавших тогда в Конгрессе США мер безопасности вызвать вспышку опасной инфекции среди конгрессменов было невозможно.
Определяют летальную дозу возбудителя инфекционной болезни или токсина не только их биологические свойства, но и глубина проникновения частиц биологического аэрозоля в дыхательные пути человека и их первичное распределение в различных отделах дыхательной системы. Только частицы с размером 1–3 мкм и меньше могут достигнуть альвеол. В альвеолах микроорганизмы фагоцитируются альвеолярными макрофагами и лейкоцитами и вместе с ними или попадают непосредственно в кровеносные капилляры легкого и по ним разносятся по всему организму, или поступают в лимфатические сосуды, оттуда в регионарные лимфатические узлы и далее в грудной проток и венозную кровь (рис. 7).
Экспериментально показано, что если размер частиц аэрозоля увеличивается с 2–3 до 12 мкм, то LD508 для возбудителя чумы повышается в 2,5 раза [27]; для возбудителя сибирской язвы — в 17 раз [26], а для возбудителя бруцеллеза — в 600 раз [28]. Токсичность рицина снижается, если увеличивается средний диаметр аэрозольных частиц. При попадании в трахею рицин высоко токсичен. Но этот же токсин, застрявший в носовых ходах изза большого размера диспергированных частиц, показывает очень низкую токсичность для экспериментальных животных (цит. по [45]).
Врач может столкнуться с тем, что штамм возбудителя инфекционной болезни, использованный для биологического нападения, прошел селекцию в лабораторных условиях. Благодаря этому он оказался способен преодолевать иммунитет, создаваемый коммерческими вакцинами, либо вызванная им болезнь не поддается лечению по типовым схемам9. Ситуация с этиологией болезни еще более запутывается, когда использованный для биологического нападения штамм генетически изменен.
По работе [57] рассмотрим простые эксперименты по получению генетически измененных штаммов возбудителя сибирской язвы и близкородственного ему малопатогенного микроорганизма Bacillus cereus. Ни B.anthracis, ни использованный в работе штамм B.cereus не имеют конъюгативных плазмид. Авторы использовали обнаруженную ими способность плазмид четырех подвидов непатогенной для человека бациллы Bacillus thuringiensis10 мобилизовать неконъюгативные плазмиды для переносов в близкородственные микроорганизмы. Крупные плазмиды B.thuringiensis pXO13, pXO14, pXO15 и pXO16 (их молекулярная масса от 50 до 120 мДа) оказались способными не только передаваться конъюгацией в B.anthracis и B.cereus, но и осуществлять мобилизацию плазмид своих новых хозяев. Вирулентные штаммы возбудителя сибирской язвы дополнительно к хромосоме содержат две крупные плазмиды, включающие гены сибиреязвенного токсина и полимерного вещества капсулы pXO1 и pXO2 соответственно (рис. 8).
Результаты этих экспериментов весьма показательны. Возбудитель сибирской язвы в результате конъюгации получил неконъюгативную плазмиду pBC16 (дорожка 3), придавшую ему устойчивость к антибиотику широкого спектра действия тетрациклину (Tcr), и приобрел способность передавать эту плазмиду в другие штаммы сибиреязвенного микроба (дорожка 4). Сама же pBC16 представляет собой специальный многокопийный вектор для клонирования генов в бациллах. Поэтому ген Tcr только один из возможных генов, которые можно передать сибиреязвенному микробу с помощью этой плазмиды. Не менее интересны результаты передачи конъюгацией pXO2 от B.anthracis к B.cereus (дорожка 7). Получив эту плазмиду от B.anthracis, B.cereus приобрел способность синтезировать важный фактор вирулентности сибиреязвенного микроба — капсулу.
Эксперименты по конструированию генетически измененных вирусов ведутся уже не менее 50 лет в рамках подходов по созданию новых вакцин и инсектицидов. Сравнительно новым подходом в конструировании опасных вирусов стало повышение их вирулентности на основе нарушения регуляции иммунных ответов макроорганизма. Такие эксперименты проводятся под предлогом изучения тонких механизмов иммунных реакций на вирусы, разработки стратегий для контроля аутоиммунных реакций и др. Они основаны не на формальном понимании вирулентности вирусов как функции так называемых генов вирулентности, т.е. чем больше таких генов у вируса, тем больше его вирулентность, и не на прямолинейном вмешательстве в геном вируса, когда его «заставляют» секретировать ген какогото токсина из инфицированной клетки (например, эксперименты по клонированию в вирусах генов нейротоксинов [4, 22]). В основе новых подходов лежит знание тонких механизмов воздействия на систему иммунных ответов организма на вирус во время инфекционного процесса. В качестве примера разберем работу R.J. Jackson с соавт. [40], исследовавших изменение вирулентности вируса мышиной оспы (вирус эктромелии11) после клонирования в его геноме гена интерлейкина4 (IL4)12.
В экспериментах авторы использовали линии мышей двух типов: чувствительных к мышиной оспе (например, BALB/c), у которых болезнь развивается как острая системная инфекция с высокими вирусными титрами в печени и селезенке, обусловливающими некроз и высокую смертность (модель натуральной оспы у человека), и резистентных к мышиной оспе (например, C57BL/6). У последних оспа развивается в субклинической форме и характеризуется низкими уровнями вирусной репликации во внутренних органах и появлением несмертельно опасных поражений.
Генетическая устойчивость мышей к вирусу эктромелии характеризуется эффективной реакцией естественных киллеров (NK) и ранним появлением сильной реакции цитолитических Тлимфоцитов (ЦТЛ) CD8+. R.J. Jackson с соавт. [40] клонировали в геноме вируса эктромелии ген IL4 и изучили влияние экспрессируемого вирусом мышиного IL4 на клеточноопосредованную иммунную реакцию во время инфекции. Ими было отмечено, что у мышей, генетически устойчивых к вирусу эктромелии, экспрессирование IL4 рекомбинантным вирусом эктромелии подавляло цитолитические реакции NK и ЦТЛ и синтез последними гаммаинтерферона. Инфицирование генетически устойчивых мышей модифицированным вирусом эктромелии приводило к развитию у них симптомов острой оспы, сопровождающейся высокой летальностью, подобно заболеванию, наблюдаемому у мышей, генетически чувствительных к этому вирусу.
Продолжение в следующем номере
__________________________________________________
1 Биотеррористический акт, совершенный в 2001 г. в США, не был раскрыт. Как и в случае с убийством президента Джона Кеннеди, ФБР вело следствие «вширь», хотя использованный террористами иммунитетпреодолевающий штамм возбудителя сибирской язвы (vaccineresistant Bacillus anthracis) Ames имелся только в нескольких лабораториях, работавших по программам Министерства обороны США. С 2002 г. в роли подозреваемого проходил микробиолог Стивен Хатфилл (Steven Jay Hatfill), но доказать его причастность к теракту в суде не удалось. В 2003 г. он подал иски против ФБР и Министерства юстиции и отсудил 5,8 млн долларов компенсации («…violating his constitutional rights and for violating the Privacy Act»). В 2008 г. в качестве подозреваемого оказался микробиолог Брюс Айвинс (Bruce Edwards Ivins), но и его вина не была доказана в суде. В июне Брюса нашли в коме в ванной комнате своего дома, отравленного туленолом. Через два дня, не приходя в сознание, он умер от почечной и печеночной недостаточности. После чего федеральный обвинитель, прокурор Джеффри Тэйлор (Geoffrey Taylor) официально заявил, что Брюс совершил самоубийство, и он был единственным преступником, организовавшим биотеррористический акт в 2001 г. Газета New York Times по этому поводу задала вопрос: «А что если бы доктор Хэтфилл совершил самоубийство в 2002 г.? Достаточно ли это было бы для правосудия, чтобы объявить о смерти преступника?»
2 Термины «эпидемиология искусственных эпидемических процессов и других умышленно вызванных биологических поражений» и «неправильная эпидемиология» используются как синонимы.
3 Русский перевод статьи J.L. Black доступен в глобальной сети — http://www.cbio.ru/v5/modules/news/article.php?storyid=1666.
4 Токсиколóгия — это наука, изучающая действие ядовитых (токсичных) веществ на уровне индивидуального организма, но она не изучает токсические поражения как массовый процесс со своими закономерностями и особенностями развития.
5 В данном контексте специфическое поражение — поражение, которое вызвано именно этим фактором, имеющее характерный для действия этого фактора механизм развития и клиникоанатомические проявления.
6 Или, если вернуться к привычной терминологии естественных эпидемических процессов, площадь эпидемического очага.
7 Биологическая рецептура — это многокомпонентная система, содержащая патогенные микроорганизмы (токсины), наполнители и стабилизирующие добавки, обеспечивающие повышение их устойчивости при хранении, применении и нахождении в аэрозольном состоянии. В зависимости от агрегатного состояния рецептуры могут быть сухими или жидкими.
8 LD50 (англ. lethal dose, 50%) — средняя доза вещества, вызывающая гибель половины членов испытуемой группы.
9 Он просто не может быть иным, так как в лабораторных условиях быстро теряет вирулентность при пересевах на искусственных питательных средах.
10 B.thuringiensis используется в сельском хозяйстве в качестве биопестицида.
11 Вирус эктромелии (семейство Pоxviridae, род Orthopoxvirus) является естественным патогеном лабораторных мышей, вызывает у них системную болезнь — мышиную оспу.
12 IL4 относится к лимфоцитарным цитокинам противовоспалительного действия. Ингибирует функции моноцитов, макрофагов и NKлимфоцитов (более подробно о его функциях см. в работах [2, 5]).