Газета «Новости медицины и фармации» Гастроэнтерология (451) 2013 (тематический номер)
Вернуться к номеру
Клинические проявления и особенности течения неспецифического язвенного колита и болезни Крона
Авторы: Элина А.А., Донецкий национальный медицинский университет им. М. Горького
Рубрики: Гастроэнтерология
Разделы: Клинические исследования
Версия для печати
В статье представлены данные об особенностях течения и диагностики неспецифического язвенного колита и болезни Крона. Проведено исследование предрасполагающих факторов возникновения данных заболеваний, а также сравнительная оценка особенностей их клинического течения и дифференциальной диагностики.
неспецифический язвенный колит, болезнь Крона, кишечник, триггерные факторы.
В настоящее время воспалительные заболевания кишечника (ВЗК), в частности неспецифический язвенный колит (НЯК) и болезнь Крона (БК), являются чрезвычайно актуальной и сложной проблемой. По данным Всемирной гастроэнтерологической организации (WGO), по тяжести течения, частоте осложнений и летальности данная патология в подавляющем большинстве стран занимает одно из ведущих мест в структуре болезней желудочнокишечного тракта (ЖКТ) [6]. При этом заболеваемость ВЗК непреклонно растет и составляет на сегодняшний день, по данным разных авторов, 30–240 случаев на 100 тыс. жителей для НЯК и 10–150 случаев для БК [2, 11, 16]. Среди причин возникновения НЯК и БК выделяют генетическую предрасположенность, инфекционные, иммунологические факторы, однако до сих пор ни одна из приведенных теорий не была подтверждена [1, 7, 8, 10]. Ряд авторов утверждает о несомненной роли предрасполагающих факторов в манифестации и/или обострении данной патологии [4, 13, 16]. Изза отсутствия четких представлений об этиопатогенезе ВЗК лечение их разработано недостаточно, часто является малоэффективным и несет значительные экономические затраты.
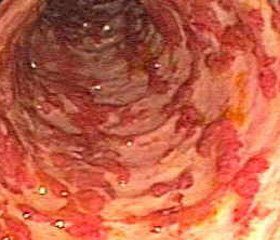
Диагностика НЯК и БК также вызывает трудности в связи с многообразием клинических проявлений, включающих поражение не только кишечника, но и других органов и систем. Клинические симптомы широко варьируют в зависимости от локализации и протяженности поражения, активности заболевания, наличия или отсутствия осложнений [2, 3, 15]. Кроме того, врачи часто сталкиваются с проблемой дифференциальной диагностики НЯК и БК, имеющих похожую клиническую картину при отсутствии патогномоничных лабораторных и иммунологических маркеров. Даже эндоскопическое исследование кишечника порой не дает однозначного ответа о наличии той или иной патологии, и единственным подтверждающим диагностическим методом остается морфологическое исследование биоптата. Целью нашего исследования было изучение предрасполагающих факторов возникновения НЯК и БК, а также оценка особенностей их клинического течения и дифференциальной диагностики.
Материалы и методы
Под нашим наблюдением находились 80 больных с подтвержденным диагнозом ВЗК за период с 2005 по 2012 год. Из них 51 (63,8 %) больной с НЯК и 29 (36,2 %) — с БК. По половому признаку больные распределены следующим образом: 43 (53,8 %) мужчины и 37 (46,2 %) женщин в возрасте от 17 до 78 лет, из которых 61 (76,3 %) пациент трудоспособного возраста. Исследования проводились на базах гастроэнтерологического отделения ЦГКБ № 3 и инфекционного отделения № 5 ЦГКБ № 1 г. Донецка.
Исследование включало в себя динамическое клиническое обследование больных ВЗК со сбором жалоб, анамнеза заболевания и жизни. Анализировались жалобы, характерные для НЯК и БК, такие как частота и консистенция стула, кишечное кровотечение, наличие патологических примесей в кале, абдоминальные боли с уточнением их характера и локализации, что ежедневно фиксировалось больными в дневниках. Оценка объективного статуса пациентов проводилась согласно общепринятым методам пальпации, перкуссии и аускультации, включая осмотр перианальной области для оценки изменений в перианальной зоне, а также пальцевое исследование прямой кишки с обязательным проведением эндоскопического исследования. В последующем осуществлялось проспективное наблюдение, в процессе которого изучались характер клинического течения НЯК и БК, регистрировались его осложнения и исходы.
Тщательно изучались возможные предрасполагающие факторы развития ВЗК, такие как курение, прием лекарственных препаратов (антибиотики, НПВС, глюкокортикоиды, оральные контрацептивы), нарушение режима и характера питания, профессиональные вредности, заболевания ЖКТ у близких родственников и аллергологический анамнез.
Все пациенты проходили комплексное лабораторное обследование — общие анализы крови и мочи, биохимический анализ крови с определением уровня глюкозы, СРБ, общего билирубина и его фракций, печеночных трансаминаз, креатинина и мочевины, общего белка.
Первоначально выявляемая клиническая картина заболевания в виде частого кашицеобразного или жидкого стула требовала исключения инфекционной природы процесса, поэтому всем больным с данной симптоматикой (67 (83,8 %) пациентов) проводилось бактериологическое исследование кала на патогенные кишечные инфекции.
Протяженность поражения толстого кишечника при НЯК и локализацию воспалительного очага при БК определяли при проведении фиброколоноскопии (ФКС). Ведущим методом диагностики патологии тонкой кишки являлось рентгенологическое исследование (пассаж бария по ЖКТ) — с целью исключения фистулизирующей и стенозирующей формы БК. В некоторых случаях терминальный отдел подвздошной кишки удавалось осмотреть эндоскопом при ФКС. Кроме того, так как данное заболевание может поражать любой отдел ЖКТ, у пациентов с диспептическими проявлениями (боль/дискомфорт в эпигастрии, чувство переполнения после еды и др.) в комплекс обследования также входила фиброэзофагогастродуоденоскопия (ФЭГДС) — 9 (31,0 %) больных [1, 3, 11]. Для диагностики внекишечных проявлений ВЗК и сопутствующей патологии использовались данные ультразвукового исследования (УЗИ) органов брюшной полости (ОБП) — 55 (68,8 %) пациентов. При необходимости индивидуально определялись показания к КТ ОБП с интестинальным контрастированием — 3 (3,8 %) больных.
У всех пациентов диагноз был подтвержден морфологически при изучении биоптатов или операционного материала стенки пораженной кишки.
Для проведения анализа были использованы методы биостатистики [9]. Частота встречаемости качественных признаков представлена в виде % ± стандартная ошибка (m%). При проведении сравнения частоты встречаемости использовался критерий хиквадрат [9]. Расчеты проводились в статистическом пакете MedStat (Лях Ю.Е., Гурьянов В.Г., 2004–2012 гг.).
Результаты исследования и их обсуждение
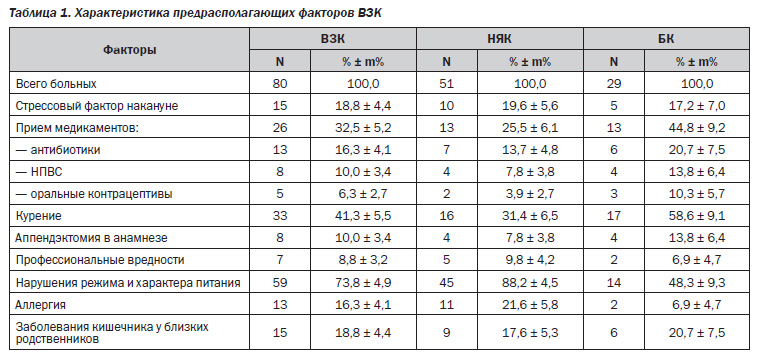
Данные, характеризующие влияние возможных негативных стимулов на ВЗК, представлены в табл. 1.
Исходя из полученных сведений, видно, что наибольшая численность больных ВЗК (59 (73,8 %) пациентов) имели погрешности в питании. Это проявлялось в первую очередь в нерегулярном приеме пищи в связи с неудовлетворительными условиями труда, а также в частом употреблении некачественных продуктов и различных пищевых аллергенов (кофе, цитрусовые, шоколад, рыбные изделия и др.), что может пересекаться с аллергологической теорией развития ВЗК [4]. При этом количество больных с НЯК было выше, чем с БК, и составило 45 (88,2 %) пациентов против 14 (48,3 %). Таким образом, можно предположить, что нарушение режима и характера питания имеет большее значение у больных с НЯК.
Оценивая роль курения в качестве триггерного фактора, установлено, что более половины всех обследованных пациентов с БК составили лица курящие или курившие ранее — 17 (58,6 %). При НЯК такие больные не были столь многочисленны и выявлены в 16 (31,4 %) случаях из 51. Различие является статистически значимым (р = 0,032) и может говорить о том, что курение является фактором риска развития БК, что согласуется с литературными данными [8, 15].
Широкое распространение в настоящее время получило бесконтрольное применение медикаментов (антибиотики, НПВС, оральные контрацептивы) — один из возможных факторов роста заболеваемости ВЗК [4, 8]. Наше исследование показало, что 26 (32,5 %) из всех больных ВЗК указывали на прием лекарственных средств по различным причинам, из которых антибиотики принимали 13 (16,3 %) пациентов, НПВС — 8 (10,0 %), а оральные контрацептивы — 5 (6,3 %) больных. Следует отметить, что в процентном отношении больные с БК, принимающие медикаменты, превышали таковых с НЯК во всех группах, что может указывать на более значительную роль данного предрасполагающего фактора именно в развитии БК. Тем не менее статистически значимых различий данных показателей не выявлено (p = 0,127), что требует дальнейшего исследования.
По нашим данным, следующим по значимости у пациентов с ВЗК являлись стрессовая ситуация, перенесенная незадолго до проявлений заболевания и/или его рецидива, а также патология кишечника у членов семьи. Последнее включало в себя различные воспалительные и функциональные заболевания тонкого и толстого кишечника, хронические запоры, синдром диареи, перенесенные инфекционные заболевания кишечника, а также патологию прямой кишки. Указанные предрасполагающие факторы наблюдались с одинаковой частотой и составили по 15 (18,8 %) больных каждый. При этом стресс перенесли 10 (19,6 %) пациентов с НЯК и 5 (17,2 %) — с болезнью Крона, а наследственная предрасположенность несколько чаще определялась у больных БК — в 6 (20,7 %) случаях из 29, чем у обследуемых с НЯК, составивших 9 (17,6 %) наблюдений из 51.
В литературе большое внимание уделяется аллергологической теории возникновения ВЗК, согласно которой поступление в организм различных аллергенов и токсинов приводит к формированию иммунологических сдвигов с развитием дисбаланса регуляции цитокинов и аутоагрессии. В качестве триггеров в данном случае могут выступать бытовые, пыльцевые, биологические, промышленные и другие аллергены, включая пищевые [4, 5, 16]. Собирая аллергологический анамнез у наших больных, выяснили, что различными формами аллергии страдают 13 (16,3 %) пациентов с ВЗК, из них у 11 (21,6 %) диагностирован НЯК, а у 2 (6,9 %) — БК, что характеризует некоторое преобладание аллергических реакций у больных с неспецифическим язвенным колитом, однако статистически значимых различий не выявлено (р = 0,163), и для окончательного ответа требуется проведение более обширного исследования.
Взаимосвязи перенесенной аппендэктомии и наличия профессиональных вредностей с возникновением ВЗК у обследованных нами пациентов также не обнаружено.
Проанализировав данные табл. 1, видим, что в целом у больных с ВЗК прослеживается связь между воздействием определенных предрасполагающих факторов и развитием заболевания, причем негативные стимулы при НЯК несколько отличаются от таковых при БК.
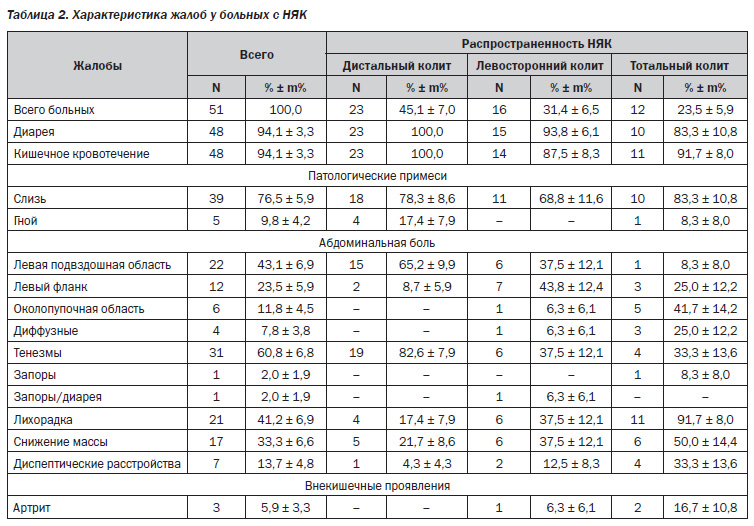
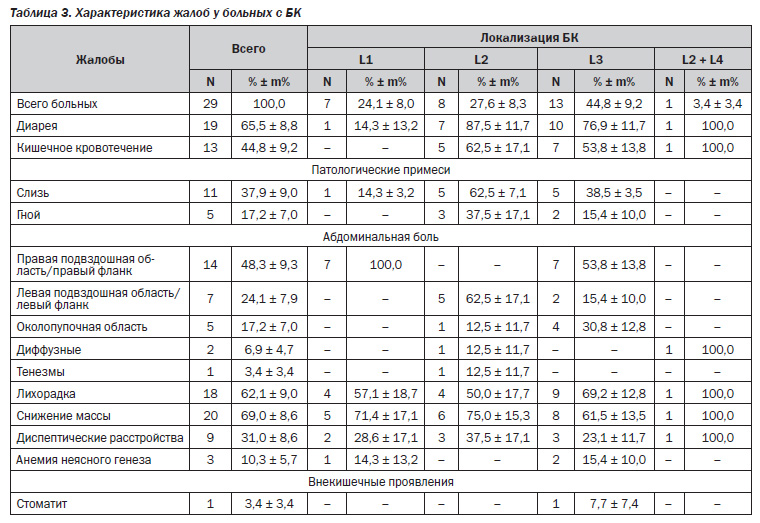
Изучая зависимость клинической картины от распространенности НЯК и локализации БК, были получены данные, представленные в табл. 2, 3.
Как следует из табл. 2, наиболее часто у больных НЯК встречался дистальный колит — 23 (45,1 %) пациента, у 16 (31,4 %) был выявлен левосторонний НЯК, а тотальный язвенный колит обнаружен у 12 (23,5 %) обследуемых, что соответствует общей тенденции, полученной другими авторами [4, 15].
При любой протяженности поражения кишечника наиболее распространенными жалобами являлись диарея и кишечное кровотечение — по 48 (94,1 %) пациентов, а также примесь слизи в кале, наблюдаемая у 39 (76,5 %) обследуемых. Так, упорные поносы зафиксированы у всех больных с дистальным колитом, у 15 (93,8 %) — с левосторонним НЯК и у 10 (83,3 %) — с тотальным поражением ободочной кишки. Кишечное кровотечение различной степени выраженности при дистальной форме НЯК отмечали также все больные — 23 (100 %), при более обширной распространенности данное проявление заболевания наблюдалось у 14 (87,5 %) обследуемых пациентов с левосторонним и у 11 (91,7 %) — с тотальным колитом.
Необходимо отметить, что важным симптомом НЯК, особенно при проведении дифференциальной диагностики с функциональными заболеваниями кишечника, являются тенезмы. Они представляют собой ложные позывы к дефекации, заканчивающиеся, как правило, отхождением газов, малоизмененной крови и патологических примесей. Тенезмы всегда свидетельствуют о воспалительном процессе в толстой кишке и, по данным литературы, характерны чаще для поражения ее дистальных отделов [1, 12, 14]. Исходя из результатов нашего исследования, тенезмы беспокоили 19 (82,6 %) пациентов с дистальным НЯК, 6 (37,5 %) больных с левосторонним колитом и 4 (33,3 %) — с вовлечением всей ободочной кишки. Различие между группами является статистически значимым (p = 0,003), что доказывает преобладание данного симптома у пациентов с проктитом или проктосигмоидитом и не противоречит мнению других авторов.
Абдоминальная боль — еще один важный симптом у больных НЯК, ее характер и локализация широко варьируют в зависимости от протяженности патологического процесса и тяжести заболевания [5, 14]. Анализ локализаций абдоминальной боли при разной распространенности НЯК показал следующее. Для больных с дистальным колитом наиболее характерными оказались боли в левой подвздошной области, их отметили 15 (65,2 %) пациентов из 23, имеющихся в данной группе. Больные с левосторонним НЯК практически одинаково часто жаловались на боли в левом фланке живота (7 (43,75 %) пациентов) и в левой подвздошной области, что составило 6 наблюдений (37,5 %). И с равной частотой — по 1 случаю из 16 (6,25 %) — на боли в околопупочной области и диффузные по всему животу. Тотальное поражение ободочной кишки чаще ассоциировалось с жалобами на боли в околопупочной области — 5 (41,7 %) наблюдений, реже — с локализациями по левому фланку и всему животу — по 3 (25,0 %) случая. У 1 (8,3 %) больного в данной группе была отмечена локализация абдоминальной боли в левой подвздошной области.
Такие не характерные для НЯК жалобы, как запоры или их чередование с диареей, беспокоили 1 (8,3 %) пациента с тотальным колитом и 1 (6,3 %) — с левосторонним.
Кишечные симптомы у части больных НЯК сопровождались лихорадкой у 21 (41,2 %) обследуемого, в 17 (33,3 %) случаях — снижением массы тела. Несмотря на то, что различия между указанными показателями по группам не были статистически значимыми (р = 0,066), наблюдалась тенденция к увеличению частоты встречаемости данных проявлений в зависимости от обширности поражения кишечника. Так, повышение температуры тела было зафиксировано у 6 (26,1 %) больных с дистальным колитом, у 7 (43,8 %) — с левосторонним НЯК и в 8 (66,7 %) из 12 случаев тотального поражения. На потерю веса указывали 5 (21,7 %) пациентов с дистальной формой заболевания, а в двух других группах данный симптом отмечали 6 (37,5 %) больных. Системные внекишечные проявления в виде артрита беспокоили 3 (5,9 %) пациентов с НЯК, из которых у 2 (16,7 %) выявлена распространенная форма колита, а у 1 (6,25 %) больного — левостороннее поражение.
Таким образом, наблюдается связь между такими клиническими проявлениями НЯК, как абдоминальные боли (р = 0,005), тенезмы (р = 0,003), повышение температуры тела (р < 0,001) и распространенность воспалительного процесса. Кроме того, наличие тех или иных симптомов может служить основанием для выбора рациональной диагностической программы с целью уточнения распространенности заболевания и, как следствие, подбора оптимальных лекарственных форм.
Согласно табл. 3, по локализации воспалительного очага при БК получены следующие данные. Сочетанное поражение толстого и тонкого кишечника L3 доминировало и встречалось у 13 (44,8 %) обследованных пациентов. Изолированные изменения толстой кишки L2 диагностированы у 8 (27,6 %) больных, а терминальный илеит L1 выявлен у 7 (24,1 %) из 29 пациентов с БК. Поражение типа L2 + L4 c локализацией процесса в желудке и ободочной кишке зафиксировано в 1 (3,4 %) случае. При этом в группе L1 самой распространенной жалобой являлась абдоминальная боль с локализацией в правой подвздошной области, наблюдаемая у всех больных. Боли имели преимущественно давящий характер и усиливались после еды. Реже, но гораздо чаще по сравнению с другими жалобами, пациенты отмечали снижение массы тела и температурную реакцию: 5 (71,4 %) и 4 (57,1 %) больных соответственно. Диарейный синдром с примесью слизи в кале наблюдался лишь в 1 (14,3 %) из 7 наблюдений, а кишечное кровотечение не было выявлено ни у одного обследуемого пациента с формой L1.
При изолированном поражении толстой кишки L2, в свою очередь, была характерна клиническая картина диареи в 7 (87,5 %) из 8 случаев, с патологическими примесями в кале в виде слизи у 5 (62,5 %) больных и гноя — у 3 (37,5 %) пациентов. Кроме того, такой симптом, как кишечное кровотечение, у больных данной группы являлся довольно распространенным и диагностирован у 5 (62,5 %) пациентов. Наиболее частая локализация абдоминальной боли при данном поражении — левая подвздошная область и левый фланк — составляет 5 (62,5 %) наблюдений. Достоверно реже у больных БК с формой L2 встречались боли в околопупочной области и диффузные по всему животу: по 1 (12,5 %) случаю. Приблизительно так же часто, как и при терминальном илеите, пациенты с колитом жаловались на повышение температуры и потерю веса: соответственно 4 (50,0 %) и 6 (75,0 %) обследуемых. Среди всех пациентов с БК тенезмы беспокоили 1 (12,5 %) больного с толстокишечной локализацией воспалительного очага.
При сочетанном поражении подвздошной и ободочной кишки важное значение имели как кишечные симптомы, так и проявления интоксикационного синдрома. Так, диарея беспокоила 10 (76,9 %) из 13 больных, а кишечное кровотечение наблюдалось у 7 (53,8 %) пациентов. Патологические примеси в кале прослеживались реже, чем при форме L2 БК: 5 (38,5 %) больных отмечали примесь слизи, а 2 (15,4 %) указывали на выделение гноя при дефекации. Абдоминальная боль локализовалась в большинстве случаев в правой подвздошной области и правом фланке — 7 (53,8 %) обследованных больных, 4 (30,8 %) пациента отмечали боли в околопупочной области, в остальных 2 (15,4 %) наблюдениях — в левом фланке живота. Ведущей жалобой больных данной группы являлась также лихорадка различной степени выраженности: от субфебрильной до пиретической при высокой активности БК, наблюдаемая в 9 (69,2 %) случаях. Кроме того, большая часть пациентов (8 (61,5 %)) указывали на снижение веса.
Клиническое течение БК с локализацией в ободочной кишке и желудке, диагностируемое у 1 больного, сочетало в себе жалобы пациентов с L2формой, такие как нарушение стула, кишечное кровотечение, общие симптомы интоксикации, а также диспептические явления, проявляющиеся тошнотой, изредка рвотой и болью в эпигастральной области. В отличие от изолированного поражения ободочной кишки, у больного с формой L2 + L4 не выявлены патологические примеси в кале, а боль в животе имела диффузный характер.
Среди всех обследованных пациентов с БК у 3 (10,3 %) наблюдалась анемия неясного генеза, 2 (15,4 %) из которых имели сочетанное поражение толстого и тонкого кишечника, а у 1 (14,3 %) воспалительный процесс локализовался в дистальном отделе подвздошной кишки. Генез данной анемии требует уточнения. По всей видимости, она обусловлена эндогенной интоксикацией или синдромом мальабсорбции. Кроме этого, у 1 (7,7 %) больного с формой L3 выявлено поражение ротовой полости (афтозный стоматит). Зафиксированные у 7 (13,7 %) больных с НЯК и у 9 (31,1 %) с БК диспептические расстройства, по всей видимости, являются клиническими проявлениями интоксикационного синдрома, а в некоторых случаях — сопутствующих заболеваний.
Исходя из данных табл. 2, 3, видно, что по сравнению с НЯК диарея и кровь в кале при БК встречались значительно реже (р < 0,001), особенно у пациентов с поражением тонкой кишки. В свою очередь, для больных БК более характерными являлись симптомы эндотоксемии, такие как лихорадка и потеря веса, наблюдаемые у большей половины пациентов (р = 0,005). Тенезмы, довольно распространенный симптом среди обследованных с НЯК, при БК практически не наблюдались.
Проанализировав результаты исследования жалоб, предъявляемых больными с ВЗК, можно отметить, что, несмотря на несомненную схожесть клинической картины НЯК и БК, каждому из данных заболеваний присущи свои характерные особенности, которые позволяют в первую очередь нацелить врача на наличие у пациента данной патологии, а затем определить правильную нозологическую форму. Тем не менее необходимо отметить, что у каждого пациента с ВЗК диагноз должен быть верифицирован эндоскопически и морфологически.
Выводы
Несмотря на значительный прогресс в понимании этиопатогенеза и клинических проявлений воспалительных заболеваний кишечника, их диагностика и лечение остаются актуальной проблемой современной гастроэнтерологии. Схожая клиническая картина НЯК и БК, агрессивное хроническирецидивирующее течение и развитие угрожающих жизни осложнений требуют дальнейшего изучения предрасполагающих факторов их развития. Кроме того, высокая распространенность системных проявлений ВЗК вызывают интерес смежных специалистов к данной патологии. Следовательно, разработка новых диагностических подходов с целью улучшения качества жизни и выживаемости пациентов с ВЗК является крайне необходимой.
1. Белоусова Е.А. Язвенный колит и болезнь Крона. — Тверь: Триада, 2002. — 128 с.
2. Ливзан М.А., Макейкина М.А. Воспалительные заболевания кишечника: современные аспекты диагностики и лечения // Гастроэнтерология. — 2012. — № 2.
3. Григорьева Г.А., Мешалкина Н.Ю. Болезнь Крона. — М.: Медицина, 2007. — 184 с.
4. Дорофеев А.Э., Звягинцева Т.Д., Харченко Н.В. Заболевания кишечника. — Горловка: Ліхтар, 2010. — 532 с.
5. Неспецифічний виразковий коліт: стандарти діагностики та лікування (методичні рекомендації) / Бойко Т.Й., Сімонова О.В. — Київ, 2009. — 43 с.
6. Практические рекомендации Всемирной гастроэнтерологической организации. Воспалительная болезнь кишечника: глобальные перспективы. Июнь 2009.
7. Стан імунорегуляції та імунний компонент синдрому ендогенної інтоксикації у хворих на неспецифічний виразковий коліт і хворобу Крона / О.О. Крилова, Т.Й. Бойко, В.Є. Кудрявцева та ін. // Запорожский медицинский журнал. — 2005. — № 3. — С. 104106.
8. Халиф И.Л., Лоранская И.Д. Воспалительные заболевания кишечника (неспецифический язвенный колит и болезнь Крона): клиника, диагностика и лечение. — М.: Миклош, 2004. — 88 с.
9. Петри А., Сэбин К. Наглядная статистика в медицине: Пер. с англ. В.П. Леонова. — М.: ГЭОТАРМедиа, 2003. — 144 с.
10. Ahmad T., Satsangi J., McGovern D. et al. The genetics of inflammatory bowel disease // Aliment. Pharmacol. Ther. — 2001. — 15(6). — 731748.
11. Consensus on the diagnosis and management Crohn’s disease // J. Crohn’s&Colitis. — 2010. — Vol. 4/1. — P. 2962.
12. Inflammatory bowel diseasefrom bench to bedside / Еd. by S. Targan, S. Shanahan, L. Karp — 2nd ed. — London: Kluwer Academic publishers, 2002. — Р. 60530.
13. Rogala L., Miller N., Graff L.A., Rawsthorne P. Populationbased controlled study of social support, selfpercieved stress, activity and work issues, and access to health care in inflammatory bowel disease // Inflamm. Bowel. Dis. — 2008.
14. Sartor R.B., Sandborn W.J. Kirsner’s Inflammatory bowel disease. — London: Saundrs, 2004. — 754 p.
15. Satsangi J., Sutherland L.R. Inflammatory Bowel Disease. — Elsevier, 2003. — 792 p.
16. Update on Crohn’s disease and ulcerative colitis // Expert Rev. Gastroenterol. Hepatol. — 2011. — 5(3). — 311314.