Газета «Новости медицины и фармации» Гастроэнтерология (478) 2013 (тематический номер)
Вернуться к номеру
Метеоризм — легкий дискомфорт или серьезная гастроэнтерологическая проблема?
Рубрики: Гастроэнтерология
Разделы: Справочник специалиста
Версия для печати
25 апреля 2013 г. в Одессе по инициативе Одесского отделения Украинской гастроэнтерологической ассоциации и при поддержке Ассоциации медицинского образования Украины состоялся научнопрактический семинар «Клиникотерапевтическая парадигма абдоминальной боли, метеоризма и стеатогепатоза в практике терапевта и гастроэнтеролога». Наряду с украинскими учеными с докладами выступили гости из СанктПетербурга д.м.н., профессор кафедры хирургической гепатологии, руководитель курса гастроэнтерологии Юрий Павлович Успенский и к.м.н. Балукова Екатерина Владимировна (СПбГМУ им. акад. И.П. Павлова).
В ходе семинара были рассмотрены такие актуальные вопросы, как лечение алкогольной и неалкогольной болезни печени, СРК, хронического панкреатита. Особое внимание было уделено проблеме метеоризма, которую рассмотрел в докладе «Метеоризм — это легкий дискомфорт или серьезная гастроэнтерологическая проблема?» проф. Ю.П. Успенский.
В начале своего выступления проф. Ю.П. Успенский процитировал М.М. Зощенко: «Ну, заболел. Подумаешь, беда какая. Пухнет, видите ли, у него живот и дышать трудно. Ну, потерпи! Ну, бутылку с горячей водой приложи к брюху…» («Медик», 1926 г.).
И тут же опроверг классика, сообщив, что проблема метеоризма значительно серьезнее, чем может показаться на первый взгляд.
Метеоризм — избыточное скопление газа в желудочнокишечном тракте вследствие его повышенного образования или нарушения выведения, проявляющееся срыгиванием, отрыжкой воздухом, ощущениями переполнения, вздутия живота с увеличением его окружности, урчанием в кишечнике, учащением пассажа (флатуленцией) кишечных газов.
Необходимость диагностики и лечения синдрома метеоризма определяется:
— ролью метеоризма как клинического маркера нарушенного кишечного пищеварения и дисбиоза кишечника (экзокринная панкреатическая недостаточность, дисбиоз кишечника и др.);
— усугублением клинических проявлений метеоризма в периоды психоэмоционального напряжения, смены климатических и временных поясов, изменения характера питания и др.);
— крайне негативным влиянием метеоризма на социальное поведение, семейные, общественные обязанности и взаимоотношения больного;
— неизбежным снижением качества жизни независимо от причины, вызвавшей развитие метеоризма.
Докладчик подчеркнул, что в основе дисбиоза кишечника лежат нарушения его микробиоты, и провел экскурс в историю лечения инфекционных болезней с применением антибиотикотерапии.
До начала ХХ века инфекционные болезни являлись основной причиной смертности и небольшой средней продолжительности жизни людей. По данным на конец ХІХ века, 51 % случаев смертности в России были вызваны инфекционными заболеваниями. Поэтому естественным было стремление найти средства борьбы с их возбудителями.
В ходе Крымской войны (1854–1855 гг.) потери русской армии убитыми составили около 30 тысяч человек, а умершими от ран — около 16 тысяч. Таким образом, суммарные боевые потери для России составили 46 тысяч человек. Смертность от болезней была значительно больше. В русской армии от болезней умерло 88 755 русских. Всего же в Крымскую войну небоевые безвозвратные потери в 2,2 раза превышали боевые.
Однако в ХХ веке с открытием пенициллина и созданием различных антибиотиков ситуация в корне меняется. И по состоянию на 1980 г. в России только в 2 % случаев причиной смертности являются инфекционные заболевания. Однако возникает новая проблема, связанная с неконтролируемым потреблением антибиотиков в мире.
Только в России в настоящее время используется свыше 30 фармакологических групп АМП, из которых порядка 200 являются оригинальными препаратами, а генериков в десятки раз больше. При этом высок удельный вес дешевых устаревших препаратов с низким профилем безопасности, таких как доксициклин, левомицетин и т.п.
По данным Американского колледжа врачей, 64 % назначений АМП в стационарах являются необоснованными. В странах Евросоюза ежегодно потребляется 13 200 т АМП, из этого количества 1/3 используется в ветеринарии, в том числе так называемые «кормовые» АМП — стимуляторы роста домашних животных.
В исследовании Marine Pollution Bulletin (2006) был проведен анализ сточных вод, в результате которого было обнаружено:
— наличие 26 видов антибиотиков и устойчивых к ним бактерий, попадающих в канализацию с человеческими фекалиями;
— уровень фармацевтических препаратов в канализации резко возрастает по утрам, во время пользования туалетами;
— антибиотики понизили эффективность «родственных бактерий», используемых при обработке сточных вод.
Неоднократное и повторяющееся воздействие различных антибактериальных средств изменило микробиоту человека, особенно в индустриально развитых странах.
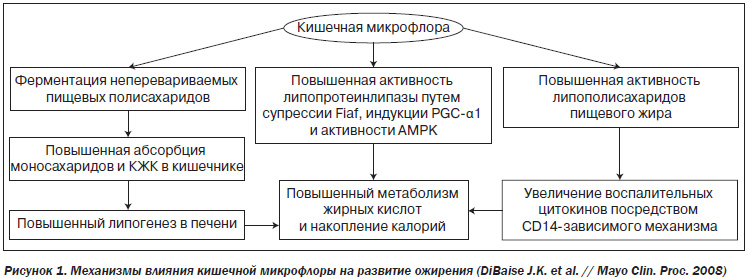
Данные, полученные в лаборатории НьюЙоркского университета, свидетельствуют о том, что изменения кишечной микрофлоры после приема антибиотиков являются во многом необратимыми. Это может приводить к значительному увеличению риска возникновения таких заболеваний, как ожирение, диабет, аллергия, астма и другие (D. Blaser, 2010).
По данным International Obesity Task Force за период 2002–2007 гг., ИМТ превышает 30 кг/м2:
— в Японии — у 15 % населения;
— в Швейцарии, Болгарии, Италии, Франции, Испании — у 20 %;
— в Германии, Финляндии, Великобритании — у 30 %;
— в России — около 25–30 %;
— в Румынии — у 40 %;
— в США — у более 50 % населения.
Нарушения микробиоты кишечника (дисрегуляция выработки факторов воспаления, гормонов, интерлейкинов) являются определяющим фактором в патогенезе расстройств, ассоциированных с метаболическим синдромом (HenaoMejia J. et. al. // Nature. 2012 Feb.).
Еще И.И. Мечников писал, что многочисленные ассоциации микробов, населяющих кишечник человека, в значительной мере определяют его духовное и физическое здоровье.
Далее проф. Ю.П. Успенский перечислил симптомы и проявления, характерные для каждой степени дисбиоза кишечника.
При дисбиозе I степени (компенсированном) наблюдаются следующие изменения в микрофлоре: снижение количества бифидобактерий, лактобактерий или и тех и других вместе на 1–2 порядка; снижение до 80 % или повышение содержания кишечных палочек с проявлением небольших титров их измененных форм. При этом клинически дисбактериоз проявляется в изменении аппетита, метеоризме, неустойчивом стуле, неравномерной окраске каловых масс.
При дисбиозе кишечника II степени (субкомпенсированном) отмечается наличие одного вида условнопатогенных микроорганизмов в концентрации не выше 105 или ассоциации условнопатогенных бактерий в небольших титрах. При этом наблюдаются боли в животе, диспептические расстройства: отрыжка, изжога, чувство распирания после приема пищи, усиление метеоризма, увеличение выраженности диареи, синдром гиповитаминоза, спорадические аллергические реакции с изменением кожных покровов.
Дисбиоз кишечника III степени (декомпенсированный) характеризуется высоким титром условнопатогенных микроорганизмов как одного вида, так и в ассоциациях, выделением патогенных микроорганизмов. Его симптомами являются повышение температуры, озноб, головная боль, слабость, синдром желудочнокишечной диспепсии, боли в животе, усиливающиеся до схваткообразных, синдром трофических расстройств, угроза развития септических состояний.
Отмечена обратная взаимосвязь повышения частоты метеоризма со снижением уровня бифидобактерий, уровнем E.coli с нормальной ферментативной активностью, а также прямая — с повышением уровня стафилококков.
В условиях дисбиоза происходит повышенное газообразование; развиваются мальдигестия и мальабсорбция, в результате чего повышается концентрация пенообразователей (белки, жиры, желчные кислоты, мукополисахариды, слизь, мыла и др.), нарушается кишечная моторика.
В результате бактериального метаболизма выделяются:
— водород (Н2) — Bacteroides clostridiformis, Fusobacterium necrophorum, Escherichia coli, Citrobacter spp., Enterobacter spp. и другие;
— метан (СН4) — Methanobrevibacter smithii, Methanospaere stadmamiae;
— аммиак (NH3) — Bacteroides fragilis;
— сероводород (Н2S) — анаэробы;
— углекислый газ (СО2) — аэробы и анаэробы.
По данным Saltzman, Sieker (1968), в норме 65–70 % кишечного газа экзогенного происхождения, 30–35 % — эндогенного. Причинами образования кишечных газов являются заглатывание воздуха (аэрофагия); диффузия из крови (N2); образование газа в просвете кишечника (бактериальный метаболизм). Они эвакуируются через пищевод, путем отрыжки воздухом, через кишечник — путем флатуленции (0,5–1,5 л/сут за 13–15 пассажей).
Заглатываемый воздух составляет около 70 % газа, содержащегося в ЖКТ. За одно глотательное движение в результате аэрофагии в желудок попадает около 2–3 мл воздуха. Факторами, влияющими на увеличение объема заглатываемого воздуха, являются разговоры во время еды, торопливое проглатывание пищи, жевание жевательной резинки, гиперсаливация, сухость слизистой полости рта.
Кишечные газы представляют собой пену, состоящую из множества мелких пузырьков, окруженных слоем вязкой слизи, изза которой нарушаются процессы абсорбции газов кишечной стенкой, что приводит к формированию порочного круга и увеличению интенсивности пенообразования.
Клиническими проявлениями синдрома метеоризма являются:
— ощущение вздутия живота;
— увеличение окружности живота;
— повышенное отхождение газов через заднепроходное отверстие (флатуленция);
— дистанционное урчание в кишечнике;
— боль (ощущение распирания) в животе по ходу толстой кишки;
— одышка и нарушение сердечной деятельности;
— психические расстройства, коморбидные соматическим проявлениям.
У больных с СРК метеоризм отмечается в 85 % случаев. Другими симптомами заболевания являются боли в животе (96 % случаев), нарушение моторики кишечника (81 %), запоры/поносы (65 %).
Условием формирования висцеральной гиперчувствительности является воздействие сенсибилизирующих факторов (кишечная инфекция, психосоциальный стресс, физическая травма), ассоциированных с абдоминальной болью. У больных с СРК нарушен процесс нисходящего подавления восприятия боли, т.е. имеется центральная антиноцицептивная дисфункция (Thompson W.G., Longstreth G.F., Drossman D.A., Heaton K.W., Irvine E.J., MullerLissner S.A. Functional bowel disorders and functional abdominal pain. Rome II: A Multinational Consensus Document on Functional Gastrointestinal Disorders // Gut, 1999; 45(Suppl. II): 11438).
Растяжение кишки избыточно образующимся газом (метеоризм) у лиц с висцеральной гиперчувствительностью является одной из ведущих составляющих формирования болевого абдоминального синдрома.
Синдром метеоризма диагностируется на основании клиникоанамнестических, физикальных, рентгенологических (повышенная пневматизация желудка и толстой кишки, высокое стояние диафрагмы, особенно левого ее купола) данных.
Методами его лечения являются:
— соблюдение диетических рекомендаций (коррекция пищевых предпочтений с устранением или ограничением продуктов, вызывающих метеоризм, и формирование адекватного пищевого поведения с целью устранению аэрофагии);
— применение этиопатогенетической терапии (устранение моторноэвакуаторных кишечных расстройств, нормализация частоты и консистенции стула, замещение нарушенной внешнесекреторной функции поджелудочной железы (полиферментная терапия — пангрол и др.)); коррекция дисбиоза кишечника — нитрофурановые препараты, пробиотики; психофармакотерапия в целях купирования психических расстройств;
— симптоматическая терапия.
Препаратами выбора в коррекции дисбиоза кишечника являются антибактериальные средства нитрофуранового ряда, среди которых можно назвать нифурател (Макмирор). Показаниями к его применению являются хронические заболевания верхних отделов желудочнокишечного тракта, ассоциированные с H.pylori (особенно эффективен в отношении штаммов H.pylori, устойчивых к метронидазолу), кишечные инфекции, обусловленные кишечным амебиазом или лямблиозом; вульвовагинальные инфекции, вызванные чувствительными к препарату возбудителями (кандида, трихомонады, бактерии, хламидии).
Макмирор лишен тех недостатков, которыми обладает фуразолидон:
— гепато, нейро и гематотоксичность;
— способность подавлять рост сапрофитной флоры кишечника;
— побочные эффекты (при приеме этого препарата многие пациенты жалуются на горечь во рту, тошноту, рвоту);
— высокая кратность приема — четыре раза в день.
Во многих странах мира фуразолидон запрещен к применению (Италия, Япония и т.д.), а в тех странах, где разрешен, курс терапии составляет не более 5–7 дней по причине тератогенных свойств препарата.
Стандартами Научного общества гастроэнтерологов России (НОГР) Макмирор рекомендован в составе первой и второй линии эрадикационной терапии.
В регионах, где резистентность H.pylori к кларитромицину более 20 %, следует рекомендовать Макмирор в дозе 200 мг 2 раза в день в течение 7–14 дней.
Междисциплинарные стандарты приняты Х съездом НОГР в 2010 г. Для терапии первой линии разработаны следующие рекомендации:
1. ИПП в стандартной дозе (20–40 мг), амоксициллин (1000 мг 2 раза в день или 500 мг 4 раза в день) в сочетании с кларитромицином (500 мг 2 раза в день), или джозамицином (1000 мг 2 раза в день), или Макмирором (нифурателом) (400 мг 2 раза в день) в течение 10–14 дней.
2. ИПП в стандартной дозе (20–40 мг), амоксициллин (1000 мг 2 раза в день или 500 мг 4 раза в день) в сочетании с кларитромицином (500 мг 2 раза в день), или джозамицином (1000 мг 2 раза в день), или Макмирором (нифурателом) (400 мг 2 раза в день) и висмута трикалия дицитрат (240 мг 2 раза в день или 120 мг 4 раза в день в течение 10–14 дней.
3. При наличии атрофии слизистой оболочки желудка и ахлоргидрии, подтвержденной рНметрией: амоксициллин (1000 мг 2 раза в день или 500 мг 4 раза в день) в сочетании с кларитромицином (500 мг 2 раза в день), или джозамицином (1000 мг 2 раза в день), или Макмирором (нифурателом) (400 мг 2 раза в день) и висмута трикалия дицитрат (240 мг 2 раза в день или 120 мг 4 раза в день) в течение 10–14 дней.
В доказательство эффективности и безопасности применения Макмирора Ю.П. Успенский привел результаты исследования, в котором была дана сравнительная оценка эффективности и безопасности эрадикации при использовании Макмирора (нифуратела) в различных схемах антихеликобактерной терапии.
В исследовании приняли участие 67 пациентов (26 мужчин и 41 женщина) с хроническим гастродуоденитом, ассоциированным с Helicobacter pylori, подтвержденным эндоскопическим и морфологическим методом. Средний возраст участников составлял 48,0 ± 10,6 года. Пациенты были разделены на три группы в соответствии с используемой схемой лечения.
Пациенты первой группы (24 человека) принимали висмута трикалия дицитрат 240 мг 2 раза в день 28 дней, амоксициллин 1000 мг и нифурател (Макмирор) 400 мг 2 раза в сутки в течение 10 дней. Пациенты второй группы (23 человека) — омепразол 20 мг, кларитромицин 500 мг и нифурател (Макмирор) 400 мг 2 раза в сутки в течение 10 дней. Третья группа (20 человек): омепразол 20 мг, амоксициллин 1000 мг и кларитромицин 500 мг 2 раза в сутки в течение 10 дней.
До и после лечения всем пациентам проводился комплекс тестов для верификации H.pylori: быстрый уреазный тест, гистологическое исследование и полимеразная цепная реакция, бактериологическое исследование кала с целью оценки частоты встречаемости такого побочного эффекта эрадикационной терапии, как дисбиоз кишечника.
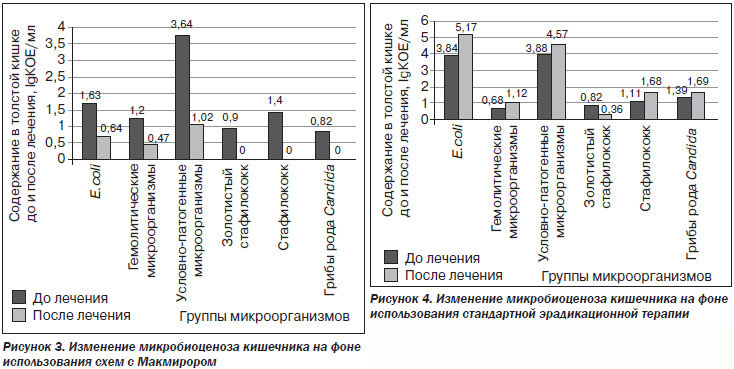
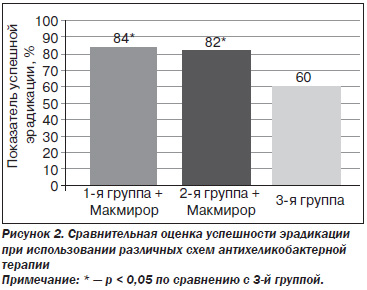
Сравнительная оценка результатов применения различных схем антихеликобактерной терапии показала, что в первой группе успешная эрадикация была достигнута в 84 % случаев, во второй — в 82 %, а в третьей (без применения Макмирора) — в 60 %.
Также было отмечено изменение микробиоценоза кишечника. На фоне терапии препаратом Макмирор отмечался рост титра бифидобактерий и лактобацилл.
Также докладчик упомянул о недавних исследованиях, которые касаются взаимодействия H.pylori и грибов рода Candida. В них дрожжеподобные микромицеты рассматриваются в качестве переносчиков H.pylori. К такому мнению ученые пришли, определив наличие генов, специфических для H.pylori, в дрожжеподобных грибах, содержащихся в ротовой полости (Siavoshi F. еt al., 2008). Эволюционно выработанные симбиотические взаимоотношения между H.pylori и дрожжеподобными грибами были описаны R. Malekzadeh et al. (AIM, 1998).
Candida spp. часто обнаруживается в молочных продуктах: в мороженом и творожных сырках — в 78,6 % проб, в сметане — в 75 %, в твороге — в 66,6 %, в кефире — в 35,3 %, в простокваше — в 28,6 %, в молоке — в 11,9–20 % проб (Реброва Р.Н., 1989).
Однако это не означает, что все эти продукты нужно исключить из употребления. Для макроорганизма с высокой иммунореактивностью вероятно транзиторное кандидоносительство, в определенных условиях развитие кандидозного дисбиоза. В случае пониженной иммунореактивности наблюдается устойчивая колонизация слизистых оболочек Candida, возможно развитие неинвазивного кандидоза — кандидозного дисбиоза кишечника (патологический процесс в просвете кишечника). Происходит резорбция эндотоксина гриба, возникают сенсибилизация, интоксикация, вторичный иммунодефицит. Низкий уровень иммунореактивности чреват развитием инвазивного кандидоза, кандидозного колита, кандидосепсиса, кандидемии (по данным исследования О.К. Хмельницкого, М.А. Шевякова).
В группу риска развития кандидоза входят пациенты с физиологическими иммунодефицитами, генетически детерминированными иммунодефицитами, СПИДом, онкологическими заболеваниями, аллергическими и аутоиммунными болезнями, заболеваниями эндокринной системы. Также его развитие возможно при нутрициологических и «криптогенных» иммунодефицитах, в период прохождения антибактериальной терапии, во время «истощающих заболеваний», стрессов, при трансплантации.
Единственным АМП (неантимикотическим средством!), к которому чувствительны грибы рода Candida, является Макмирор, что также составляет ценное преимущество препарата.
При симптоматической терапии синдрома раздраженного кишечника препаратом выбора является эспумизан, механизм действия которого основан на ослаблении поверхностного натяжения пузырьков газа в пищеварительном тракте, приводящем к их разрыву и последующему выведению из организма. Эспумизан специально разработан для лечения повышенного газообразования, вздутия живота и урчания в кишечнике, действует по всему ходу ЖКТ, поэтому может применяться как при желудочной (отрыжки, желудочный пневматоз), так и при кишечной (собственно метеоризм) диспепсии. Также достоинствами препарата являются возможность длительного применения, полное отсутствие побочных эффектов, влияния на рН ЖКТ. Препарат не всасывается в кишечнике, не замедляет и не ускоряет всасывание других веществ, не кумулируется и не способствует кумуляции, характеризуется быстрым действием и превосходной совместимостью. Эспумизан подходит для любых возрастных групп начиная с раннего детского возраста — сироп с фруктовым запахом для детей, капсулы для взрослых.