Международный неврологический журнал 2 (64) 2014
Вернуться к номеру
Цитиколин: механизм действия и клиническая эффективность при лечении ишемического инсульта, хронических цереброваскулярных расстройств и травматического повреждения головного мозга
Авторы: Савустьяненко А.В. - Донецкий национальный медицинский университет, кафедра фармакологии
Рубрики: Неврология
Разделы: Справочник специалиста
Версия для печати
Цитиколин — ноотропное лекарственное средство, которое проявляет нейропротективную и нейрорепаративную активность, улучшает волновую активность головного мозга. В исследованиях было показано, что цитиколин эффективен и безопасен при лечении ишемического инсульта в остром и подостром периоде, которое начинается, как правило, в течение первых 24 ч после развития инсульта и продолжается не менее 6 недель. Это приводит к уменьшению объема очага инсульта, смертности и частоты инвалидизации больных и, кроме того, увеличивает вероятность полного выздоровления спустя 3 месяца после инсульта. Больным рекомендуется продолжать прием цитиколина на последующих этапах реабилитации (в течение 6 месяцев — 1 года после инсульта), поскольку это вносит дополнительный вклад в улучшение их когнитивных функций. Была продемонстрирована эффективность и безопасность цитиколина при лечении хронических цереброваскулярных расстройств у пожилых лиц (улучшение памяти и поведения) и травматического повреждения головного мозга (уменьшение отека мозга, более быстрое восстановление сознания, восстановление памяти и двигательных функций в большем объеме). Однако полученные выводы нуждаются в подтверждении в более крупных исследованиях.
Цитиколін є ноотропним лікарським засобом, що проявляє нейропротективну й нейрорепаративну активність, покращує хвильову активність головного мозку. У дослідженнях було показано, що цитиколин є ефективним та безпечним при лікуванні ішемічного інсульту в гострому й підгострому періоді, яке починається, як правило, протягом перших 24 годин після розвитку інсульту й триває не менше 6 тижнів. Це приводить до зменшення об’єму вогнища інсульту, смертності й частоти інвалідизації хворих і, крім того, збільшує ймовірність повного одужання через 3 місяці після інсульту. Хворим рекомендується продовжувати прийом цитиколіну на наступних етапах реабілітації (протягом 6 місяців — 1 року після інсульту), тому що це робить додатковий внесок у поліпшення їх когнітивних функцій. Була продемонстрована ефективність та безпечність цитиколіну при лікуванні хронічних цереброваскулярних розладів у літніх осіб (поліпшення пам’яті й поведінки) і травматичного ушкодження головного мозку (зменшення набряку мозку, більш швидке відновлення свідомості, відновлення пам’яті й рухових функцій у більшому обсязі). Однак отримані висновки потребують підтвердження в більш великих дослідженнях.
Citicoline is nootropic drug that exhibits neuroprotective and neuroreparative activity, improves brain wave activity. Studies have shown that citicoline is effective and safe in the treatment of ischemic stroke in the acute and subacute period, and this treatment usually begins within the first 24 hours after stroke onset and lasts for at least 6 weeks. This leads to a reduction in infarction focus volume, mortality and disability rate of patients and, furthermore, increases the probability of complete recovery in 3 months after the stroke. Patients are recommended to continue taking citicoline at subsequent stages of rehabilitation (for 6 months — 1 year after stroke), as it makes an additional contribution to improving their cognitive functions. It was demonstrated the efficacy and safety of citicoline in the treatment of chronic cerebrovascular disorders in the elderly (improved memory and behavior) and of traumatic brain injury (decreased cerebral edema, a more rapid recovery of consciousness, memory and motor function recovery at a higher level). However, the findings need to be confirmed in larger studies.
цитиколин, ишемический инсульт, хроническое цереброваскулярное расстройство, травматическое повреждение головного мозга.
цитиколін, ішемічний інсульт, хронічний цереброваскулярний розлад, травматичне ушкодження головного мозку.
citicoline, ischemic stroke, chronic cerebrovascular disorder, traumatic brain injury.
Статья опубликована на с. 115-120
Введение
Цитиколин (цитидиндифосфатхолин, ЦДФ-холин) является мононуклеотидом, в состав которого входят рибоза, цитозин, пирофосфат и холин. В организме его основная роль сводится к участию в синтезе структурных фосфолипидов клеточных мембран, что имеет особое значение для нормального функционирования нервной ткани. Кроме того, цитиколин является экзогенным источником ацетилхолина — одного из ключевых медиаторов нервной системы [1]. Цитиколин был идентифицирован Kennedy и коллегами в 1955 г., синтезирован в 1956 г. и с тех пор активно исследуется как перспективное лекарственное средство для терапии неврологических расстройств [2]. В настоящем кратком обзоре мы представили накопленные к сегодняшнему дню данные о механизмах действия цитиколина и его эффективности и безопасности при лечении ишемического инсульта, хронических цереброваскулярных расстройств и травматического повреждения головного мозга.
Механизм действия
Нейропротекция
Цитиколин защищает мембраны нервных клеток от повреждения
Нервные клетки используют холин с двумя целями: для синтеза ацетилхолина, являющегося нейромедиатором, и фосфатидилхолина, являющегося структурным компонентом их клеточных мембран. Если ацетилхолина недостаточно, то биохимические процессы поворачиваются вспять: фосфатидилхолин высвобождается обратно из клеточных мембран, распадается до холина и становится источником синтеза медиатора. При этом мембраны повреждаются, что влечет за собой гибель клеток. Этот процесс получил название «аутоканнибализм». Спасительным в этих условиях является назначение цитиколина, поскольку ацетилхолин будет синтезироваться из холина, содержащегося в препарате, а клеточные мембраны, а следовательно и клетки, останутся целыми [3].
В дополнение к этому было продемонстрировано, что цитиколин увеличивает синтез сфингомиелина, еще одного компонента клеточных мембран, и кардиолипина, входящего в состав внутренней мембраны митохондрий [3].
Цитиколин снижает уровень «плохих» медиаторов и повышает уровень «хороших»
Известно, что одним из механизмов повреждения клеток при неврологических расстройствах является эксайтотоксичность — высвобождение в больших количествах возбуждающих медиаторов (глутамата и др.), приводящих к гибели нейронов. В связи с этим было показано, что цитиколин ингибирует высвобождение глутамата, защищая нервные клетки [4].
Выше были описаны процессы, благодаря которым цитиколин повышает содержание в мозге ацетилхолина — ключевого медиатора, играющего важную роль в обучении и памяти. Помимо этого, цитиколин увеличивает содержание в мозге допамина. Это осуществляется двумя путями: как за счет увеличения синтеза медиатора путем стимуляции тирозингидроксилазы, так и за счет уменьшения его обратного захвата. Допамин, высвобождаемый черной субстанцией, имеет важное значение в двигательном контроле [5].
Цитиколин ингибирует перекисное окисление липидов
Одним из механизмов повреждения нейронов при развитии неврологических заболеваний является перекисное окисление липидов. В ходе этого процесса активные формы кислорода атакуют клеточные мембраны, вызывая их повреждение.
Было выяснено, что цитиколин ингибирует перекисное окисление липидов посредством нескольких механизмов. Препарат способен прямо снижать образование одной из активных форм кислорода — гидроксильных радикалов (НО*) [6]. Кроме того, он увеличивает содержание в мозге одного из основных антиоксидантов — глутатиона и повышает активность глутатионредуктазы (фермент, восстанавливающий активную форму глутатиона) [3]. Наконец, как было отмечено выше, цитиколин предотвращает распад фосфатидилхолина, что препятствует высвобождению из него свободных жирных кислот. Последние, после воздействия на них радикалов кислорода, сами становятся активными радикалами и усиливают перекисное окисление липидов [7].
Цитиколин препятствует накоплению бета-амилоида
Одно из основных патоморфологических проявлений болезни Альцгеймера — накопление b-амилоидных бляшек в ткани мозга. Было показано, что повышение содержания фосфатидилхолина в клеточных мембранах приводит к уменьшению образования патологических бляшек [8].
Нейрорепарация
Было выяснено, что цитиколин, помимо нейропротективных эффектов, также усиливает нейрорепарацию. В частности, было показано, что он:
— ингибирует апоптоз за счет уменьшения экспрессии прокаспаз;
— стимулирует ангиогенез посредством влияния на пути регуляции, включающие ERK1/2 и инсулин-рецепторный субстрат-1;
— усиливает нейрогенез, о чем свидетельствовало увеличение количества BrdU/NeuN-экспрессирующих клеток;
— усиливает глиогенез, что проявлялось увеличением пролиферации и дифференцировки астроглиальных клеток;
— усиливает синаптогенез, что подтверждалось –усложнением ветвления дендритов и увеличением плотности шипиков дендритов;
— влияет на модуляцию нейротрансмиттеров, поскольку увеличивает количество NMDA-рецепторов.
Все эти эффекты были аналогичны тем, которые вызывают стволовые клетки [4].
Влияние на волновую активность
Цитиколин обращает нарушения в электрическом паттерне головного мозга, выявляемые на электроэнцефалограмме. Возрастные когнитивные расстройства обычно сопровождаются увеличением активности дельта-, тета- и быстрых бета-волн, в то время как альфа- и медленная бета-активность снижается. В то же время в исследованиях цитиколин снижал выраженность первых и увеличивал долю вторых упомянутых волн [8].
Клиническое применение
Цитиколин эффективен и безопасен при ишемическом инсульте
Острый и подострый периоды инсульта
В Корее было проведено постмаркетинговое наблюдательное исследование [9, 10], включавшее пациентов с острым ишемическим инсультом (n = 4191). Среди них 3736 пациентов получали перорально цитиколин (500–4000 мг/день) в течение первых 24 ч после развития инсульта, 455 пациентов — в срок > 24 ч после начала болезни. Длительность лечения составляла не менее 6 недель. В результате исследования было обнаружено, что в эти сроки наблюдалось улучшение всех оцениваемых показателей, включая значение по краткой версии шкалы NIHSS, индекс Бартел и значение по модифицированной шкале Ранкина (p < 0,05). Профиль переносимости цитиколина был оценен как хороший: лишь у 31 пациента (0,73 %) наблюдалось 37 побочных эффектов, среди которых наиболее часто встречались головная боль (n = 3), симптомы со стороны желудочно-кишечного тракта (n = 5), системное кровотечение (n = 4) и осложнения, связанные с инсультом (n = 8).
A. Dбvalos и соавт. [11] с помощью баз данных MEDLINE, Cochrane и Ferrer Group bibliographic database выявили рандомизированные контролируемые исследования, в которых цитиколин назначался перорально пациентам с ишемическим инсультом. Данные этих исследований были объединены и проанализированы как единый массив. В результате было установлено, что спустя 3 месяца полное выздоровление наблюдалось у 25,2 % пациентов в группе цитиколина и 20,2 % в группе плацебо (отношение шансов (ОШ) 1,33; 95% доверительный интервал (ДИ) 1,10–1,62; p = 0,0034). Таким образом, был сделан вывод, что терапия цитиколином, инициированная в течение первых 24 ч после развития умеренного и тяжелого ишемического инсульта и продолжавшаяся 6 недель, увеличивает вероятность полного выздоровления спустя 3 месяца наблюдения.
Был выполнен также метаанализ 10 рандомизированных контролируемых исследований [10, 12], включавший 2279 пациентов с ишемическим и геморрагическим инсультом. Цитиколин назначали в срок до 24 ч — 14 дней после развития инсульта, лечение продолжали от 10 дней до 6 недель. В результате было установлено, что лечение цитиколином приводило к достоверному снижению смертности и частоты инвалидизации по сравнению с плацебо (57,0 по сравнению с 67,5 %; ОШ 0,64; 95% ДИ 0,54–0,77; p < 0,001). В анализ –безопасности были включены все исследования, в которых сообщалось о смертельных исходах по состоянию на конец периода наблюдения. Достоверных различий по частоте побочных эффектов между цитиколином и плацебо получено не было: цитиколин — 179/1235 (14,5 %), плацебо — 135/966 (14,0 %; ОШ 0,99; 95% ДИ 0,77–1,21; p < 0,94).
Отдельного внимания заслуживает тот факт, что при объединении данных диффузионно-взвешенной магнитно-резонансной томографии из двух исследований было обнаружено дозозависимое снижение объема очага инсульта при лечении цитиколином [13].
Эффективность на этапах реабилитации
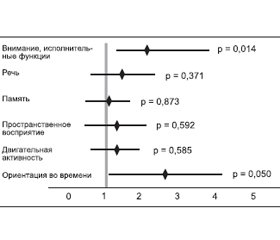
Бlvarez-Sabнn and Romбn предприняли исследование [14, 15], направленное на оценку эффективности и бе-зопасности цитиколина на этапах реабилитации после инсульта. В исследование было включено 347 пациентов, которым в течение 24 ч после развития инсульта назначали 2000 мг/день цитиколина в течение 6 недель. Затем половина из этих пациентов (172 пациента — 49,6 %) продолжили принимать 1000 мг/день цитиколина в течение 12 месяцев. Остальные пациенты лечение не получали. В результате было выяснено, что у пациентов, не принимавших цитиколин, спустя 6 месяцев наблюдались более выраженные когнитивные нарушения в таких доменах, как внимание и исполнительные функции (ОШ 1,725; 95% ДИ 1,090–2,729; p = 0,019) и ориентация во времени (ОШ 1,728; 95% ДИ 1,021–2,927; p = 0,042). Спустя 12 месяцев были зафиксированы аналогичные результаты (рис. 2). Таким образом, назначение больным цитиколина на этапах реабилитации после инсульта дает им дополнительные преимущества по сравнению с пациентами, не получающими такое лечение. Авторы отметили, что в ходе исследования не было отмечено достоверных различий между группами в отношении безопасности лечения.
/010/010_2.jpg)
Оптимальная доза
В вышеупомянутом обобщенном анализе данных из разных исследований, выполненном A. Dбvalos и соавт. [11], была предпринята попытка оценить оптимальную дозу цитиколина для лечения пациентов с ишемическим инсультом. Среди трех протестированных доз — 500, 1000 и 2000 мг/день — наиболее эффективной оказалась доза 2000 мг/день (рис. 3).
/010/010_3.jpg)
Роль цитиколина в лечении хронических цереброваскулярных расстройств у пожилых лиц
Нам удалось идентифицировать один метаанализ, в котором оценили эффективность и безопасность цитиколина при лечении хронических церебральных расстройств у пожилых лиц [16]. В него было включено 13 рандомизированных контролируемых исследований из базы данных Specialized Register of the Cochrane Dementia and Cognitive Improvement Group, которые были опубликованы до 20 января 2004 г. Все исследования были гетерогенны по дозе цитиколина, длительности лечения, критериям включения пациентов и оцениваемым исходам. Результатом метаанализа стало установление того факта, что цитиколин оказывает достоверное положительное влияние на функции памяти и поведения у данной группы пациентов. При этом не было зафиксировано достоверных эффектов в отношении внимания. Препарат хорошо переносился. Авторы указывают на необходимость проведения более длительных исследований применения цитиколина для лечения хронических церебральных расстройств у пожилых пациентов с диагнозом, выставленным на основе современных диагностических критериев.
Роль цитиколина в лечении травматического повреждения головного мозга
Начиная с 1960-х гг. было проведено несколько небольших когортных исследований и рандомизированных исследований эффективности цитиколина при травматическом повреждении головного мозга, степень которого варьировала от травматической комы до посткоммоционного синдрома. Опубликованные данные этих исследований указывают на положительное влияние цитиколина, включающее ускорение снятия отека мозга, более быстрое восстановление сознания, уменьшение периода госпитализации, восстановление памяти и двигательных функций в большем объеме, улучшение качества жизни. Однако приведенные исследования являются, как правило, одноцентровыми и не строго спланированными, поэтому их достоверность должна быть подтверждена в дальнейших работах [12, 17].
Выводы
1. Цитиколин — ноотропное лекарственное средство, которое проявляет нейропротективную и нейрорепаративную активность, улучшает волновую активность головного мозга. Нейропротекция сводится к защите клеточных мембран, снижению содержания «плохих» и повышению уровня «хороших» медиаторов, торможению перекисного окисления липидов и предотвращению накопления бета-амилоидов. Об усилении нейрорепарации свидетельствует способность цитиколина ингибировать апоптоз, стимулировать ангиогенез, нейрогенез, глиогенез, синаптогенез и влиять на модуляцию нейротрансмит-теров.
2. Цитиколин эффективен и безопасен при лечении ишемического инсульта в остром и подостром периодах, которое начинается, как правило, в течение первых 24 ч после развития инсульта и продолжается не менее 6 недель. Это приводит к уменьшению объема очага инсульта, смертности и частоты инвалидизации больных и, кроме того, увеличивает вероятность полного выздоровления спустя 3 месяца после инсульта. Больным рекомендуется продолжать прием цитиколина на последующих этапах реабилитации (в течение 6 месяцев — 1 года после инсульта), поскольку это вносит дополнительный вклад в улучшение их когнитивных функций.
3. Накопленные данные свидетельствуют об эффективности и безопасности цитиколина при лечении хронических цереброваскулярных расстройств у пожилых лиц (улучшение памяти и поведения) и травматического повреждения головного мозга (уменьшение отека мозга, более быстрое восстановление сознания, восстановление памяти и двигательных функций в большем объеме). Однако исследователи отмечают необходимость проведения более крупных исследований для того, чтобы сделать полученные выводы окончательными.
1. Citicoline induces angiogenesis improving survival of vascular/human brain microvessel endothelial cells through pathways involving ERK1/2 and insulin receptor substrate-1 / Krupinski J., Abudawood M., Matou-Nasri S. et al. // Vasc. Cell. — 2012. — V. 4, № 20. — doi: 10.1186/2045-824X-4-20.
2. Grieb P. Neuroprotective properties of citicoline: facts, doubts and unresolved issues // CNS Drugs. — 2014. — V. 28, № 3. — P. 185-193.
3. Adibhatla R.M., Hatcher J.F., Dempsey R.J. Citicoline: neuroprotective mechanisms in cerebral ischemia // J. Neurochem. — 2002. — V. 80, № 1. — P. 12-23.
4. Бlvarez-Sabнn J., Romбn G.C. The Role of Citicoline in Neuroprotection and Neurorepair in Ischemic Stroke // Brain Sci. — 2013. — V. 3. — P. 1395-1414.
5. Qureshi I., Endres J.R. Citicoline: A Novel Therapeutic Agent with Neuroprotective, Neuromodulatory, and Neuroregenerative Pro-perties // Natural Medicine Journal. — 2010. — V. 2, № 6. — P. 11-25.
6. Citicoline // Alternative Medicine Review. — 2008. — V. 13, № 1. — P. 50-57.
7. Role of Citicoline in Ischaemic Stroke / Gupta S.K., Gupta A., Gondhotra D., Gupta A., Gupta S. // JK Science. — 2008. — V. 10, № 4. — P. 160-162.
8. Conant R., Schauss A.G. Therapeutic applications of citicoline for stroke and cognitive dysfunction in the elderly: a review of the literature // Altern. Med. Rev. — 2004. — V. 9, № 1. — P. 17-31.
9. Cho H.J., Kim Y.J. Efficacy and safety of oral citicoline in acute ischemic stroke: drug surveillance study in 4,191 cases // Methods Find Exp. Clin. Pharmacol. — 2009. — V. 31, № 3. — P. 171-176.
10. Dбvalos A., Secades J. Citicoline preclinical and clinical update 2009–2010 // Stroke. — 2011. — V. 42. — P. S36-S9.
11. Oral citicoline in acute ischemic stroke: an individual patient data pooling analysis of clinical trials / Dбvalos A., Castillo J., Бlvarez-Sabнn J. et al. // Stroke. — 2002. — V. 33, № 12. — P. 2850-2857.
12. Saver J.L. Citicoline: update on a promising and widely available agent for neuroprotection and neurorepair // Rev. Neurol. Dis. — 2008. — V. 5, № 4. — P. 167-177.
13. Adibhatla R.M., Hatcher J.F. Cytidine 5'-diphosphocholine (CDP-choline) in stroke and other NS disorders // Neurochem. Res. — 2005. — V. 30, № 1. — P. 15-23.
14. Secades J.J. Probably role of citicoline in stroke rehabilitation: review of the literature // Rev. Neurol. — 2012. — V. 54, № 3. — P. 173-179.
15. Бlvarez-Sabнn J., Romбn G.C. Citicoline in vascular cognitive impairment and vascular dementia after stroke // Stroke. — 2011. — V. 42. — P. S40-S43.
16. Fioravanti M., Yanagi M. Cytidinediphosphocholine (CDP choline) for cognitive and behavioural disturbances associated with chronic cerebral disorders in the elderly // Cochrane Database Syst. Rev. — 2004. — V. 2. — CD000269.
17. Сейвер Д.Л. Цитиколин: новые данные о перспективном и широкодоступном средстве нейропротекции и нейрорепарации // Consilium Medicum Ukraina. — 2012. — Т. 6, № 8. — С. 29-33.

/010/010_1.jpg)