Журнал «Медицина неотложных состояний» 3 (58) 2014
Вернуться к номеру
Случай успешной диагностики и лечения псевдоаневризмы левого желудочка при остром инфаркте миокарда
Авторы: Пархоменко А.Н., Иркин О.И., Лутай Я.М., Вовченко В.Е., Кушнир С.П. - ННЦ «Институт кардиологии имени акад. Н.Д. Стражеско» НАМН Украины, отдел реанимации и интенсивной терапии, г. Киев
Рубрики: Медицина неотложных состояний, Кардиология
Разделы: Справочник специалиста
Версия для печати
Статья опубликована на с. 97-100
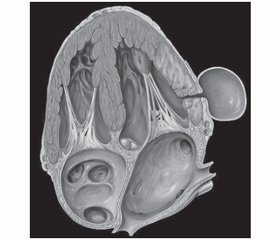
Одним из наиболее грозных и молниеносных осложнений острого Q-инфаркта миокарда (ИМ) является разрыв наружной стенки сердца. Данное осложнение, как правило, ведет к развитию тампонады сердечной сумки, электромеханической диссоциации и быстрой смерти больного. Вероятность наружного разрыва после острого инфаркта миокарда до внедрения реперфузионной терапии составляла 4–6 % [1]. Широкое использование тромболитической терапии и особенно механических методов реперфузии, а также современная стратегия медикаментозного лечения позволили сократить частоту этого осложнения до 0,5–3 % [2–5]. Известными факторами риска разрыва свободной стенки левого желудочка (ЛЖ) являются возраст, женский пол и передняя локализация ИМ [3]. В регистре GRACE риск разрыва сердца был выше также у пациентов с исходно высокой частотой сердечных сокращений, низким систолическим артериальным давлением (АД) и перенесших острое нарушение мозгового кровообращения. Маркером разрыва миокарда является также значительное повышение исходного уровня С-реактивного белка [6]. В то же время использование первичной ангиопластики, низкомолекулярных гепаринов и бета-адреноблокаторов в течение первых 24 часов, а также ИМ в анамнезе ассоциировались с меньшей вероятностью развития данного осложнения [4]. Как правило, разрыв свободной стенки ЛЖ манифестирует в течение первой недели от развития острого инфаркта миокарда. Однако не каждый разрыв наружной стенки миокарда заканчивается летально. Клиническая картина зависит от объема и скорости поступления крови в полость перикарда. Подострые варианты разрыва встречаются примерно в трети случаев и характеризуются повторными поступлениями небольшого количества крови в полость перикарда через прикрывающийся дефект свободной стенки ЛЖ [7]. В таком случае быстрое хирургическое вмешательство может спасти жизнь пациенту. Постепенное развитие патологического процесса возможно также при условии образования спаек между наружным и внутренним листками перикарда. Вследствие этого возникает полость, ограниченная перикардиальными спайками, что в случае наружного разрыва препятствует развитию тампонады сердца (рис. 1).
/97/97.jpg)
Подобный механизм является основой для формирования псевдоаневризмы ЛЖ. Аневризматический мешок псевдоаневризмы состоит из перикарда, ограниченного спайками и остатков разорвавшейся стенки ЛЖ. Полость псевдоаневризмы увеличивается в размерах в связи с постоянным поступлением крови, поэтому по объему иногда она может превышать объем ЛЖ. Учитывая выраженную турбулентность и снижение скорости кровотока в полости псевдоаневризмы, по краям ее, как правило, происходит образование тромба. Псевдоаневризма чаще развивается при инфаркте миокарда задней локализации [8]. В то же время, по данным David и соавт., разрывы миокарда с формированием псевдоаневризмы наиболее часто встречаются при боковой локализации инфаркта [9].
В большинстве случаев псевдоаневризмы обнаруживают у асимптомных пациентов после перенесенного ИМ при плановом проведении эхокардиографии (ЭхоКГ) или при обследовании пациентов по поводу прогрессирования сердечной недостаточности, нарушений сердечного ритма, эмболий или стенокардии. В настоящее время именно эхокардиография (трансторакальная или трансэзофагеальная) является основным методом диагностики псевдоаневризм [10]. Однако иногда это осложнение обнаруживают при проведении компьютерной томографии, вентрикулографии, магнитно-резонасной томографии или интраоперационно при проведении аортокоронарного шунтирования [11]. Псевдоаневризмы внешне могут быть похожи на истинные аневризмы, что может представлять определенные трудности при диагностике. Чаще всего только псевдоаневризмы небольшого размера совместимы с жизнью. При диагностике таких псевдоаневризм регистрируется, как правило, тонкий перешеек.
При псевдоаневризме одна из стенок ЛЖ состоит только лишь из тромботических масс и перикарда, поэтому риск ее разрыва очень велик и составляет, по данным разных исследований, от 30 до 45 % [12]. Причем разрыв стенки может произойти в любой момент и предугать его развитие не представляется возможным. Поэтому в большинстве случаев при псевдоаневризме выбирают хирургического тактику лечения. В целом ведение пациентов представляется следующим образом:
— при диагностике псевдоаневризмы в течение первых 2–3 месяцев от развития острого ИМ необходимо безотлагательное проведение хирургического вмешательства, так как риск разрыва очень велик;
— при диагностике псевдоаневризмы через год и более после ИМ выбор тактики определяется симптоматикой заболевания [13], размером псевдо–аневризмы и наличием противопоказаний для проведения хирургического вмешательства.
Пациенты с хроническими асимптомными псевдоаневризмами диаметром менее 3 см и без склонности к увеличению могут вестись медикаментозно [14]. По данным Moreno и соавт., при консервативной тактике ведения из 10 пациентов в течение 4 лет наблюдения от сердечно-сосудистых причин умер только 1 пациент, однако у 3 больных отмечалось развитие ишемического инсульта. При выборе такой тактики лечения для профилактики тромбоэмболических осложнений обязательным является назначение длительной антикоагулянтной терапии. В качестве альтернативы консервативной тактике ведения у пациентов с высоким риском хирургического вмешательства и тонким перешейком псевдоаневризмы возможно проведение чрескожной процедуры с постановкой заплаты, перекрывающей сообщение полости псевдоаневризмы и полости ЛЖ [16].
С практической точки зрения предпочтение хирургическому методу лечения также связано с тем, что основная масса пациентов с разрывом свободной стенки ЛЖ имеет поражение 2 и более коронарных артерий и нуждаются в проведении аортокоронарного шунтирования [10, 13, 17].
Исход оперативного вмешательства зависит от многих факторов: общего состояния пациента, выраженности сердечной недостаточности, размера инфаркта миокарда, сопутствующих заболеваний и т.д. Летальность после оперативного вмешательства колеблется в пределах 23–35 % [18–20].
В настоящее время число описаний псевдоаневризм небольшое и данные о клиническом течении заболевания невелики. В данной статье мы хотели бы представить случай эхокардиографической диагностики псевдоаневризмы ЛЖ больших размеров с последующим успешным хирургическим лечением.
Пациент С., 50 лет, поступил в отделение реанимации и интенсивной терапии ННЦ «Институт кардиологии имени акад. Н.Д. Стражеско» 16.04.08 с диагнозом острого повторного ИМ (15.04.08). В анамнезе у больного Q-ИМ в области заднедиафрагмальных отделов ЛЖ от 28.01.08, по поводу которого он прошел стационарное лечение и реабилитацию. Находился на постоянной поддерживающей терапии b-–блокаторами, статинами, антитромбоцитарными препаратами. 15.04.08 у пациента развился интенсивный ангинозный приступ со снижением АД, по поводу которого он был госпитализирован в отделение интенсивной терапии больницы по месту жительства. В связи с невозможностью стабилизации состояния 16.04.08 пациент переведен в институт кардиологии.
Несмотря на проводимую терапию (нитраты, диуретики, статины, ингибиторы АПФ, антикоагулянты, дезагреганты, антиаритмические препараты), состояние пациента оставалось тяжелым. На протяжении двух суток больной находился в состоянии кардиогенного шока, отмечались явления рецидивирующего отека легких. Параметры центральной гемодинамики поддерживали при помощи инфузии симпатомиметиков (добутамина и допамина). У больного в динамике наблюдалось повышение с последующим закономерным снижением уровня кардиоспецифических ферментов (общая креатинфосфокиназа от 1708 до 184 МЕ/л (N 35–200 МЕ/л) и аспартатаминотрансфераза от 107 до 37 МЕ/л (N 11–40 МЕ/л) в течение 5 суток наблюдения). За время наблюдения значимых изменений в показателях гемоглобина, эритроцитов и тромбоцитов не отмечалось. Сохранялся лейкоцитоз от 12,5 до 13,4 · 10 9/л в течение всего периода наблюдения. Показатели функции почек (креатинин — 106 мкмоль/л, скорость клубочковой фильтрации — 85,6 мл/мин) были близки к нормальным значениям. Показатели электролитного баланса не выходили за пределы нормальных значений. Уровень глюкозы — в пределах 6,2–6,4 ммоль/л. Показатели коагулограммы (тромбиновое время, свободный гепарин и фибриноген) за время наблюдения существенно не менялись.
По данным ЭхоКГ за 17.04.08: у больного отмечается дефект боковой и заднебоковой стенки ЛЖ с формированием псевдоаневризмы (приблизительный объем — около 200 мл). Полость псевдоаневризмы содержит большое количество тромбов, которые в основном локализуются по ее краям, наблюдается феномен спонтанного контрастирования кровотока. Большое количество эхопозитивных спаек перикарда (рис. 2).
Отмечен массивный сброс крови из левого желудочка через перешеек в полость псевдоаневризмы (рис. 3).
18.04.08 на фоне проводимой терапии удалось стабилизировать состояние пациента. Отменена инфузия прессорных аминов. Уровень систолического АД контролировался в пределах 90–100 мм рт.ст. Начата терапия бета-адреноблокаторами. У больного не рецидивировали боли ангинозного характера, однако сохранялись явления острой левожелудочковой недостаточности (ОЛЖН) (Killip 2).
Повторное эхокардиографическое исследование 21.04.08 не выявило увеличения полости псевдоаневризмы либо прогрессирования разрыва свободной стенки ЛЖ. В связи со стабилизацией гемодинамической ситуации пациент был проконсультирован кардиохирургом и 22.04.08 перведен в Институт сердечно-сосудистой хирургии имени Н.М. Амосова с целью проведения оперативного лечения. На момент перевода состояние пациента оставалось стабильным, боли ангинозного характера не беспокоили, признаков ОЛЖН не было.
23.04.08 больному была проведена резекция аневризмы (псевдоаневризмы) левого желудочка с тромбэктомией и пластикой разрыва боковой стенки левого желудочка, аортального клапана. Операция прошла успешно, и для дальнейшего лечения и реабилитации больной был переведен в ННЦ «Институт кардиологии имени академика Н.Д. Стражеско». Повторная ЭхоКГ после проведенной операции свидетельствовала об отсутствии дефекта и удовлетворительном состоянии гемодинамики (рис. 4).
Представленный случай успешной прижизненной диагностики и лечения наружного разрыва миокарда левого желудочка с формированием гигантской псевдоаневризмы левого желудочка показывает возможность поддержания сердечной деятельности при своевременном оказании неотложной помощи. При этом ранняя эхокардиографическая диагностика уже в отделении интенсивной терапии и реанимации позволила своевременно спланировать и провести успешную хирургическую коррекцию, что в итоге сохранило жизнь пациента.
1. Dellborg M., Held P., Swedberg K., Vedin A. Rupture of the myocardium. Occurrenceand risk factors // Br. Heart J. — 1985. — 54. — 11–16.
2. Ikeda N., Yasu T., Kubo N., Hirahara T., Sugawara Y., Kobayashi N. et al. Effect of reperfusion therapy on cardiac rupture after myocardial infarction [in Japanese] // Circ. J. — 2004. — 68. — 422–6.
3. Moreno R., López de Sа E., Lopez-Sendon J.L. et al. Free wall rupture in patients with acute myocardial infarction treated with primary angioplasty. Incidence and related factors // Am. J. Cardiol. — 2000. — 85. — 757–760.
4. Lopez-Sendon J., Gurfinkel E.P., López de Sa E. et al. Factors related to heart rupture in acute coronary syndromes in the Global Registry of Acute Coronary Events // Eur. Heart J. — 2010. — 31(12). — 1449–1456.
5. Yip H.K., Wu C.J., Chang H.W., Wang C.P., Cheng C.I., Chua S., Chen M.C. Cardiac rupture complicating acute myocardial infarction in the direct percutaneous coronary intervention reperfusion era // Chest. — 2003. — 124. — 565–571.
6. Anzai T., Yoshikawa T., Shiraki H., Asakura Y., Akaishi M., Mitamura H., Ogawa S. C–reactive protein as a predictor of infarct expansion and cardiac rupture after a first Q wave acute myocardial infarction // Circulation. — 1997. — 96. — 778–784.
7. Purcaro A., Costantini C., Ciampani N. et al. Diagnostic criteria and management of subacute ventricular free wall rupture complicating acute myocardial infarction // Am. J. Cardiol. — 1997. — 80. — 397–405.
8. Malcolm I.D., Fitchett D.H., Stewart D., Marpole D., Symes J. Ventricular aneurysm: false or true? An important distinction // Ann. Thorac. Surg. — 1980. — 29. — 474–477.
9. David T.E. Surgery for postinfarction rupture of the free wall of the ventricle / David T.E., editor // Mechanical complications of myocardial infarction. — Austin: RG Landes, 1993. — Р. 142–51.
10. Atik F.A., Navia J.L., Vega P.R., Gonzalez–Stawinski G.V., Alster J.M., Gillinov A.M. et al. Surgical treatment of postinfarction left ventricular pseudoaneurysm // Ann. Thorac. Surg. — 2007. — 83. — 526–31.
11. Fedakar A., Bugra O., Onk A. et al. Repair of Left Ventricular Pseudoaneurysms // Asian Cardiovasc. Thorac. Ann. — 2010. — 18. — 39–43.
12. Vlodaver Z., Coe J.I., Edwards J.E. True and false left ventricular aneurysms: propensity for the latter to rupture // Circulation. — 1975. — 51. — 567–72.
13. Eren E., Bozbuga N., Toker M.E., Keles C., Rabus M.B., Yildirim O. et al. Surgical treatment of post-infarction left ventricular pseudoaneurysm: a two-decade experience // Tex. Heart Inst. J. — 2007. — 34. — 47–51.
14. Pretre R., Linka A., Jenni R., Turina M.I. Surgical treatment of acquired left ventricular pseudoaneurysms // Ann. Thorac. Surg. — 2000. — 70. — 553–7.
15. Moreno R., Gordillo E., Zamorano J., Almeria C., Garcia–Rubira J.C., Fernandez–Ortiz A. et al. Long term outcome of patients with postinfarction left ventricular pseudoaneurysm // Heart. — 2003. — 89. — 1144–6.
16. Clift P., Thorne S., de Giovanni J. Percutaneous device closure of pseudoaneurysm of the left ventricular wall // Heart. — 2004. — 90. — e62.
17. Reardon M.J., Carr C.L., Diamond A. et al. Ischemic left ventricular free wall rupture: prediction, diagnosis, and treatment // Ann. Thorac. Surg. — 1997. — 64. — 1509–13.
18. Komeda M., David T.E. Surgical treatment of postinfarction false aneurysm of the left ventricle // J. Thorac. Cardiovasc. Surg. — 1993. — 106. — 1189–91.
19. Prête R., Linka A., Jenni R., Turina M.I. Surgical treatment of acquired left ventricular pseudoaneurysms // Ann. Thorac. Surg. — 2000. — 70. — 553–557.
20. Frances C., Romero A., Grady D. Left ventricular pseudoaneurysm // J. Am. Coll. Cardiol. — 1998. — 32. — 557–61.

/99/99.jpg)