Международный неврологический журнал 6 (68) 2014
Вернуться к номеру
Мультимодальний підхід до діагностики та лікування судинної деменції
Авторы: Король Г.М - Кафедра неврології Львівського національного медичного університету імені Данила Галицького
Рубрики: Неврология
Разделы: Справочник специалиста
Версия для печати
Вплив гострої та хронічної недостатності мозкового кровообігу на інтелектуальний потенціал хворих із досить нерівнозначними перспективами відновлення порушених функцій і працездатності визначає медико-соціальну значимість судинної деменції (СД). За даними різних авторів, когнітивні порушення судинного генезу виявляються у 5–22 % осіб старшого віку. СД характеризується множинними поліморфними психопатологічними симптомами — майже у всіх випадках трапляються розлади пам’яті, мовлення, просторової та зорової орієнтації, емоцій, поведінки, абстрактного мислення, а також зміни особистості, обмеження як соціальної, так і побутової діяльності.
Мультимодальний метод діагностики СД обґрунтовується не лише використанням загальноприйнятих багатоваріантних міжнародних критеріїв, а й вибором площин обстеження хворого, джерел походження інформації та допоміжних методів дослідження. Для діагностики СД доцільно вибирати такі площини: соматичну, загальнопсихологічну, нейропсихологічну, обстеження неврологічного та функціонального статусів.
Завдяки мультимодальному підходу до діагностики СД є реальна можливість проводити диференціальну діагностику з урахуванням конкретних, індивідуальних факторів ризику і механізмів розвитку інсульту і хронічних форм порушення мозкового кровообігу; запобігати розвитку різноманітних ускладнень, у тому числі і такого грізного, як судинна деменція, що спричиняє соціальну і побутову дезадаптацію хворих та стійку втрату працездатності; проводити адекватні терапевтичні заходи з метою зупинки прогресування порушених пізнавальних функцій.
Влияние острой и хронической недостаточности мозгового кровообращения на интеллектуальный потенциал больных с достаточно неравнозначными перспективами восстановления нарушенных функций и работоспособности определяет медико-социальную значимость сосудистой деменции (СД). Согласно данным разных авторов, когнитивные нарушения сосудистого происхождения выявлены у 5–22 % людей старшего возраста. СД характеризуется множественными психопатологическими симптомами — практически во всех случаях встречаются расстройства памяти, речи, пространственной и зрительной ориентации, эмоций, поведения, абстрактного мышления, а также изменения личности, ограничение социальной и бытовой деятельности.
Мультимодальный метод диагностики СД обосновывается не только использованием общепринятых многовариантных международных критериев, но и выбором плоскостей обследования больного, источников информации и дополнительных методов обследования. Для диагностики СД целесообразно выбирать следующие плоскости: соматическую, общепсихологическую, нейропсихологическую, обследование неврологического, функционального статусов.
Благодаря мультимодальному подходу к диагностике СД существует реальная возможность проводить дифференциальную диагностику с учетом конкретных, индивидуальных факторов риска и механизмов развития инсульта и хронических форм нарушения мозгового кровообращения; предупреждать развитие разнообразных осложнений, в том числе и такого грозного, как сосудистая деменция, которая провоцирует социальную, бытовую дезадаптацию и стойкую потерю трудоспособности у больных; проводить адекватные терапевтические мероприятия с целью остановки прогрессирования нарушенных познавательных функций.
Influence of the acute and chronic cerebrovascular insufficiency on the intellectual potential of the patients with quite unequal perspectives regarding restoration of impaired functions and performance determines medical and social importance of vascular dementia (VD). According to some authors, cognitive disorders of vascular origin are observed in 5–22 % of elderly persons. VD is characterized by multiple polymorphous psychopathological syndrome — almost in all cases there are being observed disorders of memory, speech, visual and spatial orientation, emotions, behavior, abstract thinking, as well as personality changes, loss of both social and and habitual activity.
Multimodal method in the VD diagnosis is justified not only by the use of conventional multivariant international criteria, but also by the choice of aspects of patient’s examination, informational sources and additional investigations. For VD diagnosis, it is appropriate to choose the next aspects: somatic, general psychological, neuropsychological, assessment of neurological and functional states.
Due to multimodal approach to VD diagnostics, there is real possibility to carry out differential diagnostics talking into account specific, individual risk factors and mechanisms of stroke and chronic cerebrovascular disorders; to prevent different complications, in particular such severe one as VD, which causes social and habitual dysadaptation and stable disability; to perform proper therapeutic measures in order to stop cognitive deficit progression.
деменція, мультимодальний підхід, Нейронтін.
деменция, мультимодальный подход, Нейронтин.
dementia, multimodal approach, Neurontin.
Статья опубликована на с. 62-68
Цереброваскулярні захворювання (ЦВЗ) за поширеністю і тяжкістю наслідків стали однією з актуальних проблем сучасної медицини, і зокрема неврології [1, 20, 23]. Серед окремих форм порушення мозкового кровообігу перше місце за поширеністю посідає хронічна ішемія. Висока смертність і глибока інвалідизація хворих, виражений вплив хронічної недостатності мозкового кровообігу на інтелектуальний потенціал із досить нерівнозначними перспективами відновлення порушених функцій і працездатності визначають медико-соціальну значимість вказаної проблеми [3, 5, 10]. За даними різних авторів, когнітивні порушення судинного генезу виявляються у 5–22 % осіб старшого віку [8, 16].
Судинна деменція (СД) — це мультиморбідний, гетерогенний за своєю природою синдром, що виникає за наявності різних форм цереброваскулярного патологічного процесу, переважно ішемічного, як осередкового, так і дифузного характеру. Це друга за поширеністю форма деменції. Перше місце за кількістю хворих посідає хвороба Альцгеймера (близько 50 % усіх випадків деменції). СД зустрічається у 20 % випадків, у 12 % хворих спостерігається поєднання цих форм. СД характеризується множинним, поліморфним психопатологічним синдромом — майже у всіх випадках зустрічаються розлади пам’яті, мовлення, просторової та зорової орієнтації, емоцій, поведінки, абстрактного мислення тощо. Поряд із вираженими когнітивними порушеннями виступають афективні й поведінкові розлади, а також зміни особистості, виникає непрацездатність — обмеження як соціальної, так і побутової діяльності [17, 18, 29, 34].
З клінічної позиції важливим є своєчасне встановлення початкових проявів когнітивних розладів, оскільки на ранньому етапі їх розвитку, до формування деменції, можна сподіватися на досягнення більшого успіху від терапевтичних заходів, щоб зупинити прогресування порушених пізнавальних функцій [11, 26, 28, 47]. Клінічний досвід показує, що більшість хронічних захворювань, особливо судинних уражень головного мозку, викликають таку деформацію в житті хворих, унаслідок якої більшу частину часу людина знаходиться в однобічному (патогенному) стані [21, 25].
За етіологічним, нейропсихологічним профілем СД гетерогенна, що залежить від характеру, типу, локалізації цереброваскулярного порушення та втягненої в патологічний процес ділянки головного мозку за об’ємом, за структурними рівнями [9, 15, 35]. Тому в основу клінічної, психологічної, неврологічної, нейровізуальної діагностики СД необхідно поставити принцип мультимодальності. Вказаний принцип прийнятний у різнобічних діагностичних концепціях. Мультимодальність означає, що замість уніваріантного підходу перевага надається мультиваріантному для інтеграції інформації, яка досягається різними методами дослідження [13, 37, 51].
З метою діагностики судинної деменції насамперед використовують критерії провідних світових діагностичних систем: МКХ–10, DSM–IV, NINDS–AIREN (1993 р.), а також ішемічну шкалу Хачинського (1975 р.).
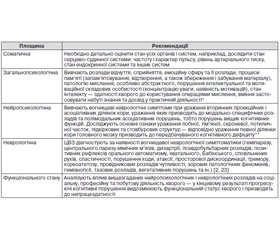
Мультимодальний метод діагностики СД обґрунтовується не лише використанням загальноприйнятих багатоваріантних міжнародних критеріїв, а також у клінічній практиці вибором площин або рядів обстеження хворого, джерел походження інформації та допоміжних методів дослідження [51]. Для діагностики СД доцільно обирати такі площини: соматичну, загальнопсихологічну, нейропсихологічну, обстеження неврологічного та функціонального статусів. Окремі площини не є закритими системами, вони є взаємопов’язаними, відкритими, доповнюють одна одну і в деяких пунктах перекриваються.
Локалізація патологічного процесу у скроневій частці, особливо в гіпокампі, викликає порушення пам’яті та неможливість навчання; при ураженні лівої частки виникає сенсорна афазія і вербальна амнезія, правої — агнозія, амнезія на візуальний невербальний матеріал.
Нейропсихологічні симптоми залежать від домінантної півкулі щодо ураження тім’яної частки. Ураження тім’яної частки півкулі, домінантної відносно мовної функції, призводить до афазії або алексії, ідеомоторної або ідеаторної апраксії. Результатом ураження тім’яної частки недомінантної півкулі можуть бути розлади сприйняття протилежної половини зовнішнього простору і втрата топографічної пам’яті, розлади просторової орієнтації, побутова апраксія, анозогнозія.
При двобічному ураженні потиличної частки можливі розвиток кіркової сліпоти, розлади кольорового сприйняття, зорові ілюзії (метаморфопсії) та зорові галюцинації.
Вищі когнітивні функції здійснюються за допомогою інтегративної взаємодії кори та підкіркових структур, а також лімбічної системи. Підкіркова деменція виникає при ураженні базальних гангліїв, таламуса, їх взаємозв’язків та прилягаючої білої речовини півкуль мозку [10, 17, 49]. Ядра зорового горба і ретикулярної формації відіграють у цьому механізмі особливо важливу роль. Префронтальна і нижня тім’яна ділянки разом із лімбічною системою відповідають за увагу, від функції цих структур залежить здатність концентрації, тому ураження підкіркової білої речовини поміж цими структурами завжди викликає розлади концентрації уваги. Двобічні таламічні інфаркти характеризуються амнезією, сповільненням психічних процесів, апатією, порушеннями уваги, гнозису, праксису, мовлення. В основі порушення вищих мозкових функцій при інфарктах у таламусі лежить функціональна деактивація кіркових відділів головного мозку [10]. Когнітивні порушення у хворих із підкірковою деменцією також необхідно трактувати з позиції функціонування фронтально-стріарних зв’язків, що регулюють психічні функції [27, 45]. Клінічним варіантом підкіркової СД вчені вважають хворобу Бінсвангера (артеріосклеротична енцефалопатія). Вона характеризується прогресуючою деменцією, вираженими неврологічними розладами, підкірковою, мозочковою, псевдобульбарною, пірамідною симптоматикою, тазовими розладами, що виникають при ураженні білої речовини півкуль мозку, однак при збереженні кори, що знаходиться в неактивному стані через розірвані зв’язки з ретикулярною формацією і зоровим горбом [6, 17, 49].
Отже, субкортикальний тип СД характеризується наявністю двобічної пірамідної симптоматики, частіше локалізованої в нижніх кінцівках, розладами ходи і постуральною нестійкістю, екстрапірамідними знаками, псевдобульбарними розладами. Для кортикального мультиінфарктного типу СД характерна наявність асиметричної вогнищевої неврологічної симптоматики [7, 16, 35].
Згідно з критеріями NINDS-AIREN, нейрорентгенологічними ознаками судинного ураження головного мозку, якими підтверджують СД, є такі: множинні інфаркти, поодинокі інфаркти у стратегічних ділянках, множинні лакуни в базальних гангліях і білій речовині, виражені ішемічні зміни перивентрикулярної білої речовини [16, 48].
За даними КТ і МРТ дослідники пропонують розглядати декілька форм СД: 1) мультиінфарктну деменцію (на КТ головного мозку є множинні ділянки інфарктів); 2) деменцію з поодинокими інфарктами в ділянках, що мають відношення до інтелекту (на КТ інфаркти в зоровому горбі, медіобазальних відділах мозку); 3) деменцію, пов’язану з дифузними змінами білої речовини півкуль, а також із множинними лакунарними інфарктами (на КТ феномен лейкоареозу: двобічне дифузне або плямисте зниження щільності білої речовини) або гіперінтенсивні перивентрикулярні вогнища на МРТ у Т2-режимі [3, 4, 17].
Першочерговими принципами терапії судинної деменції стали: запобігання виникненню або ж прогресуванню дементних симптомів, поліпшення когнітивних функцій та загальнотерапевтичні заходи.
У кожному випадку профілактика розвитку і прогресування захворювання повинна враховувати етіологічні механізми його виникнення, оскільки вона буде різною у хворих з ураженими дрібними мозковими судинами, оклюзією магістральних артерій голови або ж емболією кардіогенного генезу. Хворим із патологією дрібних судин насамперед необхідно нормалізувати артеріальний тиск, що призведе до покращення когнітивних функцій. Чітко позначене зниження артеріального тиску може спровокувати зростання мнестичних, інтелектуальних розладів, тому таким хворим доцільно проводити добовий моніторинг артеріального тиску.
Превентивні лікувальні впливи спрямовані: 1) на зменшення прогресування цереброваскулярних захворювань; 2) когнітивних і функціональних порушень:
— основні принципи лікування хворих із судинною церебральною патологією: поліпшення серцевої діяльності, нормалізація артеріального тиску; своєчасне та адекватне відновлення мозкового кровообігу; корекція реологічних властивостей крові, її в’язкості; поліпшення мікроциркуляції; запобігання розвитку набряку головного мозку; усунення вегетосудинних розладів;
— з метою поліпшення власне когнітивних функцій призначають ноотропні і пептидергічні препарати, антагоністи іонів кальцію, інші препарати (гінкго білоба, гліатилін, інстенон). У хворих із судинною деменцією, як і у всіх дементних хворих, виникає ціла низка порушень, із приводу яких необхідно проводити симптоматичну терапію.
Визначальними факторами у виборі стратегічної терапії судинної деменції є вивчення етіології, об’єктивної клінічної характеристики та ступеня вираженості когнітивного дефіциту. Досить перспективним є застосування конкурентних блокаторів NMDA-рецепторів, а саме мемантину, який має високий рівень доказів ефективності в лікуванні когнітивних порушень. Досвід свідчить, що з даної групи препаратів доцільно призначати Нейронтін.
Нейронтін є антагоністом N-метил-D-аспартатних рецепторів глутамату, що дозволяє захищати нейрони від ексайтотоксичного пошкодження при ішемії. Накопичення в синаптичній щілині надлишкової концентрації глутамату й аспартату, а також порушення їх зворотного захвату ішемізованою астроглією викликає перезбудження глутаматних рецепторів. Як наслідок, посилюється комплекс реакцій, що призводять до надлишкового внутрішньоклітинного накопичення кальцію — основного тригера кінцевих механізмів каскаду, який руйнує нервові клітини [16, 23].
Отже, при судинній мозковій недостатності з картиною когнітивних та інших неврологічних порушень активність глутаматергічної системи підвищується і в синаптичну щілину виділяється велика кількість медіатора.
Тому застосування Нейронтіну сприяє нормалізації патерна глутаматергічної передачі, що і лежить в основі нейропротекторного і позитивного симптоматичного ефекту даного препарату.
Для лікування судинної деменції Нейронтін застосовують у добовій дозі 20 мг. Лікування розпочинають із поступового підвищення дози (табл. 4).
Дані рандомізованих досліджень та клінічний досвід підтверджують, що застосування Нейронтіну суттєво покращує когнітивні функції: поліпшує пам’ять, нормалізує поведінку хворих із деменцією, підвищує щоденну активність, працездатність та адаптацію в соціальному середовищі — підвищується рівень незалежності та самостійності [8, 15]. Крім того, Нейронтін показав добру переносимість, відсутність будь-яких неприйнятних побічних ефектів.
Нейронтін можна застосовувати як монотерапію або в комбінації з інгібіторами ацетилхолінестерази [27]. Серед селективних інгібіторів рекомендується застосовувати донепезил по 5 мг 1 раз на добу або галантаміну гідробромід по 4 мг 2 рази на добу; також призначають ривастигмін по 1,5 мг 2 рази на добу і нейромідин у дозі 10 мг двічі на добу.
Медикаментозної взаємодії між інгібіторами ацетилхолінестерази та мемантином не виникає. Доцільно призначати комбіновану терапію при недостатньому ефекті одного з препаратів.
Висновок
Завдяки мультимодальному високоінформативному підходу до діагностики СД є реальна можливість:
— своєчасного встановлення початкових проявів когнітивних розладів, оскільки на ранньому етапі їх розвитку, до формування деменції, можна сподіватися на досягнення більшого успіху від терапевтичних заходів, щоб зупинити прогресування порушених функцій;
— проводити диференціальну діагностику з урахуванням конкретних, індивідуальних факторів ризику й механізмів розвитку інсульту та хронічних форм порушення мозкового кровообігу;
— запобігати розвитку різноманітних ускладнень, у тому числі і такого грізного, як судинна деменція, що спричиняє соціальну й побутову дезадаптацію та стійку втрату працездатності у хворих;
— застосовувати адекватні терапевтичні заходи, щоб зупинити прогресування порушених пізнавальних функцій.
1. Бойко А.Н. Хроническая ишемия мозга (дисциркуляторная энцефалопатия) / А.Н. Бойко, Т.В. Сидоренко, А.А. Кабанов // Consilium medicum. — 2004. — Т. 6, № 8. — С. 598–601.
2. Верещагин Н.В., Моргунов В.А., Гулевская Т.С. Патология головного мозга при атеросклерозе и артериальной гипертонии. — М.: Медицина, 1997. — 287 с.
3. Верещагин Н.В., Варакин Ю.Я. Профилактика острых нарушений мозгового кровообращения: Терапия и реальность // Журн. невропатологии и психиатрии. — 1996. — Т. 96, № 5. — С. 5–9.
4. Верещагин Н.В., Моргунов В.А., Калашникова Л.А., Гулевская Т.С. Лакунарный инфаркт — особая форма очаговой патологии головного мозга при артериальной гипертонии // Журн. невропатологии и психиатрии. — 1983. — Т. 83, № 7. — С. 1015–1021.
5. Віничук C.M. Мозковий інсульт (клініко-діагностичні, терапевтичні та прогностичні алгоритми). — К.: Медицина України, 1988. — 51 с.
6. Дамулин И.В. Дисциркуляторная энцефалопатия: патогенез, клиника, лечение. — М.: ММА, 2005. — 48 с.
7. Дамулин И.В. Нарушения ходьбы и равновесия при дисциркуляторной энцефалопатии. Клинико-нейропсихологическое и МРТ сопоставление / И.В. Дамулин, В.Г. Брызжахина, Н.Н. Яхно // Неврол. журн. — 2004. — № 4. — С. 13–18.
8. Дамулин И.В. Парфенов В.А. Нарушения кровообращения в головном и спинном мозге. Болезни нервной системы: Руководство для врачей / Под ред. Н.Н. Яхно, Д.Р. Штульман. — М., 2003. — С. 231–302.
9. Дамулин И.В. Сосудистая деменция // Неврол. журн. — 1999. — № 4. — С. 4–11.
10. Джеймс Ф.Т. Сосудистые заболевания головного мезга: Руководство для врачей / Перевод с англ.; под ред. акад. РАМН Е.И. Гусева, проф. А.Б. Гехт. — 6-е изд. — М.: ГЭОТАР-Медиа, 2007. — 608 с.
11. Захаров В.В., Яхно Н.Н. Синдром умеренных когнитивных расстройств в пожилом возрасте: диагностика и лечение // Русский медицинский журнал. — 2004. — № 10. — С. 573–576.
12. Зозуля И.С. Клинические особенности ишемического инсульта мозга с опухолеподобным течением // Врачеб. дело. — 1992. — № 5. — С. 71–72.
13. Клиническая психология / Под ред. М. Перре, У. Бауманна. — СПб.: Питер, 2007. — 1312 с.
14. Левин О.С. Алгоритмы диагностики и лечения деменции. — М., 2005. — 38 с.
15. Левин О.С. Гетерогенность умеренного когнитивного расстройства: диагностические и терапевтические аспекты / О.С. Левин, Л.В. Голубева // Консилиум. — 2006. — № 12. — С. 106–109.
16. Левин О.С. Диагностика и лечение деменции в клинической практике / О.С. Левин. — М.: МЕДпресс-информ, 2010. — 256 с.
17. Левин О.С. Дисциркуляторная энцефалопатия современные представления о механизмах развития и лечении // Consilium medicum. — 2007. — № 8. — С. 72–79.
18. Медведева А.В. Патогенез сосудистой деменции // Журн. невропатологии и психиатрии. — 1995. — Т. 95, № 5. — С. 95–100.
19. Михайленко А.А., Зинченко В.А., Холин А.В. и др. Магнитно-резонансная томография в диагностике и дифференциации мозговых инсультов // Журн. невропатологии и психиатрии. — 1992 — Т. 92, № 1. — С. 113–117.
20. Мищенко Т.С. Диагностика и лечение дисциркуляторных энцефалопатий / Т.С. Мищенко // Здоров’я України. — 2003. — № 23. — С. 84.
21. Неврология / Марко Мументалер, Хейнрих Маттле; пер. с нем.; под ред. О.С. Левина. — М.: МЕДпресс-информ, 2007. — 920 с.
22. Одинак М.М., Емелин А.Ю., Лобзин В.Ю Нарушение когнитивных функций при цереброваскулярной патологии. — СПб.: ВМА, 2006. — 158 с.
23. Суслина З.А., Варакин Ю.А., Верещагин Н.В. Сосудистые заболевания головного мозга. — М.: Медпресс-информ, 2006. — 256 с.
24. Челышева И.А. Нейропсихологические и нейровизулизационные аспекты дисциркуляторной энцефалопатии в ракурсе структурно-функциональной модели головного мозга / И.А. Челышева, Н.С. Нагорный // Журн. неврологии и психиатрии. — 2005. — № 1. — С. 65–69.
25. Чухловина М.Л. Деменция. Диагностика и лечение. — СПб.: Питер, 2010. — 272 с.
26. Яхно Н.Н., Захаров В.В. Умеренные когнитивные расстройства в пожилом возрасте. Избранные лекции по неврологии / Под ред. В.Л. Голубева. — М.: Эйдос Медиа, 2004. — С. 606–621.
27. Яхно Н.Н. Когнитивные и эмоционально-аффективные нарушения при дисциркуляторной энцефалопатии / Н.Н. Яхно, В.В. Захаров // Русский медицинский журнал. — 2002. — Т. 10, № 12–13. — С. 539–542.
28. Яхно Н.Н. Легкие и умеренные когнитивные расстройства при дисциркуляторной энцефалопатии / Н.Н. Яхно, А.Б. Локшина, В.В. Захаров // Клиническая геронтология. — 2005. — Т. 11, № 9. — С. 38–39.
29. Яхно Н.Н. Синдром умеренных когнитивных нарушений при дисциркуляторной энцефалопатии / Н.Н. Яхно, В.В. Захаров, А.Б. Локшина // Журнал неврологии и психиатрии им. С.С. Корсакова. — 2005. — Т. 105, № 2. — С. 13–17.
30. Яхно Н.Н. Сопоставление клинических и МРТ-данных при дисциркуляторной энцефалопатии. Когнитивные нарушения / Н.Н. Яхно, О.С. Левин, И.В. Дамулин // Неврол. журнал. — 2001. — № 3. — С. 10–18.
31. Amar K., Wilcock G.K., Scott M. The diagnosis of vascular dementia in the light of the new criteria // Age Ageing. — 1996. — 25 (1). — 51–55.
32. American Psychiatric Association: Diagnostic and Statistical Manual of Mental Disorders. — 4th ed. (DSM-IV). — Washington, DC, АРА, 1994.
33. Apostolova L., Cummings J. Psychiatric manifestations of dementia // Continuum. — 2007. — Vol. 13. — P. 56–65.
34. Chiu H.С., Victoroff J.I., Margolin D.M. et al. Criteria for the diagnosis of lschemic vascular dementia proposed by the State of Cahforma Alzheimer’s Disease Diagnostic and Treatment Centers // Neurology. — 1992. — 42. — 473–480.
35. Consoli D., Di Carlo A., Inzitari D. et al. Subcortical ischaemic changes in young hypertensive patients: frequency, effect on cognitive performance and relationship with markers of endothelial and haemostatic activation // Eur. J. Neurol. — 2007. — V. 14, № 11. — P. 222–1229.
36. Dilling H., Mombour W., Schmidt M.H. Internationale Klassification psychicher Storungen ICD-10 Kapitel V (F) // Klinisch-diagnostische Leitlinien (2. Auflage). — Bern: Huber, 1993.
37. Fisseni H.-J. Lehrbuch derpsychobgischen Diagnostik. — Gottingen: Hogrefe, 1990.
38. Gorehck P., Chatterjee A., Patel D. et al. Cranial computed tomographic observations in multi-infarct dementia: A controlled study // Stroke. — 1992. — 23(6). — 804–811.
39. Gupta R., Solanki R.K., Pathak V. Blood pressure is associated with cognitive impairment in young hypertensives // World J. Biol. Psychiatry. — 2007. — V. 8, № 1. — P. 1–8.
40. Hachinski V.C., Lliff L.D., Zilhka E. et al. Cerebral blood flow in dementia // Arch. Neurol. — 1975. — Vol. 32. — P. 632–637.
41. Hershey L., Modic M., Greenough P. et al. Magnetic resonance imaging in vascular dementia // Neurology. — 1987. — 37. — 29–36.
42. Lang P. The application of psychophysiological methods to the study of psychotherapy and behavior change // Handbook of Psychotherapy and Behavior Change. An Empirical Analysis / Ed. by A. Bergin, S. Garfield. — New York: Wiley, 1971. — Р. 77–125.
43. Lim C., Alexander M.P. Disorders of episodic memory // The behavioral and cognitive neurology of stroke / Еd. by O.G. Godefroy, J. Bogousslavsky. — Cambridge: University press, 2007. — P. 407–430.
44. Lobo A., Launer L., Fratighom L. et al. Prevalence of dementia and major subtypes in Europe // Neurology. — 2000. — Vol. 4 (S 5). — S. 4–9.
45. Mega M.S., Cummings J.L. Frontal-subcortical circuits and neuropsychiatnc disorders // J. Neuropsychiatry Clin. Neurosci. — 1994. — Vol. 6. — P. 358–370.
46. O’Brien M.D. Vascular dementia is underdiagniosed // Arch. Neural. — 1988. — 45. — 797–798.
47. Petersen R.C., Doody R., Kurz A. et al. Current concepts in mild cognitive impairment // Arch. Neurol. — 2001. — V. 58. — № 9. — P. 1985–1992.
48. Roman G.С. Diagnostic criterions of vascular dementia // Neurology. — 1993. — V. 43. Mb 1. — P. 250–256.
49. Roman G.C., Erkinjuntti T., Walhn A., Pantoni L. Subcortical ischaemic vascular dementia // Lancet Neurology. — 2002. — 1. — 426–436.
50. Roman G.С., Royall D.R. Executive control function a rational basis for the diagnosis of vascular dementia // Alzheimer Dis. Assoc. Disord. — 1999. — Vol. 13 (suppl. 3). — S. 69–80.
51. Seidenstucker G., Baumann U. Multimethodale Diagnostik // Klinische Psychologie. Trends in Forschung und Praxis / U. Baumann, H. Berbalk, G. Seidenstucker (Hrsg.). — Bern: Huber, 1978. — Bd. 1, S. 134–185.
52. Skoog I. Risk factors for vascular dementia a review // Dementia. — 1994. — 5. — 137–144.
53. Wetterling T., Kanitz R.D., Borgis K.J. Comparison of different diagnostic criteria for vascular dementia (ADDTC, DSM-IV. ICD-10, NINDS-AIREN) // Stroke. — 1996. — 27 (1). — 30–36.

/63/63.jpg)
/64/64.jpg)
/65/65.jpg)
/66/66.jpg)