Журнал «Актуальная инфектология» 4 (5) 2014
Вернуться к номеру
Гостра EBV-інфекція у дорослих: етіологія, епідеміологія, патогенез, клініка та лабораторна діагностика
Авторы: Дуда О.К., Колесник Р.О. — Національна медична академія післядипломної освіти ім. П.Л. Шупика, кафедра інфекційних хвороб, м. Київ
Рубрики: Инфекционные заболевания
Разделы: Справочник специалиста
Версия для печати
Останніми роками значно підвищився рівень захворюваності на гостру EBV-інфекцію, що, швидше за все, пов’язане не стільки з епідеміологічним підйомом, скільки з покращенням методів діагностики. Поліморфність клінічної картини, легкі та стерті форми, труднощі, що доволі часто виникають у діагностиці захворювання, дають підстави вважати, що офіційно зареєстрована захворюваність в Україні не відображає істинної поширеності інфекції. Реакції Пауля — Буннелля та Хоффа — Бауера, засновані на виявленні поліклональних гетерофільних антитіл, останнім часом розглядаються скоріше в історичному аспекті. У практичній медицині використовують специфічні методи діагностики: поліклональну ланцюгову реакцію та імуноферментний аналіз. Як експрес-тест для діагностики гнійно-деструктивних ускладнень рекомендовано визначення С-реактивного білка в сироватці крові. Активність імунопатологічного процесу визначається за допомогою вмісту β2-макроглобуліну.
За последнее время существенно повысился уровень заболеваемости острой EBV-инфекцией, что, скорее всего, связано не столько с эпидемиологическим подъемом, сколько с улучшением методов диагностики. Полиморфность клинической картины, легкие и стертые формы, довольно часто возникающие трудности в диагностике заболевания дают основания считать, что официально зарегистрированная заболеваемость в Украине не отображает истинной распространенности инфекции. Реакции Пауля — Буннелля и Хоффа — Бауэра, основанные на выявлении поликлональных гетерофильных антител, в последние годы рассматриваются в историческом аспекте. В практической медицине используются специфические методы диагностики: поликлональная цепная реакция и иммуноферментный анализ. Как эспресс-тест для диагностики гнойно-деструктивных осложнений рекомендовано определение С-реактивного белка в сыворотке крови. Активность иммунопатологического процесса определяется с помощью концентрации β2-макроглобулина.
In recent years, the incidence of acute EBV-infection significantly increased, which is, most likely, due to not so much to increased epidemiology, but to improved diagnostic methods. Polymorphic clinical picture, mild and obliterated forms, difficulties, which are quite often in the diagnosis of disease, give reason to believe that the incidence officially registered in Ukraine does not reflect the true spread of infection. Paul — Bunnell and Hoff — Bauer reactions, based on the identification of polyclonal heterophile antibodies, in recent years are considered rather in historical perspective. In the practical medicine, specific diagnostic methods are being used: polyclonal chain reaction and enzyme immunoassay. As rapid test for the diagnosis of purulent-destructive complications, estimation of C-reactive protein in blood serum is recommended. Activity of immunopathological process is determined by the concentration of β2-macroglobulin.
EBV-інфекція, інфекційний мононуклеоз, етіологія, епідеміологія, патологічна анатомія, клінічна класифікація, лабораторна діагностика.
EBV-инфекция, инфекционный мононуклеоз, этиология, эпидемиология, патологическая анатомия, клиническая классификация, лабораторная диагностика.
EBV-infection, infectious mononucleosis, etiology, epidemiology, pathological anatomy, clinical classification, laboratory diagnostics.
Статья опубликована на с. 15-21
Актуальність
За даними ВООЗ, близько 90 % дорослого населення інфіковані вірусом Епштейна — Барр (EBV). Первинне інфікування призводить до довічної персистенції збудника з можливою періодичною реактивацією [1]. EBV відіграє провідну роль не тільки в інфекційній, але й у неврологічній, ревматологічній, онкологічній, гематологічній та імунологічній патології. Останніми роками значно підвищилася захворюваність на гостру EBV-інфекцію — інфекційний мононуклеоз (ІМ), що, швидше за все, пов’язано не стільки з епідеміологічним підйомом, скільки з покращенням методів діагностики.
Історичні відомості
Вперше захворювання було описане Н.Ф. Філатовим у 1885 році під назвою «ідіопатичне запалення шийних залоз». Пізніше, у 1889 році, німецький вчений Пфайфер описав це захворювання під назвою «залозиста лихоманка». У 1907 році Турк, а в 1909 році — Барнс виявили характерні зміни в крові. У 1920 році Спрунт та Еванс описали «нове» захворювання під назвою «інфекційний мононуклеоз», для якого були характерними гематологічні зміни — лейкоцитоз із вираженим лімфоцитозом та моноцитозом. Через рік ці автори повідомили, що ІМ та залозиста лихоманка є одним захворюванням [2].
На інфекційну природу ІМ вказував ще Н.Ф. Філатов в 1895 році. Як збудник захворювання описувалися найрізноманітніші мікроорганізми (збудник дифтерії, стафілококи, стрептококи тощо). Довгий час етіологічним чинником ІМ вважали лістерію. Уперше про виділення з крові хворого Listerella monocytogenes hominis заявив Ніфельдт. Прибічниками лістеріозної етіології були Гуйліанеле (1939), П.П. Сахаров та І.І. Гудкова (1950). Не знайшла підтвердження й думка японських вчених Міса, Кобаяші та Широкава (1955) про рикетсіозну природу ІМ [2].
Вірусна етіологія ІМ уперше була запропонована Вісінгом (1939), Сохером (1948) та Лепіне (1962). Відкриття вірусу пов’язане з дослідженнями в галузі онкології. У 1961 році англійський хірург Беркіт описав онкологічне захворювання, що зустрічалося в деяких країнах Африки з частотою 8 випадків на 100 тисяч населення (лімфома Беркіта). У 1964 році вірусологи Майкл Епштейн та Івонна Барр, а також спеціаліст з електронної мікроскопії Джефрі Ачонга з фрагментів пухлин, що були надані Беркітом, виділили новий вид герпесвірусу — HHV-4. У 1968 році була доведена етіологічна роль цього вірусу при ІМ [2].
Етіологія
EBV належить до роду Lymphocryptovirus, підсімейства γ-herpesviridae. Виявляє тропність до лімфоцитів (В-клітин), моноцитів, макрофагів та епітеліоцитів носоглотки. Вірус не руйнує, а стимулює розмноження інфікованих В-лімфоцитів. Розрізняють два серотипи вірусу — EBV-1 та EBV-2, що також позначаються як типи А та В, вони відрізняються лише за характером експресії генів під час латентної інфекції. У процесі реплікації вірусу експресується понад 70 специфічних білків, але лише чотири з них використовують для встановлення стадії інфекційного процесу — ранній (EA), капсидний (VCA), ядерний (EBNA) та латентний мембранний білок (LMP). Кожен з антигенів утворюється в певній послідовності та індукує синтез відповідних антитіл. EBV нестійкий у зовнішньому середовищі та швидко гине під дією дезінфектантів [3].
Епідеміологія
Резервуаром та джерелом інфекції є люди з маніфестною, латентною та хронічною інфекцією. У 15–30 % хворих, які перенесли гостру EBV-інфекцію, можлива реактивація збудника, що не супроводжується ні імунологічними, ні клінічними змінами. Однак вірус виділяється зі слиною, і такі люди стають джерелом інфекції [4].
Основний шлях передачі — повітряно-крапельний, механізм — аерозольний. Зазвичай вірус виділяється зі слиною, тому можливе зараження контактним шляхом (через поцілунки, статевим шляхом, через руки, іграшки та предмети побуту). Також можлива передача при переливаннях крові та новонародженому під час пологів [4].
Сприйнятливість до інфекції висока, однак переважають стерті та легкі форми захворювання. Вірус поширений усюди. Зазвичай реєструються спорадичні випадки, іноді епідемічні спалахи в дитячих закритих колективах. Поліморфність клінічної картини, легкі та стерті форми, труднощі, що доволі часто виникають при діагностиці захворювання, є підставою вважати, що офіційно зареєстрована захворюваність в Україні не відображає істинної поширеності інфекції. Найчастіше хворіють підлітки, тому іноді ІМ називають «хворобою студентів». Сезонність не характерна, лише в літні місяці відзначається спад. Зараженню сприяють скупченість, користування загальними речами особистої гігієни, посудом, тісні побутові контакти [4].
Патогенез
Думка про те, що EBV-інфекція розвивається лише на фоні імунодефіциту, не витримує жодної критики — при настільки високій ураженості населення (90–95 %) частота загальної варіабельної імунної недостатності в популяції в середньому становить 1 : 60 000–1 : 70 000 [5]. Вхідними воротами інфекції служить слизова оболонка носоглотки та верхніх дихальних шляхів. Можна виділити чотири основні стадії патогенезу гострої EBV-інфекції:
1) первинний регіонарний лімфаденіт;
2) віремія;
3) інфекційно-алергічна стадія;
4) формування імунітету.
Первинний регіонарний лімфаденіт розвивається зазвичай у задньошийних та підщелепних лімфатичних вузлах, рідше в мезентеріальних. Але описані випадки, коли у хворих розвивалася поліаденопатія в результаті трансмісивного зараження або при пересадці кісткового мозку. У випадку порушення лімфатичного бар’єра виникають віремія та генералізація процесу. Клітинами-мішенями виступають В-лімфоцити, органами-мішенями є лімфоретикулярний апарат — лімфатичні вузли, печінка, селезінка. Зазвичай патологічний процес закінчується на першій або другій стадії з формуванням типоспецифічного нестерильного імунітету, але іноді переходить в інфекційно-алергічну стадію та набуває хвилеподібного (ациклічного) перебігу [6].
Патогенез ускладнень гострої EBV-інфекції. Причиною тромбоцитопенії є вироблення антитромбоцитарних антитіл та масивний розпад тромбоцитів у збільшеній селезінці. Гемолітична анемія розвивається внаслідок утворення холодових антитіл, автоантитіл до еритроцитів та трифосфат-ізомерази. Обструкція верхніх дихальних шляхів є наслідком гіпертрофії піднебінних мигдаликів та лімфатичних вузлів кільця Вальдейєра — Пирогова, а також приєднання вторинної бактеріальної флори (зазвичай бета-гемолітичний стрептокок групи С) [7].
Патогенез екзантеми при гострій EBV-інфекції. На сьогодні причина розвитку екзантеми залишається нез’ясованою. Узагальнюючи, можна запропонувати такі три теорії:
1) унаслідок цитолітичної дії антибактеріальних препаратів (АБП);
2) унаслідок нашарування на вже існуючу хронічну алергію;
3) унаслідок стимуляції В-лімфоцитів із формуванням автоімунного процесу.
Екзантему при гострій EBV-інфекції зазвичай пов’язують із прийомом антибактеріальних препаратів пеніцилінового ряду. Однак останні дані свідчать про те, що на фоні прийому будь-яких інших АБП із цитолітичною дією (цефалоспорини, фторхінолони, макроліди, аміноглікозиди) може розвинутися екзантема. Це можна пояснити зменшенням частоти використання пеніцилінів та появою нових АБП [3].
Спочатку екзантему на фоні прийому АБП пеніцилінового ряду намагалися пояснити алергенністю самого пеніциліну, але ця теорія не знайшла свого підтвердження. Першими, хто запропонував пов’язати розвиток висипки на фоні ІМ та цитолітичну дію АБП, були Берштейн (1950), Лібрах (1951) та Хант (1954). Вони припустили, що внаслідок розпаду мікрофлори кишечника під дією АБП у кров та інші рідини організму потрапляє величезна кількість гаптенів. Це, в свою чергу, призводить до сенсибілізації організму. С.Д. Носов (1964) у роботі «Руководство по инфекционным болезням» писав, що під впливом інфекційного агенту (ще не була доведена етіологічна роль EBV у розвитку ІМ) активуються В-лімфоцити, а отже, виробляється велика кількість антитіл та формується автоімунна реакція. Однак у 30 % пацієнтів екзантему не можна пов’язати з прийомом АБП [3].
Друга теорія також не знайшла свого підтвердження, тому що у хворих із екзантемою рівень IgЕ залишається в межах норми. Автоімунна теорія найбільше підтверджена фактами, тому що в пацієнтів з екзантемою значно частіше виникають автоімунні ураження — гепатит, гломерулонефрит, пневмоніт. Останнім часом з’являється все більше даних про роль EBV у розвитку розсіяного склерозу, синдрому хронічної втоми, системного червоного вовчака та ревматоїдного артриту [7].
Патологічна анатомія
Повідомлення про патологоанатомічні дослідження при гострій EBV-інфекції нечисленні, тому що летальні випадки трапляються рідко. Морфологія вивчена в основному на біопсії органів — лімфатичні вузли, печінка, селезінка.
На ранніх стадіях захворювання патологічний процес у лімфатичних вузлах обмежується проліферацією ретикулярних і лімфоїдних клітин з утворенням крупних мононуклеарних форм. У період розпалу хвороби у зв’язку з проліферацією одноядерних клітинних елементів (великі клітини з широкою облямівкою базофільної протоплазми) структура органа стає нечіткою. Одночасно з проліферацією мононуклеарів відмічається гіперплазія ретикулярних клітин. У ряді випадків в лімфатичних вузлах визначалися вогнищеві та розповсюджені некрози. При повторній біопсії в періоді пізньої реконвалесценції структура лімфатичної тканини повністю відновлювалася. Проліферація мононуклеарних клітин також відбувається в перитонзилярних тканинах, глотковому кільці та стінці глотки [8].
Характерними змінами в печінці є утворення лімфоїдноклітинних інфільтратів та ретикуло-ендотеліальних елементів, що розташовані перипортально та всередині часточок. Архітектоніка печінки, як правило, не змінюється. А.Ф. Блюгер відмічає, що при жовтушних формах ІМ з’являються одиничні жовчні тромби та відкладення жовчного пігменту в гепатоцитах центральних зон часточок. На відміну від епідемічного гепатиту при ІМ реакція мезенхіми різко переважає над змінами паренхіми. При повторних біопсіях печінки відмічається відставання відновлення морфологічної структури печінки порівняно з відновленням її функціональних можливостей. У періоді пізньої реконвалесценції відмічається повне відновлення структури печінкової тканини [8].
Зміни за типом лімфоїдно-клітинної інфільтрації також описані й в інших органах — легені, серце, нирки, ЦНС. При менінгоенцефалітах на розтині знаходили набряк головного мозку, некрози та численні інфільтрати. Ці спостереження свідчать про те, що в основі патологічного процесу при ІМ лежить проліферація лімфоїдної та ретикулярної тканини [8].
Клініка
Інкубаційний період становить 4–15 днів (у середньому близько тижня). Єдиної клінічної класифікації досі не існує. Наводимо класифікацію М.А. Андрейчина та А.О. Руденко (2003) із додатками:
1. Форма захворювання:
— латентна:
а) субклінічна;
б) інапарантна;
— маніфестна:
а) типова;
б) атипова:
– респіраторна;
– кишкова (у тому числі псевдоапендикулярна);
– токсико-алергічна;
– змішана.
2. Ступінь тяжкості:
— легкий;
— середньої тяжкості;
— тяжкий.
3. За тривалістю перебігу:
— гострий (до 1 місяця);
— підгострий (від 1 до 3 місяців);
— затяжний (від 3 до 6 місяців).
4. Результат захворювання:
— одужання (формування нестерильного імунітету);
— хронізація:
а) хронічна латентна;
б) хронічна рецидивуюча:
— онкологічний;
— системні автоімунні захворювання.
5. Ускладнення:
— абдомінальні;
— гематологічні;
— неврологічні;
— із боку дихальної системи;
— із боку серцево-судинної системи;
— внаслідок приєднання вторинної бактеріальної флори;
— нефрологічні.
Типова форма зустрічається в 56–72 % випадків. Захворювання починається гостро. Хворі скаржаться на значну загальну слабкість, що не відповідає даним об’єктивного огляду, ломоту в тілі, головний біль, підвищення температури тіла, рідше — на болі при ковтанні та закладеність носа. Звертає на себе увагу характерний вид хворого — набряклі повіки та надбрівні дуги, напіввідкритий рот, сухі та почервонілі губи. Класична температурна крива неправильного типу, хвилеподібна, іноді абортивна. Тривалість лихоманки — 1–3 тижні. Периферичні лімфатичні вузли збільшуються на 2–3-й день захворювання. Рідко реєструється стертий початок, коли першим симптомом захворювання є збільшення шийних груп лімфатичних вузлів. До кінця першого тижня хвороби формується основний симптомокомплекс: інтоксикаційний синдром, тонзиліт, фарингіт, лімфаденопатія та гепатоспленомегалія. Тонзиліт може бути катаральним, лакунарним та виразково-некротичним з утворенням нальотів, що нагадують дифтеритичні. Лакунарна та виразково-некротична ангіна є наслідком приєднання вторинної бактеріальної флори. Унаслідок ураження слизової оболонки задніх хоан хворі скаржаться на закладеність носа без нежитю. Лімфаденопатія відзначається в усіх хворих. Найчастіше вражаються підщелепні та задньошийні лімфовузли, рідше — пахвинні, пахові, кубітальні, як правило, симетрично. У 15–30 % пацієнтів на 3–5-й день захворювання з’являється екзантема (макулопапульозна, дрібноплямиста, папульозна, петехіальна). Зазвичай висипку можна пов’язати з прийомом АБП. Через 1–3 дні екзантема безслідно зникає та повторно не з’являється. Гепатоспленомегалія спостерігається в більшості хворих, збільшення селезінки завжди випереджає збільшення печінки, з’являється на 3–5-й день хвороби та зберігається до одного місяця [10].
Респіраторна форма характеризується стертим початком: підвищення температури тіла рідко досягає фебрильних цифр (тип температурної кривої абортивний), хворі скаржаться на головний біль, ломоту в тілі, загальну слабкість, першіння в горлі та закладеність носа. При об’єктивному огляді відзначається фарингіт, що поруч із незначно вираженими симптомами інтоксикації може бути єдиним клінічним проявом EBV-інфекції.
Кишкова форма. Зустрічається в 3–5 % випадків. Пацієнти скаржаться на незначне підвищення температури тіла, рідкі випорожнення без патологічних домішок, бурчання в животі, зниження апетиту та загальну слабкість. При об’єктивному огляді привертає увагу невідповідність стану хворого об’єктивним даним — пацієнти апатичні, сонливі, іноді депресивні. Запідозрити EBV-інфекцію в таких випадках допомагають характерні зміни гемограми.
Псевдоапендикулярна форма. Характеризується локалізованим ураженням лімфатичних вузлів апендикулярного відростка. Клінічно проявляється симптомокомплексом, що характерний для гострого апендициту. Діагноз встановлюється лише лабораторно.
Токсико-алергічна форма. Основним проявом захворювання є екзантема та автоімунні ураження. Зазвичай розвивається на фоні хронічних алергій. Характерною ознакою токсико-алергічної форми EBV-інфекції є наростання проявів захворювання на фоні лікування. Будь-які медичні препарати можуть погіршувати стан хворого.
При легких формах симптоми інтоксикації виражені помірно, температура не вище 38–38,5 °С, лімфатичні вузли незначно збільшені. Носове дихання не утруднене. Гепатоспленомегалія нерідко відсутня. Показники функціональних проб печінки зазвичай не змінені.
До середньотяжких форм належать випадки з вираженими проявами інтоксикації. Температура, як правило, фебрильна. Відмічається в’ялість, апатія, зниження апетиту. Усі інші симптоми гострої EBV-інфекції також виражені значно сильніше. Тонзиліт зазвичай лакунарний, носове дихання утруднене.
Для тяжкої форми характерні бурхливий початок і різко виражені всі клінічні прояви захворювання: значна інтоксикація, літична температура тіла, сильний головний біль, млявість, адинамія. Тонзиліт лакунарний або виразково-некротичний. Гепатолієнальний синдром сильно виражений, біохімічні показники значно змінені.
Ускладнення при гострій EBV-інфекції розвиваються доволі рідко, але можуть бути досить тяжкими. Реактивний гепатит реєструється більше ніж у 90 % пацієнтів, клінічно максимально виражений на 2–3-му тижні захворювання. У кожного другого хворого спостерігається помірна тромбоцитопенія, що починається з кінця першого тижня хвороби та триває близько 3–4 тижнів. Гемолітична анемія зустрічається в 0,5–3 % пацієнтів. Гемоліз зазвичай помірний, із максимальною вираженістю на 2–3-му тижні захворювання. Обструкція верхніх дихальних шляхів зазвичай зустрічається в дітей [10].
Розрив селезінки (спонтанний або травматичний) відзначається в 0,1–0,2 % хворих на гостру EBV-інфекцію, як правило, на 2–3-му тижні захворювання. Пацієнти скаржаться на помірний або різкий біль у животі з іррадіацією в ліве плече й надключичну ділянку. Масивна кровотеча супроводжується перитонеальними симптомами й гіповолемічним шоком. Симптомами, що насторожують, є тахікардія понад 100 уд/хв та нейтрофільоз. Показане екстрене оперативне втручання [10].
Неврологічні й нефрологічні ускладнення та ускладнення з боку дихальної й серцево-судинної систем при гострій EBV-інфекції розвиваються менше ніж в 1 % випадків, але характеризуються дуже тяжким перебігом [10].
Результати захворювання залежать від вираженості імунної дисфункції та імуногенетичної схильності до EBV-асоційованих захворювань. Одужанням при гострій EBV-інфекції прийнято вважати відсутність клінічних симптомів захворювання, зсувів у базових лабораторних показниках та виявлення ДНК вірусу в одиничних В-лімфоцитах або епітеліальних клітинах.
Лабораторна діагностика
У загальному аналізі крові зазвичай відзначається лейкоцитоз, лімфоцитоз, помірно підвищена ШОЕ. Однак у ряді випадків захворювання може перебігати з нормальною і навіть зниженою кількістю лейкоцитів. Іноді на початку захворювання відмічається незначний зсув лейкоцитарної формули вліво. Особливо велике значення для діагностики гострої EBV-інфекції має наявність у периферичній крові атипових мононуклеарів. Віроцити в більшості випадків з’являються на першому тижні захворювання. Однак у деяких хворих вони можуть почати виявлятися лише на 2–4-му тижні захворювання, а іноді навіть у стадії реконвалесценції. Діагностичним порогом вважається рівень 10 %, але, на нашу думку, для дорослих він є дещо завищеним. При аналізі 218 історій хвороб лише в 68,5 % хворих рівень віроцитів перевищував пороговий. Тому поява атипових мононуклеарів у крові в будь-якій кількості дозволяє запідозрити у хворих гостру EBV-інфекцію. Мононуклеарна реакція може зберігатися до 3–6-го місяців.
Більше ніж у 80 % хворих у біохімічному аналізі крові виявляється підвищення показників активності печінкових ферментів. Пік підвищення лужної фосфатази, АлАТ, АсАТ та білірубіну наступає на 5–14-й день, ГГТП — на 1–3-й тиждень хвороби. Іноді рівень ГГТП залишається підвищеним до 12 місяців, хоча більшість печінкових тестів нормалізується протягом трьох місяців. Рівень білірубіну, як правило, підвищується в 2–3 рази, реєструється в 45 % хворих, клінічно жовтуха виявляється лише в 5 % пацієнтів [3].
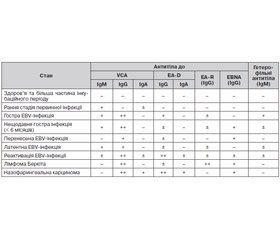
Реакції Пауля — Буннелля та Хоффа — Бауера засновані на виявленні поліклональних гетерофільних антитіл. Однак останнім часом вони перестали використовуватися й розглядаються скоріше в історичному плані. У практичній медицині використовують специфічні методи діагностики: полімеразну ланцюгову реакцію та імуноферментний аналіз (табл. 1).
Після потрапляння в лімфоцити EBV починає продукувати антигени в певній послідовності: поверхневий антиген, ранній антиген, ядерний антиген, мембранний антиген. У відповідь на це організм виробляє антитіла різних класів, виявлення яких дозволяє не тільки діагностувати EBV-інфекцію, але й визначати строки інфікування. EA з’являються в ранню фазу літичного життєвого циклу вірусу (при гострій первинній інфекції або реактивації хронічної EBV-інфекції). Антитіла класу IgG до EA при гострій EBV-інфекції з’являються на 1–2-му тижні хвороби та зникають у середньому через 3–4, максимум через 6 місяців. Наявність антитіл до ранніх антигенів без анти-EBNA IgG в крові свідчить про первинну інфекцію. Іноді антитіла до ранніх антигенів у людей, які одужали, можуть зберігатися протягом довгого часу. Антитіла до ранніх антигенів виявляються також при хронічній активній EBV-інфекції [7].
Наявність EBNA свідчить про присутність у клітині вірусного геному, але не дозволяє говорити про активну репродукцію вірусу. Обстеження, виконане на першому тижні, у 10–15 % хворих дає негативний результат. Антитіла до ядерного антигену EBNA з’являються на 6–8-му тижні й зберігаються протягом всього життя. Цей антиген можна знайти в лімфоцитах хворих на гостру EBV-інфекцію, у клітинах лімфоми Беркіта та назофарингеальної карциноми [7].
Ознакою активності вірусної інфекції є наявність МА та VCA. VCA стимулює вироблення специфічних антитіл класу IgM із першого тижня захворювання, класу IgG — з третього тижня, що зберігаються пожиттєво. Тому виявлення анти-VCA IgM свідчить про гостру інфекцію, а виявлення тільки анти-VCA IgG — про перенесене захворювання [7].
Як експрес-тест для діагностики гнійно-деструктивних ускладнень при гострій EBV-інфекції рекомендоване визначення С-реактивного білка (С-РБ) у сироватці крові. При неускладненому перебігу інфекційного мононуклеозу рівень С-РБ в крові не перевищує 45 мг/л (у нормі ≤ 10 мг/л за Н.У. Тицу) і корелює з такими показниками, як ШОЕ та лейкоцитоз. При цьому вміст С-РБ > 100 мг/л відзначається при тяжких формах захворювання, що зазвичай супроводжується вираженим ураженням лімфоїдної тканини глотки. Таким чином, при показнику С-РБ у крові < 50 мг/л та з урахуванням клінічного статусу слід утримуватися від призначення антибактеріальної терапії [11].
Активність імунопатологічного процесу, пов’язаного з EBV-інфекцією, можна визначити за допомогою вмісту бета-2-макроглобуліну в сироватці крові. Рекомендовано проводити дослідження перед закінченням етіотропного лікування та/або перед випискою із стаціонару. Рівень бета-2-макроглобуліну, вищий за 3,0 г/л, вказує на наявність запального процесу та є ознакою того, що хворі не одужали [11].
При будь-яких формах захворювання рекомендується обстеження хворих на ВІЛ-інфекцію. Для визначення етіологічного чинника інфекційного мононуклеозу, окрім обстеження на EBV, необхідно дослідити сироватку крові хворого на HHV-6 та HHV-7 (особливо в дітей першого року життя для виключення екзантеми субітум), CMV. За наявності реактивних змін у печінці обов’язковим є обстеження на вірусні гепатити (IgM до HAV, HBsAg, IgM до HBcAg, сумарні антитіла до HCV).
Висновки
1. Останніми роками значно підвищився рівень захворюваності на гостру EBV-інфекцію, що, скоріше за все, пов’язано не стільки з епідеміологічним підйомом, скільки з покращенням методів діагностики.
2. Поліморфність клінічної картини, легкі та стерті форми, труднощі, що доволі часто виникають при діагностиці захворювання, дають підстави вважати, що офіційно зареєстрована захворюваність в Україні не відображає істинної поширеності інфекції.
3. Реакції Пауля — Буннелля та Хоффа — Бауера, засновані на виявленні поліклональних гетерофільних антитіл, останнім часом розглядаються скоріше в історичному аспекті. У практичній медицині використовують специфічні методи діагностики: полімеразну ланцюгову реакцію та імуноферментний аналіз.
4. Як експрес-тест для діагностики гнійно-деструктивних ускладнень при гострій EBV-інфекції рекомендоване визначення С-РБ (бажано кількісний) у сироватці крові.
5. Активність імунопатологічного процесу визначається за допомогою вмісту бета-2-макроглобуліну в сироватці крові.
1. Семейство герпесвирусов на современном этапе / Т.К. Кускова, Е.Г. Белова // Лечащий врач. — 2004. — № 5.
2. Медицинская микробиология / Под ред. В.И. Покровского. — М.: ГОЭТАР-медицина, 1998.
3. Возіанова Ж.І., Глей А.І. Інфекційний мононуклеоз, спричинений вірусом Епштейна — Барр // Мистецтво лікування. — 2005. — № 5. — С. 8–12.
4. Казмирчук В.Е., Мальцев Д.В. Клиника, диагностика и лечение герпесвирусных инфекций человека. — К.: Феникс, 2009. — 248 с.
5. Buckley R. H. Humoral immunodeficiency // Clin. Immunol. Immunopathol. — 1986. — 40. — 13–24.
6. Дитячі інфекційні хвороби (Клінічні лекції): Підручник / Під ред. проф. С.О. Крамарєва. — К., 2003.
7. Schooley R.T. Epstein-Barr virus (infectious mononucleosis) // Mandell. Principles and Practice of Infectious Diseases. — 5th ed. — 2000. — 1599–1608.
8. Инфекционные болезни у детей: Пер. с англ. / Под ред. Д. Марри. — М.: Практика, 2006. — 928 с.
9. Краснов В. В. Инфекционный мононуклеоз. Клиника, диагностика, современные принципы лечения. — СПб.; Н. Новгород, 2003.
10. Инфекции, вызываемые вирусом Эпштейн — Барра, включая инфекционный мононуклез // Внутренние болезни. Книга 4 / Под ред. Е. Браунвальда. — М.: Медицина, 1994. — С. 101–109.
11. Маврутенков В.В. Епштейна-Барр інфекція: імунопатогенез, клініка, діагностика та лікування: Автореф. дис… д-ра мед. наук. — К., 2009. — 40 с.

/19/19.jpg)