Журнал «Медицина неотложных состояний» 7 (62) 2014
Вернуться к номеру
Целевой температурный менеджмент в клинической практике интенсивной терапии критических состояний
Авторы: Царев А.В. — Кафедра анестезиологии и интенсивной терапии ГУ «Днепропетровская медицинская академия» МЗ Украины
Рубрики: Медицина неотложных состояний
Разделы: Справочник специалиста
Версия для печати
Освещены современные представления о механизмах нейропротекции, показаниях и противопоказаниях к клиническому применению, возможных осложнениях, а также будущих направлениях использования целевого температурного менеджмента в реаниматологии.
Висвітлено сучасні уявлення про механізми нейропротекції, показання і протипоказання до клінічного застосування, можливі ускладнення, а також майбутні напрямки використання цільового температурного менеджменту в реаніматології.
This article considers the current understanding of the mechanisms of neuroprotection, indications and contraindications for clinical use, possible complications, as well as future directions for use of the target temperature management in critical care medicine.
целевой температурный менеджмент, терапевтическая гипотермия, гипертермия, интенсивная терапия.
цільовий температурний менеджмент, терапевтична гіпотермія, гіпертермія, інтенсивна терапія.
target temperature management, therapeutic hypothermia, hyperthermia, intensive care.
Статья опубликована на с. 186-191
История клинического применения терапевтической гипотермии (ТГ) в современной медицине составляет чуть более 200 лет. Так, в 1812 г. Baron de Larrey, военный хирург наполеоновской армии, использовал гипотермию с целью обезболивания при ампутациях конечностей на поле боя. Особое значение имеют фундаментальные работы П.И. Бахметьева (1860–1913). Первый случай клинического применения ТГ относится к 1937 г., когда T. Fay провел охлаждение тела (путем обкладывания пакетами со льдом) до 32 °С на протяжении 24 часов пациентке с онкозаболеванием для предотвращения метастазирования. В 1941 г. Smith и Fay сообщили о более быстром восстановлении сознания при использовании ТГ при тяжелой черепно-мозговой травме (ЧМТ). W.G. Begelow и соавт. (1950) начали использовать ТГ с целью нейропротекции при кардиохирургических вмешательствах. H.L. Rosomoff и R. Gilbert (1955) продемонстрировали прямую зависимость между температурой тела и внутричерепным давлением. D.W. Benson и соавт. (1959) применили ТГ в раннем периоде постреанимационной болезни и показали лучший уровень выживаемости таких больных [1]. Большие экспериментальные исследования были проведены академиком В.А. Неговским и его школой, результатом чего стал выход в 1960 г. монографии «Оживление организма и искусственная гипотермия» [2]. В Украине большой опыт клинического применения гипотермии был накоплен Л.П. Чепким и А.И. Трещинским, что обобщено в монографии «Лечебная гипотермия» (1969) [3].
Необходимо отметить, что к 1959 г. существовал целый ряд показаний для использования ТГ вне оперативных вмешательств. Однако в последующие 30 лет количество работ, посвященных клиническому применению ТГ, резко снизилось в сравнении с большим числом экспериментальных работ [4]. Повторное рождение терапевтической гипотермии связано с открытием в 1987 г. П. Сафаром и соавт. нейропротекторного эффекта мягкой гипотермии, которая оказалась более безопасной, нежели ранее применявшаяся умеренная гипотермия, использование которой лимитировалось развитием ряда побочных эффектов, таких как аритмии, коагулопатия, инфекционные осложнения и пр. [5, 6]. В настоящее время ТГ рассматривается как наиболее многообещающий физический метод нейропротекторной защиты головного мозга, поскольку с позиций доказательной медицины не существует ни одного эффективного метода фармакологической нейропротекции в нейрореанимационной практике.
Точками приложения терапевтической гипотермии в современной реаниматологии являются как ишемически-реперфузионное повреждение головного мозга (постреанимационная болезнь, ишемический и геморрагический инсульт, асфиксия новорожденных, черепно-мозговая травма), так и спинальная травма, печеночная энцефалопатия, острый респираторный дистресс-синдром, острый инфаркт миокарда и пр.
Наиболее изученным в клинике является использование ТГ для лечения постреанимационной болезни. Было выделено три варианта ТГ: 1) protective (протективная) — индуцируется до момента клинической смерти; 2) preservative (предохранительная) — проводимая в момент клинической смерти на фоне реанимационных мероприятий; 3) resuscitative (реанимационная) — после восстановления самостоятельного кровообращения в постреанимационном периоде. В клинической практике согласно международным рекомендациям используется реанимационная ТГ [7].
Другой важной проблемой является разработка методов борьбы с лихорадками центрального генеза при травматических и нетравматических повреждениях головного мозга, рефрактерных к фармакологическим вмешательствам, путем обеспечения терапевтической нормотермии, подразумевающей контроль температуры ядра тела (Тсо) у лихорадящих пациентов с поддержанием ее в пределах нормальных значений.
Объединение указанных двух проблем привело к формированию в 2011 г. нового термина — «целевой температурный менеджмент» (Target temperature management), который, согласно принятому решению международной консенсусной конференции, пришел на смену термину «терапевтическая гипотермия». Профиль целевого температурного менеджмента включает в себя три различные фазы: 1) индукция; 2) поддержание; 3) реверсия — возврат к температурному статусу, поддерживаемому внутренним физиологическим контролем [8].
Физиологические аспекты терморегуляции. Продукция энергии в организме является результатом метаболизма глюкозы, белков и липидов. В последующем, в процессе транспорта электронов и окислительного фосфорилирования, энергия превращается в тепло, которое распределяется в организме и обеспечивает поддержание температуры тела на уровне 37 °С. Продукция тепла зависит от активности метаболизма. Интегративным центром регуляции температуры ядра тела является гипоталамус. При этом в контроль температуры организма вовлечены также нейромедиаторы, такие как норадреналин, дофамин, ацетилхолин, нейропептиды и простагландины, в частности простагландин Е2. Для температуры ядра тела характерны циркадные колебания, контролируемые секрецией мелатонина в супрахиазматических ядрах. Энергия в процессе нейронального метаболизма преимущественно используется для восстановления мембранного потенциала после клеточной деполяризации. В конечном итоге большая часть энергии, используемой в процессе нейронального метаболизма, трансформируется в тепло, и таким образом продукция тепла головным мозгом является важной характеристикой церебральной метаболической активности. У животных выявлены достоверные колебания температуры головного мозга в диапазоне 2–3 °С в ответ на поведенческий стимул [9–11].
Необходимо подчеркнуть, что, имея не более 2–3 % массы тела, головной мозг использует 20 и 25 % от общего потребления организмом кислорода и глюкозы соответственно. При столь высокой метаболической активности 95 % всей потребленной головным мозгом глюкозы утилизируется в процессе аэробного дыхания и только 5 % — в анаэробных условиях. Температура головного мозга первично зависит от 3 факторов: локальной продукции тепла, температуры крови в сосудах и церебральной скорости кровотока.
Примечательно, что имеется закономерность снижения интенсивности потребления кислорода по мере перехода от эволюционно более молодых передних отделов мозга к более старым задним отделам. Максимальная интенсивность дыхания установлена в коре больших полушарий, в то время как в остальных отделах головного мозга снижение скорости потребления кислорода происходит в следующей последовательности: мозжечок и промежуточный мозг — средний и продолговатый мозг — спинной мозг, причем последний имеет наименьшую интенсивность дыхания [9–11].
Механизмы нейропротекторного действия гипотермии. Глубина, а соответственно и тяжесть ишемически-реперфузионного повреждения головного мозга увеличивается при повышении температуры тела на 0,5 °С или более 37 °С. Скорость образования свободных радикалов и реакция глутаматного каскада прямо пропорционально зависят от уровня внутриишемической температуры. Гипертермия активирует NMDA-рецепторы, что, в свою очередь, увеличивает уровень внутриклеточного кальция и свободнорадикального повреждения за счет индуцирования активации арахидоновой кислоты. Причем начальное нейрональное повреждение после ишемии-реперфузии является триггером последующей хронической воспалительной реакции, реализуемой клетками микроглии, которая вызывает развитие прогрессирующей нейродегенерации [9, 11].
В целом в настоящее время выделяют следующие механизмы нейропротекторного действия ТГ:
— ингибирование деструктивных энзиматических реакций (на 1,5 % при снижении Тсо на 1 °С);
— супрессия свободнорадикальных реакций;
— протекция пластичности липопротеинов цитоплазматических мембран;
— снижение потребления кислорода в регионах головного мозга с низким кровотоком;
— улучшение доставки кислорода в ишемические зоны головного мозга и снижение внутричерепного давления;
— снижение внутриклеточного лактатацидоза;
— ингибирование биосинтеза и продукции эксайтотоксичных нейротрансмиттеров [9–11].
Снижение Тсо на 1 °С в среднем снижает скорость церебрального метаболизма на 6–7 %. Необходимо отметить, что в здоровом головном мозге применение анестетиков, вызывающих молчание электроэнцефалограммы, снижает скорость церебрального потребления кислорода (CMRO2) только на 50 % за счет блокирования активного метаболизма. В то же время гипотермия понижает CMRO2 практически до нуля, то есть снижает базальный метаболизм головного мозга. Так, снижение CMRO2 происходит на 7 % при понижении Тсо на каждый градус в диапазоне температур 38–28 °С за счет ингибирования активного метаболизма, а при 28 °С и 18 °С CMRO2 снижается до 50 и 100 % соответственно за счет подавление базального метаболизма [5].
Церебральный метаболизм изменяется линейно с температурой головного мозга, в среднем на 6–8 % при изменении температуры ядра тела на 1 °С. Так, у анестезированных собак при Тсо 28 °С церебральный метаболизм составляет только 50 % по сравнению с уровнем метаболизма при Тсо 37 °С.
Молекулярно-клеточные механизмы действия охлаждения организма при повреждении головного мозга также связаны с ослаблением проапоптических сигналов, таких как цитохром С, реализующих активацию каспаз (каспазозависимый апоптоз). Происходит активация антиапоптических механизмов (Erk-путь, Akt-путь), повышение экспрессии р53, что способствует репарации после фокальной ишемии. Отмечается снижение маркеров оксидативного и NO-зависимого стресса. Низкие температуры также предотвращают повышенную проницаемость гематоэнцефалического барьера за счет ингибирования матрикса металлопротеиназами и предохранения протеинов базального слоя [8, 10, 11].
Клиническое применение гипотермии при критических и терминальных состояниях. По современной классификации, под индуцированной гипотермией понимают снижение температуры ядра тела < 36 °С. Используют следующую классификацию уровней терапевтической гипотермии: мягкая (mild) — 35,9–34 °С, умеренная (moderate) — 33,9–32 °С, умеренно-глубокая (moderate-deep) — 31,9–30 °С, глубокая (deep) — менее 30 °С, сверхглубокая (profound) — 16–4 °С. Было показано, что применение мягкой или умеренной гипотермии улучшает функциональный и морфологический исход со стороны головного мозга. Напротив, использование сверхглубокой гипотермии (15 °С) не улучшает неврологические функции и приводит к ухудшению гистологической картины мозга [10, 12].
Постреанимационная болезнь. Проведенное в 2002 г. в Европе мультицентровое клиническое испытание мягкой терапевтической гипотермии при внегоспитальной остановке кровообращения (Hypothermia After Cardiac Arrest — HACA) у 136 пациентов (целевая Тсо 33 °С в течение 24 часов наружным охлаждением при помощи пакетов со льдом со скоростью охлаждения 0,3–0,9 °С/час) в сравнении с группой нормотермии (n = 137) показало хороший неврологический исход через 6 месяцев у 55 % пациентов, которым применялась ТГ, по сравнению с 39 % в контрольной группе. В связи с чем, согласно рекомендациям как Европейского совета по реанимации (ERC, 2010), так и Американской ассоциации сердца (AHA, 2010), в постреанимационном периоде необходимо обеспечить гипотермию тела до 32–34 °С в течение 12–24 часов как единственный эффективный метод нейропротекции у данной категории больных, реально влияющий на уровень выживаемости и качество неврологического восстановления [4].
Терапевтическая гипотермия должна быть индуцирована как можно раньше после восстановления самостоятельного кровообращения. Результаты рандомизированных исследований показали, что использование ТГ увеличило выживание с отношением разницы 2,5 (95% доверительный интервал 1,8–3,3) и обеспечило улучшение неврологического исхода с отношением разницы 2,5 (95% доверительный интервал 1,9–3,4) в постреанимационном периоде [8, 11].
В исследовании было показано, что уровень осложнений при проведении ТГ в группе пациентов с остановкой кровообращения с клиникой кардиогенного шока не отличался от контрольной группы [11].
Авторы показали на примере 873 пациентов с проведением ТГ развитие следующих осложнений: пневмонии — 38 % случаев, кровотечений, требовавших проведения гемотрансфузии, — 5 %, серьезных нарушений ритма — 29 % случаев [13]. Влияние ТГ на биоэлектрическую активность сердца в постреанимационном периоде до конца не исследовано. Было показано кардиопротекторное действие ТГ на миокард за счет снижения потребления кислорода и улучшения миокардиального энергетического метаболизма [14].
В очень небольшой группе пациентов (n = 5) с остановкой кровообращения по механизму фибрилляции желудочков в процессе проведения ТГ в постреанимационном периоде скорость мозгового кровотока снижалась в средней мозговой артерии либо соответствовала развитию церебральной вазоконстрикции. Изменение показателя SjO2 достоверно коррелировало с изменением уровня РаСО2: так, снижение РаСО2 на 1 кПа приводило к снижению SjO2 на 9,5 %. При этом снижение уровня РаСО2 приводило к снижению скорости кровотока в средней мозговой артерии [15].
Черепно-мозговая травма. В исследовании, проведенном у 43 пациентов, изучалась эффективность и безопасность пролонгированной ТГ (> 48 часов) с тяжелой ЧМТ. Целевая Тсо — 32–33 °С, средняя длительность ТГ — 8 суток (от 2 до 19 суток). В результате хороший неврологический исход был отмечен у 20 пациентов. Среди осложнений регистрировалось развитие пневмонии в 45 % случаев, из них смерть от сепсиса — в 5 %, снижение количества лейкоцитов и тромбоцитов на 10-й день, развитие гипокалиемии в момент проведения индукции ТГ [16]. Проводится целый ряд исследований ТГ при ЧМТ, однако в настоящий момент для рутинного использования данный метод не рекомендуется.
Инсульты. Проводятся активные исследования ТГ при инсультах, при этом было показано, что даже незначительное снижение Тсо до 35,5 °С на протяжении 6 часов обеспечивает 5% снижение абсолютного риска смерти. Показана высокая эффективность мягкой ТГ при ЧМТ как при стандартном времени экспозиции (12–24 ч), так и пролонгированной — от 2 до 19 суток, без существенных осложнений [8, 10].
Неонатальная постаноксическая энцефалопатия. В рандомизированном контролируемом клиническом испытании, включавшем 239 новорожденных, было продемонстрировано снижение летальности и улучшение неврологических исходов при проведении ТГ (33,5 °С) на протяжении 72 часов [8].
Фульминантная печеночная недостаточность, характеризующаяся выраженной печеночной энцефалопатией. В эксперименте мягкая гипотермия снижает уровень аммиака в ликворе и внутриклеточном пространстве, а также внутричерепное давление, предотвращает аммиак-индуцированный отек головного мозга. ТГ сохраняет ауторегуляцию мозгового кровотока за счет снижения уровня провоспалительных цитокинов, таких как TNF-a. В последних рекомендациях по интенсивной терапии фульминантной печеночной недостаточности (US Acute Liver Failure Study Group) в случае развития внутричерепной гипертензии, рефрактерной к стандартным методам терапии, рекомендуется проведение мягкой ТГ (33–35 °С). Проводилось исследование ТГ у пациентов с острой печеночной недостаточностью, вызванной отравлением ацетоминофеном (то есть с исходно здоровой печенью), с целью купирования внутричерепной гипертензии. Целевая Тсо составила 32–35 °С [10].
Острый респираторный дистресс-синдром — показано снижение летальности на 34 % в сравнении с группой нормотермических больных [10].
Клинические аспекты проведения гипотермии в реаниматологии. В настоящее время рекомендуется выполнение следующих требований в технологии проведения ТГ:
— мониторинг: температура ядра (внутрипищеводная, тимпанитная, ректальная), контроль показателей системы гемостаза, содержания газов крови и электролитов, уровня гликемии и лактата, показателей гемодинамики;
— длительность — 12–24 часа;
— целевая температура ядра 33–34 °С;
— проведение искусственной вентиляции легких;
— для купирования холодовой дрожи — аналгоседация, миорелаксанты, применение клонидина, нефопама, дексмедетомидина. Наиболее оптимальным, использующимся за рубежом препаратом для купирования дрожи считается агонист k-опиоидных рецепторов — меперидин;
— медленное согревание — 0,25–0,5 °С/час [11].
Побочными эффектами ТГ являются повышение вязкости крови, холодовой диурез, однако без нарушения функции почек, повышенный риск развития пневмонии. При этом развитие серьезных аритмий редко встречается при Тсо 33 °С, даже у больных с ишемией миокарда [11]. Противопоказаниями к проведению ТГ являются: беременность, кардиогенный шок (систолическое артериальное давление менее 90 мм рт.ст. при инфузии симпатомиметиков), передозировка лекарственными препаратами и наркотиками, тяжелая системная инфекция, наличие синдрома полиорганной недостаточности, предшествующая коагулопатия (при этом проведение фибринолитической терапии не является противопоказанием) [7, 10].
В настоящее время используют следующие технологии индуцирования гипотермии:
1) путем внутривенной инфузии 4 °С 0,9% NaCl или раствора Рингера лактата в дозе 30 мл/кг, со скоростью введения 100 мл/мин (рис. 1А);
2) использование самоклеющихся гидрогельсодержащих замороженных пакетов (рис. 1Б);
3) неинвазивного индуцирования гипотермии интраназальной системой охлаждения RhinoChill (BeneChill, Inc.), обеспечивающей доставку испаряющегося перфторуглеродного соединения в полость носа (рис. 1В, 1Г);
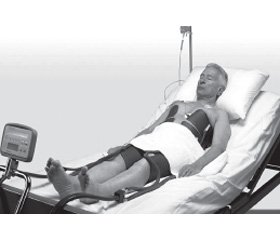
4) наружного охлаждения циркуляцией холодной воды гипотермами Blanketrol (CSZ) (рис. 1Д), ThermoSuit Systems (LRS) (рис. 1Е), использование самоклеющихся гидрогельсодержащих пакетов гипотермом Arctic Sun 2000 (рис. 1Ж);
5) эндоваскулярного охлаждения гипотермами Innercool System (рис. 1З) и CoolGard 3000.
Контролируемая нормотермия. Лихорадка — стереотипная адаптивная реакция на разнообразные инфекционные или другие воспалительные стимулы. Включает в себя комплекс нейроэндокринных, вегетативных и поведенческих реакций, координируемых гипоталамусом. Температура мозга в значительной степени зависит от уровня метаболической активности ткани мозга. Церебральный клеточный метаболизм — главная детерминанта температуры мозга, и незначительные изменения температуры мозга приводят к значительным изменениям в метаболизме нейронов, а следовательно, и функционировании мозга. Поэтому контроль и поддержание оптимальной температуры мозга являются важными факторами для обеспечения его функционирования.
Лихорадка — характерный компонент вторичного повреждения при черепно-мозговой травме, субарахноидальном кровоизлиянии или инсультах. При этом необходимо подчеркнуть, что поддержание нормотермии у пациентов с травматическими и нетравматическими повреждениями головного мозга обеспечивает снижение степени тяжести вторичного повреждения.
Причиной гипертермии у больных в критическом состоянии выступают инфекции, синдром отмены алкоголя либо препаратов, травматические и нетравматические повреждения головного мозга, венозный тромбоэмболизм, инфаркт миокарда, желудочно-кишечные кровотечения, острый панкреатит, некалькулезный холецистит, адреналовая недостаточность, острая кишечная непроходимость и гипертиреоидизм. Целый ряд препаратов, используемых в отделении реанимации и интенсивной терапии (ОРИТ), такие как антибиотики, антиконвульсанты, препараты с антихолинергическим эффектом и симпатомиметики, может вызвать пирогенные реакции. Эпизоды фебрильного подъема температуры тела могут быть связаны с проведением гемотрансфузии.
Проведенный анализ у более чем 20 тыс. пациентов, которые находились на лечении в ОРИТ, показал развитие лихорадки у 44 %, а тяжелой лихорадки — у 8 % пациентов. При этом развитие гипертермии наблюдалось наиболее часто у пациентов с травматическими и нетравматическими повреждениями головного мозга, пациентов молодого возраста, у мужчин, а также имевших по шкале АРАСНЕ II ≥ 25 баллов. При этом пациенты с лихорадкой или тяжелой лихорадкой имели положительные результаты микробиологических посевов в 17 и 31 % соответственно. Лихорадка ассоциировалась с высоким риском смерти [8, 11].
Наиболее высокая частота развития лихорадки при критических состояниях у пациентов с повреждением головного мозга. Так, в ретроспективном анализе 6759 пациентов в ОРИТ неврологического профиля с длительностью пребывания в реанимационном отделении более 2 суток было показано, что развитие невысокой лихорадки (37,5–38,4 °С), умеренной лихорадки (38,5–39,0 °С) и тяжелой лихорадки (> 39,0 °С) было отмечено у 37, 18 и 17 % пациентов соответственно [8].
Тяжесть ишемически-реперфузионного повреждения головного мозга при черепно-мозговой травме, ишемическом и геморрагическом инсульте, постреанимационной болезни увеличивается при повышении температуры тела на 0,5 °С или более 37 °С [9]. Гипертермия наблюдается у 68 % пациентов с ЧМТ, а у пациентов с субарахноидальным кровоизлиянием — в 70 % случаев. Причем при ЧМТ раннее (в течение первых 48 часов) развитие гипертермии ассоциировано с очень плохими исходами. При инсультах в первые 7 дней у 43 % пациентов развивается гипертермия, которая также ассоциирована с ухудшением исходов заболевания и повышением летальности. В целом считается, что повышение температуры тела на 1 °С увеличивает риск плохого исхода у нейрореанимационных пациентов на 2,2 % [12]. Причем повышение температуры тела у пациентов в критических состояниях ассоциируется с высоким уровнем летальности, плохими исходами и увеличением длительности пребывания как в ОРИТ, так и в больнице.
Это обусловливает актуальность проблемы борьбы с лихорадками центрального генеза, рефрактерными к фармакологическим вмешательствам, у данной категории пациентов путем обеспечения контролируемой нормотермии, подразумевающей контроль температуры ядра тела у лихорадящих пациентов с поддержанием ее в пределах нормальных значений. Нами используется метод контролируемой нормотермии у пациентов в критическом состоянии (ЧМТ, инсульты) с лихорадками центрального генеза, рефрактерными к фармакологическим методам коррекции [17].
Таким образом, разработка методов обеспечения целевого температурного менеджмента и внедрение их в клиническую практику являются перспективным направлением интенсивной терапии, которое позволит улучшить исходы при критических состояниях.
1. Усенко Л.В., Царев А.В. Искусственная гипотермия в современной реаниматологии // Общая реаниматология. — 2009. — № 1. — С. 21–23.
2. Неговский В.А. Оживление организма и искусственная гипотермия. — М.: Медгиз, 1960. — 302 с.
3. Чепкий Л.П., Трещинский А.И. Лечебная гипотермия. — К.: Здоров’я, 1969. — 202 с.
4. Bernard S., Buist M. Induced hypothermia in critical care medicine: A review // Critical Care Medicine. — 2003. — V. 31. — Р. 2041–2051.
5. Behringer W., Bernard S., Holzer M., Polderman K., Tiaineu M., Roine R.O. Prevention of postresuscitation neurologic dysfunction and injury by the use of therapeutic mild hypothermia / Еd. Paradis N.A., Halperin A.R., Kern K.B., Wenzel V., Chamberlaine D.A. // Cardiac Arrest: The science and practice of resuscitation medicine. (2nd ed.). — Cambridge University Press; 2007. — Р. 848–884.
6. Therapeutic hypothermia in resuscitation: The Safar vision // ITASS, Spring, 2004. — P. 49–52.
7. Deakin C.D., Nolan J.P., Soar J., Sunde K., Koster R.W., Smith G.B., Perkins G.D. European Resuscitation Council Guidelines for Resuscitation 2010. Section 4. Adult advanced life support // Resuscitation. — 2010. — V. 81. — P. 1305–1352.
8. Nunnally M.E. et al. Targeted temperature management in critical care: A report and recommendations from five professional societies // Critical Care Medicine. — 2011. — V. 39. — P. 1113–1125.
9. Mayer S.A., Sessler V.A. Therapeutic Hypothermia. — New York: Marcel Dekker, 2005. — 402 p.
10. Nunnally M.E. Therapeutic Hypothermia in the ICU. — SCCM, 2010. — 210 p.
11. Lundbye J.B. Therapeutic hypothermia after cardiac arrest. Clinical application and management. — Springer, 2012. — 122 p.
12. Polderman K.H., Herold I. Therapeutic hypothermia and controlled normothermia in the ICU: Practical considerations, side effects, and cooling methods // Critical Care Medicine. — 2009. — V. 37. — P. 1101–1120.
13. Nielsen N. Outcome after cardiac arrest with focus on therapeutic hypothermia — A report from the hypothermia network // Resuscitation. — 2008. — V. 77 (Suppl.). — P. S27.
14. Tiainen M., Parikka H., Makijarvi M., Takkunen O., Sarna S., Roine R. Arrhythmias and heart rate variability during and after therapeutic hypothermia for cardiac arrest // Critical Care Medicine. — 2009. — V. 37(2). — P. 403–409.
15. Bisschops L., Hocdemackers, Simons K., Van der Hoeven J. Cerebral blood flow and cerebrovascular reactivity during hypothermia after cardiac arrest // Resuscitation. — 2008. — V. 77(Suppl.). — P. S29.
16. Bernard S.A., MacJones B., Buist M.D. Experience with prolonged induced hypothermia in severe head injury // Critical Care. — 1999. — V. 3. — P. 167–172.
17. Царьов О.В., Усенко Л.В., Кобеляцький Ю.Ю. Інформаційний лист про нововведення в сфері охорони здоров’я. — К.: Укрмедпатентінформ, 2012. — № 1. — 4 с.

/190/190.jpg)