Газета «Новости медицины и фармации» Пульмонология. Аллергология. Антимикробная терапия (530) 2015 (тематический номер)
Вернуться к номеру
Особенности лечения негоспитальных пневмоний на амбулаторном этапе. Применение кларитромицина (Клабакс ОD) и левофлоксацина (Локсоф) в современных схемах лечения пациентов с негоспитальной пневмонией
Авторы: Юдина Л.В. — доцент кафедры фтизиатрии и пульмонологии НМАПО им. П.Л. Шупика, г. Киев
Рубрики: Аллергология , Пульмонология
Разделы: Справочник специалиста
Версия для печати
Статья опубликована на с. 18-23
Негоспитальная пневмония (НП) — одно из наиболее распространенных заболеваний с серьезным прогнозом. Заболеваемость пневмонией в Европе колеблется от 2 до 15 случаев на 1000 человек в год. В США ежегодно регистрируют 5,6 млн больных НП, из которых 1,7 млн госпитализируют (среди этих пациентов ежегодно умирает более 60 тысяч человек). На протяжении года общее количество взрослых больных НП (18 лет и старше) в 5 странах Европы (Великобритания, Франция, Италия, Германия, Испания) превышает 3 млн лиц. По данным официальной статистики, в 2012 году в Украине заболеваемость НП составляла 414,4, а в Киеве — 339,2 на 100 тыс. взрослого населения. Смертность от НП в 2012 году в Киеве была на уровне 11,4 на 100 тыс. взрослого населения, а в Украине — 11,8. Больничная летальность в Киеве составляла 1,72 %, а в Украине — 1,11 %.
Основными и наиболее авторитетными источниками информации для врачей по вопросам диагностики и лечения больных НП являются рекомендации (консенсусы), подготовленные ведущими специалистами по результатам проспективных рандомизированных сравнительных контролируемых исследований с учетом постулатов доказательной медицины.
Лечение негоспитальной пневмонии достаточно хорошо изучено и представлено во многих международных и региональных рекомендациях, однако проблема рациональной антибактериальной терапии больных НП не теряет актуальности и в настоящее время. Это требует постоянного обновления национальных рекомендаций в соответствии с накоплением международного опыта. Под руководством академика Ю.И. Фещенко в Украине были разработаны медицинские рекомендации по лечению и диагностике пневмоний, которые являются результатом согласованного решения экспертов [21]. Рекомендации даны на основе детального анализа результатов всех исследований в этой сфере, опубликованных за последние 10 лет в отечественной и зарубежной литературе. Сюда вошли зарубежные консенсусы по ведению взрослых пациентов с НП: российского респираторного общества и международной ассоциации по клинической и антимикробной химиотерапии (РРТ и МАКМАХ, 2010), Британского торакального общества (BTS, 2009), Европейского респираторного общества (ERS, 2005), Американского общества инфекционных болезней/Американского торакального общества (IDS/ATS, 2007).
НП — это острое заболевание, которое возникло во внебольничных условиях или позже 4 часов после выписки из стационара либо же диагностировано в первые 48 часов от момента госпитализации. Заболевание сопровождается симптомами инфекции нижних дыхательных путей (лихорадка, кашель, выделение мокроты, возможно гнойного характера, боль в груди и одышка), а также рентгенологическими признаками новых очагово-инфильтративных изменений в легких при отсутствии очевидной диагностической альтернативы.
Диагноз негоспитальной пневмонии, безусловно, требует применения антибиотиков (АБ), которые являются основой лечения у таких больных. Антибактериальную терапию необходимо начинать сразу после установления диагноза, особенно у тех пациентов, которые нуждаются в госпитализации. Абсолютно неприемлемо промедление со срочным назначением антибиотиков пациентам с тяжелым течением заболевания из-за отсутствия результатов бактериоскопии и посева мокроты, поскольку задержка введения первой дозы антибиотика на 4 часа и больше значительно повышает риск смерти таких больных.
Выбор места лечения — важный вопрос для врача после установления диагноза НП, так как он определяет объем лечебно-диагностических процедур и затраты на лечение. В соответствии с современными принципами ведения взрослых пациентов с НП значительная часть их может лечиться в амбулаторных условиях. В связи с этим особое значение уделяется определению критериев или показаний к госпитализации, которые базируются на ряде известных клинико-лабораторных шкал.
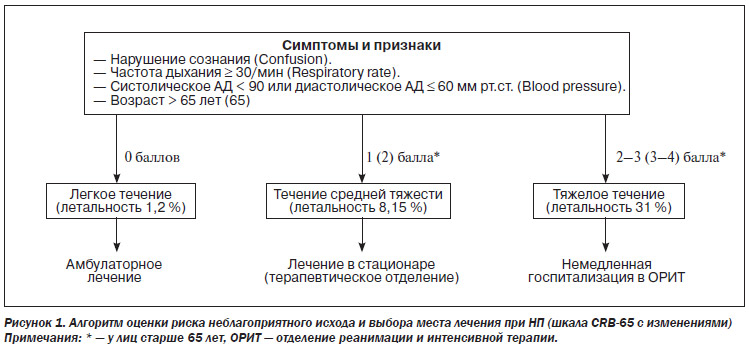
Наиболее простой и доступной для рутинного использования в амбулаторных условиях является прогностическая шкала CRB-65. В ее основе лежит модифицированная шкала Британского торакального общества, в которой предусмотрена оценка 4 параметров: возраста, нарушения сознания, частоты дыхания, уровней систолического и диастолического артериального давления (АД). Исходя из вероятности летального исхода, пациенты делятся на 3 группы в соответствии с тяжестью течения болезни и преимущественным местом лечения (рис. 1). Минимальное количество баллов по этой шкале составляет 0, максимальное — 4.
Основой лечения больных с НП является антимикробная терапия, стратегия которой относится к числу сложных и до конца еще не решенных вопросов современной пульмонологии. Наличие большого арсенала антибактериальных препаратов, с одной стороны, расширяет возможности лечения различных инфекций, а с другой — требует от врача-клинициста осведомленности о многочисленных антибиотиках и их свойствах (спектр действия, фармакокинетика, побочные эффекты и т.д.), умения ориентироваться в вопросах микробиологии, клинической фармакологии и других смежных дисциплинах. Для удобства подбора антибактериальных препаратов целесообразно выделять клинические группы пациентов с НП. В таких группах учитывается сопутствующая патология (хроническое обструктивное заболевание легких, сахарный диабет, застойная сердечная недостаточность, цереброваскулярные заболевания, диффузные заболевания печени и почек с нарушением их функций, хронический алкоголизм и пр.), предварительная антибактериальная терапия (прием системных АБ на протяжении 2 последовательных дней за последние 3 месяца) и тяжесть течения заболевания. Между этими группами могут быть отличия не только в этиологической структуре, распространенности резистентных штаммов известных видов возбудителей, но и в последствиях заболевания. Разделение пациентов с НП на клинические группы определяет тактику лечения. Как правило, антибактериальная терапия назначается эмпирически, основываясь на наличии возможных наиболее часто встречаемых возбудителей, а клинический успех лечения рассматривается как золотой стандарт эффективности препарата. Арсенал современных антибактериальных средств велик, поэтому следует придерживаться определенных критериев выбора, которым должен отвечать антибиотик, назначаемый больному НП. При выборе оптимального препарата основными ориентирами для практического врача являются:
— спектр антимикробной активности препарата;
— фармакокинетика/фармакодинамика антибиотика;
— уровень региональной резистентности микроорганизмов;
— учет сопутствующей патологии у пациента;
— данные о последнем приеме антибактериальных препаратов (когда, какие);
— данные об эффективности различных антибактериальных препаратов с позиций доказательной медицины и адекватной оценки.
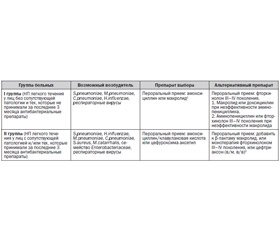
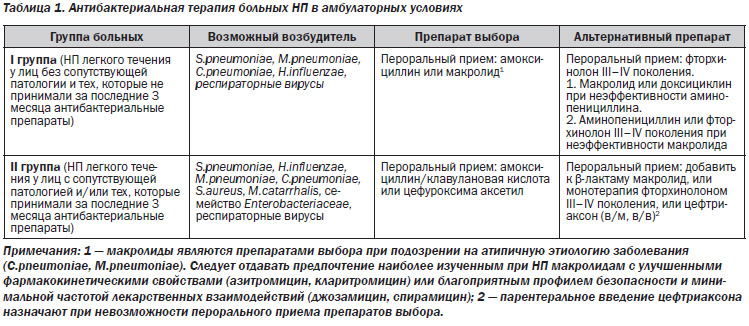
Согласно приказу № 127 МЗ Украины от 19.03.2007 года все больные НП условно делятся на 2 группы (табл. 1), в каждой из которых в зависимости от возраста, тяжести состояния, сопутствующей патологии и других факторов можно предположить наличие того или иного возбудителя. Учитывая известные ограничения традиционной этиологической диагностики негоспитальной пневмонии, а также тот факт, что примерно в половине случаев возбудитель не определяется, рекомендовано начинать лечение с эмпирической терапии.
К I группе относят больных НП с нетяжелым течением, которые не требуют госпитализации, без сопутствующей патологии и других модифицирующих факторов, а также тех, которые в последние 3 месяца не принимали антибактериальные препараты. Наиболее частыми возбудителями у таких пациентов являются S.pneumoniae, M.pneumoniae, C.pneumoniae, H.influenzae (как правило, у курильщиков) и респираторные вирусы. У 30–50 % пациентов возбудителя не определяют вообще, поэтому проводить рутинную микробиологическую диагностику нецелесообразно. Определенную ценность могут иметь данные эпидемиологических исследований (групповая заболеваемость лиц молодого возраста в организованных коллективах характерна при инфекции, вызванной S.pneumoniae или M.pneumoniae). У пациентов этой группы адекватного клинического эффекта можно достичь при пероральном приеме антибактериального препарата в виде монотерапии. Препаратами первой линии являются амоксициллин или макролид (азитромицин, кларитромицин, спирамицин). In vitro амоксициллин не перекрывает весь спектр потенциальных патогенов, однако по данным контролируемых клинических исследований не выявлено достоверных клинических различий в эффективности лечения с применением АБ этих групп, а также отдельных представителей класса макролидных антибиотиков. При отсутствии эффекта предлагается воспользоваться препаратами второго ряда (респираторные фторхинолоны III–IV поколения).
Наряду с аминопенициллинами и респираторными фторхинолонами макролиды обоснованно заняли свою нишу в терапии больных негоспитальной пневмонией. Кларитромицин (Клабакс OD) — один из наиболее исследованных макролидов с улучшенными фармакокинетическими свойствами. Это полусинтетический препарат, относящийся к 14-членным макролидам. Как и другие макролиды, кларитромицин обладает высокой активностью в отношении многих грамположительных бактерий — Staphylococcus (метициллиночувствительных), Streptococcus (включая пневмококки), Enterococcus, Listeria monocytogenes, Corynebacterium diphtheriae. К кларитромицину чувствительны некоторые грамотрицательные бактерии — Moraxella catarrhalis, Neisseria, Campylobacter jejuni, Helicobacter pylori (активность против последнего микроорганизма выше, чем у других макролидов). Кларитромицин является одним из двух макролидов (наряду с азитромицином), обладающих клинически значимой активностью в отношении Haemophilus influenzae. Приблизительно половина дозы кларитромицина, поступая в организм, метаболизируется в печени с образованием активного метаболита — 14-гидроксикларитромицина, который по антибактериальной активности не уступает предшественнику. Активный метаболит 14-гидроксикларитромицин также хорошо проникает в жидкости и ткани дыхательной системы, хотя достигаемые при этом концентрации ниже в сравнении таковыми при приеме исходного вещества [5]. 14-гидроксикларитромицин обладает выраженной активностью в отношении важнейшего возбудителя инфекций дыхательной системы — H.influenzae. Благодаря синергизму со своим активным метаболитом кларитромицин сохраняет высокую активность, даже если уровень препарата в крови несколько ниже минимальной подавляющей концентрации. Данное свойство положительно отличает кларитромицин от большинства других представителей группы макролидов, подавляющее действие которых на H.influenzae, кроме азитромицина, является недостаточным [5–7]. Как и другие макролиды, кларитромицин высокоактивен в отношении атипичных бактерий — Mycoplasma, Ureaplasma, Chlamydia, Legionella, Rickettsia. Максимальная плазменная концентрация достигается менее чем через 3 ч после перорального приема. Кларитромицин легко проникает в ткани и жидкости тела, причем особенно активно накапливается в ткани легких, где его концентрация в 5–6, а в эпителиальных клетках — в 20 раз выше, чем в плазме крови [5, 8]. Аналогичные показатели для слизистой носа и ткани миндалин составляют 2–4 раза [5]. Альвеолярные макрофаги накапливают кларитромицин в количествах, превышающих сывороточный уровень в 200–400 раз. Он также концентрируется в клетках иммунной системы [6]. Так, в гранулоцитах содержание кларитромицина в 20–38, а в мононуклеарах — в 16–24 раза выше, чем во внеклеточной жидкости [9]. За счет этого возможен транспорт АБ непосредственно в очаг воспаления.
Интересно и то, что при наличии атипичных микобактерий и Pseudomonas aeruginosa кларитромицин применяется в комбинации с другими антимикробными препаратами, значительно повышая эффективность проводимой терапии за счет разрушения биопленок.
В настоящее время существует и пролонгированная форма препарата, при которой осуществляется медленное и постепенное высвобождение активного вещества по мере продвижения таблетки по желудочно-кишечному тракту, в результате чего интенсивное тканевое накопление кларитромицина обеспечивает его постоянное присутствие в высоких концентрациях в очаге инфекции (органах дыхания). Достигая высокой сывороточной концентрации, кларитромицин пролонгированного действия (Клабакс OD) хорошо проникает в ткани, накапливается в них, но при этом и в крови поддерживаются достаточно высокие концентрации препарата. Использование антибиотиков внутрь, особенно пролонгированных форм (Клабакс OD), значительно уменьшает риск распространения бактериальной инфекции, нивелирует потребность в дополнительных затратах (шприцы, спирт и т.п.), минимизирует проявления токсического действия препарата, оптимально при лечении в поликлинических условиях и, что очень важно, повышает комплайенс. Клабакс OD применяется 1 раз в сутки, обеспечивая высокий терапевтический эффект. Для лечения НП достаточно 7-дневного курса терапии.
Антимикробный спектр кларитромицина, включающий атипичную флору, S.pneumoniae, H.influenzae, а также новых пролонгированных форм препарата определяет его востребованность в терапии данной категории пациентов. Кларитромицин является препаратом выбора при этиотропной терапии негоспитальной пневмонии, вызванной C.pneumoniae, L.pneumoniae и M.pneumoniae, а также в случае неэффективности стартовой терапии бета-лактамами или при аллергии на них.
Наличие дополнительных свойств (противовоспалительные, иммуномодулирующие, мукорегуляторные) наряду с высокой антибактериальной активностью обеспечивает быстрое регрессирование симптомов и улучшение состояния пациентов с негоспитальной пневмонией при терапии кларитромицином. Помимо антибактериального эффекта, обусловленного нарушением синтеза белка на рибосомах бактерий, у кларитромицина имеются выраженные дополнительные антимикробные свойства:
— постантибиотический эффект в отношении некоторых возбудителей (S.pneumoniae, H.influenzae и M.catarrhalis) [12, 13];
— подавление факторов вирулентности Pseudomonas aeruginosa — кларитромицин способен подавлять двигательную активность данного возбудителя и его способность к формированию биопленок [14].
Другими особенностями кларитромицина, выделяющими его из ряда макролидов, являются:
— лучшая всасываемость в желудочно-кишечном тракте;
— более высокая кислотоустойчивость, стабильность в кислой среде;
— биодоступность при приеме внутрь до 55 %;
— бактерицидный эффект при высокой концентрации препарата.
Следует отметить, что при нетяжелом течении пневмонии вряд ли оправдано стремление некоторых врачей к обязательному назначению парентеральных антибиотиков. Современные антибактериальные препараты характеризуются хорошей биодоступностью при приеме внутрь, а также одинаковой клинической эффективностью с парентеральными препаратами, поэтому в подавляющем большинстве случаев оправдано лечение таблетированными препаратами, нередко в виде монотерапии. Одним из них может быть кларитромицин. При отсутствии эффекта от бета-лактамов и макролидов рекомендовано использовать респираторные фторхинолоны (левофлоксацин (ЛФ), моксифлоксацин).
Ко II группе относят больных с НП легкого течения, с наличием сопутствующей патологии (хроническое обструктивное заболевание легких, почечная и сердечная недостаточность, цереброваскулярная патология, опухоли, сахарный диабет, хронические заболевания печени разной этиологии, психические расстройства, алкоголизм), которые не требуют госпитализации, и/или тех, которые принимали в последние 3 месяца антибактериальные препараты. Возбудителями НП у этих пациентов являются S.рneumoniae (в том числе антибиотикорезистентные штаммы), H.influenzae, S.aureus, M.catarrhalis, респираторные вирусы. Следует учитывать и возможность грамотрицательной инфекции, вызванной представителями семейства Enterobacteriaceae (E.coli, Klebsiella spp.), особенно у людей пожилого возраста. Необходимо предвидеть также вероятность анаэробной инфекции при наличии НП у лиц с несанированной полостью рта, клинико-анамнестическими данными о наличии неврологических заболеваний и/или нарушением акта глотания. Рутинная микробиологическая диагностика у этих больных также малоинформативна и практически не влияет на выбор антибиотиков. Однако примерно у 20 % пациентов этой группы может возникнуть потребность в госпитализации из-за неэффективного амбулаторного лечения и/или обострения/декомпенсации сопутствующих заболеваний. Учитывая возможность наличия у больного резистентного S.pneumoniae, а также грамотрицательной инфекции, препаратами первого ряда считаются защищенные аминопенициллины и цефалоспорины. У пациентов II группы может не быть эффекта от препаратов первого ряда, это связано с тем, что причиной НП является атипичный возбудитель. При наличии атипичной флоры или непереносимости бета-лактамов следует добавить один из современных макролидов (азитромицин, кларитромицин).
Отсутствие эффекта от такой комбинации требует перехода на препараты второго ряда (фторхинолоны III–IV поколения: левофлоксацин (Локсоф) или моксифлоксацин). Фторхинолоны обладают широким спектром антимикробной активности. Эти препараты проявляют природную активность в отношении практически всех потенциальных возбудителей негоспитальной пневмонии. Фторхинолоны III–IV поколений (их называют новыми, или респираторными) характеризуются повышенной активностью в отношении S.pneumoniae и внутриклеточных патогенов. Новые ФХ обладают повышенной в сравнении с классическими фторхинолонами (офлоксацин, ципрофлоксацин) активностью в отношении S.pneumoniae. Высокая антипневмококковая активность новых ФХ наблюдается независимо от чувствительности пневмококка к пенициллину и/или макролидам [15]. Также очевидно превосходство новых ФХ и в отношении атипичных возбудителей (M.pneumoniae, C.pneumoniae, L.pneumophila). И наконец, эти антибиотики унаследовали высокую активность классических ФХ против H.influenzae и M.catarrhalis. Не вызывает сомнений, что респираторные ФХ являются приемлемой альтернативой макролидам, амоксициллину/клавуланату и пероральным цефалоспоринам в лечении негоспитальной пневмонии. К очевидным достоинствам ФХ III–IV поколения следует добавить возможность приема один раз в сутки и использование их в рамках ступенчатой терапии [16]. Левофлоксацин занимает видное место в современных схемах лечения взрослых пациентов с НП, не подлежащих госпитализации, а также в условиях стационара. Левофлоксацин — это левовращающий изомер офлоксацина, L-офлоксацин. Он в 8128 раз активнее, чем D-офлоксацин. Левофлоксацин характеризуется в 2 раза большей активностью, чем офлоксацин, и, следовательно, не уступает в активности ципрофлоксацину. ЛФ обладает уникальной, почти 100% биоэквивалентностью при пероральном применении. Левофлоксацин, как и другие ФХ, обладает бактерицидным типом действия и широким антимикробным спектром. ФХ активны в отношении большинства энтеробактерий, грамотрицательных бацилл (гемофильная палочка, включая бета-лактамазoпродуцирующие штаммы) и грамотрицательных кокков (гоннококк, менинигококк, моракселлы, включая бета-лактамазопродуцирующие штаммы), а также синегнойной палочки. Ранние ФХ (ципрофлоксацин, офлоксацин) имеют некоторую активность в отношении стафилококков и еще меньшую — против стрептококков и энтерококков в отличие от новых ФХ, включая левофлоксацин, высокоактивных в отношении золотистого стафилококка (за исключением метициллиноустойчивых штаммов), коагулазонегативных стафилококков, стрептококков, включая пневмококк. Формирование резистентности к левофлоксацину возможно, однако в настоящее время устойчивость к препарату развивается наиболее медленно и не является перекрестной с другими антибиотиками [12].
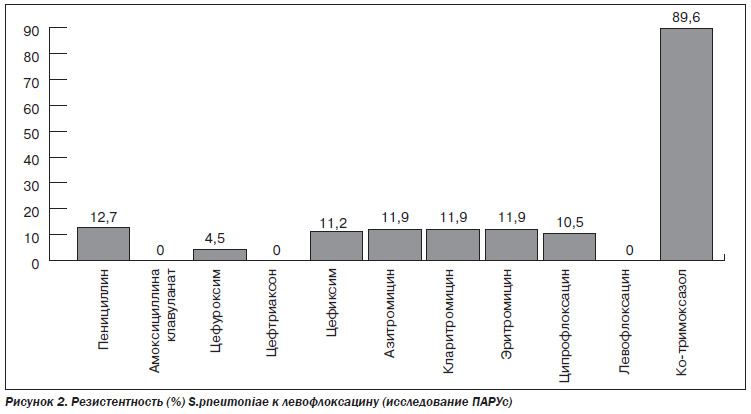
В настоящее время имеются отечественные данные о резистентности S.pneumoniae к левофлоксацину (рис. 2), которые показывают высокую чувствительность пневмококка к данному препарату. Исследование проведено на основе данных ряда клиник (Киева, Днепропетровска, Винницы и других городов) Украины.
Столь высокая активность левофлоксацина делает препарат весьма привлекательным для лечения пациентов с НП как амбулаторно, так и в стационарных условиях.
Левофлоксацин (Локсоф) имеет некоторые фармакокинетические преимущества перед другими ФХ. Это определяется устойчивостью молекулы к трансформации и метаболизму в организме больного. Длительный период полувыведения позволяет назначать ЛФ один раз в день, что повышает комплайентность пациентов. Левофлоксацин подвергается метаболизму всего на 5 %. Около 35 % ЛФ связывается с белками сыворотки крови, поэтому препарат хорошо распределяется в тканях [17]. Следует подчеркнуть, что ФХ, включая ЛФ, отлично проникают в различные ткани, создавая высокие концентрации в почках, простате, женских половых органах, желчи, органах желудочно-кишечного тракта, бронхиальном секрете [18], альвеолярных макрофагах, легочной паренхиме, костях, а также в цереброспинальной жидкости, поэтому данные препараты могут широко применяться при инфекциях практически любой локализации. Кроме того, хорошее внутриклеточное проникновение обеспечивает их активность в отношении атипичных патогенов.
Левофлоксацин проявил себя как наиболее безопасный ФХ с низким уровнем гепатотоксичности (1/650 000). Левофлоксацин наряду с офлоксацином и моксифлоксацином более безопасен в отношении патологического влияния на центральную нервную систему. Кардиоваскулярное негативное воздействие ЛФ наблюдалось значительно реже, чем при использовании других ФХ (1/15 млн назначений, у спарфлоксацина — в 13 % случаев). Диарея, тошнота и рвота — наиболее частые побочные эффекты, связанные с ЛФ, однако они встречаются гораздо реже, чем при приеме других ФХ. Выявлено, что увеличение дозы ЛФ до 1000 мг/сут не приводит к росту числа побочных эффектов, а их вероятность не зависит от возраста пациента [19]. В целом уровень побочных реакций, связанных с ЛФ, наиболее низкий среди ФХ, а переносимость ЛФ может быть расценена как очень хорошая [20].
Таким образом, современные рекомендации по лечению небольничной пневмонии позволяют грамотно назначить эмпирическую терапию этого заболевания. На амбулаторном этапе препаратами выбора являются аминопенициллины, макролиды или респираторные фторхинолоны. Макролиды назначаются в том случае, если нет эффекта от аминопенициллинов или пациент принимал их в течение последних 3 месяцев, а также если имеется аллергия на эти препараты. При подозрении на атипичную этиологию НП (С.рneumoniae, L.pneumophila и M.pneumoniae) препаратами выбора являются макролиды. Предпочтение отдается наиболее изученным при НП макролидам с улучшенными фармакокинетическими свойствами (азитромицин, кларитромицин) или благоприятным профилем безопасности и минимальной частотой лекарственных взаимодействий. Кларитромицин — высокоэффективное и широко апробированное лекарственное средство. Антимикробный спектр этого макролида, включающий атипичную флору, S.pneumoniaе, H.influenzae, а также новые пролонгированные формы препарата (Клабакс OD) определяют его востребованность в терапии данной категории пациентов.
Препаратом второго ряда при лечении пациентов с НП является левофлоксацин. Опыт его применения убедительно доказывает, что это высокоэффективный препарат, сопоставимый по степени эффективности с другими новыми фторхинолонами. Практически в равной степени левофлоксацин (Локсоф) эффективен в отношении как грамположительной, так и грамотрицательной аэробной флоры, а также обладает высокой активностью в отношении атипичных возбудителей. Левофлоксацин имеет практически идеальные фармакокинетические параметры и две лекарственные формы, пероральную и парентеральную, что позволяет максимально оптимизировать дозы и схемы лечения и применять его в рамках ступенчатой терапии. Высокая бактерицидная активность левофлоксацина в сочетании с высокими значениями максимальных концентраций, хорошим проникновением в ткани обеспечивают его максимальный терапевтический эффект.
1. Zhanel G.G. et al. // Antimicrob. Agents Chemother. — 2003. — 47. — 1867–1874.
2. Zhanel G.G. et al. // Antimicrob. Chemother. — 2003. — 52. — 83–88.
3. Whitney C. et al. // N. Engl. J. Med. — 2003. — 348. — 1737–176.
4. Юдина Л.В. Выбор антибиотика при негоспитальной пневмонии: как не ошибиться в выборе // Український пульмонологічний журнал. — 2013. — № 3, додаток.
5. Peters H.D., Clissold S.P. // Drugs. — 1992. — Vol. 44, № 1. — P. 117–164.
6. Zuckerman J.M. // Infect. Dis. Clin. N. Am. — 2004. — Vol. 18. — P. 621–649.
7. Langtry H.D., Brogden N.R. // Drugs. — 1997. — Vol. 53, № 6. — P. 973–1004.
8. Fraschini F., Scaglione F., Pintucci G. et al. // Journal of Antimicrob. Chemotherapy. — 1991. — Vol. 27, suppl. A. — P. 61–65.
9. Белобородова Н.В. // Педиатрия. — 2007. — № 2. — С. 42–44.
10. Верткин А.Л., Оралбекова Ж.М., Скотников А.С. Современные макролиды в лечении внегоспитальной пневмонии. http://www.lvrach.ru/2012/09/15435521/
11. Klugman K.P., Capper T. Levofloxacin in vitro activity and synergistic activity in combination with other antibacterials against antibiotic-resistant S.pneumoniae, and selection of resistant mutants. Abstract E9 // Abstracts of the 35th Interscience Conference on Antimicrobial Agents and Chemotherapy. — Washington, DC: American Society for Microbiology, 1995. — 87.
12. Tenover F.C., Hughes J.M. The challenges of emerging infectious diseases: Development and spread of multiply-resistant bacterial pathogens // JAMA. — 1996. — 275. — 300–304.
13. Report оf the ASM Task Force on Antibiotic Resistance. American society for microbiology // Antimicrob. Agents Chemother. — 1995. — 39 (suppl.). — 223.
14. Multiple-Antibiotic-Resistant Pathogenic Bacteria — A Report on the Rockefeller University Workshop // N. Engl. J. Med. — 1994. — 330. — 1247–1251.
15. Marcus A., Isert D., Klesel N., Selbert C. Killing activity of levofloxacin (LEV) and ciprofloxacin (CIP) against Streptococcus pneumoniaein vitro and in vivo // Program and Abstracts of the Thirty-Fifth Interscience Conference on Antimicrobial Agents and Chemotherapy. — San Francisco, CA, 1995. — Abstract E30. — Р. 90.
16. File T.M. Fluoroquinolones and respiratory tract infections // Infect. Dis. Clin. Pract. — 1997. — 9 (suppl. 2). — 559–566.
17. Kim M.K., Nightingale C.H. Pharmacokinetics and pharmacodynamics of the fluoroquinolones // Andriole V.T., ed. The quinolones. — 3rd ed. — San Diego: Academic Press, 2000. — 169–202.
18. Nacamori Y., Miyashita Y., Nacatu K. Levofloxacin: Penetration into sputum and once-daily treatment of respiratory tract infection // Drugs. — 1995. — 49 (suppl. 2). — 418–419.
19. Fish D.N. Fluoroquinolones adverse effects and drug interactions // Pharmacotherapy. — 2002. — 21 (10, pt 2). — 253–272.
20. Экономическая оценка эффективности лекарственной терапии (фармакоэкономический анализ) / Под ред. проф. Воробьева П.А. — М.: Ньюдиамед, 2000.
21. Негоспітальна пневмонія у дорослих осіб: епідеміологія, етіопатогенез, класифікація, діагностика, антибактеріальна терапія (національна угода) / Ю.И. Фещенко (ред.) // Украінський пульмонологічний журнал. — 2013. — 3(81), додаток. — С. 20.