Журнал «Медицина неотложных состояний» 3 (66) 2015
Вернуться к номеру
Нарушения глотания при инсультах 3. Особенности ведения пациента с дисфагией
Авторы: Сорокин Ю.Н. - Ростовский государственный медицинский университет, Россия
Рубрики: Медицина неотложных состояний
Разделы: Справочник специалиста
Версия для печати
Ведение пациента с дисфагией требует постоянного контроля глотательной функции, правильной организации процесса кормления и подбора консистенции пищи. Восстановлению глотательной функции способствуют проведение реабилитационных упражнений, рефлексотерапия, электростимуляция глоточных мышц, транскраниальная магнитная стимуляция и метод биологической обратной связи. Антибиотикотерапия рекомендуется лишь при верифицированной пневмонии.
Ведення хворого на дисфагію потребує постійного контролю ковтальної функції, правильної організації процесу годування та подбору консистенції їжі. Відновленню ковтальної функції сприяє проведення реабілітаційних вправ, рефлексотерапія, електростимуляція глоткових м’язів, транскраніальна магнітна стимуляція і метод біологічного зворотного зв’язку. Антибіотикотерапію рекомендовано лише за умови верифікованої пневмонії.
Management of a patient with dysphagia requires constant monitoring of swallowing function, proper organization of the feeding process and selection of food consistency. Rehabilitation exercises, reflexotherapy, electrical stimulation of the pharyngeal muscles, transcranial magnetic stimulation and biofeedback method promote the recovery of swallowing function. Antibiotic therapy is recommended only when pneumonia is verified.
реабилитационные упражнения при дисфагии.
реабілітаційні вправи при дисфагії.
rehabilitation exercises for dysphagia.
Статья опубликована на с. 144-149
В предыдущих публикациях «Нарушения глотания при инсультах. 1. Особенности клинических проявлений» и «Нарушения глотания при инсультах. 2. Методы исследования глотательной функции» рассмотрены прогностическое значение дисфагии у больных с мозговыми инсультами, анатомо–физиологические особенности глотательной функции, патогенез, топические особенности, клинические проявления, методы клинического и параклинического исследования нарушений глотания.
Контроль питания и правила кормления пациента с инсультом и нарушением глотания
Необходимо контролировать консистенцию и объем пищи с целью улучшения транзита пищевого болюса. Стандартной практикой является изменение консистенции пищи и жидкости (необходим переход на мягкую пищу и густую жидкость), а также запрет приема пищи через рот для самых тяжелых больных. Вместе с тем, если это возможно, питание через рот является предпочтительным [14].
Для профилактики аспирации у больных с нарушениями глотания необходимы правильные организация процесса кормления и подбор консистенции пищи. При этом одной–единственной диеты при дисфагии не существует. Стандарты модификации твердой и жидкой пищи у больных с инсультами и нарушением глотания различаются в разных странах.
Правила кормления больных с инсультами, имеющих нарушения глотания:
— пациенты с имеющейся аспирацией должны начинать принимать пищу только после получения инструкций для предотвращения аспирации;
— необходима тщательная ревизия полости рта перед приемом пищи (для удаления накопившихся бактерий со слизистой полости рта) и после окончания кормления (оставшаяся пища может быть аспирирована);
— нужен контроль над необходимостью использования зубных протезов; зубы и протезы необходимо чистить не менее 2 раз в день, чтобы быть уверенным в чистоте полости рта;
— кормление необходимо проводить только в положении сидя (туловище под углом 90°), с опорой под спину, при необходимости можно обеспечить поддержку пациента подушками; нельзя кормить лежащего пациента;
— прием пищи должен проводиться в спокойной обстановке. Пациент должен есть не торопясь и не отвлекаясь на разговоры, телевизор, радио;
— необходимо наблюдать за симптомами дисфагии во время приема пищи и в течение 30 минут после еды; при этом в течение 30–60 минут должно сохраняться вертикальное или близкое к нему положение тела пациента для обеспечения пищеводного клиренса и желудочной секреции и уменьшения рефлюкса;
— проводящий кормление должен находиться на уровне глаз пациента;
— одномоментно можно давать только небольшое количество пищи, кратность приема при этом необходимо увеличить;
— при кормлении пищу закладывают с непораженной стороны небольшими порциями;
— во время кормления необходимо обеспечить наклон головы кпереди, нельзя запрокидывать голову пациента кзади;
— кормление проводится с чайной металлической ложки и с низкой скоростью (пациенты с правополушарными инсультами отличаются импульсивностью и склонностью к глотанию в слишком быстром темпе);
— не рекомендуется использовать столовые ложки и ложки из пластика у пациентов с повышенным рефлексом прикуса;
— необходимо научить пациента брать пищу и подносить ее ко рту рукой или сразу двумя руками. Если он может пользоваться для еды ложкой, нужно сделать ручку ложки толще — это облегчит ее удержание (можно использовать кусок резинового шланга или сделать ручку из дерева);
— в момент проглатывания пищи необходимо поворачивать голову в сторону поражения — в сторону паретичных мышц глотки или языка;
— необходимо удостовериться в завершении глотания, прежде чем предлагать следующую порцию;
— если больной не может всасывать жидкость, нужно научить его пить с ложки; поощряется безо–пасное глотание из широкой чашки или стакана;
— для стимуляции глотания можно использовать трубочку для питья или поильник с длинным носиком, который препятствует отклонению головы кзади и, таким образом, уменьшает риск аспирации;
— необходимо научить пациента подносить пищу или жидкость к середине рта, а не сбоку, и брать пищу в рот, используя губы, а не зубы;
— необходимо научить больного держать губы сомкнутыми, а рот закрытым, когда он жует или проглатывает пищу. Если нижняя губа отвисает книзу, нужно научить пациента поддерживать ее пальцами;
— после еды необходимо проследить, чтобы во рту не оставались кусочки пищи, — нужно прополоскать рот или очистить ротовую полость салфеткой. Если пациент поперхнулся, надо дать возможность откашляться, поить при этом не следует, так как жидкость легко проникает в дыхательные пути.
Требования к пище при кормлении больных с инсультами, имеющих нарушения глотания:
— пища должна выглядеть аппетитно;
— добавление лимонной кислоты в пищу улучшает глотательный рефлекс за счет улучшения вкуса и стимуляции кислотой;
— пища должна быть достаточно теплой, так как пациентам с дисфагией необходимо длительное время для ее приема. Если больной не чувствует теплую пищу во рту, кормить нужно едой комнатной температуры;
— твердую и жидкую пищу необходимо предлагать в разное время, напитки следует давать до или после приема пищи;
— лучше всего переносится полужесткая пища: запеканка, густой йогурт, протертые овощи и фрукты, жидковатые каши, желе, суфле, котлеты;
— необходим подбор консистенции пищи (мягкая пища, густое пюре, жидкое пюре) и жидкости (консистенция мусса, йогурта, густого киселя, сиропа, воды). Во все жидкости рекомендуется добавлять загустители, например крахмал или пищевой желатин. Следует помнить, что при более жидких пище или питье труднее сделать безопасный (без аспирации) глоток. Супы или твердые продукты можно довести до однородной массы с помощью блендера или миксера;
— рекомендуются сухофрукты и кисломолочные продукты (кефир, простокваша), особенно лежачим больным со склонностью к запорам;
— рекомендуется обеспечить пациента достаточным количеством солей калия (курага, изюм, капуста, картофель, инжир) и магния (каши из гречневой и овсяной крупы);
— необходимо исключить из рациона продукты, часто вызывающие аспирацию, — жидкость обычной консистенции (вода, соки, чай), или легко крошащиеся — хлеб, печенье, орехи;
— не рекомендуются мясо кусками и цитрусовые, волокна которых тяжело пережевываются;
— не рекомендуется смешивать пищу и напитки в один прием — пить желательно до или после еды.
В общем виде специальная диета включает 4 различные консистенции: плотная жидкость, протертая, измельченная и мягкая рубленая пища. При мягкой диете исключаются все жесткие, мелкие и волокнистые частицы пищи. При этом мясо может иметь 3 консистенции: рубленое, измельченное и молотое.
Рубленая пища является фактически полужесткой и более предпочтительной по сравнению с пюре, так как в ней больше волокнистых структур, стимулирующих глотание. Протертая пища имеет консистенцию пудинга и обычно легче глотается, чем более привычная диета, поскольку при этом она является достаточно густой, чтобы формировать пищевой комок, стимулирует чувствительность слизистой рта и улучшает возможность глотания. В то же время при кормлении протертой пищей также имеется риск аспирации. Меньший риск развития аспирации имеют больные, получающие густые жидкости, по сравнению с получавшими пищу жидкой консистенции (ОШ = 0,13; 95% ДИ 0,04–0,39; р < 0,001) [10].
Различают 4 типа консистенции жидкости [2]:
1) консистенция мусса (жидкость держится на вилке);
2) консистенция йогурта (жидкость стекает с вилки крупными каплями);
3) консистенция сиропа (жидкость окутывает вилку, но быстро стекает с нее);
4) консистенция воды (жидкость сразу стекает с вилки).
В остром периоде инсульта консистенцию жидкостей подбирают в зависимости от возможностей больного. При этом сначала предпочтительнее использовать для кормления густую жидкость (мусс, йогурт, кисель, кефир), которая гораздо легче проглатывается, чем вода, поскольку медленнее проходит по ротоглотке и тем самым оставляет больше времени для подготовки к началу глотания. Затем постепенно, по мере восстановления функции глотания, переходят к более текучим жидкостям. До восстановления у больного функции глотания необходимо избегать жидкостей обычной консистенции (вода, соки, чай, молоко). Если пациент очень плохо глотает жидкости, можно добавить жидкость в твердую пищу и довести пищу до консистенции жидкого пюре. Не рекомендуется использовать сухую пищу — хлеб, печенье, крекеры, орехи.
В связи с тем, что в целом больные с инсультами потребляют недостаточное количество жидкости и характеризуются дегидратацией, особенно пациенты с аспирацией, выявленной при проведении видеофлюороскопии, получающие густые жидкости и принимающие диуретики, необходим прием достаточного количества жидкости в течение суток.
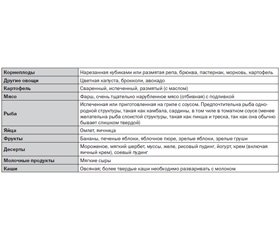
Продукты, являющиеся наиболее легкими для глотания, представлены в табл. 1 [2].
Дополнительные возможности восстановления глотательной функции
Для облегчения процесса глотания возможно использование компенсаторных (позиционных) приемов, позволяющих компенсировать слабость мышц, обеспечивающих акт глотания.
Для восстановления глотательной функции очень важным является осуществление комплекса упражнений лечебной физкультуры, направленных на нарастание мышечной силы и улучшение координации мышц, участвующих в акте глотания. Выбор конкретных приемов из всего комплекса реабилитационных орофарингеальных упражнений зависит от степени выраженности дисфагии и возможностей пациента. Занятия противопоказаны при тяжелом общем состоянии, гипертермии, повышенном артериальном давлении или быстрой утомляемости больного.
Вместе с тем эффективность компенсаторных приемов считается спорной. Реабилитационные упражнения, способствующие увеличению силы мышц, обеспечивающих акт глотания, позволяют в 1,5 раза быстрее и в большей степени восстановить функцию глотания, что сопровождается и снижением частоты развития пневмоний [13].
Компенсаторные приемы:
— изменение положения головы (поворот в сторону поражения — в сторону паретичных мышц глотки или языка) для уменьшения вероятности аспирации;
— пригибание подбородка к грудине перед моментом проглатывания пищи, которое способствует сопоставлению надгортанника и черпаловидно–подгортанной складки и приводит к закрытию дыхательных путей во время глотания;
— в дополнение к этому приему возможен одновременный наклон туловища кпереди;
— двойное глотание — осуществление повторного глотательного движения с целью минимизации рефлюкса после глотания и предотвращения новой аспирации;
— кашель после глотания — осуществление кашлевых движений после проглатывания пищи с целью предотвращения аспирации.
Реабилитационные упражнения:
— прием Шейкер — в положении лежа на спине поднимать голову в течение нескольких секунд, повторяя это 20 раз. Способствует улучшению открытия верхнего сфинктера пищевода за счет укрепления надподъязычной мышцы и уменьшению тем самым остатков пищи в глотке после глотания;
— прием Мендельсона — длительное сокращение надподъязычных мышц с целью обеспечения подъема гортани, открытия верхнего сфинктера пищевода и закрытия дыхательных путей;
— прикоснуться кончиком языка к мягкому небу с открытым ртом, а затем — с закрытым (6–8 раз);
— крепко удерживая кончик языка зубами, сделать глотательное движение (должно ощущаться напряжение в глотке и затруднение в начале глотания);
— глотание капли воды из пипетки;
— при возможности: глотание слюны, капель воды, сока или просто имитация глотательных движений (выполнять упражнение только после консультации с врачом);
— имитирование знакомых движений (6–8 раз):
– жевание;
– покашливание;
– рвотные движения;
– зевание с широко раскрытым ртом, с шумом втягивая воздух;
– зевание с закрытым ртом;
– изображение свиста без звука, напрягая ротовую полость;
– полоскание горла;
– храпение на вдохе и на выдохе (подражание спящему);
– прожевывание и глотание манной каши;
– глотание большого куска;
– сильно надуть щеки и удерживать их в этом состоянии 5–6 секунд;
— произношение звуков (6–8 раз):
– твердо произносить гласные звуки «а», «э», «и», «о», «у»;
– поочередно повторять звуки «и/у». Глоточные мышцы должны напрягаться;
– твердо произнести звуки «а» и «э» (как бы тужась);
– высунув язык, имитировать звук «г»;
– беззвучно произносить звук «ы», выдвигая вперед нижнюю челюсть;
– на сколько хватает выдоха тянуть звук «м», сомкнув губы;
– постукивая пальцами по гортани на одном выдохе, тянуть звук «и» то низко, то высоко;
– произносить несколько раз, удерживая кончик высунутого языка пальцами, звуки «и/а» (разделяемые между собой паузой);
– высунуть язык и, не убирая его, произносить звук «г» пять раз.
Новыми лечебными методиками являются нейромышечная электростимуляция глоточных мышц (чрескожная и внутриглоточная), транскраниальная магнитная стимуляция и метод биологической обратной связи. Использование электростимуляции глоточных мышц позволяет увеличить вероятность выраженного клинического улучшения функции глотания более чем в 5 раз (ОШ = 5,4; 95% ДИ 2,37–12,31) и вероятность восстановления функции глотания — более чем в 3 раза (ОШ = 3,2; 95% ДИ 1,29–7,95) при уменьшении проявлений аспирации на 30 % и риска развития аспирационных осложнений — в 5 раз (ОШ = 0,22; 95% ДИ 0,05–0,86). Уменьшению проявлений дисфагии статистически значимо способствуют также иглорефлексотерапия (ОШ = 0,24; 95% ДИ 0,13–0,46; p < 0,0001) и поведенческая терапия (ОШ = 0,52; 95% ДИ 0,30–0,88; p = 0,01) [4, 7, 9].
Транскраниальная магнитная стимуляция по 20 минут в день в течение 5 дней способствовала улучшению времени реакции глотания, уменьшению числа аспираций жидкости и остатков пищи, но не оказывала эффекта на время орофарингеального транзита и закрытие гортани [11]. В Японии непосредственно перед кормлением широко применяется массаж при помощи льда, что улучшает нарушенный праксис глотания, инициацию глотательных действий и сухое глотание [8].
Организация адекватного питания
Уменьшение количества принимаемой пищи и повышенный расход энергии создают угрозу истощения больного с инсультом. При недостаточном обеспечении адекватного питания посредством приема пищи через рот, а также в случае высокого риска развития аспирации необходимо рассмотреть альтернативные методы пищевой поддержки — энтеральный и парентеральный [14]. Энтеральные методы включают питание посредством назогастрального зонда или чрескожной эндоскопической гастростомии. Парентеральное питание используется в случае невозможности применения энтерального — при противопоказании или непереносимости последнего, и должно быть ограниченным во времени.
Раннее питание через назогастральный зонд улучшает выживаемость больных, поэтому рекомендуется постановка зонда в первые 48 часов после развития инсульта. Вместе с тем зондовое питание только частично уменьшает риск развития пневмоний, что связывают с богатым содержанием микроорганизмов в ротовой полости; любые нарушения нормального питания при этом способствуют развитию инфекций нижних дыхательных путей.
Назогастральный зонд легко устанавливается, но и так же легко засоряется, и легко может быть намеренно извлечен самим пациентом или непреднамеренно удален в случае плохого закрепления, при умывании, одевании пациента или при его любых других движениях, при рвоте. В целом смещение назогастрального зонда происходит у 58–100 % пациентов [6].
Удаление назогастрального зонда может быть более ранним у больных с полушарным инсультом по сравнению с пациентами с поражением ствола мозга, у более молодых, с легким началом заболевания и с лучшим восстановлением функционального состояния [5].
В случае невозможности восстановления безо–пасного глотания в краткосрочной перспективе (в течение 3–4 недель) необходимо осуществлять организацию энтерального питания посредством чрескожной эндоскопической гастростомии (предпочтительнее по сравнению с хирургической), что может быть отложено на несколько недель. Есть сведения о 5–кратном уменьшении смертности в течение 6 недель при питании с помощью чрескожной эндоскопической гастростомии по сравнению с питанием через назогастральный зонд, что связывают с использованием небольших порций пищи. При необходимости длительной нутритивной поддержки (более одного месяца) чрескожная эндоскопическая гастростомия также более предпочтительна по сравнению с назогастральным зондом, поскольку является более удобной [6, 12].
У пациентов со сниженным глоточным рефлексом возможно применение периодического ротоглоточного кормления, при котором перед каждым приемом пищи зонд вводится в глотку через рот, порции пищи и пищевые добавки вводятся со скоростью не более 50 мл/мин, после чего зонд удаляется и промывается водой.
Для энтерального питания используют специальные энтеральные гиперкалорические полисубстратные сбалансированные смеси из расчета 2200–3000 ккал/сут. Применяют смеси нутризон, нутризон энергия, нутрикомп АДН стандарт, у больных сахарным диабетом — нутрикомп АДН файбер и другие — по 500–2000 мл/сут (25–150 мл/ч).
Энтеральные смеси можно назначать в виде единственного способа питания через зонд, а также в качестве смешанного энтерально–перорального или энтерально–парентерального питания. При этом можно пить смесь через трубочку или наливая в стакан, как питьевой йогурт.
Полное парентеральное питание представляет собой внутривенное введение 500–1000 мл 10–15% раствора аминокислот (инфезол 40 и инфезол 100), 1000 мл 20% раствора глюкозы и 500 мл 20% раствора жировой эмульсии 2–3–го поколений (липофундин, Medialipid, Structolipid и LipoPlus, SMOF Lipid соответственно). При этом глюкозу и глюкозосодержащие растворы можно вводить не ранее чем через 7–10 суток после поступления пациента при условии стабильных показателей глюкозы сыворотки крови (не более 10 ммоль/л).
Более технологичными являются системы парентерального питания «все в одном» (кабивен, оликлиномель, нутрикомп липид). При этом в одном контейнере, представляющем собой трехсекционный мешок, содержатся растворы аминокислот, глюкозы и жировых эмульсий в различных комбинациях и могут включаться электролиты. Такая технология обеспечивает использование одной инфузионной системы и одного инфузионного насоса и стабильную скорость введения содержимого [1].
Рекомендуется также использование пищевых добавок, что ассоциируется с сокращением пролежней и увеличением потребления энергии и белка [7].
Антибиотикотерапия
Профилактическое назначение антибактериальных препаратов у больных с инсультами является недопустимым, поскольку обусловливает подавление роста чувствительных к ним эндогенных микроорганизмов и размножение — резистентных, что в дальнейшем потребует применения более дорогих антибиотиков.
Антибиотикотерапия рекомендуется лишь в следующих случаях:
— повышение температуры тела более 37 °С;
— ослабленное дыхание при аускультации легких и появление одышки;
— нарушение откашливания;
— катетеризация мочевого пузыря;
— образование пролежней.
С учетом наибольшей доли грамотрицательной микрофлоры, стафилококка и анаэробных бактерий в этиологии госпитальных пневмоний у больных с тяжелыми формами инсульта при первых признаках пневмонии до получения результатов определения чувствительности к антибиотикам следует назначать антибиотики широкого спектра действия — цефалоспорины I–IV поколения (в сочетании с аминогликозидами) или фторхинолоны II–IV поколения (ципрофлоксацин, левофлоксацин, гатифлоксацин, моксифлоксацин), часто в сочетании с метронидозолом или с современными макролидами (табл. 2) [3].
В зависимости от тяжести состояния назначают внутримышечно (в/м), внутривенно (в/в) струйно или капельно цефазолин (I поколение) — по 1–2 г в/в каждые 8 ч (до 6 г/сут), препараты III поколения: цефтриаксон — до 100 мг/кг/сут (до 4 г/сут) 1 раз в сутки, цефотаксим — по 1–2 г каждые 4–12 ч (до 12 г/сут), цефтазидим — по 1–2 г каждые 8 ч или по 2 г каждые 12 ч в/м, в/в (струйно медленно за 5 мин или капельно в течение 30–60 мин), цефепим (IV поколение) — по 0,5–2 г через 12 ч. Метронидазол вводят по 500–750 мг в/в каждые 8 ч.
В связи с высокой ото– и нефротоксичностью аминогликозидов I поколения применяются препараты II поколения. Гентамицин и тобрамицин назначаются по 3–5 мг/кг/сут в 1–2 введения парентерально. Препаратом резерва может быть аминогликозид III поколения амикацин, который вводят по 15–20 мг/кг/сут в 1–2 введения. При этом аминогликозиды не эффективны в отношении пневмококка и уступают другим эффективным антистафилококковым антибиотикам как более токсичные.
Эффективной является комбинация цефалоспоринов и фторхинолонов II–IV поколения, особенно респираторных. Ципрофлоксацин (II поколение) назначают по 200–400 мг 2 раза в сутки в/в (лучше — капельно в течение 30 мин). Левофлоксацин (III поколение) принимают по 500 мг 1–2 раза в сутки в/в капельно (100 мл готового раствора) или внутрь перед едой (запивая 0,5–1 стаканом воды). Препараты IV поколения назначают 1 раз в сутки в виде в/в капельной инфузии, используя готовые флаконы с 400 мг препарата (гатифлоксацин — 200 мл, моксифлоксацин — 250 мл), или внутрь — по 400 мг.
Возможна монотерапия карбапенемами: имипенем — по 0,25–1 г каждые 6 ч (до 4 г/сут), меропенем — по 0,5–2 г каждые 8–12 ч.
Возможна также комбинация цефалоспоринов с современными макролидами, которые являются одной из самых безопасных и наименее токсичных групп антибиотиков. Внутрь независимо от приема пищи назначают кларитромицин по 0,25–0,5 г каждые 12 ч, спирамицин — по 6–9 млн МЕ/сут в 2–3 приема. В/в капельно кларитромицин вводят по 0,5 г каждые 12 ч в 250 мл 0,9% раствора натрия хлорида в течение 45–60 мин, а спирамицин — по 4,5–9 млн МЕ/сут в течение 1 ч в 3 введения, растворив вначале в 4 мл воды для инъекций, а затем добавив 100 мл 5% раствора глюкозы.
Возможно сочетанное применение комбинированных защищенных антисинегнойных уреидопенициллинов (тикарциллин/клавулановая кислота, пиперациллин/тазобактам) с амикацином. Вводят эти комбинированные препараты в виде 30–минутных в/в инфузий каждые 6–8 ч: тикарциллин с клавулановой кислотой — по 3/0,1 г; пиперациллин/тазобактам — по 2/0,25–4/0,5 г.
В большинстве случаев при адекватном выборе антибиотиков длительность антибиотикотерапии составляет 7–10 дней. При атипичных пневмониях или стафилококковой этиологии длительность лечения возрастает. При пневмониях, вызванных грамотрицательными энтеробактериями или сине–гнойной палочкой, лечение должно продолжаться не менее 21–42 дней.
Заключение
Таким образом, ведение пациента с дисфагией требует постоянного контроля глотательной функции, правильной организации процесса кормления и подбора консистенции пищи. Восстановлению глотательной функции способствуют проведение реабилитационных упражнений, рефлексотерапия, электростимуляция глоточных мышц, транскраниальная магнитная стимуляция и метод биологической обратной связи. Антибиотикотерапия рекомендуется лишь при верифицированной пневмонии.
1. Зингеренко В.Б. «Все в одном» — инновационная технология полного парентерального питания / В.Б. Зингеренко, А.Е. Шестопалов // Медицина неотлож. состояний. — 2010. — № 4. — С. 21–24.
2. Мультидисциплинарный подход в ведении и ранней реабилитации неврологических больных. Методич. пособие. Часть 3. Логопедия. Глотание / О.В. Камаева, П. Монро, З.Ф. Буракова [и др.] — СПб.: Питер, 2003. — 25 с.
3. Пирадов М.А. Пневмонии у больных с тяжелым инсультом / М.А. Пирадов, Ю.В. Рябинкина, Е.В. Гнедовская // Русский медицинский журнал: Неврология. Психиатрия. — 2008. — Т. 16, № 26. — С. 1718–1721.
4. Стрельникова И.А. Опыт применения аппарата VOCASTIM у больных с дисфагией в остром периоде инсульта / И.А. Стрельникова, И.Е. Повереннова, М.А. Неклюдова // Практич. медицина. — 2013. — № 1. — С. 66–69.
5. Associating factors regarding nasogastric tube removal in patients with Dysphagia after stroke / J.H. Lee, S.B. Kim, K.W. Lee [et al.] // Ann. Rehabil. Med. — 2014. — Vol. 38(1). — Р. 6–12.
6. ESPEN guidelines on parenteral nutrition: geriatrics / L. Sobotka, S.М. Schneider, Y. Berner [et al.] // Clin. Nutr. — 2009. — Vol. 28. — Р. 461–466.
7. Geeganage C. Interventions for dysphagia and nutritional support in acute and subacute stroke [Електроннийресурс] / C. Geeganage, J. Beavan, S. Ellender, P.M. Bath // Cochrane Database Syst. Rev. — 2012. — Vol. 17. — Р. 10. — Режим доступа к журн.: http://www.ncbi.nlm.nih.gov/pubmed/23076886
8. Nakamura T. Usefulness of ice massage in triggering the swallow reflex / T. Nakamura, I. Fujishima // J. Stroke Cerebrovasc. Dis. — 2013. — Vol. 22(4). — Р. 378–382.
9. Noninvasive brain stimulation may improve stroke–related dysphagia: a pilot study / S. Kumar, C.W. Wagner, C. Frayne [et al.] // Stroke. — 2011. — Vol. 42(4). — Р. 1035–1040.
10. Reduced incidence of aspiration with spoon–thick consistency in stroke patients / P.B. Diniz, G. Vanin, R. Xavier, M.A. Parente // Nutr. Clin. Pract. — 2009. — Vol. 24(3). — Р. 414–418.
11. Shaker R. Management of Dysphagia in Stroke Patients / R. Shaker, J.E. Geenen // Gastroenterol. Hepatol. (N.Y.). — 2011. — Vol. 7(5). — Р. 308–332.
12. Singh S. Dysphagia in stroke patients / S. Singh, S. Hamdy // Postgrad. Med. J. — 2006. — Vol. 82(968). — Р. 383–391.
13. Swallowing Function Rehabilitation Training Using for Preventing of Pneumonia after Stroke [Электронный ресурс] / W. Wang, H. Yang, B. Li [et al.] // Chinese J. of Nosocomiology. — 2009. — Vol. 24. — Режим доступа к журн.: http://en.cnki.com.cn/Article_en/CJFDTOTAL–ZHYY200924018.htm
14. World Gastroenterology Organisation Practice Guidelines: Dysphagia / J.R. Malagelada, F. Bazzoli, A. Elewaut [et al.]. — World Gastroenterology Organisation, 2007. — 14 р.

/146/146.jpg)
/148/148.jpg)