Резюме
Проведены гистологические исследования у 20 детей с синдромом недифференцированной соединительнотканной дисплазии, которым выполняли оперативное вмешательство в клинике ортопедии и травматологии для детей НИИ травматологии и ортопедии ДонНМУ им. М. Горького с 2006 по 2013 год. Выполнен анализ биоптатов кости, скелетной мышцы, фасции. При выраженном экссудативно-инфильтративном компоненте воспалительной реакции в костной ткани у лиц с ДСТ преобладает остеоцитарная резорбция и компенсаторное замещение ее фиброзными элементами. Локальные проявления лимфоцитарной инфильтрации сухожилий и перимизия сопровождаются преимущественно остеокластической резорбцией с компенсаторным остеогенезом в эндосте. Установлена зависимость прочности и функции соединительной ткани от воспалительно-репаративного процесса в главных ее элементах — коллагене и эластине. Чем он выше, тем значительнее изменения сухожилий, мышц, кости и сосудов.
Проведено гістологічні дослідження у 20 дітей із синдромом недиференційованої сполучнотканинної дисплазії, яким виконували оперативне втручання в клініці ортопедії і травматології для дітей НДІ травматології та ортопедії ДонНМУ ім. М. Горького з 2006 по 2013 рік. Виконано аналіз біоптатів кістки, скелетного м’яза, фасції. При вираженому ексудативно-інфільтративному компоненті запальної реакції в кістковій тканині в осіб з ДСТ переважає остеоцитарна резорбція і компенсаторне заміщення її фіброзними елементами. Локальні прояви лімфоцитарної інфільтрації сухожиль і перимізія супроводжуються переважно остеокластичною резорбцією з компенсаторним остеогенезом в ендості. Встановлено залежність міцності й функції сполучної тканини від запально-репаративного процесу в головних її елементах — колагені й еластині. Чим він вищий, тим значніше зміни сухожиль, м’язів, кістки й судин.
Histological studies were carried out in 20 children with undifferentiated connective tissue dysplasia syndrome who underwent surgery in orthopedics and traumatology clinic for children at Research institute of traumatology and orthopedics of Donetsk national medical university named after M. Horkyi from 2006 to 2013. The analysis of bone biopsy specimens, skeletal muscle, fascia has been carried out. In significant exudative infiltrative component of the inflammatory response in the bone tissue of patients with connective tissue dysplasia, osteocyte resorption and its compensatory replacement by fibrous elements predominate. Local manifestations of lymphocytic infiltration of the tendons and perimysium are associated with predominantly osteoclastic resorption with compensatory bone formation in the endosteum. The dependence of the strength and function of the connective tissue on the inflammatory-reparative process in its main elements — collagen and elastin has been established. The higher it is, the greater the changes in the tendons, muscles, bones and blood vessels.
Статья опубликована на с. 85-89
Синдром недифференцированной дисплазии соединительной ткани (ДСТ) характеризуется широкой распространенностью, разносторонностью и склонностью к прогрессированию. Так, по данным И.А. Викторовой и Г.И. Нечаевой [4], он охватывает до 80 % популяции. В зависимости от возраста и места проживания, расовой принадлежности недифференцированная дисплазия соединительной ткани наблюдается у 26–80 % населения. Чаще она встречается у африканских детей. 74–85 % детей школьного возраста имеют НДСТ в виде разных ее проявлений [5].
Указанные выше характеристики ДСТ важны и требуют изучения, но особого внимания заслуживает склонность к прогрессированию, т.к. она ведет к непоправимым патологическим изменениям в организме детей, затем взрослых. Это непосредственно связано с влиянием негативных факторов окружающей среды, нарушением питания, снижением уровня жизни населения [6].
Высказывается мнение, что в основе патологии соединительной ткани лежат изменения наследственной информации клеток, которые передаются последующим генерациям клеток [8]. Мутации половых клеток связывают с длительным негативным экологическим воздействием токсикантов среды обитания на организм. Сторонниками энзо-, эндогенных причин механизма патологической перестройки соединительной ткани являются Л.Я. Рожинская [7], Л.П. Арабская с соавт. [1]. Ими показано, что при постоянном воздействии экострессов изменяется внутренняя среда организма, метаболические процессы в СТ, ее структура и химический состав, минеральный обмен, что способствует нарушению механизма развития (роста) и регуляции соединительной ткани.
Синдром недифференцированной дисплазии соединительной ткани представляет собой врожденный мезенхимальный дефект [3]. В организме ребенка он создает условия для развития и деформирования, дезорганизации тканевых структур, процессов метаболизма органов и систем полостей, опорно-двигательного аппарата [4]. Обширность повреждений связана с тем, что изменение одного из компонентов СТ негативно влияет на структуру и количество других компонентов, вызывая патологию структур и нарушение механических свойств.
По данным ВОЗ, ДСТ опорно-двигательной системы занимает первое место среди заболеваний детского возраста, поэтому ее признаки являются приоритетным направлением для исследований.
Цель: изучить морфологические особенности соединительной ткани у детей с синдромом недифференцированной соединительнотканной дисплазии опорно-двигательной системы.
Материалы и методы
Проведены гистологические исследования у 20 детей с синдромом недифференцированной соединительнотканной дисплазии с костно-суставной патологией, которым выполняли оперативное вмешательство в клинике ортопедии и травматологии для детей НИИ травматологии и ортопедии Донецкого национального медицинского университета им. М. Горького с 2006 по 2013 год. Выполнен анализ биоптатов кости, скелетной мышцы, фасции.
Фрагменты кости фиксировали в 10% растворе нейтрального формалина, декальцинировали 5% раствором муравьиной кислоты, обезжиривали в спиртах возрастающей крепости и заливали парафином. Остальные ткани обрабатывали обычным образом, но без декальцинации. Готовили гистологические срезы толщиной 6–8 мкм, которые окрашивали гематоксилин-эозином [9].
Результаты и их обсуждение
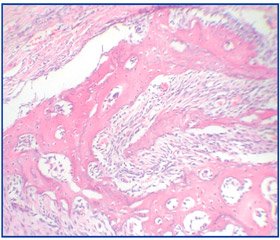
При микроскопии органов локомоторного аппарата установили выраженный полиморфизм проявлений дисплазии СТ. Наибольшую гетерогенность структурных изменений обнаружили в костной ткани, что во многом зависело от состояния связок и сухожилий мышц. Так, в участках с относительно сохраненным строением сухожилий, которые отличались истончением пучков волокон, расширением и отеком основного аморфного вещества без признаков лейкоцитарной инфильтрации (рис. 1), имели место признаки прорастания кровеносных сосудов (КС) со стороны надкостницы (рис. 2). Обращала на себя внимание гидропическая трансформация эндоста, сопровождавшая расширенные КС, стаз эритроцитов в просвете сосудов, а также широкие и многочисленные каналы остеонов.
Данные факты свидетельствуют об изменении архитектоники остеогенеза в нагруженной зоне кости: в норме сила тяги сухожилия сопровождается аппозиционным ростом кости. У наших пациентов увеличение тканевой плотности КС и диаметра каналов остеонов, происходящее на фоне отека эндоста и обеднения его камбиальными клетками типа остеогенных или фибробластоподобных при отсутствии остеокластов, могут быть подтверждением остеоцитарного остеолизиса костной ткани компактной кости. Обращала на себя внимание неравномерность концентрации периваскулярных клеточных элементов — доминирование их в участках КС, расположенных в надкостнице, и практическое их отсутствие в составе эндоста. Это может отражать формирование особых (измененных) метаболических условий в эндосте, препятствующих миграции, пролиферации и/или дифференцировке камбиальных остеогенных клеток. Тем не менее наряду с описанными каналами остеонов у таких пациентов выявлялись локальные участки фибробластического замещения широких каналов остеонов (рис. 3).
/87.jpg)
/88.jpg)
Это явилось свидетельством нарушений локального содержания остеогенных индукторов, например снижения парциального давления кислорода в условиях вазодилатации и замедления кровотока, как следствие, камбиальные стромальные клетки дифференцируются не в остеогенные, а в юные фибробласты. Гипоксические условия способствуют их активации и последующему фибриллогенезу: между клетками выявили тонкие оксифильные пучки волокон. Очевидно, повреждение пучков коллагеновых волокон сухожилий протеолитическими ферментами лейкоцитов (матричными металлопротеиназами-9) и снижение опорной функции костной ткани в данных условиях являются отражением нарушения локомоторного аппарата. При этом индукция фибриллогенеза в компактной кости может стать компенсаторным механизмом, способствующим фиксации связочного аппарата к костной ткани при нарушении кровоснабжения и препятствующим дальнейшей деградации и разломам кости.
В иных участках костной ткани, где сухожилия имели признаки выраженной лейкоцитарной инфильтрации (рис. 4), выявлялись лакуны остеокластической резорбции (рис. 5).
Вокруг резорбционных лакун с остеокластами межклеточный матрикс костной ткани отличался низкой тканевой плотностью лакун с остеоцитами, иногда выявлялись участки костного матрикса с пустыми лакунами.
Степень лейкоцитарной инфильтрации связок и сухожилий значимо варьировала у пациентов — от диффузной (рис. 4) до ограниченной перитенонием или эпитенонием (рис. 6). Обращала на себя внимание специфика клеточного состава лейкоцитов, формирующих инфильтраты. При диффузном типе инфильтрации среди лейкоцитов преобладали макрофаги, встречались единичные нейтрофилы, лимфоциты, что свидетельствовало о развитии макрофагальной фазы воспалительно-репаративного процесса. Напротив, при локальных инфильтратах в их составе преобладали лимфоциты, а макрофаги были единичными, нейтрофилы — не встречались. Последняя картина может быть отражением развития аутоиммунного процесса в связках и сухожилиях, направленного на деградацию генетически модифицированного коллагена, что имеет место при недифференцированных дисплазиях СТ. Вполне логично в данной ситуации (аутоиммунная деградация коллагеновых волокон) активизировать остео–генез с целью компенсаторного сохранения опорной функции локомоторного аппарата.
Действительно, по мере уменьшения явлений лейкоцитарной инфильтрации и остеокластической резорбции появлялись локальные участки остеогенеза (рис. 7), где располагались многочисленные функционально активные остеобласты. Как правило, активные остеобласты выявлялись в эндосте каналов остеонов, а не со стороны надкостницы. То есть прочностные свойства костной ткани в таких условиях должен был обеспечить интерстициальный рост. Данный факт можно назвать феноменом «избегания»: ввиду отсутствия условий для пери–остального остеогенеза (гипоксия, венозное полнокровие, избыток ферментов деградации коллагена) остеогенез перемещается в глубокие зоны кости, где его обеспечивают остеобласты эндоста.
Заключение
Таким образом, проявления компенсаторных реакций со стороны костной ткани у пациентов с дисплазией СТ зависят от состояния и характера воспалительно-репаративного процесса в сухожилиях и мышцах. При выраженном экссудативно-инфильтративном компоненте воспалительной реакции в костной ткани у лиц с ДСТ преобладает остеоцитарная резорбция и компенсаторное замещение ее фиброзными элементами. Локальные проявления лимфоцитарной инфильтрации сухожилий и перимизия сопровождаются преимущественно остеокластической резорбцией с компенсаторным остеогенезом в эндосте. В любом случае вторичная альтерация тканей независимо от преобладания экссудативного или инфильтративного компонента воспаления сопровождалась выраженными микроциркуляторными нарушениями в виде вазодилатации, венозного полнокровия и стаза эритроцитов, что замедляло репарацию тканей локомоторного аппарата.
Список литературы
1. Альбицкий В.Ю., Винярская В.И. Возможности использования критериев качества жизни для оценки состояния здоровья детей // Рос. педиатр. журнал. — 2007. — № 5. — С. 54-56.
2. Арабська А.П., Антіпкін О.Г., Поворознюк В.В. Особливості взаємозв’язків паратгормону, кальцитоніну та їх вплив на структурно-функціональний стан кісткової тканини за умов інкорпорації радіонуклідів у дітей, народжених після аварії на ЧАЕС // Ендокринологія. — 2000. — Т. 5, № 1. — С. 70-80.
3. Жулев Н.М., Лобзев В.С., Бадзгарадзе Ю.В. Мануальная терапия и вертебрология: Рук. для врачей. — СПб., 1992. — 588 с.
4. Калачева А.Г., Громова О.А., Керимкулова Н.В. Нарушения формирования соединительной ткани у детей как следствие дефицита магния // Лечащий врач. — 2012. — № 3. — С. 59-64.
5. Кашина В.Л., Кастюрина К.О. Особенности метаболизма СТ и иммунологической реактивности у мальчиков с системной дисплазией СТ // Актуальные проблемы профилактической медицины: тез. докл. Всеукр. научно-практ. конф. молодых ученых. — К., 2000. — С. 14-15.
6. Ключников С.О. Перспективы применения L-корнитона в педиатрии // Consilium medicоm. Педиатрия. — 2007. — № 2. — С. 116-119.
7. Рожинская Л.Я. Системный остеопороз: Практ. рук. — М.: Изд. Мокеев, 2000. — 196 с.
8. Рудковский А.И. Нарушение кровотока в позвоночных артериях при нестабильности в двигательных сегментах шейного отдела позвоночника: Автореф. дис… канд. мед. наук.: спец. 14.01.11 «Нервные болезни». — М., 2012. — 24 с.
9. Саркисов Д.С. Микроскопическая техника: Руководство для врачей и лаборантов / Д.С. Саркисов, Ю.Л. Перов. — М., 1996. — С. 628-703.

/87.jpg)
/88.jpg)