Статья опубликована на с. 51-54
Вступ
У виникненні та персистуванні бронхіальної астми (БА) у дітей значне місце посідають фактори, що справляють індукуючий вплив (екзогенні специфічні чинники — алергени), які впродовж хвороби змінюються в одного хворого, а також можуть комбінуватися. На тлі генетичної схильності до розвитку БА ці екзогенні тригерні фактори викликають запалення в бронхах та/або гострий бронхоспазм, причому у дітей раннього віку провідну роль серед цих пускових факторів відіграють харчові алергени [1]. У дітей раннього віку харчова алергія (ХА) має значний поліморфізм, що стосується не лише органів-мішеней, але й клінічної вираженості патологічного процесу: від анафілактичного шоку до замаскованих форм [5].
З кожним роком поширеність алергічних захворювань серед дитячого населення зростає, а терміни появи алергічних реакцій та захворювань неухильно наближаються до дати народження. Помолодшання алергічної патології призвело до зсуву піку захворюваності на ранній вік, у якому ХА посідає провідне місце в структурі алергічної патології. ХА є першим проявом генетичної схильності до розвитку атопії, а також тригерним фактором у розвитку респіраторних, шкірних, гастроінтестинальних проявів [6]. Клінічна картина ХА у дітей раннього та дошкільного віку характеризується варіабельністю перебігу: від виражених гострих форм до субклінічних [4] або замаскованих [8]. Окрім того, змінилися акценти в терапії алергічних захворювань, зокрема БА, вони зсунулися в бік профілактичних заходів у міжнападному періоді та полягають в оздоровленні оточення хворої дитини, вилученні причинно-значущих алергенів [9]. З огляду на це виявлення ХА у пацієнтів із БА для елімінації з їх раціону причинно-значущого алергену, імовірно, дозволяє не лише полегшити перебіг трофалергії, але й зменшити тяжкість і кількість нападів БА.
Результати досліджень та обговорення
БА належить до числа найбільш частих захворювань дитячого віку [5] та найбільш поширених алергічних захворювань органів дихання в дітей [1], якому притаманне помолодшання в останні роки [2] із формуванням і закріпленням гіперреактивності бронхів у ранньому віці, зокрема на першому році життя. Дослідження ролі атопічної конституції в розвитку БА в дітей в останні роки відзначилися відкриттям гена атопії, що локалізується на 11-й хромосомі, а також верифікацією окремих параклінічних маркерів, зокрема певних HLA-антигенів [3], що асоціюються із розвитком у майбутньому атопічної БА в дітей. Розвиток БА в дітей тісно пов’язаний з комплексом генетичних та екологічних факторів. Крім етіологічної (сенсибілізуючої) дії алергенів на організм дитини, в розвитку БА велике значення мають провокуючі фактори, що викликають загострення хвороби, причому на сучасному етапі ці фактори не обмежуються виключно аероалергенами [7]. Так, вилучення з дієти дітей першого року життя окремих облігатних харчових алергенів призводить до зниження частоти бронхіальної обструкції в пацієнтів з атопічною конституцією.
Однак високий рівень сенсибілізації до троф–алергенів, на думку інших авторів [1], лише в 7,2 % пацієнтів пубертатного віку мав значення пускового фактора в розвитку бронхіальної обструкції, а в дошкільнят причинного значення в розвитку БА набуває полівалентна алергія [2]. БА поширена серед дитячого населення, має місце ранній старт бронхообструктивного синдрому, тому важливим є удосконалення методів виявлення замаскованої ХА у пацієнтів з БА для вдосконалення лікування цих пацієнтів шляхом усунення контакту з причинно-значущими в розвитку БА харчовими алергенами.
Виходячи з цього, для розробки діагностичних критеріїв виявлення замаскованої ХА у дітей з БА нами проведено комплексне обстеження 100 дітей, які хворіли на БА. Сформовано дві клінічні групи порівняння: першу (І), основну, групу становили 50 дітей, у яких БА перебігала на тлі ХА, другу (ІІ) групу порівняння становили 50 дітей, хворих на БА без ХА. Групи формувалися за принципом випадкового відбору. При створенні клінічних груп групоформуючою ознакою була наявність у хворих комплексу діагностичних щодо ХА ознак — клінічних проявів підвищеної чутливості до харчових продуктів в анамнезі в поєднанні з різко позитивними внутрішньошкірними пробами з харчовими алергенами та наявністю в сироватці крові специфічних до троф–алергенів імуноглобулінів класу Е (IgE).
За основними клінічними характеристиками групи були порівнянними. У табл. 1 наведений розподіл пацієнтів клінічних груп порівняння за статтю, віком та місцем проживання.
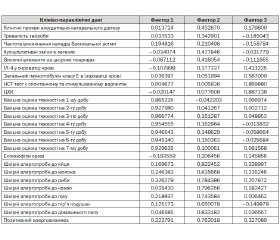
Для створення математичної моделі діагнозу ХА в дітей раннього та дошкільного віку, хворих на БА, проведений багатофакторний, дисперсійний та регресійний аналізи результатів комплексного клініко-параклінічного обстеження пацієнтів, які увійшли до клінічних груп порівняння. У табл. 2 подано результати багатофакторного аналізу головних компонентів діагнозу ХА в дітей, хворих на БА.
Дослідження головних компонентів структури діагнозу ХА за допомогою багатофакторного аналізу основних показників клінічного спостереження за дітьми, даних анамнезу та параклінічних особливостей дозволило створити факторну структуру клініко-параклінічної моделі ХА в дітей, хворих на БА. Ця структура може бути подана у вигляді математичної формули:
ХА у дітей з БА = 0,22F1 + 0,76F2 + 0,33F3,
де F1 — фактор, головними компонентами якого є особливості клінічного перебігу бронхообструктивного синдрому, вираженого за бальною системою оцінки тяжкості загального стану хворих упродовж перебування в стаціонарі. Факторне навантаження ступеня тяжкості бронхообструктивного синдрому, що відображують коефіцієнти кореляції, на 1-шу добу становило 0,87, на 2-гу добу — 0,93, на 3-тю добу — 0,97, на 4-ту добу — 0,95, на 5-ту добу — 0,95, 6-ту добу — 0,95, 7-му добу — 0,93;
F2 — фактор, головними компонентами якого виступають ознаки гіперчутливості до харчових алергенів, позитивний власний алергоанамнез та еозинофілія в периферичній крові. Факторне навантаження даних показників, що відображають коефіцієнти кореляції, знаходиться в межах 0,74–0,84;
F3 — фактор, головними компонентами якого є показники киснезалежної мікробіцидності еозинофільних гранулоцитів крові за даними НСТ-тесту, а також високий вміст загального IgE та інтерлейкіну-4 у сироватці крові. Факторне навантаження даного показника сягає 0,87.
Отже, проведений багатофакторний аналіз дозволив встановити факторну структуру діагнозу ХА в дітей, хворих на БА, за допомогою основних компонентів, що охоплювали результати клініко-параклінічного обстеження хворих та мали виражені, статистично вірогідні кореляційні зв’язки з даною нозологічною формою.
Методом дисперсійного аналізу встановлена кумулятивна значущість виділених факторів у виявленні ХА в пацієнтів раннього та дошкільного віку, хворих на БА. Так, перший фактор має показник кумулятивної цінності (дисперсії) 32,3 %, тобто включає близько 1/3 компонентів, необхідних для математичного опису ХА. Другий фактор (F2) додає до опису цього діагнозу ще 19 %, отже, два перші фактори мають кумулятивну значущість 51,3 %. Кумулятивна цінність F3 визначає даний діагноз за допомогою вже 60,0 % компонентів, які можна використовувати в діагностичному процесі. Враховуючи те, що критерії Нейзера для всіх вивчених факторів перевищували 1,0, що свідчило про їх вагомість та статистичну значущість, видається доцільним включити їх до регресійного аналізу головних компонентів ХА в обстежених пацієнтів з метою прогнозування даної нозологічної форми на підставі створеної математичної моделі в дітей, хворих на БА.
Методом множинної регресії створений клініко-параклінічний образ ХА у дітей, хворих на БА, з використанням визначених нами на попередньому етапі аналізу головних компонентів багатофакторного аналізу даної патології, що можна подати за допомогою такої математичної формули:
ХА в дітей з БА = 0,66 + 0,07Х1 + 0,001Х2 + 0,06Х3 – 0,05Х4 + 0,05Х5 + 0,03Х6 – 0,05Х7,
де Х1 — фактор, що включає клініко-анамнестичні вказівки на наявність проявів атопічного діатезу в дитини (р = 0,07);
Х2 — фактор, обумовлений високим вмістом ІЛ-4 у сироватці крові (р = 0,003);
Х3 і Х4 — фактори, обумовлені тяжкістю перебігу бронхообструктивного синдрому на 1-шу та 4-ту добу стаціонарного лікування, вираженою за бальною системою оцінки тяжкості загального стану пацієнтів (р = 0,005);
Х5 — фактор, що включає позитивні результати внутрішньошкірних алергопроб з алергенами курячого яйця (р < 0,001);
Х6 і Х7 — фактори, обумовлені позитивними результатами внутрішньошкірних алергопроб з побутовими алергенами: пір’ям (р = 0,001), домашнім пилом (р < 0,0001).
Коефіцієнт множинної кореляції розробленої математичної моделі ХА в обстежених дітей становив 0,93, що з високою точністю не лише відображає створену математичну модель, але й дозволяє прогнозувати дану патологію в пацієнтів раннього та дошкільного віку, хворих на БА. Так, за наявності в дитини даної констеляції виділених показників можна із статистичною вірогідністю й точністю (коефіцієнт детермінації 0,86) прогнозувати наявність у дитини, хворої на БА, харчової алергії, що можна подати у вигляді математичної формули:
ХА в дітей з БА = 0,14Х1 + 0,18Х2 + 0,61Х3 – 0,56Х4 + 0,45Х5 + 0,25Х6 – 0,49Х7.
Дослідження особливостей перебігу бронхообструктивного синдрому в обстежених дітей, які мали ознаки ХА, при надходженні їх до стаціонару, а також під час лікування протягом перших 4 діб не виявило вірогідних відмінностей залежно від особливостей анамнезу та клініко-параклінічних результатів обстеження. Це, на нашу думку, свідчить про те, що перебіг бронхіальної обструкції в дітей, хворих на БА, має свої закономірності розвитку, що не впливають на перебіг ХА.
Отже, на підставі проведеного багатофакторного аналізу клініко-параклінічних компонентів структури діагнозу ХА у хворих на БА дітей раннього та дошкільного віку виділені найбільш значущі з них, які можна використовувати в математичній моделі, що дозволяє не лише описати дану нозологію, але й спрогнозувати її наявність.
Висновки
1. Дослідження головних компонентів структури діагнозу харчової алергії за допомогою багатофакторного аналізу основних показників клінічного спостереження за дітьми дозволило створити факторну структуру клініко-параклінічної моделі ХА в дітей, хворих на БА.
2. Проведений багатофакторний аналіз дозволив встановити факторну структуру діагнозу харчової алергії в дітей, хворих на бронхіальну астму, за допомогою основних компонентів, що охоплювали результати клініко-параклінічного обстеження хворих та мали виражені, статистично вірогідні кореляційні зв’язки з даною нозологічною формою.
3. Методом дисперсійного аналізу встановлена кумулятивна значущість виділених факторів у виявленні харчової алергії в пацієнтів раннього та дошкільного віку, хворих на бронхіальну астму.
4. Методом множинної регресії створений клініко-параклінічний образ харчової алергії у дітей, хворих на бронхіальну астму, з використанням визначених головних компонентів багатофакторного аналізу даної патології.

/52.jpg)
/53.jpg)