Статья опубликована на с. 43-48
Діарею (гострий гастроентерит) визначають як часті (3 і більше рази на добу) рідкі випорожнення (рідкі настільки, що набувають форми посуду, в який вони потрапляють), що спостерігаються протягом 24 годин і більше (ВООЗ, 1988), супроводжуються надлишковою втратою води й електролітів. У дітей раннього віку діареєю вважають об’єм випорожнень, що перевищує 15 г/кг/добу. У віці 3 років — коли об’єм випорожнень понад 200 г/добу [1].
У 2014 році Європейське товариство дитячої гастроентерології, гепатології та нутриціології (ESPGHAN) уточнило визначення гострого гастроентериту. Гострий гастроентерит визначається як розрідження консистенції випорожнень та/або збільшення частоти випорожнень до 3 і більше разів на добу, з гарячкою або блюванням або без них. При цьому більш характерною вважається зміна консистенції випорожнень, а не їх частоти, особливо це стосується дітей перших місяців життя. Гостра діарея зазвичай триває менше ніж 7 днів і не більше ніж 14 днів [2].
Важливими факторами ризику розвитку гострих діарей вважають бідність, погане водопостачання, незадовільні санітарні умови, низьку вагу при народженні, раннє штучне вигодовування, невідповідне харчування, дефіцит мікронутрієнтів (особливо вітаміну А та цинку) [3].
Ротавірусна діарея (гастроентерит) — гостре вірусне захворювання, яке характеризується симптомами діареї, загальної інтоксикації, ураженням шлунково-кишкового тракту, розвитком симптомів токсикозу з ексикозом [4].
Джерелом ротавірусної інфекції є тільки людина (хворий або носій вірусу). Збудник виявляють у фекаліях (в 1 г міститься до 1010–1011 вірусів) із перших днів розвитку клінічних симптомів і до 7–9-го дня, рідше — упродовж 2–3 тижнів. Більш тривало виділяють ротавіруси діти з порушеннями імунітету, супутніми захворюваннями, лактазною недостатністю.
Ротавірусна інфекція є найбільш поширеною причиною гострої діареї в немовлят і маленьких дітей у всьому світі. За узагальненими даними, 95 % дітей до 5-річного віку переносять ротавірусний гастроентерит. Щороку в світі реєструється понад 125 млн випадків цього захворювання серед дитячого населення, близько 2–3 млн дітей до 5 років із ротавірусним гастроентеритом потребують госпіталізації. Близько 20 % смертей, що пов’язані з діареєю, асоційовані з ротавірусною інфекцією. Не існує істотної різниці в поширеності ротавірусної інфекції між економічно розвиненими країнами й такими, що розвиваються. Високий рівень гігієни в країні теж істотно не впливає на частоту цієї хвороби. У той же час у країнах із високим рівнем охоплення щепленнями проти ротавірусу переважна частка гострих вірусних гастроентеритів пов’язана з норовірусами — РНК-умісними вірусами родини Caliciviridae. У США частка ротавірусної інфекції становить від 5 до 10 % випадків гастроентериту в дітей перших 5 років, проте характеризується тяжким перебігом (гарячка, блювота, дегідратація) і високим ризиком різноманітних ускладнень. Порівняно з іншими причинами гастроентериту ротавірусна інфекція частіше асоціюється з тяжкими симптомами (наприклад, гарячка, блювання) [5].
Ротавірусний гастроентерит обумовлює близько 40 % всіх амбулаторних відвідувань лікаря дітьми з розладами випорожнень. А в дітей до 5-річного віку ця частка сягає 50 % усіх госпіталізацій з приводу діареї. Під час сезонних піків захворювання цей показник зростає до 70 % і більше [6]. На ротавірусну інфекцію припадає близько 25 % випадків так званої діареї мандрівників. Ротавірусна інфекція, особливо в дітей раннього віку, може перебігати безсимптомно, що створює умови для поширення захворювання. Ротавірусна інфекція має досить чітку сезонність, з підйомом в осінній період і подальшим збільшенням у зимовий, що пов’язують зі здатністю вірусу виживати при низьких температурах.
За останні роки роль ротавірусної інфекції в патології у дітей істотно збільшилась. Ймовірно, причиною цього є не тільки збільшення кількості цих захворювань, але й покращання можливостей діагностики — від визначення ротавірусу у випорожненнях методом електронної мікроскопії або ротавірусного антигену й антитіл класу IgM та IgG методом імуноферментного аналізу, визначення РНК ротавірусів методом полімеразної ланцюгової реакції [4].
В Україні ротавірусна інфекція статистично почала реєструватись тільки на початку 90-х років минулого сторіччя. Тоді показники захворюваності в окремі роки коливались від 0,94 до 3,18 % на 100 тис. населення. Упродовж останніх років реєструються сезонні спалахи ротавірусної інфекції, особливо в південних районах країни [7].
За даними проф. О.І. Сміяна зі співавторами (2012), актуальність вивчення ротавірусної інфекції полягає в тому, що поряд зі значним поширенням захворювання відсутня настороженість лікарів, які обслуговують дитяче населення, щодо даної патології, а рання клінічна діагностика є досить складною. Часто можуть розвиватися тяжкі ускладнення, які вимагають госпіталізації дитини й можуть супроводжуватися формуванням вірусоносійства [8, 9]. Інкубаційний період ротавірусного гастроентериту становить у середньому 1–2 дні. Захворювання розпочинається гостро. Розгорнута картина захворювання формується вже у перші 12–24 години й проявляється фебрильною температурою протягом 2–4 діб, інтоксикацією (слабкість, нездужання, стомлюваність, головний біль, міалгія тощо), водянистими випорожненнями без патологічних домішок, блюванням. Захворювання може супроводжуватися катаральними симптомами. При цьому в певної частини дітей катаральні явища виникають раніше диспептичного синдрому, а в більшості дітей передують гіпертермії. Хворі, як правило, скаржаться на нежить, закладеність носа, подразнення в горлі, сухий кашель, а при об’єктивному обстеженні виявляють гіперемію та зернистість м’якого піднебіння, передніх дужок, язичка, задньої стінки глотки. Катаральні ознаки нетривалі та повністю зникають через 3–4 дні. Ознаки гастроентериту з’являються у хворих майже одночасно з інтоксикаційним синдромом і характеризуються бурчанням та неприємним відчуттям, болем у животі, зниженням апетиту, нудотою, повторним блюванням і частими рідкими випорожненнями. Біль у животі частіше має дифузний характер, але може локалізуватися в епігастральній ділянці та часто супроводжується бурчанням. Нудота та блювання, за даними різних авторів, виявляються в 68–85 % дітей і залежать від тяжкості захворювання. Діарейний синдром характерний для всіх хворих із першого дня захворювання. Випорожнення відносно рясні, водянисті, жовтуватого кольору й смердючі, без патологічних домішок. Майже в половині випадків спостерігаються пінисті випорожнення. Кратність дефекації може бути різною — від 2–3 разів до 10–15 і навіть більше за добу. Позиви до дефекації мають імперативний характер. Діарейний синдром, як правило, нетривалий, і нормалізація випорожнення відбувається не пізніше 5–6-го дня хвороби, або триває 7–10 днів і, як правило, закінчується одужанням [8–10]. Крім зазначених вище симптомів, характерні екстрацеребральні, такі як анорексія та дратівливість. Ці симптоми відзначаються в 90 % хворих дітей і виникають майже одночасно, що дозволило закордонним дослідникам охарактеризувати ротавірусну інфекцію як DFV-синдром (діарея — гарячка — блювання) [8].
Сучасна лабораторна діагностика базується на використанні різноманітних діагностичних методів та тест-систем, методів експрес-діагностики і залежить від можливостей лабораторії та кваліфікації персоналу. На сьогодні все більш популярними стають експрес-методи діагностики, які дають можливість швидко поставити діагноз, забезпечити ізоляцію дитини й адекватне лікування. Серед останніх доволі популярними є методи, що ґрунтуються на реакції латекс-аглютинації. На сьогодні є доволі значний вибір тест-систем для діагностики ротавірусної інфекції на основі реакції латекс-аглютинації. У той же час актуальними залишаються імуноферментні методи діагностики, які є високочутливими та специфічними, метод електрофорезу вірусних РНК у поліакриламідному гелі або агарозі, метод виявлення вірус-специфічних РНК шляхом гібридизації (дот-гібридизація), полімеразна ланцюгова реакція, реакція непрямої гемаглютинації та реакція гальмування непрямої гемаглютинації, метод електронної мікроскопії та імунної електронної мікроскопії [12].
У своїй діяльності ми успішно використовували CITO TEST ROTA, який є швидким однокроковим імунохроматографічним методом для якісного виявлення антигенів ротавірусів у зразках фекалій. Під час тестування зразок вступає в реакцію із забарвленим кон’югатом (антиротавірусні моноклональні антитіла — червоні мікросфери), який був заздалегідь нанесений та висушений на мембрані тесту. Потім суміш мігрує вздовж мембрани під дією капілярної сили. У випадку позитивного результату специфічні антитіла, присутні на мембрані, захоплюють забарвлений кон’югат. Суміш продовжує просуватися вздовж мембрани до імобілізованих антитіл, розміщених на конт-рольній ділянці тесту, і лінія зеленого кольору завжди має з’являтися. Наявність цієї зеленої лінії служить підтвердженням достатньої кількості використаного зразка, заповнення капілярів мембрани, а також як внутрішній контроль якості для реагентів. При позитивному результаті на тестовій смужці з’являється червона лінія. Інтенсивність червоної лінії на тестовій ділянці смужки буде залежати від концентрації антигенів, присутніх у зразку. Результат тесту оцінюється через 10 хвилин від нанесення відповідного матеріалу. Згідно з інструкцією виробника, тест має чутливість > 99 % та специфічність 98 %.
Що стосується питання госпіталізації, то, згідно з останніми рекомендаціями ESPGHAN (2014), діти з гострим гастроентеритом повинні бути госпіталізовані у випадку:
— шоку;
— значного зневоднення (> 9 % від маси тіла);
— неврологічних порушень (млявість, судоми, інше);
— вираженого блювання або блювання з жовчю;
— відмови від пероральної регідратації або неможливості її проведення;
— при підозрі на хірургічний стан;
— за відсутності умов для безпечного спостереження й лікування вдома [2].
З практичної точки зору лікування ротавірусної діареї, як і гострої діареї іншої етіології, має складатися з декількох етапів. На першому етапі треба вирішити питання з харчуванням, яке має бути дещо модифіковане. Якщо дитина знаходилась на грудному вигодовуванні, доцільно його продовжити, але зменшити обсяг 1–2 годувань на 30–40 %, відповідно скорочуючи тривалість прикладання до грудей. Ураховуючи, що в більшості дітей раннього віку на тлі ротавірусної інфекції реєструються клініко-лабораторні ознаки вторинної лактазної недостатності вже від перших днів хвороби, які зберігаються в терміни понад п’ять діб, доцільним є призначення ферменту лактази на 5 днів, під час кожного годування [13]. У разі штучного годування слід продовжити годувати, зменшивши обсяг 1–2 годувань на 30–40 %, перевівши дитину на 5–7 діб на низьколактозні/безлактозні молочні суміші. Старші діти мають споживати легкі нежирні овочеві страви, 3-денний кефір, низьколактозні молочні суміші. Додатково можна призначити терті яблука, морквяний суп по 10–20 мл на прийом (100–200 мл на добу), які є природним джерелом калію та пектинів.
Наступним кроком має бути проведення регідратаційної терапії. Для цього бажано визначити ступінь зневоднення, виходячи з величини гострої втрати маси тіла (МТ). Для цього можна користуватися такими схемами. У дітей до року: 1-й ступiнь дегідратації — зменшення маси тіла до 5 % вiд початкової; 2-й ступiнь — зменшення МТ до 6–10 % від початкової; 3-й ступiнь — зменшення МТ до 11–15 % від початкової; гіповолемічний шок — зменшення МТ понад 15 %. У дітей, старших 1 року: 1-й ступінь дегідратації — зменшення МТ до 3 % вiд початкової; 2-й ступiнь — зменшення МТ до 6 % від початкової; 3-й ступiнь — зменшення МТ до 9 % від початкової. Втрата понад 12 % — гiповолемiчний шок. Найкращими клінічними ознаками зневоднення, за останніми рекомендаціями, є збільшений час наповнення капілярів, порушення тургору шкіри й патологічний тип дихання.
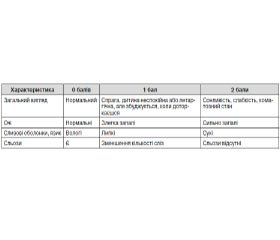
Останні рекомендації ESPGHAN (2014) пропонують наступну шкалу дегідратації (табл. 1).
Для регідратації дитини доцільно використовувати стандартизовані розчини, такі як регідрон, регідрон оптим, ораліт, цитроглюкосолан, гастроліт, біогая ОРС. Дитині треба забезпечити фізіологічні потреби в рідині в межах 800–1000 мл/добу. Додатково дитині до 2 років треба дати випити 50–100 мл рідини після кожного випорожнення. Дітям віком понад 2 роки — 100–200 мл рідини після кожного випорожнення. Якщо в дитини було блювання, треба зробити перерву на 10 хв, потім давати рідину по 1 чайній ложці кожні 2–3 хвилини, далі по 2–3 столові ложки кожні 15 хвилин. Крім того, можна давати трохи підсолені овочеві відвари чи рисовий відвар, підсолений курячий бульйон, неміцний чай без цукру (краще зелений), відвар із сухофруктів, додаючи 3 грами солі на літр рідини.
Якщо в дитини більш виражена дегідратація, вона перебуває в стаціонарі й звичайна пероральна регідратація ускладнена, доцільним є застосування ентеральної регідратації з використанням назогастрального зонду. Така ентеральна регідратація є більш фізіологічною, ніж внутрішньовенний шлях введення рідини, і має менше побічних ефектів. Рекомендований об’єм рідини 40–50 мл/кг протягом 3–6 годин (швидкий тип регідратації) або протягом 24 годин. При тяжкому зневодненні застосовують внутрішньовенний шлях уведення рідини. Показаннями до в/в введення рідини є гіповолемічний шок, порушення свідомості, тяжкий ацидоз, відсутність ефекту від ентеральної регідратації, нестримне блювання, значне здуття живота, кишкова непрохідність.
Якщо в дитини, особливо раннього віку, триває блювання, згідно з рекомендаціями ESPGHAN, доцільно призначити ондансетрон у вікових дозах. Рекомендується одноразове введення в дозі 0,1 мг/кг (максимально 4 мг) внутрішньом’язово або внутріш-ньовенно повільно. Лоперамід на сьогодні не рекомендований для використання при гострій діареї в дітей.
Наступним кроком лікування гострих діарей є застосування сорбентів. Наш власний досвід говорить про достатню клінічну ефективність використання високодисперсного діоксиду кремнію: атоксилу, полісорбу, силарду, який має виражені сорбційні властивості, виявляє дезінтоксикаційну дію. Препарат практично не всмоктується із шлунково-кишкового тракту. ESPGHAN рекомендує використовувати з цією метою діосмектит.
З метою зменшення втрат рідини комітет рекомендує використовувати антисекреторний препарат рацекадотрил. Для дітей препарат випускається в гранулах для пероральної суспензії.
Наступний крок сучасного лікування гострого гастроентериту в дітей — призначення цинку. Дітям до 6 міс. цинк призначається в дозі 10 мг/день, дітям віком понад 6 міс. — 20 мг/день упродовж 10–14 діб. Призначення препарату скорочує тривалість діареї й запобігає розвитку ускладнень.
Наступним важливим кроком лікування гострої ротавірусної діареї є призначення пробіотиків, які сприяють зменшенню тривалості діареї.
На думку проф. С.О. Крамарева (2012), основним напрямком лікування ротавірусної інфекції є регідратаційна терапія, проте використання деяких допоміжних методів лікування дозволяє полегшити прояви та зменшити тривалість симптомів хвороби [14]. Результати багатьох досліджень свідчать про позитивний вплив пробіотичних препаратів на перебіг гострих та персистуючих діарей [15–17]. Ефект застосування пробіотиків залежить від штаму, дози препарату. Кращий ефект спостерігається при лікуванні вірусних діарей і при призначенні пробіотиків з першого дня захворювання.
Більшість дослідників зазначають, що пробіотики скорочують тривалість діареї та зменшують час стаціонарного лікування.
За даними авторів, тривалість діареї зменшується, порівняно з монотерапією із застосуванням регідратації, на 0,8–79,2 години (у середньому 24 години) [14, 16].
У своїй практиці ми маємо вже значний досвід використання при ротавірусних діареях у дітей вітчизняного пробіотичного препарату Субалін, який належить до класу самоелімінуючих антагоністів. Одна доза препарату містить не менше 1 • 109 живих ліофілізованих мікробних клітин Bacillus subtilis. Бактерії роду Bacillus дуже поширені в природі, і зокрема в тих об’єктах, з якими людина контактує найбільш тісно, — харчових продуктах, воді, повітрі тощо.
Завдяки плазміді, що кодує синтез секреторного інтерферону, Bacillus subtilis здатні виробляти альфа-2-інтерферон, ідентичний лейкоцитарному людському інтерферону, завдяки чому препарат має чітку противірусну дію. Крім того, цей штам бактерій продукує понад 80 антибіотикоподібних речовин та ферменти, які руйнують патогенні мікроорганізми, закислюють середовище, створюючи несприятливі умови для життєдіяльності патогенних мікроорганізмів.
Субалін добре відомий клініцистам, у медичній науковій літературі є численні публікації щодо його ефективності при гострій діареї в дітей. Так, головний дитячий інфекціоніст проф. С.О. Крамарев зі співавторами (2014) у своїй роботі зазначає, що був проведений літературний пошук із вивчення клінічних особливостей вірусних діарей у дітей залежно від збудника. Встановлено, що серед пацієнтів із гострою кишковою інфекцією (ГКІ) ротавірусна інфекція була в 25,9 % хворих. Проведений літературний пошук показав ефективність використання пробіотиків, що містять різноманітні штами, для лікування ГКІ. Це проявилося в скороченні інтоксикаційного синдрому, діареї, гарячки на 2–3 дні. Авторами було показано, що у сучасних умовах використання як складника етіопатогенетичної терапії пробіотика Субалін, який містить культуру Bacillus subtilis, для лікування вірусних діарей у дітей є перспективним [18]. Професор О.К. Колоскова зі співавторами (2014) зазначає, що альфа-2-інтерферон, який синтезується Bacillus subtilis у процесі презентації антигену Th0-лімфоцитам, індукує експресію специфічного рецептора IL-12, що стимулює рецептор IL-18 на Т-лімфоцитах, що, у свою чергу, так само синтезується В. subtilis при ІФН-β, а це є необхідним для розвитку Тh1-імунної відповіді та активації макрофагів. Завдяки противірусній ефективності, зумовленій здатністю синтезувати інтерферон, пробіотик Субалін виявився ефективним при різноманітних вірусних захворюваннях та гострих кишкових інфекціях у дітей. Щодо лікування вірусних кишкових інфекцій у дітей, цікавим є саме здатність Субаліну до посиленого синтезу позаклітинного альфа-2-інтерферону людини при збереженні високої антагоністичної активності щодо патогенних та умовно-патогенних збудників. З огляду на патогенез захворювання, комплексну дію та практичний досвід застосування препарату при зазначеній вище патології Субалін може розглядатись як важлива частина комплексного лікування пацієнтів із діареями вірусної природи [19].
У роботі І.Б Псахіс та Т.Є. Маковської (2014) було зазначено, що Субалін демонструє високу антагоністичну активність до представників патогенної і умовно-патогенної флори, а щодо ряду збудників більш виражену дію, ніж антибактеріальні та протигрибкові препарати [20].
У публікації Н.Г. Шпікули та К.М. Легези (2013) на основі аналізу літератури зроблений висновок, що Субалін з успіхом використовується при лікуванні хворих на гострі кишкові інфекції різноманітної етіології. За даними цих авторів, противірусний та імуномодулюючий ефекти Субаліну дають змогу використовувати його як для посилення етіотропного впливу при багатьох вірусних інфекціях, так і в разі виникнення потреби доліковування таких хворих і для запобігання рецидивам вірусних інфекцій у дітей. На сьогодні жива антагоністично активна культура Bacillus subtilis, що входить до складу Субаліну, цілком задовольняє усі вимоги, що висуваються до сучасних пробіотиків, а антивірусна активність препарату, зумовлена його здатністю до синтезу альфа-2-інтерферону, дозволяє рекомендувати його для комплексного лікування не тільки кишкові інфекції, але й багатьох інших захворювань вірусної етіології [21].
У роботі проф. А.І. Бобровицької зі співавторами (2014) зроблений висновок, що питома вага ротавірусної інфекції в структурі ГКІ щороку збільшується. При лікуванні гострих кишкових інфекцій з токсикозом та ексикозом у дітей раннього віку в амбулаторних умовах можна використовувати пероральну регідратацію. Своєчасна та правильно організована пероральна регідратація при гострих кишкових інфекціях з ексикозом 1-го ступеня дозволяє попередити несприятливий перебіг хвороби. Однак поряд із регідратаційною терапією при гострих кишкових інфекціях у дітей раннього віку важливе значення має специфічна терапія. Застосування препарату Суба-лін сприяє скороченню клінічних проявів ротавірусної інфекції [22].
Наш власний досвід використання Субаліну показав його добру переносимість і відсутність побічної дії в поєднанні з високою клінічною ефективністю при гострих ротавірусних діареях, що проявлялось у більш швидкій редукції діарейного синдрому, меншій тривалості температурної реакції, більш швидкому відновленні нормального самопочуття дитини. У своїй практиці ми використовували Субалін для дітей до 12 років у дозі по 1 фл. 2 рази на добу впродовж 10 днів. Вміст флакону розчиняють кип’яченою охолодженою водою (з розрахунку 1–2 чайні ложки води на 1 дозу препарату) упродовж 1–2 хвилин до утворення гомогенної суспензії. Отриману суспензію потрібно запити невеликою кількістю води за 30–40 хвилин перед їжею. У дітей після 12 років доцільно використовувати Субалін форте по 1 капсулі 2 рази на добу впродовж 10 днів.
Висновки
1. Гострі ротавірусні діареї є актуальною проблемою сучасної педіатрії. Для своєчасної діагностики ротавірусної інфекції, її вчасного лікування й локалізації доцільно використовувати швидкі діагностичні експрес-тести для визначення антигену збудника у випорожненнях.
2. Лікування гострої ротавірусної діареї вимагає адекватної пероральної регідратації.
3. Застосування пробіотичного препарату Субалін, який має здатність до синтезу альфа-2-інтерферону та понад 80 антибіотикоподібних речовин, дозволяє полегшити перебіг хвороби та скоротити інтенсивність та тривалість гострої діареї в дітей.
Список литературы
1. World Gastroenterology Organisation practice guideline: Acute diarrhea. — 2008. — 29 р.
2. Guarino A., Ashkenazi S., Gendrel D., Vecchio A., Shamir R., Szajewska H. European Society for Pediatric Gastroenterology, Hepatology, and Nutrition/European Society for Pediatric Infectious Diseases Evidence-Based Guidelines for the Management of Acute Gastroenteritis in Children in Europe: Update 2014 // JPGN. — 2014. — Vol. 59 (1). — Р. 132-152.
3. Pediatric Nutrition in Practice / Ed. by B. Koletzko. — Basel: Karger, 2008. — 305 р.
4. Михайлова Е.В., Шульдяков А.А., Кошкин А.П., Левин Д.Ю. Ротавирусная инфекция у детей. — Саратов: ЧСМУ, 2006. — 80 с.
5. Крамарев С.А., Закордонец Л.В. Ротавирусная инфекция: эпидемиология и профилактика // Здоровье ребенка. — 2011. — № 1 (28). — С. 53-56.
6. David I. Bernstein. Rotavirus Overview // The Pediatric Infectious Disease Journal. — 2009. — Vol. 28 (3). — Р. 50-53.
7. Соловйов С.О., Трохименко О.П., Обертинська О.В., Жолнер Л.Г. Адаптація до умов культивування in vitro ротавірусів людини g1- та g2-генотипів, виділених на території України // Наукові вісті НТУУ «КПІ». — 2010. — № 3. — С. 33-37.
8. Сміян О.І., Бинда Т.П., Сміян К.О. Сучасний погляд на клінічну картину гострих кишкових інфекцій у дітей // Вісник СумДУ. Серія 142 «Медицина». — 2012. — № 2. — С. 142-152.
9. Одинец Т.Н., Каримов И.З. Современные представления о ротавирусной инфекции // Сучасні інфекції. — 2008. — № 3. — С. 77-83.
10. Малый В.П., Волобуева О.В. Вирусные диареи // Международный медицинский журнал. — 2006. — Т. 12, № 4. — С. 69-75.
11. Пипа Л.В., Леньга В.Р., Піддубна О.В. Ротавірусна інфекція у дітей: особливості клініки і діагностики // Лаб. діагностика. — 2008. — № 2. — С. 31-38.
12. Дзюблик І.В., Трохименко О.П., Ковалюк О.В. Принципи та методи лабораторної діагностики ротавірусної інфекції // Український хіміотерапевтичний журнал. — 2003. — № 1 (16). — С. 54-60.
13. Усачова О.В., Тарасенко Н.В. Місце лактазної недостатності в патогенезі ротавірусної інфекції та можливості її корекції // Запорожский медицинский журнал. — 2014. — № 4 (85). — С. 45-49.
14. Крамарев С.О., Євтушенко В.В., Мощич О.П., Євтушенко О.М., Маєвська Є.А., Бабак В.В. Ефективність різних схем терапії ротавірусного гастроентериту у дітей // Современная педиатрия. — 2012. — № 2 (42). — С. 1-5.
15. Goldin B.R., Gorbach S.L. Clinical Indications for Probiotics: An Overview // Clinical Infectious Diseases. — 2008. — Vol. 46. — P. 96-100.
16. Allen S.J., Martinez E.G., Gregorio G.V., Dans L.F. Probiotics for treating acute infectious diarrhoea // Cochrane Database of Systematic Reviews. — 2010. — Issue 11.
17. Fedorak R.N., Madsen K.L. Probiotics and Prebiotics in Gastrointestinal Disorders // Curr. Opin. Gastroenterol. — 2004. — Vol. 20 (2). — P. 146-155.
18. Крамарев С.О., Виговська О.В., Палатна Л.О., Євтушенко В.В., Марков А.І., Євтушенко О.М., Дзюба О.Л. Вірусні діареї у дітей: клінічні прояви, інновації в лікуванні // Здоровье ребенка. — 2014. — № 7 (58). — С. 21-29.
19. Колоскова О.К., Білоус Т.М., Гарас М.Н. Патогенетичне обґрунтування оптимізації лікування вірусних діарей у дітей за допомогою спороутворювальних бацил, здатних до самоелімінації // Актуальна інфектологія. — 2014. — № 3 (4). — С. 185-188.
20. Псахис И.Б., Маковская Т.Е. Современные возможности и перспективы использования пробиотиков группы самоэлиминирующихся антагонистов в терапии инфекционных заболеваний // Здоровье ребенка. — 2014. — № 4 (55). — С. 91-95.
21. Шпікула Н.Г., Легеза К.М. Корекція дисбіозу у минулому і сьогодні. Терапевтичні можливості сучасних бацилярних препаратів // Інфекційні хвороби. — 2013. — № 3. — С. 93-99.
22. Бобровицкая А.И., Беломеря Т.А., Данилюк А.Н., Думчева Т.Ю., Ткаченко И.М., Захарова Л.А., Заяц В.Ю. Актуальные вопросы острых кишечных инфекций в последние годы // Актуальна інфектологія. — 2014. — № 1 (2). — С. 21-27.

/45.jpg)