Статтю опубліковано на с. 19-22
У структурі захворюваності періоду новонародженості кон’югаційна жовтяниця є одним із найбільш поширених станів і зустрічається приблизно в 60 % доношених і 80 % недоношених новонароджених [1, 5]. У сучасних умовах транзиторні жовтяниці новонароджених супроводжуються високим рівнем білірубіну в сироватці крові й часто набувають затяжного перебігу [6].
Активне вивчення останніми десятиріччями причин зростання частоти пролонгованого перебігу некон’югованої гіпербілірубінемії засвідчило міцний зв’язок із такими пре- та перинатальними факторами, як інфікування матері, захворювання під час вагітності, різноманітна хронічна екстрагенітальна патологія (цукровий діабет, захворювання серцево-судинної системи, органів травлення, нирок, анемія), стимуляція та індукція пологової діяльності, гестаційний вік дитини, вага при народженні та інші [3]. Недостатнє споживання рідини й калорій, значна втрата маси тіла, затримка дефекацій також розглядаються як фактори ризику виникнення жовтяниці новонароджених. Серед причин, що впливають на пролонгований перебіг неонатальної жовтяниці, приділяється увага гіпоксичному впливу, коли затримується дозрівання глюкуронілтрансферазної системи і виникає ди-соціація білірубін-альбумінового комплексу [2]. Порушення обміну білірубіну, відповідно до новітніх досліджень, визначаються взаємозв’язком генетичних особливостей з активністю ферментних систем, які відповідають за транспортування, кон’югацію та екскрецію білірубіну [4].
Широкий етіологічний спектр неонатальних жовтяниць обумовлює складність патогенетичних механізмів захворювання. Ранні неонатальні жовтяниці, як правило, спричинені підвищеним фізіологічним руйнуванням еритроцитів у немовлят, що обумовлює зростання некон’югованого білірубіну, рівень якого визначає нейротоксичність. Пролонгований перебіг неонатальних жовтяниць (після -14-го дня життя в доношеної дитини й 21-го дня в недоношеної) [5] може свідчити про ознаки, які лежать в основі порушень гепатобіліарної системи, а саме механічні й паренхіматозні ураження. Найбільш частим варіантом жовтяниці, з яким зустрічається педіатр при амбулаторному спостереженні, є пролонгований перебіг неонатальної жовтяниці, етіологія якої залишається невизначеною [7].
Питання терапії пролонгованої кон’югаційної жовтяниці (ПКЖ) в практичній педіатрії досі залишається дискутабельним. Як показує клінічний досвід, застосування фототерапії, яка є методом лікування ранньої неонатальної жовтяниці, у більш пізні терміни (пізніше першого місяця життя) визначається низькою ефективністю. Суперечливим питанням є доцільність призначення інфузійної терапії при затяжній кон’югаційній гіпербілірубінемії, яка не тільки потребує стаціонарного лікування, але і є інвазивним методом утручання. За твердженнями деяких учених, рівень непрямого жиророзчинного білірубіну не може бути знижений шляхом парентерального введення розчинів (глюкози та ін.) [10]. Згідно з рекомендаціями Американської академії педіатрії, внутрішньовенне введення рідини та випоювання дитини не є необхідними для лікування жовтяниці в немовлят, у яких відсутні прояви зневоднення [10]. Застосування фенобарбіталу, який належить до облікових препаратів і є індуктором мікросомальних ферментів печінки, у деяких батьків викликає негативне сприйняття, тому його призначення не завжди є можливим та виправданим, особливо при амбулаторному лікуванні даної патології. Синтетичні металопорфірини, що раніше широко використовувались при лікуванні непрямих гіпербілірубінемій, на сучасному етапі не застосовуються через їх фототоксичний ефект [8].
У низці протоколів при лікуванні холестазу рекомендоване використання препаратів урсодезоксихолевої кислоти (УДХК) [8, 9]. УДХК, гідрофільна жовчна кислота, є природним компонентом жовчі й має широкий спектр дії, у тому числі холеретичний, антихолестатичний, літолітичний, гепатопротекторний, імуномодулюючий, гіпохолестеринемічний ефекти. У даний час УДКХ широко застосовується в дитячій гепатології, у тому числі в лікуванні дітей з хронічними гепатитами, холестатичними ураженнями печінки — первинним та вторинним біліарним цирозом печінки, первинним склерозуючим холангітом, біліарним рефлюкс-гастритом та рефлюкс-езофагітом, для профілактики холестазу, асоційованого з тривалим парентеральним годуванням та патологією кишечника. Низька токсичність, гепатопротективні, антихолестатичні та літолітичні властивості УДХК є підставою для її застосування при лікуванні жовтяниць різної етіології в новонароджених. Слід відмітити, що відомостей про застосування УДХК у дітей перших місяців життя на сьогодні недостатньо, у літературі зустрічаються суперечливі дані про ефективність використання УДХК в неонатології.
Отже, лікування дітей із ПКЖ на сьогодні залишається дискутабельним питанням. Немає чітко розроблених рекомендацій щодо ведення дітей з затяжною непрямою гіпербілірубінемією, а ефективність існуючих методів лікування не завжди є достатньою, що обґрунтовує необхідність вивчення ефективності патогенетично обґрунтованих неінвазивних методів лікування ПКЖ.
Метою роботи стало вивчення ефективності застосування УДХК у лікуванні ПКЖ.
Матеріал і методи дослідження
До клінічного спостереження залучено 35 дітей віком від 15 днів до 3 місяців із ПКЖ: 15 дітей, яким у комплекс базисної терапії було включено препарат урсодезоксихолевої кислоти (Урсофальк) у дозі 15–20 мг/добу на 1 кг маси тіла, увійшли до 1-ї групи; 20 дітей, які отримували традиційне (базисне) лікування (сорбенти, інфузії 5% розчину глюкози, пробіотики), становили 2-гу групу. Пролонгованою (затяжною) вважали жовтяницю з тривалістю понад 14 днів у доношеної та понад 21 день у недоношеної дитини [5]. Обидві групи були ідентичними за гендерними ознаками. Усі пацієнти були включені в аналіз ефективності та переносимості.
Ефективність УДХК у лікуванні дітей із ПКЖ оцінювалась на підставі даних динаміки клінічних проявів захворювання й показників біохімічного аналізу сироватки крові. Комплекс досліджень включав аналіз анамнестичних даних, клінічний огляд, загальний аналіз крові, дані біохімічного дослідження крові — рівень некон’югованої та кон’югованої фракції білірубіну, трансаміназ, лужної фосфатази, ультразвукове дослідження немовлят.
Дані досліджень оброблені методами математичної статистики, використовувалися параметричні методи (критерій Стьюдента). Критичним вважали рівень значимості 5 %. Аналіз даних проводився за допомогою програми Excel XP.
Результати дослідження і їх обговорення
Загальний стан дітей обох груп із ПКЖ розцінювався як задовільний у 15 (42,8 %) дітей та середнього ступеня тяжкості у 20 (57,1 %) немовлят. Тяжкого стану серед дітей обох груп у жодному випадку не виявлено.
При об’єктивному обстеженні дітей із затяжним перебігом кон’югаційної жовтяниці в переважної більшості немовлят (74,3 %) спостерігався фізіологічний гіпертонус, майже в половини дітей (45,7 %) — періоральний ціаноз; мармуровість шкірних покривів було виявлено у 12 (34,3 %) випадках, тремор підборіддя — в 11 (31,4 %) немовлят, тремор верхніх та нижніх кінцівок — у 3 (8,6 %) дітей, акроціаноз — у 2 (5,7 %) немовлят, м’язову дистонію — у 20 % випадків. Рефлекси новонароджених у всіх дітей визначались згідно з віком. У структурі супутньої патології статистично значимими були гіпоксичні ураження ЦНС та функціональні порушення шлунково-кишкового тракту (ШКТ). Гіпоксичне ураження ЦНС діагностовано в переважної більшості немовлят із ПКЖ (48,5 %). Кількість дітей з гіпоксичним ураженням ЦНС у першій і другій групах істотно не різнилась (40,0 % дітей 1-ї групи і 55,0 % у 2-й групі). Зв’язку між гіпоксичним ураженням ЦНС та рівнем сироваткового білірубіну й тривалістю гіпербілірубінемії в обстежених групах виявлено не було (р > 0,05). У дітей із ПКЖ зустрічались клінічні ознаки функціональних порушень ШКТ (зригування, метеоризм, розріджені випорожнення, запори чи збільшення частоти дефекацій) — у 7 (46,6 %) немовлят 1-ї групи та в 56 (30,0 %) дітей 2-ї групи. У 5 (14,3 %) немовлят обох груп із ПКЖ тургор та еластичність м’яких тканин були знижені.
У переважної більшості немовлят жовтяниця з’явилась на 2-гу — 3-тю добу життя, а сформовані групи не відрізнялись за часом появи жовтяниці. В обох групах жовтяниця визначалась відповідно до модифікованої шкали Крамера переважно в зонах 1–2 та 1–3: у дітей 1-ї групи зона 1–2 — у 4 (26,6 %) дітей, зона 1–3 — у 5 (33,3 %), у 2-й групі — у 6 (30,0 %) та 5 (25,0 %) дітей відповідно. Інша частка дітей мала жовтушне забарвлення в зонах 1–4: у 1-й групі — 2 (13,3 %) дитини, 1–5 — 4 (26,6 %) немовлят, у 2-й групі — 3 (15,0 %) та 6 (30,0 %) дітей відповідно. Таке розподілення жовтяниці вказувало на орієнтовний рівень загального білірубіну сироватки (ЗБС) в межах 150–200 мкмоль/л, що в подальшому було підтверджено лабораторно. Середній показник ЗБС крові в дітей 1-ї групи становив 208,9 ± 20,5 мкмоль/л, у дітей 2-ї групи — 198,19 ± 8,3 мкмоль/л (р > 0,05).
Клінічне спостереження показало, що в переважної більшості (73,3 %) немовлят 1-ї групи, які отримували в комплексному лікуванні препарат УДХК, відмічалось швидке зменшення інтенсивності жовтяниці (помітне зниження іктеричного забарвлення шкіри та склер) уже на 3–4-й день прийому препарату. Жовтушність шкірних покривів у них визначалась у зонах 1–3 за модифікованою шкалою Крамера, що відповідає орієнтовному значенню ЗБС 200 мкмоль/л (при надходженні — зона 1–5), а на 7-й день — у зонах 1–2 (орієнтовний рівень ЗБС 150 мкмоль/л), і вже через 10–14 днів візуальні прояви жовтяниці не визначались у 13 (86,6 %) дітей основної групи. У 2-й групі зменшення інтенсивності жовтяниці було менш виражене. Так, після 7-ї доби традиційного лікування візуальні прояви жовтяниці в більшості немовлят (60,0 %) зберігалися в зонах 1–4 за шкалою Крамера (орієнтовний рівень ЗБС у межах 250 мкмоль/л). Через 2 тижні лікування лише в 7 (35,0 %) немовлят із групи порівняння не було візуальних проявів жовтяниці; іктеричність шкіри зберігалась у переважної більшості дітей (65,0 %) і визначалась у зонах 1–2 (орієнтовний рівень ЗБС 150 мкмоль/л). Отже, порівняльний аналіз свідчить, що кількість дітей без візуальних проявів жовтяниці на 10–14-ту добу лікування була істотно більшою в групі немовлят, які отримували препарат УДХК, порівняно з дітьми, яким було проведене традиційне лікування (р < 0,05).
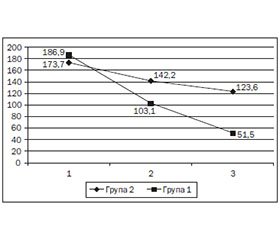
Лабораторне обстеження дітей в динаміці виявило певні відмінності залежно від лікування. Так, рівень непрямого білірубіну на початку лікування в 1-й групі становив 186,9 ± 5,2 мкмоль/л, у 2-й групі — 173,7±7,2 мкмоль/л; р > 0,05 (рис. 1).
Через тиждень проведеного лікування зниження рівня непрямого білірубіну спостерігалось в обох групах. Однак у групі, що отримувала в комплексній терапії препарат УДХК, значення непрямого білірубіну зменшилось на 83,8 ± 6,1 мкмоль/л і становило 103,1 ± 4,3 мкмоль/л, а у групі порівняння — на 31,5 ± 4,2 мкмоль/л і рівень непрямого білірубіну становив 142,2 ± 5,8 мкмоль/л; р < 0,05. Проведене лабораторне дослідження через 2 тижні засвідчило подальше зниження рівня білірубіну в обстежених групах — до 51,5 ± 3,9 мкмоль/л у 1-й групі й до 123,6 ± 4,7 мкмоль/л у групі порівняння; р < 0,05 (рис. 1).
Разом із нормалізацією рівня непрямої фракції білірубіну в дітей 1-ї групи, які отримували препарат УДХК, відмічалась позитивна динаміка активності сироваткових трансаміназ. Показник ферменту АлАТ зменшився в 7 (46,5 %) немовлят; активність його до лікування становила 45,3 ± 9,5 МО/л, після проведеної терапії — 35,30 ± 6,54 МО/л (р > 0,05). Зниження активності АсАТ з 57,0 ± 7,1 МО/л на початку лікування до 49,3 ± 4,2 МО/л після лікування (р > 0,05) спостерігалось у 9 (60,0 %) дітей 1-ї групи.
Результати проведеного через 2 тижні ультразвукового дослідження в 5 (33,3 %) немовлят, які отримували препарат УДХК, засвідчили зменшення розмірів печінки та покращання структури її паренхіми (до лікування ознаки підвищеного навантаження на гепатобіліарну систему при УЗД діагностувались у 9 (60,0 %) немовлят 1-ї групи). Позитивна динаміка клініко-параклінічних ознак жовтяниці в дітей 1-ї групи супроводжувалась швидким покращанням загального стану, апетиту, середньодобової прибавки маси тіла. Це сприяло прискоренню темпів одужання та зменшенню тривалості перебування дітей в стаціонарі.
Отже, результати проведених досліджень довели, що в більшості дітей, які отримували УДХК (Урсофальк), відзначалося більш швидке зменшення інтенсивності жовтяниці на відміну від дітей групи порівняння. Уключення препарату УДХК в комплексну терапію дітей з ПКЖ позитивно впливає на клінічний перебіг жовтяниці, сприяє швидшій регресії клініко-параклінічних ознак цього захворювання та прискорює темпи одужання. Призначення Урсофальку не супроводжується появою дисфункцій шлунково-кишкового тракту (кишкові кольки, запори, діарея та інше), не зареєстровано випадків алергічної реакції на прийом препарату. Під час проведеного дослідження випадків відміни препарату у зв’язку з появою побічних ефектів не було.
Список литературы
1. Seyyedrasooli A., Valizadeh L., Hosseini M.B., Asgari Jafarabadi M., Mohammadzad M. Effect of Vimala Massage on Physiolo-gical Jaundice in Infants: A Randomized Controlled Trial // J. Caring Sci. — 2014 Sep. — 3 (3). — Р. 165-173. Published online 2014 Sep 1. doi: 10.5681/jcs.2014.018.
2. Глуховська О.О. Чинники пролонгованого перебігу неонатальних жовтяниць // Педіатрія, акушерство та гінекологія. — 2009. — № 6. — С. 9-11.
3. Mesić I., Milas V., Medimurec M., Rimar Z. Unconjugated pathological jaundice in newborns // Coll. Antropol. — 2014 Mar. — 38 (1). — Р. 173-8.
4. Zhou Y., Wang S.N., Li H., Zha W., Peng Q., Li S., Chen Y., Jin L. Quantitative trait analysis of polymorphisms in two bilirubin metabolism enzymes to physiologic bilirubin levels in Chinese newborns // J. Pediatr. — 2014 Dec. —165 (6). — Р. 1154-1160.e1. doi: 10.1016/j.jpeds.2014.08.041. Epub 2014 Sep 26.
5. Наказ № 255 від 27.04.2006. Про затвердження клінічного протоколу надання неонатальної допомоги дітям «Жовтяниці новонароджених». — К., 2006. — 38 с.
6. Неонатология: Практическое руководство / Под ред. Н.Н. Володина. — М.: ГЭОТАР-Медиа, 2007. — 848 с.
7. Логинова А.А. Билирубинсвязывающая функция альбумина при пролонгированной неонатальной желтухе // Педиатрия. — 2011. — Т. 90, № 1. — С. 13-19.
8. Queensland Maternity and Neonatal Clinical Guideline: Neonatal jaundice: prevention, assessment and management [електронний ресурс]. — 2009. Режим доступу: http://www.health.qld.gov.au/cpic/resources/mat_guidelines.asp
9. Шадрін О.Г., Марушко Т.Л., Басараба Н.М., Шадрін В.О. Питання оптимізації терапії кон’югаційної жовтяниці новонароджених // Перинатологія і педіатрія. — 2009. — № 4 (40). — С. 51-53.
10. Management of hyperbilirubinemia in the newborn infant 35 or more weeks of gestation. American Academy of Pediatrics. Clinical practice quideline. Subcommitee on hyperbilirubinemia // Pediatric. — 2004 . — Vol. 114, № 1. — Р. 297-316.
/21.jpg)