Статья опубликована на с. 77-85
Можно не придавать очень большого значения
головным болям после спинномозговой анестезии,
но нельзя же отрицать факта, что изредка
эти головные боли, развившись поздно, достигают
таких невыносимых степеней, что и больной,
и врач положительно не знают, что предпринять
для их успокоения.
С.С. Юдин, 1925 [8]
Определение
Согласно определению Международного общества головной боли (International Headache Society), постпункционная головная боль — это головная боль, которая развивается не более чем за 5 дней после дуральной пункции, появляется или усиливается не более чем за 15 минут после перехода в вертикальное положение, облегчается не более чем за 15 минут после перехода в горизонтальное положение и сопровождается хотя бы одним из следующих симптомов: ригидность шеи, звон в ушах, снижение слуха, фотофобия, тошнота. Эта головная боль должна исчезнуть за 7–14 дней после спинальной пункции; если она продолжается, ее называют головной болью ликворного свища [2].
Причина
Не вполне ясна. Наилучшее объяснение — ликворная гипотензия вследствие утечки ликвора сквозь отверстие в твердой и паутинной оболочках, превышающей темп продукции ликвора. Потеря лишь 10 % объема ликвора может вызвать ортостатическую головную боль [2].
Боль объясняют двумя механизмами. Первый — рефлекторное расширение сосудов, церебральных и менингеальных, вследствие ликворной гипотензии. Второй — проседание головного мозга с натяжением чувствительных к боли внутричерепных структур в вертикальном положении. Натяжение верхних шейных спинальных нервов (С1–С3) вызывает боль в шее и надплечьях. Натяжение V черепных нервов (nervi trigemini) вызывает лобную головную боль. Натяжение IX (nervi glossopharyngei) и X (nervi vagi) черепных нервов вызывает боль в затылке (рис. 1).
Факторы риска, зависящие от пациента
Возраст: чаще у молодых лиц — от 31 до 50 лет [1–10, 12]. Это объясняют либо большей эластичностью оболочки и растяжением отверстия в ней, большей податливостью эпидурального пространства и большей чувствительностью рецепторов сосудов головного мозга [3, 4], либо большей подвижностью головного мозга, либо меньшим отклонением иглы Квинке от строго перпендикулярного направления [10]. Давно известно, что после 60 лет постпункционная головная боль наблюдается очень редко, а после 70 лет — практически не бывает.
Что касается детей, то раньше считали, что у них головные боли бывают редко, но, по-видимому, о них просто меньше сообщали. В последние годы о них пишут все чаще [2].
Индекс массы тела: головная боль бывает чаще у худых, так как у полных выше внутрибрюшное и зависящее от него эпидуральное давление — ликвор у полных вытекает меньше [3, 4].
Головные боли в анамнезе — риск постпункционной цефалгии вчетверо выше [2].
Пол: вдвое чаще у женщин, что объясняют большей эластичностью твердой оболочки и зиянием отверстия в ней и тем, что эстрогены повышают чувствительность рецепторов к субстанции Р [1–7].
Беременность: у родильниц как после кесарева сечения, так и после спинального обезболивания вагинальных родов (еще чаще, так как схватки и потуги увеличивают потерю ликвора через дефект оболочки). Это объясняется быстрым снижением внутрибрюшного давления, уменьшением кавальной компрессии, сужением эпидуральных вен и падением эпидурального давления — ликвор вытекает с большей силой [1–7].
Факторы риска, зависящие от иглы
Качество иглы зависит от производителя: лучше отшлифованные иглы безопаснее.
Калибр: чем толще игла, тем выше вероятность головной боли (табл. 1).
Кончик иглы: большинcтво авторов подтверждают меньший риск головной боли после пункции иглой с карандашевидным кончиком (pencil-point) по сравнению с обычным (Quincke-point). Хотя раньше считали, что это объясняется расслоением, а не разрезанием волокон твердой оболочки (поэтому эти иглы называли атравматичными), современные данные сканирующей электронной микроскопии показывают, что эти иглы довольно грубо разрывают твердую и паутинную оболочки, образуя лоскуты по краям отверстия и «зыбь» паутинной оболочки; воспалительная реакция после такого разрыва может вызывать воспалительный отек, ограничивающий утечку ликвора. В отношении влияния на риск цефалгии других моделей игл (ball-pen, Atraucan) данные противоречивы.
Факторы риска, зависящие от врача
Поза пациента во время пункции и сразу после нее, по-видимому, не влияет на риск головной боли.
Доступ: парамедианный (околосрединный) сложнее в исполнении, но реже приводит к головной боли.
Ориентация среза иглы Quincke: лучше латерально, при парамедианном доступе — и вентрально. Хотя современные данные сканирующей электронной микроскопии показывают, что эта игла при любой ориентации среза образует одинаковые U-образные лоскуты, напоминающие вскрытую жестяную консервную банку, клинические данные говорят о меньшем риске постпункционной головной боли [1–7].
Мандрен в игле перед попаданием в подпаутинное пространство позволяет, во-первых, избежать заноса в него тканевой «пробки», во-вторых, получить ликвор сразу после извлечения мандрена (а если в игле была эта «пробка», потребуется напрасная повторная пункция), в-третьих, использовать «эффект ступеньки» иглы Quincke-point фирмы Becton-Dickinson. Введение мандрена в иглу перед ее извлечением после инъекции может снизить риск головной боли [2].
Количество пункций: головная боль наблюдается значительно чаще после повторных пункций, чем после однократных [2]. К тому же при повторных попытках возможен крючок на кончике иглы, рвущий оболочки.
Проявления
Эта боль, как правило, уменьшается при надавливании на область эпигастрия, так как при этом сдавливается нижняя полая вена. При этом врач надавливает правой рукой ниже правого края реберной дуги, подложив левую руку под спину больного, сохраняя такое давление около одной минуты (Шифман Е.М., 2004 [4]).
Начало боли: как правило, не сразу, а через сутки-двое, в 66 % случаев — в течение первых двух суток, в 90 % случаев — в течение первых трех суток, обычно — от 6 часов до 3 суток. Описаны казуистические случаи возникновения боли сразу после пункции, но это должно нацелить врача на поиски другой, более опасной причины [12].
Продолжительность: от 2–3 дней до 1–2 недель, если дольше — называют головной болью ликворного свища. Однако для нашей диагностики это не имеет значения, так как при осмотре мы не знаем, как долго будет длиться головная боль.
Локализация: двусторонняя, симметричная, как правило, лобно-затылочная, иногда с иррадиацией в оба надплечья. Если же боль стала асимметричной или появились любые признаки неврологической очаговости — следует тут же подумать о таком редком и опасном осложнении ликворной гипотензии, как внутричерепная субдуральная гематома (см. далее).
Характер боли: давящий или пульсирующий.
Позиционные изменения: минимум в горизонтальном положении (лежа), максимум — в вертикальном (сидя или стоя) — главный патогномоничный признак.
Усиливается эта боль также при любом натуживании и движениях головы.
Как правило, отмечается положительный признак Гютше (англ. Gutsche sign): в позе стоя при нажатии на живот (лучше в эпигастрии и правом подреберьи — прижимаются ворота печени и нижняя полая вена, набухают эпидуральные вены, повышается эпидуральное и ликворное давление вокруг спинного мозга) в течение примерно минуты боль заметно уменьшается (см. эпиграф), но не всегда.
Возможны сопутствующие явления: ригидность шеи, звон в ушах, снижение слуха, фотофобия, тошнота, рвота, нарушения зрения. Но они вовсе не обязательны.
Дифференциальная диагностика
Эти боли могут также сопровождаться шумом в ушах, нарушением зрения и даже судорогами, что может приводить к гипердиагностике эклампсии (Шифман Е.М., 2004 [4]).
Цефалгия после спинальной пункции может иметь разные причины (см. ниже). Даже без операции и спинальной анестезии головная боль наблюдается у 39 % родильниц [2].
Дифференциальная диагностика постпункционной головной боли [12]
— Вирусный, химический или бактериальный менингит.
— Внутричерепное кровотечение.
— Тромбоз церебральных вен.
— Внутричерепная опухоль.
— Неспецифическая головная боль.
— Апоплексия гипофиза.
— Церебральный инфаркт.
— Вклинение ствола головного мозга.
— Синусная головная боль.
— Мигрень.
— Действие медикаментов (например, кофеина, амфетаминов).
— Преэклампсия.
Но она может быть признаком значительно более грозных проблем (табл. 2).
Акушерским анестезиологам, обычно встречающим сразу три фактора риска: женский пол, молодость и беременность — и поэтому особо настороженным в отношении головной боли, не надо забывать, что она не всегда вызвана спинальной анестезией. Прежде всего полезно измерить АД — не гестоз ли это?
Синдром Вольфа — Шальтенбранда [англ. Wolff — Schaltenbrand syndrome] — ликворная гипотензия, вызванная другими причинами, обычно спонтанным разрывом оболочек спинного мозга, и также проявляется позиционной (исчезающей в лежачей позе) головной болью.
Поскольку головная боль после спинальной анестезии у молодых людей, особенно у родильниц, не редкость, и анестезиологи, и акушеры прежде всего думают о ликворной гипотензии. Но если наряду с головной болью появляются менингизм, фотофобия, гипертермия, не следует забывать о таком редком, но опасном осложнении, как менингит.
Прогноз
В большинстве случаев постпункционная головная боль проходит без последствий, как с лечением, так и без него, но иногда может стать хронической, затянувшись на месяцы и даже годы [2]. Уже поэтому ее надо лечить сразу и следить за ее характером, особенно нетипичным, асимметричным, так как ее последствия могут быть катастрофическими.
Внутричерепная субдуральная гематома
Если постпункционная головная боль не уменьшается, а приобретает новый характер (не зависит от положения тела и сопровождается очаговыми проявлениями), следует прежде всего подумать о возможности внутричерепной субдуральной гематомы. В литературе описано более полусотни таких случаев [2].
Причина. Под твердой мозговой оболочкой находятся так называемые «мостовые вены» (англ. bridging veins), по которым верхние вены большого мозга (лат. venae superiores cerebri) сообщаются с верхним сагиттальным синусом (лат. sinus sagittalis superior). Эти «мостовые вены» — короткие, тонкостенные и прямые (не извитые) — являются «слабым звеном» при проседании головного мозга вследствие ликворной гипотензии (рис. 2).
При сильном натяжении эти вены могут разорваться, что приводит к образованию субдуральной гематомы, часто — со смещением головного мозга вбок (рис. 3).
Факторы риска: беременность, дегидратация, аномалии церебральных сосудов, сахарный диабет, хронический алкоголизм, коагулопатия или прием антикоагулянтов, повторные пункции, большое постпункционное отверстие.
Частота — примерно 1 : 500 000, чаще слева, почему чаще слева — не ясно. Возможны двусторонние гематомы. Обычно гематома возникает в теменно-затылочной или лобно-теменной области, но изредка — между полушариями [2].
Проявления: постпункционная головная боль, не облегчаемая консервативными мерами, меняющая характер с постурального на непостуральный (то есть уже не зависящий от положения тела) и сопровождаемая снижением уровня сознания, рвотой, очаговыми проявлениями: птозом, парезами, плегиями [2].
Диагностика требует тщательного неврологического обследования и срочной компьютерной или ЯМР-томографии. Внутричерепная субдуральная гематома может развиться не только после дуральной пункции, но и при спонтанной интракраниальной гипотензии — болезни Шальтенбранда.
Лечение. На доброкачественное течение лучше не рассчитывать, поскольку внутричерепная субдуральная гематома угрожает жизни. Если сохраняется сознание и симптоматика не нарастает, толщина гематомы не более 1 см, нет смещения головного мозга, возможно лечение эпидуральной пломбировкой [2] на фоне консервативных мер с повторными неврологическими и томографическими исследованиями. Но при обширных гематомах или нарастании симптоматики (появление судорог, снижение уровня сознания) требуется неотложное хирургическое вмешательство для удаления гематомы.
Прогноз зависит от объема и расположения гематомы (при межполушарном расположении около четверти больных не выживает), а также своевременности диагноза и лечения.
Внутричерепное субарахноидальное кровоизлияние
Частота. Значительно реже, чем субдуральное, возможно и субарахноидальное внутричерепное кровотечение, если у пациента наблюдалась недиагностированная аневризма внутричерепной артерии, обычно у основания мозга. До 2009 года опубликовано лишь 11 таких случаев после спинальной анестезии [2].
Причины. Такие аневризмы бывают нередко (1,8 % случайных находок при ЯМР-обследованиях) и могут быть причиной спонтанного субарахноидального кровотечения при повышении АД. Но спинальные пункции, особенно повторные, снижая ликворное давление, повышают трансмуральную разницу давления в аневризме; тогда она может разорваться даже при незначительной артериальной гипертензии.
Фактор риска — перепады АД во время анестезии.
Проявления — характерное для субарахноидального кровоизлияния внезапное, «как выстрел», начало головной боли.
Лечение — с участием нейрохирурга.
Профилактика. При наличии выявленной внутричерепной аневризмы лучше избегать спинальной анестезии. Альтернативы: либо наркоз с предупреждением «всплесков» артериальной гипертензии, либо эпидуральная анестезия в опытных руках без нечаянного дурального прокола. Повторные спинальные пункции также опасны, если не исключена внутричерепная аневризма. Наконец, при любой спинальной анестезии вазопрессоры следует вводить осторожно, титруя их эффект.
Интрацеребральное кровоизлияние
Кровоизлияние может произойти и внутри головного мозга, в частности после резкого подъема АД при чрезмерной коррекции гипотензии во время спинальной анестезии [2]. Этому может способствовать наличие мальформации сосудов полушарий.
Вклинение ствола головного мозга
Описан случай ущемления крючка головного мозга мозжечковым наметом (рис. 4, позиция 1) через 15 дней после спинальной анестезии со смертельным исходом [2].
Нарушения слуха
Хотя субклиническое или даже определяемое клинически снижение слуха после спинальной анестезии известно давно, мало кто из молодых анестезиологов знает о такой возможности. Одни авторы считают, что, по юридическим соображениям, следует предупреждать об этом пациентов перед спинальной анестезией, другие — что это лишь приведет к ненужному страху [2].
Частота. Клинически значимые субъективные нарушения слуха: его снижение, звон, жужжание или гудение в ушах — выявлены (без аудиометрии) у 0,4 % пациентов после 9277 спинальных анестезий. Аудиометрически снижение слуха на одно или оба уха выявляют у 10–50 % больных, но клинически заметное снижение — менее чем у четверти из этих 10–50 % [2].
Механизм. Причина снижения слуха, как и постпункционной головной боли, — ликворная гипотензия. Эндолимфа улитки внутреннего уха сообщается с субдуральным пространством головного мозга, а перилимфа — с субарахноидальным пространством мозга. Ликворная гипотензия после спинальной пункции нарушает работу кортиева органа.
Факторы риска те же, что и для постпункционной головной боли: возраст пациента, калибр и модель иглы.
Почему нарушения слуха наблюдаются реже, чем постпункционная головная боль? Потому что, во-первых, эти нарушения могут быть субклиническими, во-вторых, у 7 % взрослых имеется анатомическая обструкция водопровода улитки, а у 30 % — функциональная его обструкция. У них изменения ликворного давления не передаются перилимфе. Этим же объясняются случаи односторонних нарушений слуха.
Клинические проявления: снижение слуха, звон, жужжание или гудение в ушах — встречаются редко. При аудиометрии чистыми тонами снижение слуха выявляется значительно чаще, причем больше в диапазоне низких частот, что объясняют меньшей толщиной и большей податливостью базальной мембраны ближе к верхушке улитки, где происходит трансдукция низкочастотных звуков [2].
Дифференциальная диагностика. Нечаянная пункция оболочек спинного или головного мозга как причина нарушений слуха возможна при межлестничной блокаде плечевого сплетения, альвеолярной или инфильтрационной блокаде в стоматологии. Синдром Меньера (эндолимфатическая водянка) проявляется также звоном или шумом в ушах и снижением слуха (механизм похож, но базальная мембрана улитки смещается не из-за низкого давления перилимфы, а из-за высокого давления эндолимфы), однако раньше появляются и более выражены вестибулярные нарушения. Операции на ухе и любые операции под общей анестезией, особенно с искусственным кровообращением, также могут приводить к нарушениям слуха. Ототоксичность присуща ряду медикаментов: петлевым диуретикам (фуросемиду, буметаниду, этакриновой кислоте), антибиотикам (аминогликозидам, эритромицину, ванкомицину), аспирину, нестероидным противовоспалительным средствам (кеторолаку, напроксену, пироксикаму), противоопухолевым средствам (цисплатину, винкристину, винбластину).
Лечение: устранение ликворной гипотензии (как при постпункционной головной боли). Обычно эффективна эпидуральная пломбировка аутокровью [2].
Прогноз. Нарушения слуха после спинальной пункции проходят бесследно более чем в 95 % случаев. Необратимые нарушения очень редки.
Нарушения зрения
Нарушения зрения из-за параличей черепных, особенно глазодвигательных, нервов отмечались еще Квинке, но сейчас, хоть изредка возможны, известны не всем анестезиологам. А их надо знать: несмотря на общую первичную причину (ликворную гипотензию), их механизм, прогноз и, главное, лечение сильно отличаются от таковых для постпункционной головной боли и нарушений слуха.
Определения. Диплопия — двоение в глазах, субъективное ощущение, очень дискомфортное для больного из-за нарушения бинокулярного зрения. Косоглазие (лат. strabismus): сходящееся (лат. esotropia, strabismus convergens) или расходящееся (лат. exotropia, strabismus divergens) — объективно заметная непараллельность зрительных осей, являющаяся причиной диплопии и приносящая из-за неэстетичности субъективные страдания больному.
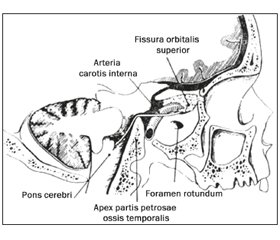
Механизм. Длительное проседание головного мозга при ликворной гипотензии различного происхождения может приводить к натяжению, компрессии и ишемии некоторых черепных нервов с их дегенерацией [2]. Особо подвержен ей отводящий нерв, пересекающий артерии у основания мозга и огибающий под почти прямым углом верхушку каменистой части височной кости (рис. 5).
Этим объясняются позднее (от дней до недель) начало параличей, длительное (от недель до месяцев) течение и сходящееся косоглазие.
Факторы риска: относительно молодой возраст (80 % — у людей моложе 50 лет, 30 % — моложе 30 лет) и пункция толстой иглой. Частые (1 : 140) случаи диплопии наблюдались в середине ХХ века после продленной спинальной анестезии иглами G16. Правда, в 2001 году описан один случай во Франции после пункции иглой Уайтэкра G25 при спинальной анестезии для кесарева сечения [2]. Половой предрасположенности, в отличие от постпункционной головной боли, не выявлено.
Частота. Параличи черепных нервов после спинальной анестезии во времена толстых игл встречались не так уж редко: от 1 : 8000 до 1 : 300, сейчас — намного реже: от 1 : 100 000 до 3,7 : 100 000 нейроаксиальных анестезий. Из 95 случаев, вошедших в обзор мировой литературы 1966–2002 гг., 47 % отмечались после спинальной анестезии, 18 % — после миелографии, 12 % — после диагностической поясничной пункции, 11 % — после нечаянного дурального прокола при эпидуральной анестезии, 4 % — после продленной спинальной анестезии. Описаны также случаи параличей глазодвигательных нервов после лечебных интратекальных инъекций, шунтирования желудочков мозга по поводу гидроцефалии и при спонтанной ликворной гипотензии [2].
Первые проявления параличей глазодвигательных мышц отмечались через 1 день — 3 недели после дуральной пункции (описан даже случай сразу после нее у 6-летнего ребенка), но чаще всего — между 4-м и 10-м днями [2]. Почти всегда этим параличам предшествует постпункционная головная боль, хотя иногда она может появиться позже или прекратиться до появления паралича. Описан случай пареза дивергенции глаз с диплопией через 17 дней после спинальной анестезии иглой Квинке G20 у 64-летнего мужчины вовсе без позиционной головной боли, но с ЯМР-признаками ликворной гипотензии [2].
Пораженные нервы: в большинстве случаев (92–95 %) — отводящий (VI, nervus abducens), около 80 % случаев — с одной стороны (рис. 6), иногда возможны дополнительные параличи глазодвигательного (III, nervus oculomotorius) или вращательного нерва (IV, nervus trochlearis). Точное разпознавание параличей последних нервов затруднено из-за выраженного сходящегося косоглазия. Один случай сочетанного поражения IV и VI нервов в Бельгии был распознан из-за параличей этих нервов с разных сторон [2].
/84.jpg)
Диагноз. Если паралич глазодвигательного нерва (III, IV, или VI) изолированный (без нарушений функций других нервов), наступил не позднее 3 недель после дуральной пункции и ему предшествовала типичная постпункционная головная боль, вероятно, что этот паралич является осложнением дуральной пункции. ЯМР-томографические признаки ликворной гипотензии: «понижение» ствола мозга, диффузное утолщение твердой оболочки и субдуральное скопление жидкости — не специфичны для параличей вследствие дуральной пункции и могут отсутствовать после прекращения постпункционной головной боли. А ведь именно тогда эти параличи и появляются. Поэтому ЯМР-томография нужна разве что для исключения других, более серьезных причин паралича, требующих специфического лечения. В частности, такие параличи или судороги возможны при внутричерепной гематоме или гигроме [2].
Дифференциальная диагностика. Паралич nervus abducens возможен также вследствие опухолей, ишемии, травмы, аневризмы, энцефалита, миастении и множественного склероза. В большинстве случаев найти причину параличей не удается [2]. Таким образом, косоглазие — еще не причина обвинять анестезиолога, а если оно появилось позднее 21-го дня от дуральной пункции, его вина абсолютно исключена. Мало ли может быть других причин поражения черепных нервов?
Лечение и прогноз. Эпидуральная пломбировка аутокровью, которая очень эффективная для лечения головной боли после дуральной пункции, не помогает при парезах глазодвигательных нервов: к моменту их появления функция и даже структура растянутого и ишемизированного нерва уже сильно пострадали. Единственный случай довольно быстрого улучшения (рис. 6) описан анестезиологами из Сеула [11]. Там у 43-летнего мужчины на 6-й день после начала постуральной головной боли из-за спонтанной ликворной гипотензии вследствие утечки ликвора на шейном уровне (от С4 до С6) началось двоение в глазах. Объективно — сходящееся косоглазие, особенно заметное при взгляде вправо (рис. 6, А–С). Диагноз: правосторонний паралич отводящего нерва. Через 10 дней после начала паралича выполнена под контролем флюороскопии эпидуральная пломбировка аутокровью (8 мл — до ощущения распирания) на уровне между С4 и С5. На следующий день головная боль почти исчезла, но двоение в глазах уменьшилось лишь частично. Через 2 месяца косоглазия не было (рис. 6, D).
В большинстве случаев косоглазие проходит самостоятельно, но это требует времени: от 2 недель до 8 месяцев. В этот период для уменьшения дискомфорта назначают либо повязку на глаз (дешевле), либо призменные очки (дороже). Корригирующие операции на окологлазных мышцах имеют свои риски, поэтому их можно рассматривать не ранее 8 месяцев: описаны случаи полного спонтанного выздоровления и годы спустя [2].
Профилактика. Минимизировать утечку ликвора: использовать тонкие иглы, лучше pencil-point, при развитии постпункционной головной боли рекомендовать постельный режим. Необычно раннее применение эпидуральной пломбировки аутокровью (в первые сутки от начала постпункционной головной боли) не оправданно. Во-первых, риск косоглазия очень низок. Во-вторых, если оно все же наступит, могут обвинить пломбировку (особенно обидно будет, если причиной головной боли была не анестезия, а диагностическая пункция или болезнь Шальтенбранда). В-третьих, пломбировка может действительно утяжелить симптомы при нераспознанной внутричерепной субдуральной гематоме [2].
/78.jpg)
/82.jpg)
/83.jpg)
/84.jpg)

/78_2.jpg)
/80.jpg)
/81.jpg)