Статья опубликована на с. 82-101
Острое кровотечение в просвет органов пищеварительного канала (ОКПОПК) до настоящего времени остается сложной и во многом нерешенной медицинской проблемой [9, 10, 15, 16, 19]. Несмотря на современные достижения хирургии, анестезиологии и реаниматологии, трансфузиологии и эндоскопии, результаты лечения данной категории больных по-прежнему остаются весьма далекими от желаемых. Летальность даже в специализированных клиниках достигает 10–15 %. Особенно велика летальность среди лиц старше 60 лет (до 40 %), у пациентов с циррозом печени (до 65 %), а также при рецидиве кровотечения (до 20 %) [2, 3, 11, 13].
Причин, обусловливающих высокую летальность, достаточно много. Это и увеличение числа пациентов, причем преимущественно за счет так называемых неязвенных кровотечений. В последнее время значительно увеличилось число пациентов с циррозом печени и кровотечением из варикозно расширенных вен пищевода и/или желудка [5, 7, 12, 14, 20].
Это связано и с поздней обращаемостью за медицинской помощью. Причем это касается как больных с запущенным основным заболеванием (например, язвенная болезнь, осложненная пенетрацией или стенозом, цирроз печени в стадии декомпенсации, тяжелая соматическая патология, осложненная образованием острых язв и эрозий, и т.д.), так и больных, обращающихся за помощью в поздние сроки от начала непосредственно самого кровотечения [1, 4, 8]. В результате значительно увеличивается число больных, поступающих в тяжелом и крайне тяжелом состоянии, когда даже в прямом смысле героические усилия врачей не в состоянии спасти жизнь пациенту.
Не менее важными причинами являются ошибки, допущенные при диагностике источника кровотечения, назначении инфузионно-трансфузионной и антисекреторной терапии, выборе способа и объема операции, а также технические ошибки, допущенные во время хирургического вмешательства, погрешности в ведении послеоперационного периода, порой запоздалое и недостаточно активное лечение осложнений [6, 17, 18].
Все сказанное свидетельствует о многих нерешенных проблемах лечения пациентов с ОКПОПК и необходимости как поиска новых, более совершенных подходов к организации оказания специализированной медицинской помощи населению, так и разработки и усовершенствования диагностических, тактических и лечебных установок.
Цель исследования — представить итоги 35 лет работы специализированного центра, а также наработанные за это время организационные, диагностические и тактические рекомендации по лечению пациентов с ОКПОПК.
Материал и методы
С 1981 по 2015 год в клинике хирургии Донецкого национального медицинского университета, которая является базой городского специализированного центра, на лечении находилось более 22 000 пациентов с ОКПОПК в возрасте от 14 до 96 лет.
Наиболее частые причины ОКПОПК представлены в таблице 1. Обращает на себя внимание существенное увеличение числа пациентов с неязвенными кровотечениями, и в первую очередь с кровоточащими острыми язвами и эрозиями слизистой оболочки и кровотечением из варикозно расширенных вен пищевода и/или желудка, особенно в последние годы. При этом число пациентов с язвенной болезнью на протяжении 35 лет существенно не изменилось и колебалось в пределах от 345 в 1985 г. до 382 в 2012 г.
Следует отметить, что в последние годы существенно возросло число пациентов с ОКПОПК, длительно принимающих антикоагулянты (варфарин и др.), нестероидные противовоспалительные препараты, а также салицилаты. Кровотечения у этих пациентов крайне тяжело поддаются консервативной терапии, а оперативное лечение либо сопряжено с чрезвычайно высоким риском из-за тяжести основного заболевания, либо вообще не показано, когда, например, кровоточит практически вся поверхность слизистой оболочки желудка.
Наиболее часто источник ОКПОПК находился в верхних отделах пищеварительного канала: пищеводе, желудке, двенадцатиперстной кишке (выше связки Трейца) — у 90 % пациентов. В нижних отделах пищеварительного канала — тощей, подвздошной, толстой кишке (ниже связки Трейца) — он располагался у 8,5 % пациентов; причина и локализация источника кровотечения осталась невыясненной у 1,5 % пациентов.
Длительность кровотечения более 24 ч отмечена у 45 % пациентов. В своей практической деятельности мы использовали следующую классификацию ОКПОПК [6].
Классификация ОКПОПК
1. По этиологическому признаку.
1.1. Кровотечение, обусловленное заболеваниями органов пищеварения (язвенная болезнь, опухоли, неспецифические колиты и т.д.).
1.2. Кровотечение, не связанное с органической патологией органов пищеварительного канала (острые язвы и эрозии, болезни крови, синдром портальной гипертензии и т.д.).
1.3. Ложное кровотечение (проглоченная кровь при кровоточивости десен или необильном легочном кровотечении).
1.4. Кровотечение невыясненной этиологии.
2. По локализации источника кровотечения: кровотечение из пищевода, желудка, двенадцатиперстной, тощей, подвздошной, ободочной и прямой кишок, сочетанное.
3. По клиническому течению.
3.1. Скрытое кровотечение.
3.2. Явное кровотечение:
— продолжающееся: струйное/диффузное (капельное просачивание или подтекание «потоком»);
— остановившееся/состоявшееся кровотечение.
4. По степени тяжести кровопотери:
— кровопотеря легкой степени (дефицит ОЦК составляет менее 20 %);
— кровопотеря средней степени тяжести (дефицит ОЦК составляет 20–30 %);
— кровопотеря тяжелой степени (дефицит ОЦК составляет 31–40 %);
— кровопотеря крайне тяжелой степени тяжести (дефицит ОЦК составляет более 40 %).
5. По степени геморрагического шока:
— кровотечение с компенсированным шоком;
— кровотечение с субкомпенсированным шоком;
— кровотечение с декомпенсированным обратимым шоком;
— кровотечение с декомпенсированным необратимым шоком.
Результаты и обсуждение
Организация оказания помощи пациентам с ОКПОПК — одна из главных задач, правильное решение которой позволяет существенно улучшить результаты лечения этой крайне тяжелой патологии.
На сегодняшний день бесспорным является то, что лечение всех больных с ОКПОПК должно осуществляться только в условиях специализированных хирургических центров, обеспеченных не только современным лечебно-диагностическим оборудованием, необходимыми медикаментами и инфузионными средами, но и прежде всего высококвалифицированными специалистами — хирургами, эндоскопистами-хирургами, врачами интенсивной терапии, анестезиологами, специалистами по нутритивной поддержке и др.
Диагностика ОКПОПК
Диагноз ОКПОПК устанавливается на основании данных анамнеза, клинического и лабораторного обследования, при этом наиболее информативным является эндоскопическое исследование.
Главными задачами врача при ОКПОПК являются:
— правильная оценка тяжести состояния пациента;
— своевременная диагностика источника кровотечения;
— достижение надежного локального гемостаза;
— обязательная параллельная коррекция кровопотери;
— лечение основного и сопутствующих заболеваний.
Причем вероятность благоприятного исхода значительно возрастает при успешном решении именно всех перечисленных задач!
При осмотре больного в первую очередь оценивают общее состояние больного.
Критерии оценки степени тяжести больного с ОКПОПК приведены в таблице 2.
Диагностика геморрагического (гиповолемического) шока
Основные симптомы геморрагического (гиповолемического) шока:
— бледная, цианотичная, мраморного вида, холодная, влажная кожа;
— симптом бледного пятна ногтевого ложа;
— учащенное дыхание;
— нарушение функции центральной нервной системы (поведение неадекватно или же сознание затемнено) и почек (олиго- или анурия);
— пульс слабого наполнения;
— снижение систолического артериального давления;
— уменьшение амплитуды артериального давления, нередко аритмия, выраженный систолический шум над верхушкой сердца;
— кратковременное обморочное состояние.
Диагностически-тактический алгоритм при ОКПОПК представлен на рисунке 1.
При удовлетворительном состоянии больного или состоянии средней тяжести в приемном отделении выполняют:
— объективное исследование пациента (сбор жалоб, анамнеза болезни и жизни, объективное обследование) с параллельным изучением лабораторных показателей крови и мочи (общий анализ крови и мочи, амилаза крови и т.д.);
— пальцевое исследование прямой кишки и определяют характер ее содержимого;
— аспирацию содержимого желудка с помощью зонда и промывание желудка. Последнее позволяет существенно повысить точность и эффективность следующего этапа обследования — ургентной фиброэзофагогастродуоденоскопии (ФЭГДС).
Если во время эндоскопического обследования источник кровотечения установлен, осуществляют эндоскопический гемостаз (при продолжающемся кровотечении) или эндоскопическую профилактику рецидива кровотечения (при остановленном кровотечении). Больных госпитализируют в отделение интенсивной терапии (ОИТ) для проведения комплексной инфузионной и медикаментозной терапии.
В тех случаях, когда во время экстренной ФЭГДС патологии со стороны пищевода, желудка и начального отдела двенадцатиперстной кишки не выявлено, в условиях ОИТ в течение 4–6 часов больных готовят и выполняют экстренную фиброколоноскопию (ФКС) или ирригографию.
Если и эти исследования не позволяют установить источник и причину кровотечения, то повторно выполняют ФЭГДС. Если и это не дало необходимого результата, можно думать, что источник кровотечения, скорее всего, расположен в тощей или подвздошной кишке. В этом случае целесообразно выполнить контрастное исследование тонкой кишки (энтерографию) или селективную мезентерикографию.
Больных, находящихся в тяжелом или крайне тяжелом состоянии, состоянии геморрагического шока, без обследования в приемном отделении сразу госпитализируют в ОИТ, где без промедления начинают интенсивное корригирующее лечение! Если состояние больного удалось стабилизировать, обследование проводят по вышеописанной схеме.
Пациентам с продолжающимся кровотечением и неэффективными попытками эндоскопического гемостаза в течение 30 мин показано выполнение экстренного оперативного вмешательства независимо от степени тяжести кровопотери.
Эти пациенты из эндоскопического отделения должны быть сразу же доставлены в операционную.
Корригирующая инфузионная и медикаментозная терапия шока и кровопотери проводится непосредственно на операционном столе, в т.ч. и во время операции.
Если в процессе лечения отмечаются признаки рецидива кровотечения (снижение АД, показателей крови, рвота кровью и т.д.), больному показана экстренная операция, целью которой является выявление источника кровотечения и его остановка.
При подозрении на ОКПОПК, если исключить его в приемном отделении не представляется возможным, больной должен быть госпитализирован в хирургическое отделение для наблюдения.
Все перемещения пациента с ОКПОПК в стационаре для проведения диагностических или лечебных мероприятий должны осуществляться на каталке в лежачем положении.
Дифференциальная диагностика
В течении острого кровотечения в просвет органов пищеварительного канала выделяют два периода: скрытый и явный.
Наиболее частыми признаками ОКПОПК в скрытый период являются: слабость (наблюдается практически у 100 % больных), побледнение кожи (у 70–90 %), головокружение (у 60–80 %), мелькание «мушек» перед глазами, шум в ушах, тремор рук, холодный пот, сердцебиение, обморок (у 10–30 %).
Перечисленные симптомы являются проявлением гиповолемии и, как следствие, — гипоксии мозга. Степень их выраженности зависит от интенсивности кровотечения, исходного состояния больного и компенсаторных возможностей организма.
Вместе с тем все вышеуказанные симптомы или их сочетания могут наблюдаться при различных состояниях: кровотечении (наружном кровотечении, причина, как правило, травма; кровотечении в брюшную полость — прерванная трубная беременность, спонтанный разрыв селезенки; травма — разрыв паренхиматозного органа, отрыв брыжейки кишки и др.; кровотечении в просвет органов пищеварительного канала), инфаркте миокарда, перитоните, остром панкреатите (особенно в стадии эндотоксинового шока), кровотечении на фоне перфоративной язвы, анемии различного генеза, тромбозе мезентериальных сосудов (острой сосудистой недостаточности кишечника), онкопатологии.
Осмотр больного и короткий опрос позволяют врачу достаточно быстро заподозрить ту или иную патологию, а применение вспомогательных методов диагностики — установить ее точно.
Осмотр больного позволяет определить, имеется ли наружное кровотечение. Боль за грудиной является частым симптомом инфаркта миокарда (основной метод диагностики — ЭКГ). Сведения о недавно полученной травме живота должны натолкнуть на мысль о возможности разрыва паренхиматозного органа, отрыва брыжейки кишки и т.д. с внутрибрюшным кровотечением. УЗИ, а также лапароскопия и лапароцентез, в т.ч. с использованием «шарящего» катетера (кровь в животе), позволяют установить правильный диагноз.
Возникшая накануне боль в животе может быть проявлением спонтанного разрыва селезенки, прервавшейся трубной беременности, острой сосудистой недостаточности кишечника, перитонита. Методы диагностики: УЗИ, лапароскопия, лапароцентез, в т.ч. с использованием «шарящего» катетера. Болью в животе может сопровождаться и острый панкреатит. Исследование активности амилазы/диастазы крови/мочи, УЗИ и КТ позволяют подтвердить диагноз.
Боль в животе может наблюдаться при кровотечении на фоне перфоративной язвы. Для установления диагноза используют: обзорную рентгенографию органов брюшной полости на предмет свободного газа, пневмогастрографию, ФЭГДС.
Могут отсутствовать все вышеперечисленные симптомы и анамнестические данные. В этом случае причиной слабости, побледнения кожных покровов, головокружения и т.д. могут быть: острое кровотечение в просвет пищеварительного канала, онкопататология, анемия. Очередность диагностических мероприятий следующая: исследование прямой кишки пальцем (на перчатке — кал обычного цвета, мелена или кровь и т.д.), исследование желудочного содержимого с помощью зонда (обычное желудочное содержимое, кровь, содержимое типа «кофейной гущи» и т.д.), ФЭГДС, фиброколоноскопия, УЗИ, КТ.
В явный период ведущими клиническими признаками ОКПОПК являются кровавая рвота (гематемезис) и кровавый кал. Причем если кровавая рвота наблюдается у 60–70 %, то кровавый кал является более постоянным признаком ОКПОПК и наблюдается практически у всех больных.
Исключение составляют так называемые молниеносные формы кровотечения, когда пациент умирает раньше, чем появляются мелена или кровавая рвота (табл. 3).
ОКПОПК следует дифференцировать от легочного кровотечения, при котором кровавая рвота имеет пенистый характер и сопровождается кашлем. В легких нередко выслушивают разнокалиберные влажные –хрипы.
Анамнестические данные и данные объективного обследования, позволяющие заподозрить причину или источник ОКПОПК, представлены в таблице 4.
Эндоскопическая диагностика
Основным методом инструментальной диагностики ОКПОПК является эндоскопическое исследование.
Основные задачи эндоскопического исследования при ОКПОПК:
— установить источник кровотечения и его локализацию;
— установить степень активности кровотечения (продолжающееся или остановившееся кровотечение);
— при продолжающемся кровотечении по возможности добиться местного гемостаза с помощью эндоскопических методик;
— при остановившемся кровотечении определить степень надежности гемостаза и провести эндоскопическую профилактику его рецидива.
Показанием к выполнению экстренного эндоскопического исследования является даже подозрение на наличие кровотечения в просвет органов пищеварительного канала.
Чем раньше оно выполнено, тем выше его диагностическая и прогностическая ценность. Эндоскопическое исследование должно быть выполнено сразу после поступления больного в стационар, независимо от того, продолжается кровотечение или остановилось.
Противопоказаниями к выполнению эндоскопического исследования являются:
— агональное состояние пациента;
— тяжелое общее состояние (низкое артериальное давление, шок и т.д.);
— острое нарушение мозгового кровообращения;
— сердечно-легочная декомпенсация;
— тяжелое психическое заболевание;
— резкая деформация шейного отдела позвоночника;
— отсутствие адекватного контакта с пациентом.
Эндоскопическая характеристика источника кровотечения
Все кровотечения делят на продолжающиеся (активные) и остановившиеся (состоявшиеся).
Типы активного кровотечения (по интенсивности):
— струйное — кровотечение пульсирующей струей;
— массивное — интенсивное поступление крови, когда невозможно точно определить место кровотечения на слизистой оболочке;
— диффузное: капельное (просачивание) — на поверхности слизистой оболочки после отмывания струей воды тотчас появляется капля крови без четко видимого дефекта слизистой оболочки; потоком (подтекание) — кровь течет от места повреждения по стенке.
В постгеморрагическом периоде при эндоскопическом осмотре выделяют признаки остановившегося кровотечения:
— наличие в полости желудка неизмененной и/или редуцированной крови, сгустков крови;
— фиксированный пристеночный тромб-сгусток — сгусток, прикрепленный к поврежденному участку слизистой оболочки и устойчивый к отмыванию;
— видимый сосуд на дне язвы в виде красноватого бугорка — «часового» тромба или в виде блестящего «жемчужного» бугорка в дне, крае язвы или выступающего над поверхностью ее дна;
— плоское черное пятно или точка на слизистой оболочке (отложение гематина).
Три первых признака служат критерием высокого риска рецидива кровотечения!
При наличии гематинового струпа и точечных отложений гематина риск рецидива кровотечения невелик.
Эндоскопический гемостаз
Все современные способы эндоскопического воздействия на источник кровотечения делят на три основные группы: медикаментозные, физические и механические.
Медикаментозные методы:
— инъекции в область кровоточащего сосуда вазоконстрикторов, прокоагулянтов, склерозирующих препаратов, этанола.
Физические методы:
— электрокоагуляция (диатермо- и гидродиатермо-, моно- и биполярная электрокоагуляция);
— термокоагуляция (криокоагуляция и термокаутеризация);
— аргоно-плазменная коагуляция;
— радиоволновая коагуляция;
— лазерная фотокоагуляция.
Механические методы:
— клипирование эндоскопическими клипсами;
— лигирование эластичными кольцами и эндоскопическими петлями;
— инфильтрационный метод — гидрокомпрессия перивазальных тканей (для этой цели используют физиологический раствор).
Все перечисленные методы эндоскопического воздействия на источник кровотечения могут применяться как для остановки продолжающегося кровотечения, так и для профилактики его рецидива.
Выбор способа эндоскопического гемостаза
Пептическая язва, острые язвы слизистой оболочки, синдром Маллори — Вейсса
Эндоскопический гемостаз (продолжающееся кровотечение) — предпочтение следует отдавать инъекционному и инфильтрационному методам с последующим применением термокаутеризации, диатермоэлектрокоагуляции или аргоно-плазменной коагуляции сгустка (кровоточащего сосуда) и/или перивазальных тканей.
Эндоскопическая профилактика рецидива кровотечения — подразумевает выполнение контрольных лечебных эндоскопических исследований с использованием медикаментозных, физических и механических методов воздействия на источник крово–течения.
Критерии прекращения эндоскопической профилактики:
— очищение язвенного дефекта от геморрагического или некротического налета;
— исчезновение видимых в дне или выстоящих в просвет тромбированных сосудов;
— гладкое, покрытое фибрином дно язвенного дефекта.
Кровоточащие опухоли
Доброкачественные опухоли. При полипе — электроэксцизия полипа с помощью диатермической петли. При больших размерах полипа (удалить которые одномоментно невозможно) — инъекции вазоконстрикторов и физиологического раствора в основание или ножку полипа (ишемизация полипа), диатермокоагуляция или термокоагуляция кровоточащей поверхности. В дальнейшем решается вопрос о возможности поэтапной электроэксцизии полипа или выполнения полостного оперативного вмешательства.
Злокачественные опухоли. Инъекционный способ гемостаза малоэффективен! После визуализации источника кровотечения выполняют аргоно-плазменную коагуляцию или термокаутеризацию сгустка, кровоточащей поверхности (сосуда).
Синдром портальной гипертензии
При активном кровотечении — постановка зонда Блейкмора по общепринятой методике. Основными методами эндоскопического гемостаза при кровотечении из варикозно расширенных вен пищевода являются наложение резиновых колец или эндопетель, склерозирующая терапия. При кровотечении из варикозно расширенных вен желудка в целях гемостаза применяют эмболизацию или наложение резиновых колец. Склерозирующая терапия малоэффективна и дает тяжелые осложнения.
Тактика лечения ОКПОПК
Последовательность лечебно-диагностических мероприятий в стационаре при ОКПОПК:
— полное лабораторное обследование;
— интенсивная инфузионная и медикаментозная корригирующая терапия;
— определение величины кровопотери;
— эндоскопический мониторинг (частота контрольно-лечебных эндоскопических исследований зависит от степени риска рецидива кровотечения);
— определение тактики лечения больного на основании данных инструментальных и лабораторных методов исследования, а также эффективности проводимой корригирующей терапии;
— очистительные клизмы для удаления крови, излившейся в кишечник.
Определение величины кровопотери, инфузионную и медикаментозную корригирующую терапию проводит врач-анестезиолог, эндоскопический мониторинг — врач-эндоскопист, а тактику лечения определяет старший дежурный хирург.
Лабораторная диагностика в условиях стационара
Перечень обязательных (рутинных) лабораторных обследований: общий анализ крови (обязательно с развернутой формулой), количество тромбоцитов в периферической крови, креатинин, мочевина, сахар крови и мочи, коагулограмма, общий анализ мочи, общий белок (перечисленные обследования необходимо выполнять в динамике, прежде всего у пациентов с тяжелой и крайне тяжелой степенью кровопотери), а также билирубин, трансаминазы сыворотки крови, группа крови и резус-принадлежность, ФЛГ, серологическое обследование на сифилис.
Следует помнить о том, что острое кровотечение язвенной этиологии, несмотря на анемию, зачастую сопровождается умеренным лейкоцитозом. Случается, что количество лейкоцитов находится в пределах нормы. Причем выраженность лейкоцитоза пропорциональна степени кровопотери: чем тяжелее кровопотеря, тем больше лейкоцитов в периферической крови. У 1/3 больных обнаруживается сдвиг формулы влево. При этом отмечается относительная лимфо- и моноцитопения.
При тяжелых кровотечениях наблюдается снижение количества эозинофилов, вплоть до полного их исчезновения. Лейкопения более характерна для кровотечений при циррозе печени, полипах желудка, эрозивно-язвенном гастрите. Значительное увеличение числа лейкоцитов на фоне анемии в сочетании с другими клиническими данными позволяет заподозрить острый лейкоз как возможную причину острого кровотечения.
Хорошо известно, что любое кровотечение сопровождается снижением показателей гемоглобина, гематокрита и количества эритроцитов. Степень их изменения также пропорциональна тяжести кровопотери. При массивных, особенно рецидивирующих, кровотечениях в периферической крови появляются молодые форменные элементы с развитием анизо- и пойкилоцитоза.
Отдельные вопросы комплексного лечения ОКПОПК
Поскольку вопросы интенсивной инфузионной и медикаментозной корригирующей терапии, определения величины кровопотери достаточно подробно изложены в специальной литературе, заострим внимание читателя лишь на некоторых из них. К ним относятся: подавление желудочной секреции, системная гемостатическая терапия, нутритивная поддержка и эндоскопический мониторинг.
Подавление желудочной секреции. Обязательным компонентом лечения ОКПОПК из верхних отделов пищеварительного канала (за исключением злокачественных опухолей) является назначение препаратов, подавляющих желудочную секрецию. Для этого целесообразно использовать:
— плюс ингибиторы протонной помпы: контролок (пантопразол), нексиум (эзомепразол), омез (омепразол) — 80 мг в/в болюсно, затем по 8 мг/ч в течение 3–5 и более суток с последующим переходом на пероральный прием;
— плюс антацидные препараты: тальцид, маалокс, гастал, альмагель, гестид, ренни;
— плюс препараты, оказывающие защитное действие на слизистую оболочку желудка и двенадцатиперстной кишки: вентер (сукральфат) или де-нол.
Системная гемостатическая терапия. Все системные гемостатические средства делят на две группы: ускоряющие коагуляцию (свежезамороженная плазма, препараты витамина К, факторы свертывания, терлипрессин, октаплекс, новосэвен) и ингибирующие фибринолиз (транексамовая кислота, аминокапроновая кислота, апротинин).
N.B.! На сегодняшний день лишь два препарата реально доказали свой высокий гемостатический эффект — октаплекс и новосэвен.
Октаплекс (международное название — Coagulation factor IX, II, VII and X in combination) — концентрат протромбинового комплекса.
Новосэвен — рекомбинантный коагуляционный фактор VIIа. Частота осложнений — тромбозы сосудов центрального синуса, инсульт, инфаркт миокарда, тромбоз глубоких вен, ДВС-синдром — не превышает 1 %.
Все остальные препараты для так называемой системной гемостатической терапии при ОКПОПК в лучшем случае могут лишь создавать те или иные более благоприятные условия для достижения локального гемостаза, но при этом не оказывают непосредственного гемостатического действия!
Кроме препаратов октаплекс и новосэвен, при остром кровотечении в просвет органов пищеварительного канала в качестве вспомогательных средств можно рекомендовать транексамовую кислоту, реместип (терлипрессин) и дицинон (этамзилат натрия).
Таким образом, на сегодняшний день для системной гемостатической терапии могут быть рекомендованы:
1. Октаплекс (концентрат протромбинового комплекса). Вводится внутривенно медленно, вначале со скоростью 1 мл в 1 минуту, в последующем по 2–3 мл в 1 минуту, с соблюдением асептических условий.
Доза зависит от начального и целевого значения международного нормализованного отношения (МНО). В таблице 5 приведены примерные дозы (мл/кг массы тела восстановленного препарата), необходимые для нормализации МНО (< 1,2 в течение 1 ч) при его различных исходных уровнях.
2. Новосэвен (рекомбинантный коагуляционный фактор VIIа). Вводится внутривенно болюсно по 60–120 мкг/кг массы тела за одну инъекцию в течение 2–5 минут.
3. Транексамовая кислота — вводится внутривенно из расчета 10–15 мг на 1 кг массы тела. Гемостатический эффект превосходит таковой аминокапроновой кислоты.
4. Реместип (терлипрессин) — кровотечение из варикозно расширенных вен пищевода: 1 мг (1000 мкг) в/в болюсно или в виде кратковременной инфузии каждые 4–6 ч на протяжении 3–5 дней. Для профилактики рецидива терапию продолжают в течение 24–48 ч после остановки кровотечения. Другие кровотечения из органов пищеварительного канала: 1 мг каждые 4–6 ч (препарат также может быть использован как средство первой помощи независимо от хирургического вмешательства при подозрении на кровотечение из верхних отделов пищеварительного канала).
5. Дицинон (этамзилат натрия) — эффект препарата проявляется через 5–15 мин после внутривенной инъекции 250–500 мг, максимальный эффект достигается через 1–2 ч после введения.
При дефиците факторов свертывания (заболевания крови — гемофилия и др.) показано применение:
— свежезамороженной плазмы — ее гемостатический эффект основан на высоком содержании факторов свертывания крови и их ингибиторов;
— концентрата фактора VIII (антигемофильный фактор А, Коэйт-ДВИ) — катализирует реакцию превращения протромбина в тромбин и образование фибринового сгустка. При внутривенном введении 40–50 МЕ/кг эффект наступает в течение 15 минут и обеспечивает повышение фактора VIII на 80–100 %. Показания к введению препарата ограниченны, в основном применяется для профилактики кровотечений в предоперационном периоде у лиц, страдающих гемофилией;
— криопреципитата — является продуктом обработки и концентрации донорской плазмы. Препарат содержит факторы свертывания крови (VIII, XIII, Виллебранда, фибриноген и фибронектин) и применяется при дефиците указанных факторов, ДВС-синдроме;
— викасола (менадиона натрия бисульфит) — повышает свертываемость крови за счет усиления выработки в печени факторов II (протромбин), VII (проконвертин), IX (плазменный тромбопластин), X. Эффект проявляется через 16–18 часов (!) после внутримышечного введения 2 мл водного раствора препарата.
Нутритивная поддержка. Основным методом нутритивной поддержки является пероральный прием различных сбалансированных стандартных полимерных смесей высокой питательной плотности.
Эндоскопический мониторинг является обязательным компонентом лечения ОКПОПК, который позволяет проводить профилактику рецидива кровотечения и своевременно выявлять непосредственно сам рецидив кровотечения. Частота контрольно-лечебных эндоскопических исследований зависит от степени риска рецидива кровотечения.
Общие принципы хирургической тактики при ОКПОПК
Показания и виды хирургических вмешательств:
— экстренные (срочные, неотложные) операции — выполняются безотлагательно в связи с неэффективностью эндоскопических методов гемостаза при продолжающемся или рецидивном кровотечении;
— отсроченные операции — вмешательства, выполняемые в связи с ненадежным гемостазом (для того чтобы избежать рецидива кровотечения) в ближайшие 6–8, 36 и 72 часа с момента госпитализации, что зависит от степени риска рецидива кровотечения (высокой, умеренной, незначительной);
— ранние плановые операции — вмешательства, выполняемые после проведения полноценного обследования и необходимой подготовки, по сути в плановом порядке.
Операцию не производят, если пациент:
— отказывается от операции;
— находится в пред- или агональном состоянии.
В таких случаях применяют комплексную корригирующую и медикаментозную терапию, а также по возможности проводят эндоскопическую профилактику рецидива кровотечения.
Выполнение любого оперативного вмешательства при ОКПОПК должно отвечать следующим требованиям:
— надежно останавливать кровотечение;
— избавлять больного от заболевания, которое явилось причиной кровотечения;
— сопровождаться минимальной травматичностью, летальностью и числом послеоперационных осложнений.
Немаловажное значение в исходе операции играет фактор времени. Хирургическое вмешательство должно выполняться без спешки, но достаточно быстро.
Задачами хирургического лечения при ОКПОПК являются:
— установление локализации источника кровотечения;
— устранение источника кровотечения и по возможности основного заболевания, осложнившегося ОКПОПК;
— восстановление пассажа содержимого по желудочно-кишечному тракту или его отведение наружу (при высоком риске несостоятельности швов межкишечных анастомозов);
— декомпрессия желудочно-кишечного тракта;
— дренирование брюшной полости.
Основной вид обезболивания при операциях по поводу ОКПОПК — комбинированный эндотрахеальный наркоз с применением мышечных релаксантов.
Хирургический доступ. Основным доступом при оперативном лечении ОКПОПК является срединная лапаротомия.
При выполнении хирургического вмешательства на органах желудочно-кишечного тракта вместо капроновых или лавсановых нитей предпочтение следует отдавать синтетическим рассасывающимся нитям Vicryl (Ethicon, Шотландия) на атравматической игле, которые рассасываются в течение 1,5–3 месяцев и практически не вызывают длительного воспаления в зоне анастомоза, как капроновые или лавсановые нити.
Тактика лечения отдельных видов ОКПОПК
Острое язвенное гастродуоденальное кровотечение. У всех пациентов, поступающих с состоявшимся (остановленным) кровотечением, а также у пациентов, у которых продолжающееся кровотечение было остановлено эндоскопически при поступлении, должна быть определена степень риска рецидива кровотечения. От этого во многом зависит дальнейшая тактика лечения.
Классификация эндоскопических стигмат (признаков) острого язвенного гастродуоденального кровотечения (J. Forrest, 1974):
F-I (Forrest I) — продолжающееся кровотечение:
F I A — струйное кровотечение;
F I B — диффузное кровотечение.
F-II — состоявшееся (остановленное) кровотечение:
F II A — тромбированный сосуд (красный, черный, белый);
F II А v(+) — «жемчужный» бугорок или «часовой» тромб с жемчужным ободком;
F II А v(–) — «часовой» тромб без жемчужного ободка;
F II B — фиксированный сгусток;
F II C — мелкие тромбированные сосуды (красные, черные точки).
F-III — признаки кровотечения отсутствуют (дно дефекта слизистой оболочки покрыто фибрином).
Частота рецидива кровотечения составляет:
— F IA — 90 %;
— F IB — 30 %;
— F IIA — 20 %;
— F IIB — 50 %;
— F IIC — < 5 %;
— F III — < 5 %;
— при стигматах кровотечения и признаках шока — 79 %;
— только при стигматах кровотечения — 61 %;
— только при признаках шока — 66 %.
Тактика лечения больного во многом зависит от эндоскопической характеристики источника кровотечения. Больным, входящим в группу F I, показано применение активных методов эндоскопического гемостаза или выполнение экстренного хирургического вмешательства.
Группа F II свидетельствует об определенном риске рецидива кровотечения, т.е. ненадежном гемостазе. Причем наибольшая его вероятность отмечена при F IIB и F IIA. Данной категории больных показано проведение комплексного консервативного лечения или выполнение отсроченной операции.
Рецидив кровотечения практически не наблюдается при F III. Поэтому этим больным показано проведение противоязвенной и симптоматической восстановительной терапии.
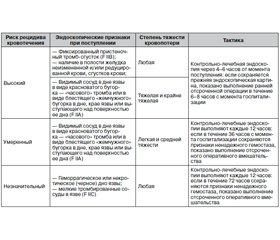
На основании анализа результатов хирургического лечения пациентов с острым язвенным гастродуоденальным кровотечением были разработаны критерии определения риска рецидива кровотечения, а также хирургическая тактика (табл. 6).
К дополнительным факторам, увеличивающим риск рецидива кровотечения, относятся:
— АД < 100 мм рт.ст.;
— диаметр язвы двенадцатиперстной кишки — более 1,5 см, желудка — более 2 см;
— глубокая (пенетрирующая) язва;
— стеноз пилородуоденального сегмента, непроходимый для эндоскопа;
— сопутствующая патология в стадии суб- и декомпенсации;
— возраст пациента старше 70 лет.
Факторы надежного гемостаза:
— фибринозный налет на дне язвы;
— стабильная гемодинамика;
— отсутствие данных, свидетельствующих о нарушении периферического кровообращения (микроциркуляции).
Степень риска рецидива кровотечения может меняться в динамике на фоне проводимой консервативной терапии и лечебных эндоскопий (от высокой к незначительной и наоборот).
При появлении признаков надежного гемостаза, а именно: фибринозного налета на дне язвы, стабильной гемодинамики, отсутствия данных, свидетельствующих о нарушении периферического кровообращения (микроциркуляции), больные могут быть переведены в хирургическое отделение для проведения реабилитационного лечения и определения показаний к выполнению ранней плановой операции.
Если у больного имеются клинические или эндоскопические признаки рецидива кровотечения без явлений геморрагического шока, целесообразно использовать эндоскопические методы гемостаза. Если кровотечение остановлено, продолжают комплексное лечение и осуществляют дальнейший эндоскопический мониторинг.
При неэффективности эндоскопического гемостаза в течение 30 минут, а также у больных с рецидивом кровотечения и явлениями геморрагического шока показано выполнение экстренного оперативного вмешательства с проведением противошоковой терапии непосредственно на операционном столе в процессе подготовки и во время проведения экстренного хирургического вмешательства.
Показания к выбору способа и объема хирургического вмешательства при остром язвенном гастродуоденальном кровотечении
Операциями выбора при локализации язвы в желудке являются:
— резекция желудка с сохранением привратника (надпривратниковая резекция желудка) — если имеется возможность сохранить иннервацию препилорического и пилорического отдела желудка;
— резекция желудка по Бильрот-І (Реаn, Вillrоth; Shcoemaker, Shcmieden) — если невозможно сохранить иннервацию препилорического и пилорического отдела желудка;
— иссечение язвы — у пациентов, находящихся в состоянии геморрагического шока, с кровопотерей тяжелой и крайне тяжелой степени, с сопутствующей патологией в стадии субкомпенсации.
При язве желудка может быть выполнено клиновидное иссечение язвы или иссечение язвы со стороны слизистой оболочки желудка.
Операциями выбора при локализации язвы в двенадцатиперстной кишке являются:
— резекция желудка по Бильрот-І (Реаn, Вillrоth; Shcoemaker, Shcmieden; типа Тоmoda) — при стенозе выхода из желудка;
— иссечение язвы со стороны слизистой оболочки двенадцатиперстной кишки или выведение кратера язвы за пределы пищеварительного канала.
При иссечении язвы двенадцатиперстной кишки предпочтение следует отдавать дуоденопластике.
При локализации кровоточащей язвы на передней, передне-верхней или передне-нижней стенке двенадцатиперстной кишки применяют методики Джадда — Танаки, Джадда — Хорсли.
При расположении язвы на верхней или верхне-задней, нижней или задне-нижней стенке двенадцатиперстной кишки с пенетрацией в гепатодуоденальную связку и поджелудочную железу, а также на задней стенке двенадцатиперстной кишки, в том числе и гигантской, рекомендуется применять методики операций, специально разработанные для этих локализаций язв.
При сочетании кровоточащей язвы со стенозом и расположением язвы на передней стенке двенадцатиперстной кишки используют методику Барри — Хилла, а при ее локализации на задней стенке — методику расширяющей пилоро- или дуоденопластики.
Операциями выбора при локализации язвы в желудке и двенадцатиперстной кишке являются:
— резекция желудка по Бильрот-І (Реаn, Вillrоth; Shcoemaker, Shcmieden; типа Тоmoda);
— селективная ваготомия с антрумэктомией.
У пациентов, находящихся в состоянии геморрагического шока, с кровопотерей тяжелой и крайне тяжелой степени, с сопутствующей патологией в стадии субкомпенсации операцией выбора является иссечение язвы.
В связи с большим числом осложнений (рецидив кровотечения — 7–17 %, летальность — 8–10 %) такие оперативные вмешательства, как ушивание/зашивание кровоточащей язвы или прошивание кровоточащего сосуда в язве, выполнять не рекомендуется!
Эти оперативные вмешательства могут быть использованы лишь как способ временного гемостаза в ходе операции, после чего язва должна быть иссечена или выведена за пределы пищеварительного канала.
В связи с большим числом послеоперационных осложнений резекцию желудка по Бильрот-ІІ при язвенном гастродуоденальном кровотечении применять не рекомендуется.
Показанием к выполнению раннего планового оперативного вмешательства (т.е. после проведения полноценного обследования и необходимой предоперационной подготовки) является осложненное течение язвенной болезни:
— повторные (неоднократные) кровотечения;
— малигнизация язвы (по данным биопсии);
— пенетрация язвы;
— гигантские язвы желудка (более 3 см в диаметре) и двенадцатиперстной кишки (2 см и более в диаметре);
— стеноз выхода из желудка.
У пациентов с сопутствующей патологией в стадии декомпенсации необходимо ограничиться применением всего комплекса консервативной терапии в связи с непереносимостью даже минимальной операции.
Рецидивные (пептические) язвы анастомоза
Основным методом лечения является консервативный, который включает:
— эндоскопические гемостаз и профилактику рецидива кровотечения;
— подавление желудочной секреции;
— коррекцию кровопотери (инфузионную и медикаментозную терапию);
— системную гемостатическую терапию.
При неэффективности всего комплекса консервативных мероприятий показано выполнение экстренного хирургического вмешательства.
При пептической язве гастроэнтероанастомоза операцией выбора является резекция желудка по Бильрот-I (с предварительной мобилизацией двенадцатиперстной кишки по Кохеру) или резекция желудка по Ру; при сочетании пептической язвы с демпинг-синдромом — реконструктивная гастроеюнопластика по Захарову — Henley или комбинированная еюногастропластика.
При пептической язве гастродуоденоанастомоза также возможно выполнение резекции желудка по Бильрот-I (с предварительной мобилизацией двенадцатиперстной кишки по Кохеру) или резекции желудка по Ру в сочетании с селективной ваготомией.
При рецидиве язвенной болезни после селективной проксимальной, стволовой или селективной ваготомии с иссечением язвы предпочтение следует отдавать селективной или стволовой ваготомии в сочетании с антрумэктомией или резекции желудка по Бильрот-I.
При рецидиве язвы после ее иссечения без ваготомии можно выполнить селективную или стволовую ваготомию с антрумэктомией или резекцию желудка по Бильрот-I.
Лишь у больных, находящихся в крайне тяжелом состоянии, целесообразно выполнение минимального по объему хирургического вмешательства — иссечения язвы. В данном случае основной задачей операции является остановка кровотечения и спасение жизни больному.
У остальных больных вопрос о необходимости выполнения оперативного вмешательства решается в плановом порядке.
Кровоточащие острые язвы и эрозии пищеварительного канала
Основой лечения является комплексная консервативная терапия, которая включает:
— эндоскопический гемостаз и профилактику рецидива кровотечения — при острых язвах. При этом контрольно-лечебные эндоскопические исследования выполняют каждые 12 часов до исчезновения признаков ненадежного гемостаза; при наличии сгустка крови, прикрывающего разрыв слизистой оболочки, эндоскопические исследования выполняют каждые 6 часов;
— подавление желудочной секреции;
— коррекцию кровопотери (инфузионную и медикаментозную терапию);
— системную гемостатическую терапию;
— обязательное лечение основного и сопутствующих заболеваний!
При множественных острых эрозиях следует добиваться окончательного гемостаза только консервативными мероприятиями:
— подавлением желудочной секреции;
— коррекцией кровопотери (инфузионная и медикаментозная терапия);
— системной гемостатической терапией;
— обязательным лечением основного и сопутствующих заболеваний.
При отсутствии эффекта от комплексного лечения у больных с кровоточащими острыми язвами показано экстренное хирургическое вмешательство. Операцией выбора является иссечение острой язвы.
Профилактика образования острых язв и эрозий слизистой оболочки органов пищеварительного канала является чрезвычайно важной задачей.
У больных, перенесших достаточно травматичные оперативные вмешательства, с тяжелыми травмами, ожогами, на фоне тяжелых соматических (в т.ч. хирургических) заболеваний, которые сопровождаются сердечно-сосудистой, дыхательной, печеночной, почечной недостаточностью, дегидратацией, гиповолемией, интоксикацией, а также на фоне запущенных стадий злокачественных новообразований, некоторых инфекционных заболеваний в комплекс лечебных мероприятий обязательно должны быть включены препараты, снижающие желудочную секрецию.
Аналогичный подход должен быть использован и при необходимости применения, особенно длительного, препаратов, обладающих ульцерогенным действием (ацетилсалициловая кислота, стероидные гормоны, НПВС и др.).
Кровотечение, обусловленное синдромом портальной гипертензии
Следует помнить о том, что у больных с синдромом портальной гипертензии источником кровотечения могут быть не только варикозно расширенные вены, но и острые или хронические язвы желудка и двенадцатиперстной кишки, эрозии слизистой оболочки, чаще желудка, синдром Маллори — Вейсса и др.
Тактика лечения пациентов с синдромом портальной гипертензии во многом зависит от функционального резерва печени, который оценивают в соответствии с критериями Child-Pugh (1964–1972). Эти критерии позволяют дать приблизительную оценку операционного риска (табл. 7).
Класс А (низкого риска, сумма баллов не превышает 6) имеет субнормальные показатели, т.е. больные, входящие в эту группу, имеют компенсированное течение цирроза печени; класс В — у больных отмечается субкомпенсированное течение цирроза печени (сумма баллов от 7 до 9); класс С — у больных имеется декомпенсация заболевания (крайне высокого риска, сумма баллов 10–15 и более).
У последней категории больных отмечаются выраженные нарушения 3 и более параметров. Кроме того, к группе С относят больных, имеющих два показателя, оцененных в 3 балла, или характеризующихся одним из следующих признаков: альбумин менее 28 г/л, билирубин более 68 мкмоль/л, протромбиновый индекс менее 50 %.
Основными направлениями консервативного и малотравматичного лечения острого кровотечения из варикозно расширенных вен пищевода и желудка являются:
— снижение давления в системе воротной вены, что предотвращает возникновение повторного гипертонического криза и тем самым снижает вероятность возникновения рецидива кровотечения, а также способствует созданию более благоприятных условий для образования тромба в поврежденной вене: октреотид — 50 мкг в/в струйно в 10 мл физиологического раствора, а затем по 25–50 мкг/ч в виде длительных инфузий на протяжении 3–5 дней (1 мл 0,01% р-ра — 100 мкг растворяют в физиологическом растворе и вводят в течение 2–4 часов, что обеспечивает необходимую скорость инфузии 50–25 мкг/ч);
— подавление желудочной секреции;
— корригирующая терапия острой кровопотери;
— профилактика и лечение печеночной недостаточности;
— применение зонда-обтуратора Блейкмора;
— системная гемостатическая терапия;
— эндоскопические методы гемостаза.
Хирургическое лечение
Методы хирургического лечения кровотечений из варикозно расширенных вен пищевода и желудка можно условно разделить на две группы:
— шунтирующие операции, которые обеспечивают сброс портальной крови в систему нижней полой вены (условно-радикальные операции): неселективное портосистемное шунтирование (портокавальный, центральный спленоренальный, мезентерикокавальный, калиброванный портокавальный анастомозы) и селективное портосистемное шунтирование (дистальный спленоренальный анастомоз);
— операции, предусматривающие разъединение вен пищевода и желудка (паллиативные операции).
Рентгенэндоваскулярные методы лечения: трансюгулярное внутрипеченочное портосистемное шунтирование (TIPS) — как правило, применяется как этап подготовки больного к трансплантации печени.
В настоящее время спленэктомия как самостоятельная операция практически не применяется.
Решающее значение в выборе метода хирургического вмешательства имеет состояние регионарной гемодинамики, т.е. портопеченочной циркуляции.
Выбор способа и объема операции. Сосудистые анастомозы показаны больным циррозом печени класса А по Child-Pugh с удовлетворительными параметрами центральной и печеночной гемодинамики, а также с нормальными значениями маркеров цитолиза.
Прямые вмешательства на варикозно расширенных венах показаны больным циррозом печени класса В.
У больных циррозом печени класса С целесообразно применять весь комплекс консервативной терапии в связи с бесперспективностью применения любых хирургических вмешательств.
На высоте гастроэзофагеального кровотечения при отсутствии данных комплексного обследования больного и неэффективности консервативной терапии операцией выбора является перевязка вен пищевода и желудка, а также циркулярное прошивание кардии.
Противопоказаниями к операции являются тяжелая печеночно-почечная недостаточность и коматозное состояние больного.
Синдром Маллори — Вейсса
Лечение абсолютного большинства больных с синдромом Маллори — Вейсса — консервативное:
— эндоскопический гемостаз и профилактика рецидива кровотечения. При этом контрольно-лечебные эндоскопические исследования выполняются каждые 12 часов до исчезновения признаков ненадежного гемостаза; при наличии сгустка крови, прикрывающего разрыв слизистой оболочки, эндоскопические исследования выполняют каждые 6 часов;
— подавление желудочной секреции;
— коррекция кровопотери (инфузионная и медикаментозная терапия);
— системная гемостатическая терапия;
— коррекция основной и сопутствующей патологии.
Лишь в исключительных случаях, при неэффективности всего комплекса консервативного лечения, показано выполнение экстренного хирургического вмешательства.
Операцией выбора является высокая гастротомия, экономное иссечение краев разрыва с последующим сшиванием образовавшегося дефекта слизистой оболочки, альтернативой может служить прошивание кровоточащих сосудов трещины, а также прошивание их через серозную оболочку органа под контролем введенного в желудок эндоскопа.
Острокровоточащие опухоли пищеварительного канала
Среди всех острокровоточащих злокачественных опухолей пищеварительного канала наиболее часто встречается рак желудка (у 79 % больных), реже — рак ободочной и прямой кишок (у 18,5 %) и очень редко — злокачественные новообразования пищевода (у 1,5 %), тонкой кишки (у 1 %).
Доброкачественные опухоли чаще всего локализуются в желудке и в прямой кишке (у 81 % больных), реже — в ободочной кишке (у 11 %), тонкой кишке (у 7 %) и очень редко — в пищеводе (у 1 %).
Из общего числа больных в верхних отделах пищеварительного канала — в пищеводе, желудке и в двенадцатиперстной кишке острокровоточащие новообразования располагаются у 74 % больных, в толстой кишке — у 25 %, а в тощей и подвздошной кишке — у 1 %.
В связи с этим основным методом диагностики является экстренное эндоскопическое исследование.
В 82 % наблюдений источником кровотечения является злокачественная опухоль и лишь у 18 % — доброкачественная.
По гистологической структуре злокачественных опухолей наиболее часто наблюдается рак — у 97,5 % больных, саркома — у 2,5 %.
Среди доброкачественных новообразований чаще встречаются полипы (у 70 % больных). Ворсинчатая опухоль толстой кишки наблюдается у 17 % больных, лейомиома — у 11 % больных, а ангиофиброма, невринома и др. — у 2 %.
Комплексное консервативное лечение кровоточащих опухолей пищевода, желудка и двенадцатиперстной кишки включает:
— применение эндоскопических методик гемостаза и профилактики рецидива кровотечения. При этом контрольно-лечебные эндоскопические исследования выполняют каждые 12 часов до исчезновения признаков ненадежного гемостаза; при наличии сгустка крови, прикрывающего разрыв слизистой оболочки, эндоскопические исследования выполняют каждые 6 часов;
— полноценную коррекцию кровопотери и других нарушений гомеостаза;
— системную гемостатическую терапию;
— применение октреотида в дозе до 50 мкг в/в струйно в 10 мл физиологического раствора, а затем по 25–50 мкг/ч в виде длительных инфузий на протяжении 3–5 дней (1 мл 0,01% р-ра — 100 мкг растворяют в физиологическом растворе и вводят в течение 2–4 ч, что обеспечивает необходимую скорость инфузии 50–25 мкг/ч);
— применение препаратов обволакивающего действия.
Комплексное консервативное лечение кровоточащих опухолей тощей, подвздошной и толстой кишок включает:
— полноценную коррекцию кровопотери и других нарушений гомеостаза;
— системную гемостатическую терапию;
— применение октреотида в дозе до 50 мкг в/в струйно в 10 мл физиологического раствора, а затем по 25–50 мкг/ч в виде длительных инфузий на протяжении 3–5 дней (1 мл 0,01% р-ра — 100 мкг растворяют в физиологическом растворе и вводят в течение 2–4 ч, что обеспечивает необходимую скорость инфузии 50–25 мкг/ч).
Показаниями к экстренному оперативному вмешательству являются:
— профузное кровотечение, не поддающееся эндоскопической остановке;
— длительно (36 часов и более) сохраняющийся высокий риск развития рецидива кровотечения (при лечебно-контрольных эндоскопиях сохраняется диффузная обильная кровоточивость опухоли, крупные тромбированные сосуды на поверхности опухоли, сгустки крови на поверхности опухоли, неизмененная кровь в полости органа);
— подозрение на опухоль тонкой кишки и клинические признаки продолжающегося кровотечения.
Всем остальным пациентам хирургическое вмешательство выполняется после остановки кровотечения, всестороннего обследования и проведения полноценной предоперационной подготовки. Исключение составляют пациенты, у которых операционный риск достигает крайней степени.
Выбор способа и объема хирургического вмешательства зависит от локализации и распространенности опухоли. Операция во всех случаях должна выполняться в соответствии с онкологическими принципами радикальности.
Радикальные операции при раке желудка:
— при локализации опухоли дистальнее угла желудка — субтотальная резекция желудка;
— при локализации опухоли проксимальнее угла желудка — гастрэктомия.
Радикальные операции при раке тощей и подвздошной кишок:
— резекция тонкой кишки, отступя от края опухоли не менее 10 см вместе с удалением соответствующего сегмента брыжейки с расположенными в ней лимфатическими узлами. При локализации опухоли в дистальных сегментах подвздошной кишки (в пределах участка в 60 см от илеоцекального угла) особенности кровоснабжения и метастазирования требуют вместе с резекцией кишки выполнения правосторонней гемиколэктомии с наложением илеотрансверзоанастомоза.
Радикальные операции при раке ободочной кишки:
— при раке слепой и восходящей ободочной кишки — правосторонняя гемиколэктомия с резекцией 25–30 см тонкой кишки, перевязкой и пересечением подвздошно-ободочной и правой ободочной артерий, а также пересечением правой ветви средней ободочно-кишечной артерии у места ее деления;
— при раке печеночного изгиба — расширенная правосторонняя гемиколэктомия с перевязкой и пересечением у основания подвздошно-ободочной, правой ободочной и средней ободочной артерий; объем резекции включает: 25–30 см подвздошной кишки, слепую, восходящую, печеночный изгиб и проксимальные 2/3 поперечной ободочной кишки;
— при раке средней части поперечной ободочной кишки — субтотальная колэктомия с перевязкой правой, средней и левой ободочной артерий; при тяжелом состоянии больного — сегментарная резекция поперечной ободочной кишки;
— при раке левого изгиба ободочной кишки удаляются дистальные 2/3 поперечной ободочной кишки, нисходящая и проксимальная часть сигмы с перевязкой основного ствола средней ободочной артерии и ее правой ветви, отступя 4–5 см от развилки сосуда и левой ободочной артерии и ее нисходящей ветви в месте формирования краевого сосуда;
— при раке нисходящей ободочной и сигмовидной кишки — левосторонняя гемиколэктомия с обязательной перевязкой и пересечением нижней брыжеечной артерии у ее основания;
— при раке средней трети сигмовидной кишки — удаление всей сигмовидной кишки;
— при раке нижней трети сигмовидной кишки — резекция сигмовидной кишки (сохраняется лишь верхняя треть сигмовидной кишки) с пересечением нижней брыжеечной артерии у места ее отхождения от аорты, перевязкой верхней прямокишечной артерии, удалением корня брыжейки сигмовидной кишки.
Паллиативные операции. При наличии отдаленных метастазов и операбельности опухоли целесообразно выполнить удаление опухоли (резекция желудка, резекция кишечника и т.д.).
Если во время неотложной операции выявлена неудалимая опухоль желудка, то единственным способом достижения гемостаза следует считать деваскуляризацию опухоли путем перевязки питающих ее сосудов.
Выбор способа и объема хирургического вмешательства при доброкачественных опухолях
При доброкачественных неэпителиальных опухолях (лейомиома и др.) возможно выполнение экономного иссечения участка стенки органа, несущего опухоль, или резекции части органа вместе с опухолью (резекция желудка, резекция кишки и т.д.).
Операцией выбора при кровоточащих полипах является эндоскопическая полипэктомия, выполнение которой возможно при первичной эндоскопии. Полостное вмешательство предпринимается лишь в тех случаях, когда эндоскопическое удаление их невозможно.
Редкие причины острого кровотечения в просвет органов пищеварительного канала
Причины и локализация редких причин ОКПОПК представлены в таблице 8 (литературные и собственные данные).
Все редкие причины острого кровотечения в просвет органов пищеварительного канала можно разделить на несколько основных групп:
— патология органов пищеварительной системы — пищевода, желудка, тонкой и толстой кишок, печени и поджелудочной железы (в т.ч. последствия травм, перенесенных оперативных вмешательств, медикаментозного лечения и др.);
— болезни системы крови;
— врожденные (наследственные) и приобретенные ангиодисплазии;
— заболевания соединительной ткани, обмена веществ и лимфатической системы;
— инфекционные и паразитарные заболевания.
Среди редких причин ОКПОПК чаще других кровотечение наблюдается при дивертикулах пищеварительного канала, неспецифических колитах, заболеваниях крови и сосудов, ожогах, пептической язве пищевода, грыже пищеводного отверстия диафрагмы. Остальные причины острого кровотечения в просвет пищеварительного канала встречаются крайне редко.
В диагностике этих заболеваний ведущая роль принадлежит правильно собранному анамнезу, а также данным объективного, инструментального (эндоскопическое, рентгенологическое, ультразвуковое исследование и др.) и лабораторного (клиническое, биохимическое, бактериологическое исследование и др.) обследования.
Лечение редких причин острого кровотечения в просвет пищеварительного канала, как правило, консервативное. Необходимость выполнения экстренного хирургического вмешательства возникает крайне редко.
При локализации источника кровотечения в пищеводе, желудке и двенадцатиперстной кишке основными принципами лечения являются:
— применение эндоскопических методик гемостаза и профилактики рецидива кровотечения. При этом контрольно-лечебные эндоскопические исследования выполняют каждые 12 часов до исчезновения признаков ненадежного гемостаза; при наличии сгустка крови, прикрывающего разрыв слизистой оболочки, эндоскопические исследования выполняют каждые 6 часов;
— полноценная коррекция кровопотери и других нарушений гомеостаза;
— подавление желудочной секреции;
— системная гемостатическая терапия;
— применение октреотида в дозе до 50 мкг в/в струйно в 10 мл физиологического раствора, а затем по 25–50 мкг/ч в виде длительных инфузий на протяжении 3–5 дней (1 мл 0,01% р-ра — 100 мкг растворяют в физиологическом растворе и вводят в течение 2–4 ч, что обеспечивает необходимую скорость инфузии 50–25 мкг/ч);
— лечение основного и сопутствующих заболеваний.
При локализации источника кровотечения в тощей, подвздошной и толстой кишке основными принципами лечения являются:
— полноценная коррекция кровопотери и других нарушений гомеостаза;
— системная гемостатическая терапия;
— применение октреотида в дозе до 50 мкг в/в струйно в 10 мл физиологического раствора, а затем по 25–50 мкг/ч в виде длительных инфузий на протяжении 3–5 дней (1 мл 0,01% р-ра — 100 мкг растворяют в физиологическом растворе и вводят в течение 2–4 ч, что обеспечивает необходимую скорость инфузии 50–25 мкг/ч);
— лечение основного и сопутствующих заболеваний.
Показанием к экстренному оперативному вмешательству является профузное кровотечение, не поддающееся полноценной консервативной терапии.
Заключение
Анализируя 35-летний опыт лечения больных с ОКПОПК, мы пришли к следующим выводам. Одним из важных направлений, с нашей точки зрения, является уменьшение числа больных с кровотечением. Поскольку у 95–96 % больных оно возникает на фоне таких распространенных заболеваний, как язвенная болезнь, опухоли пищеварительного канала, цирроз печени, заболевания сердца, легких, сосудов (острые язвы и эрозии слизистой оболочки) и др., большое значение приобретает их своевременная диагностика, а также адекватное плановое консервативное или оперативное лечение.
Это позволит, в свою очередь, значительно уменьшить количество осложнений форм заболеваний и, следовательно, улучшить качественные показатели лечения больных с кровотечением. Особенно это касается пациентов пожилого и старческого возраста, а также с тяжелой основной или сопутствующей патологией. Однако эта задача в первую очередь должна решаться на уровне первичного звена оказания медицинской помощи населению, т.е. в условиях центров первичной медико-санитарной помощи — семейными врачами.
Известно, что ОКПОПК может осложнять течение более 180 заболеваний. Поэтому очень важной задачей является, прежде всего, знание возможных причин ОКПОПК, а также использование всего комплекса клинико-лабораторных и инструментальных методов диагностики.
Лишь своевременно и правильно установленный диагноз в большей степени гарантирует назначение патогенетически обоснованной терапии и позволяет прогнозировать большее число благоприятных исходов лечения. Не менее важным является применение всего комплекса современных методов как консервативного, так и оперативного, в т.ч. эндоскопического, лечения больных.
Наконец, большое значение имеет дальнейшее улучшение организации помощи пациентам с ОКПОПК. В общем, это справедливо для всех хирургических патологий, как экстренных, так и плановых. Выход в одном — в создании крупных хирургических центров как в больших городах, так и межрайонных. Вместе с тем эти центры должны иметь в своем составе все необходимые вспомогательные подразделения для оказания качественной помощи пациентам, оснащенные современным диагностическим и лечебным оборудованием, обеспеченные необходимыми медикаментами, инфузионными средами и обязательно — качественным шовным материалом.
Лишь выполнение перечисленных основных условий позволит улучшить качество оказания помощи больным с ОКПОПК. В противном случае поставленная задача останется лишь добрым пожеланием.
Таким образом, проблема лечения пациентов с ОКПОПК весьма далека от своего окончательного разрешения, что диктует необходимость дальнейших активных научных изысканий в этом направлении.
/84.jpg)
/86.jpg)

/85.jpg)
/87.jpg)
/88.jpg)
/90.jpg)
/92.jpg)
/94.jpg)
/98.jpg)