Газета «Новости медицины и фармации» 4 (567) 2016
Вернуться к номеру
Медичні новини Medscape. Новини конференції
Разделы: Справочник специалиста
Версия для печати
Статья опубликована на с. 18 (Мир)
Великі дослідження стали розчаруванням на Тижні нирки
Пем Гаррісон, 11 листопада 2015
Перше дослідження було спрямоване на оцінку застосування високих доз аторвастатину для захисту нирок пацієнтів, яким проводиться хірургічне втручання на серці.
Друге дослідження, SIRS, присвячене стероїдам в кардіохірургії, оцінювало вплив метилпреднізолону на гостре ушкодження нирок у хворих, які перенесли операцію в умовах штучного кровообігу.
Третє дослідження, FAVOURED, оцінювало роль омега-3 жирних кислот та аспірину щодо наслідків судинних втручань у хворих із захворюваннями нирок.
Статини не захищають нирки
У своєму дослідженні Фредерік Біллінгс, д.м.н. з Університету Вандербільта в Нешвіллі, штат Теннессі, і його колеги відстежували гостре ушкодження нирок у 820 хворих, які перенесли операцію, їх рандомізували на тих, які отримували високу дозу аторвастатину, і тих, які отримували плацебо.
Автори припустили, що дія механізмів, які призводять до ГУН, буде нівельована, якщо пацієнтам, які не приймали статини, призначити високу дозу аторвастатину за добу до операції і продовжити його прийом до виписки зі стаціонару, а пацієнтам, які вживають статини, призначити високу дозу аторвастатину в день операції і продовжувати його прийом до виписки зі стаціонару.
Проте гіпотеза не підтвердилась; не було ніякої різниці у показниках пошкодження нирки між групами аторвастатину й плацебо (20,8 проти 19,5 % відповідно; Р = 0,75)
У пацієнтів із ХХН, які раніше не приймали статини, цифри були невеликі. Однак масштаби негативного ефекту високих доз аторвастатину щодо пошкодженні нирок були вражаючими, сказав доктор Біллінгс, і це підвищило ризик ушкодження нирок.
У статин-наївних пацієнтів без захворювань нирок різниця в пошкодженні нирок була незначна, «але це було клінічно важливим; 8 % різниці у гострому пошкодженні нирок є клінічно значущими», пояснив доктор Біллінгс.
Стероїди не захищають нирки
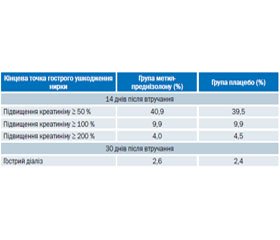
У дослідженні SIRS проведена оцінка впливу метилпреднізолону на гостре ушкодження нирок у 7286 пацієнтів, які перенесли операцію в умовах штучного кровообігу (Lancet. 2015; 386: 1243-1253).
Пацієнти були рандомізовані для внутрішньовенного введення метилпреднізолону (250 мг на початку анестезії і ще 250 мг на початку штучного кровообігу) та групу плацебо.
«В умовах штучного кровообігу виникає системна запальна реакція, яка активує комплемент, запальні цитокіни та інші медіатори запалення. Це, у свою чергу, збільшує проникність ендотелію, посилює пошкодження органа, захворюваність і смертність, включаючи гостре пошкодження нирок, — сказав дослідник Аміт Гарг, доктор медицини з лондонського центру медичних наук в Онтаріо, Канада. — Ми були зацікавлені в кортикостероїдах, оскільки вони пригнічують цю запальну відповідь».
Утім ніякої різниці між групами метилпреднізолону і плацебо не виявлено.
«Не було виявлено ніякої користі стероїдів у тих, хто мав або не мав хронічну хворобу нирок до операції», — повідомив доктор Гарг.
Через профіль несприятливих ефектів доз стероїдів, що використовувались в цьому дослідженні, дослідники створили рекомендацію 1-го рівня про невикористання цих препаратів за даних обставин.
Риб’ячий жир не покращує судинний доступ при хворобах нирок
Для пацієнтів, які перебувають на гемодіалізі, «артеріовенозна фістула вважається оптимальним вибором для судинного доступу», сказав дослідник Ешлі Айріш, MD, з госпіталю Фіони Стенлі в Перті, Австралія. «Але вони є найважчими у догляді, тому що артеріовенозні фістули мають дуже високі показники тромбозу і вони часто не досягають «зрілості», тому насправді ви не можете їх використовувати».
У дослідженні FAVOURED, відомому як «Вплив омега-3 жирних кислот (риб’ячий жир) та аспірину на формування судинного доступу при хвороби нирок», вчені припустили, що плейотропний вплив риб’ячого жиру на запалення та функції тромбоцитів може допомогти покращити цю ситуацію.
567 пацієнтів з 4-ю або 5-ю стадією хронічної хвороби нирок були рандомізовані для призначення на 3 місяці високоякісного риб’ячого жиру 4 г на день або плацебо і спостерігалися протягом 12 місяців. Підгрупа пацієнтів також отримувала щоденно 100 мг аспірину або плацебо.
Кінцевою точкою служило поєднання тромбозу артеріовенозної фістули, непрохідність артеріовенозної фістули і ненадійність пункційного доступу артеріовенозної фістули.
«Майже половина всіх пацієнтів в дослідженні не мала придатної для використання артеріовенозної фістули через 12 місяців після операції», — повідомив доктор Айріш.
У підгрупі пацієнтів, рандомізованих за прийомом аспірину, показник неспроможності артеріовенозної фістули був схожий на результати групи риб’ячого жиру та плацебо (45 проти 43 %).
«Не важливо, ти старий чи молодий, мав захворювання судин, діабет або ні, — сказав доктор Айріш. — Риб’ячий жир не допоміг, як і аспірин».
Цільові показники артеріального тиску можуть бути незалежними від альбумінурії
Пем Гаррісон
У пацієнтів з помірною та тяжкою стадіями хронічної хвороби нирок (ХХН) підвищений систолічний артеріальний тиск пов’язаний зі стрімким зниженням функції нирок незалежно від наявності або відсутності альбумінурії, вважають автори нового дослідження.
У дослідженні було задіяно дані пацієнтів із ХХН, включених у дослідження, присвячене захисту серця і нирок (SHARP). Дослідження встановило, що ризик інфаркту міокарда або інсульту в пацієнтів із ХХН був знижений, коли призначали статини для зменшення рівня холестерину ліпопротеїнів низької щільності.
На початку дослідження 20 % з 6000 пацієнтів мали ШКФ нижче за 15 мл/хв/1,73 м2, 40 % — від 15 до 30 мл/хв/1,73 м2, 40 % — від 30 до 60 мл/хв/1,73 м2.
Перед оцінкою наявності альбумінурії спостерігалось 32% збільшення ризику термінальної стадії хвороби нирок на кожні 10 мм рт.ст. підвищення систолічного артеріального тиску (відношення ризиків (ВР) — 1,32; 95% довірчий інтервал (ДІ) — 1,23–1,41).
Після поправки на наявність альбумінурії ризик знизився до 10 %, хоча й залишався значним (ВР 1,1; 95% ДІ 1,03–1,18).
Для пацієнтів з високим рівнем альбумінурії кожні 20 мм рт.ст. підвищення систолічного артеріального тиску були пов’язані із середнім зниженням ШКФ до 0,7 мл/хв/1,73 м2 на рік.
У пацієнтів з низьким рівнем альбумінурії, а також в осіб з невиявленою альбумінурією щорічне зниження ШКФ було подібним — по 0,6 мл/хв/1,73 м2.
Призначення введення рідини з огляду на рівень центрального венозного тиску запобігає контраст-індукованій нефропатії
Will Boggs, MD. January 07, 2016.
New York (Reuters Health). — http://bit.ly/1OatHoA and http://bit.ly/1RrHbAM / J. Am. Coll. Cardiol. Intv. 2015.
Моніторинг центрального венозного тиску (ЦВТ) дозволяє зробити призначення рідини безпечним і достатнім для профілактики контраст-індукованої нефропатії (КІН) у пацієнтів із хронічними захворюваннями нирок і застійною серцевою недостатністю, повідомили дослідники з Китаю.
Частота КІН становить понад 20 % у хворих з хронічною хворобою нирок (ХХН), ускладненою хронічною серцевою недостатністю (ХСН). Пацієнти із значним ризиком розвитку КІН повинні отримувати адекватну гідратацію до і після введення контрасту, зазначає команда в JACC: серцево-судинні втручання, онлайн 9 грудня.
Доктор Чень Ген і його колеги з Генерального госпіталю Китайської народно-визвольної армії в Пекіні порівняли введення рідини з моніторингом ЦВТ і без нього для профілактики КІН у рандомізованному дослідженні у 264 пацієнтів із ХХН і ХСН.
ЦВТ-керована група отримала значно вищі середні сумарні об’єми фізіологічного розчину (1827 мл), ніж стандартна група (1202 мл), і мала більший об’єм діурезу (1461 проти 806 мл).
Загальна частота розвитку КІН становила 22,7 %, але вона був значно нижчою при ЦВТ-керованій гідратації, ніж у стандартній групі (15,9 проти 29,5 %, р = 0,006).
Число пацієнтів з ростом креатиніну сироватки вище за 0,3 мг/дл і > 50 % від вихідного рівня було істотно нижчим у ЦВТ-контрольованій групі (19,7 і 3,79 % відповідно), ніж у контрольній групі (34,8 і 9,85 %).
Пацієнти з фракцією викиду лівого шлуночка нижче від 40 % і ті, які мають низький рівень ЦВТ, матимуть користь від ЦВТ-контрольованої гідратації.
Відсоток припинення гідратації внаслідок гострого набряку легенів був низьким і подібним в обох групах.
Пацієнти в групі ЦВТ-контрольованої гідратації мали вірогідно більш низькі показники інфаркту міокарда, нирково-замісної терапії та основних небажаних кумулятивних подій у наступні 90 днів порівняно з контрольною групою.
Як і очікувалося, пацієнти, у яких розвинулась КІН, мали більш високі показники основних небажаних подій і смертності від усіх причин, ніж ті, в кого не розвинулась КІН.
Моніторинг протеїнурії у пацієнтів з цукровим діабетом 2-го типу
Liang H., Kennedy С., Manne S., Hsiang-Ling Lin J., Dolin P. //BMJ Open Diabetes Res. Care. 2015; 3(1)
Мета. Керівництво з діабету Національного інституту охорони здоров’я та якості медичних послуг (NICE) Великобританії рекомендує як мінімум щорічний моніторинг пацієнтів із цукровим діабетом 2-го типу (ЦД2) з приводу протеїнурії. До цього часу мало публікацій щодо частоти моніторингу протеїнурії при ЦД2 і його зв’язку з факторами ризику ниркових ускладнень. Ми прагнули описати моніторинг протеїнурії в пацієнтів із ЦД2.
Дизайн. У цьому дослідженні у базі клінічних практичних досліджень Великобританії були обрані пацієнти з ЦД2 віком 40 років і старше з початком антидіабетичної терапії у 2007–2012 рр. (запис до когорти). Вимогою був щонайменше 1 рік спостереження до та після запису в когорту. Тест вважався таким, що відбувся, якщо медичний або лабораторний код вказував на дослідження рівня альбуміну або білка в сечі. Відсоток пацієнтів з як мінімум одним виконаним дослідженням був обчислений через 1 рік після входження в когорту та протягом подальшого спостереження. Модель пропорційних ризиків Кокса була використана для оцінки відсотків ризиків пацієнтів, які мають перший скринінг, для регулювання вихідних коваріат.
Результати. Було включено 65 790 пацієнтів (середній вік 63 роки, чоловіки — 57,5 %, середня тривалість спостереження 41 місяць), з яких 49 707 (75,6 %) пацієнтів мали принаймні один тест на рік після початку антидіабетичної терапії і 59 400 (90,3 %) мали принаймні один тест у будь-який час протягом наступного спостереження. З часом, з початком антидіабетичної терапії та після ряду змін в лікуванні, моніторинг протеїнурії знизився і був незалежно пов’язаний з віком, статтю, курінням і часом початку антидіабетичної терапії. 12,3 % протестованих пацієнтів з ЦД2 мали позитивний результат на протеїнурію на час першого скринінгу через 1 рік після початку антидіабетичної терпаії.
Висновки. Отримані висновки мали субоптимальне узгодження з керівництвом NICE з моніторингу протеїнурії в пацієнтів з ЦД2 і з тим, що рівень моніторингу виявився залежним від множинних клінічних факторів.

/18_m.jpg)