Статья опубликована на с. 135-139
Дорсалгии — междисциплинарная проблема, так как они могут наблюдаться при неврологических, ортопедических, ревматологических, соматических и других заболеваниях. По происхождению выделяют вертеброгенную (спондилогенную) дорсалгию, связанную с патологией позвоночника, и невертеброгенную, которая вызвана растяжением связок и мышц, соматическими заболеваниями, психогенными факторами и др. [2].
Распространенность боли в нижней части спины и дорсалгий в Западной Европе и США достигает 40–80 %, хронические боли испытывает 10–20 % населения, при этом 5 % обращаются к врачам общей практики, а 1–2 % получают помощь в стационарах. Значимость синдрома обычно определяется не угрозой для жизни, а снижением ее качества у пациента и его семьи, экономической нагрузкой на общество и нередко отсутствием эффекта от традиционного лечения. Спондилогенная дорсалгия (СД) в 60–90 % случаев обусловлена дегенеративно-дистрофическими процессами в позвоночнике [2], а именно в позвонках, межпозвоночных суставах, дисках, связочном аппарате, лежащими в основе развития спондилеза, спондилоартроза и остеохондроза. Вертеброгенная (механическая) боль в пояснице является одной из наиболее распространенных жалоб пациентов, в Соединенных Штатах на нее приходится более 6 миллионов случаев в год. Примерно две трети взрослых страдают от механической боли в пояснице хотя бы раз в жизни, что является наиболее распространенной жалобой в амбулаторной медицине и стоит на третьем месте по финансовой составляющей после онкопатологии и сердечно-сосудистых заболеваний [9]. Боль в пояснице является одной из наиболее распространенных жалоб в учреждениях первичного звена медицинской помощи, но патогенез и представление о возникновении люмбалгии патофизиологически многогранны [2, 6, 9].
В структуру патогенеза дорсалгий включены возрастные изменения — остеохондроз, фасеточный синдром с наличием соответствующих биомеханических нарушений, первичные и рефлекторные миофасциальные синдромы, энтезопатии, радикулопатии, травмы и микротравмы в анамнезе. Даже незначительные травмы при декомпенсации межпозвоночного диска, фасеточных суставов могут выступить триггером развития клинической картины [7, 10]. Мы хотим обратить внимание на патогенез болей в спине не с позиции исключительно вертеброгенного фактора, а с учетом центральных механизмов формирования боли.
Основные категории вертеброгенной патологии в неврологической практике следующие.
Радикулопатии в классическом смысле развиваются вследствие патологической компрессии нервного корешка в межпозвоночном отверстии вследствие дегенеративных изменений, нестабильности и/или грыжей межпозвоночного диска. Также радикулопатии возникают вследствие спинального стеноза. Манифестируют болью, снижением и/или отсутствием рефлексов, чувствительными нарушениями. Дискогенные радикулопатии развиваются вследствие дегенерации межпозвоночного диска, которая отчетливо видна к третьей декаде жизни. Удельный вес диск-ассоциированной симптоматики, например, в США не превышает 3 % [5]. Излюбленная локализация межпозвоночных грыж — уровень L4-L5 и L5-S1 [6].
Фасеточный синдром имеет локальные и экстравертебральные симптомы, ведущие маркеры — боль и миофасциальные нарушения как саногенетическая реакция на блокирование поврежденного позвоночно-двигательного сегмента. Дугоотростчатые суставы являются истинными синовиальными суставами, с совместным пространством, гиалиновыми хрящевыми поверхностями, синовиальной жидкостью и фиброзной капсулой. Наличие ноцицептивных и вегетативных нервных волокон в различных тканевых структурах фасеточных суставов предполагает, что эти структуры могут вызывать боль при перегрузке и аномальной нагрузке. Вещество Р представляет собой хорошо известный воспалительный медиатор, который может повышать чувствительность ноцицепторов, что приводит к хронической боли. Простагландины, известные медиаторы воспаления, также высвобождаются из фасеточных суставов [7].
Синдром конского хвоста вызывается массивной медианной экструзией ядерного материала или ростом опухоли в позвоночный канал. Классически манифестирует двусторонним ишиасом или нижним парапарезом с нарушением функции тазовых органов (до 90 % пациентов). Вначале наблюдается задержка мочи с последующим недержанием. Чувствительные расстройства присутствуют в области промежности или перианальной области у 60–80 % больных [7, 8]. При синдроме конского хвоста возможно развитие комплексного регионарного болевого синдрома. Стеноз позвоночного канала — важнейшая неврологическая проблема, являющаяся триггером хронической шейной или поясничной боли. Нет четкой корреляции между симптомами стеноза и расой, профессией, полом, телосложением. Прогрессирующее сужение позвоночного канала может происходить само по себе или в сочетании с острой патологией межпозвоночного диска. Врожденный и/или приобретенный стеноз позвоночного канала является фактором риска возникновения очаговой неврологической симптоматики.
Миофасциальный болевой синдром в чистом виде рассматривается как декомпенсация порочного двигательного стереотипа с наличием триггерных участков в мышцах и нарушением их функции. Локализация болей не связана с зоной ответственности периферического нерва. Уменьшение боли наблюдается при релаксации мышцы.
Мышечно-скелетные боли (фибромиалгия) — одна из распространенных жалоб, предъявляемых пациентами. В 1972 году Смайт описал обобщенную боль и болезненность при пальпации в определенных точках, и спустя 4 года термин «фибромиалгия» был введен для определения синдрома заболевания. Этиология и патогенез фибромиалгии до сих пор неизвестны. Это заболевание с большой вероятностью имеет полиэтиологическую основу. Считается, что изменения в активности нейронов в центральной нервной системе, аномальный метаболизм биогенных аминов и иммунологических расстройств могут, среди прочего, способствовать развитию этого заболевания. Жалобы не характерны и очень субъективны, что существенно затрудняет определение различий между фибромиалгией и синдромом хронической усталости, психосоматических расстройств. Лечение фибромиалгии является сложным и долгосрочным. Антидепрессанты и психотерапия имеют жизненно важное значение. Эффективность локально используемых агентов также акцентируется. Фибромиалгия стала в последние годы серьезной социальной проблемой в развитых странах. Поэтому очень важно надлежащим образом диагностировать фибромиалгию и осуществить ее соответствующее лечение, которое устраняет симптомы заболевания в максимальной степени [12].
По продолжительности болевой синдром может быть острым, подострым и хроническим: острая боль длится до 6 нед., хроническая — свыше 12 нед. Нейрофизиологические реакции и патобиохимические изменения при хроническом болевом синдроме, в свою очередь, приводят к развитию патопсихологических изменений в головном мозге. К таким проявлениям относятся существенные изменения психики, в частности возникновение устойчивости боли к действию лекарственных средств и терапевтических манипуляций, а также возможно развитие витальной депрессии.
Боль в состоянии полностью уничтожить человека как личность. Она причиняет невыносимые страдания пациенту и нередко деформирует его психику. Некупируемая физическая боль и психологические переживания приводят к отчаянию, ощущению бессилия перед обстоятельствами, чувству одиночества и ненужности обществу, зависимости от врачей и ближайшего окружения. Патопсихологические изменения при длительной и мучительной боли могут привести пациента в состояние суицидальной готовности.
При хронической вертеброгенной патологии клиницист имеет несколько зачастую взаимосвязанных проблем:
— локальная (фасеточные суставы с наличием дегенеративных и воспалительных изменений, энтезопатия мышц и связок), требующая длительного использования нестероидных противовоспалительных препаратов (НПВП), и как следствие — наличие рисков по гастроинтестинальным событиям;
— проблема хронической боли, нуждающаяся в длительном, если не постоянном применении антидепрессантов.
Согласно унифицированному клиническому, протоколу МЗ Украины № 311 от 25.04.2012 № 311 для контроля хронического болевого синдрома используются нестероидные противовоспалительные и противоревматические средства. Фармакотерапия при остеоартрозе основывается на использовании симптом-модифицирущих препаратов быстрого (анальгетики, НПВП, трамадол) и медленного действия (гиалуроновая кислота, диацереин, глюкозамин, хондроитина сульфат, соединение сои/авокадо) [1].
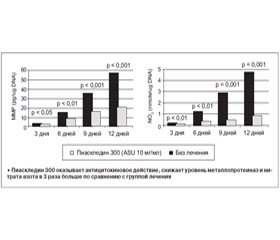
Новым для Украины структурно-модифицирующим препаратом, который входит как в европейские, так и в международные рекомендации по лечению ОА (EULAR, OARSI), является Пиаскледин 300 (ASU). В состав этого препарата входит комплекс неомыляемых фитостеролов, полученных методом молекулярной дистилляции из экстрактов масел авокадо и сои. Препарат выпускается только Laboratories Expanscience (Франция) и не имеет аналогов в мире. Одним из основных механизмов действия Пиаскледина 300 является его влияние на экспрессию цитокинов [1, 4]. Пиаскледин ингибирует ИЛ‑1, предотвращая его повреждающее действие на хондроциты и синовиоциты, стимулирует синтез коллагена и протеогликанов. Он угнетает ИЛ‑1β-cтимулированный синтез металлопротеазы (МП) (коллагеназы и стромелизина) хондроцитами, экспрессию ИЛ‑6 и ИЛ‑8, а также простагландина Е2, что обусловливает как антикатаболическое действие на матрикс хряща, так и ингибицию вторичного воспаления в тканях сустава, а именно: в синовиальной оболочке, энтезах, субхондральной кости и непосредственно в гиалиновом хряще (рис. 1).
/137_2.jpg)
Пиаскледин доказал свою эффективность в многочисленных европейских исследованиях. Выраженная эффективность и уменьшение потребности в НПВП были продемонстрированы в многоцентровом двойном плацебо-контролируемом исследовании, которое продолжалось в течение 3 месяцев у пациентов обоих полов в возрасте от 45 до 80 лет с остеоартрозом коленного сустава. Все параметры эффективности были значительно улучшены (р < 0,01) в обеих группах по сравнению с группой плацебо. Потребление анальгетиков и НПВП уменьшилось более чем на 50 % у 71 % пациентов, получавших 300 мг Пиаскледина или 600 мг, по сравнению с 36 % пациентов, получавших плацебо (табл. 1).
Эффективность Пиаскледина в дозе 300 и 600 мг/день была лучше, чем плацебо, на всех конечных точках, без каких-либо различий, наблюдаемых между двумя дозами. Пиаскледин показал симптоматическую эффективность по сравнению с плацебо в лечении остеоартроза, действуя от месяца до двух и показывая стойкий эффект после окончания лечения [5, 11].
Для контроля центральных механизмов хронической боли хорошо зарекомендовал себя мультимодальный антидепрессант тразодон (Триттико). Тразодон — это современная альтернатива амитриптилину в комплексном лечении пациентов с хроническим болевым синдромом.
Коллегией Всемирного конгресса по нейропсихофармакологии (Канада, Монреаль, 2002 г.) тразодон (Триттико) определен как атипичный антидепрессант с преимущественным седативным и анксиолитическим действием, первый и единственный представитель антагонистов рецепторов к серотонину 2-го типа и ингибиторов обратного захвата серотонина (SARI) в Украине. По своим фармакологическим показателям тразодон относится к группе антагонистов серотониновых рецепторов (5НТ) и селективных ингибиторов обратного захвата серотонина (СИОЗС). Из всех свойственных ему видов лекарственного воздействия блокада серотониновых рецепторов выражена сильнее по сравнению с угнетением обратного захвата серотонина. Тразодон (Триттико) действует как антагонист на серотониновые рецепторы 2А-подтипа и как частичный агонист 5НТ1а-рецепторов (рис. 2).
/138.jpg)
Это обусловливает его широкое применение при лечении депрессии, нарушений сна, при тревоге, сексуальных дисфункциях. Высокая эффективность тразодона (Триттико) определена при лечении фибромиалгии [3, 12] (рис. 3).
В онкологической практике у пациентов с выраженным болевым синдромом тразодон при сопоставимой эффективности превосходил по переносимости амитриптилин. Таким образом, тразодон (Триттико) модулирует восприятие соматической боли на уровне ЦНС и позволяет эффективно воздействовать на психологические компоненты болевого синдрома, включая депрессию и тревогу.
Список литературы
1. Денисюк В.И., Денисюк Е.В. Остеоартроз: стандарты диагностики и лечения согласно результатам доказательной медицины. http://www.umj.com.ua/article/10897/osteoartroz-standarti-diagnostiki-ta-likuvannya-za-rezultatami-dokazovoi-medicini
2. Иванова М.Ф., Евтушенко С.К. Дорсалгия, обусловленная дегенеративно-дистрофической патологией позвоночника // Новости медицины и фармации. — 2010. — 15 (335).
3. Чистик Т. Роль антидепрессантов в лечении хронического болевого синдрома // Новости медицины и фармации. Неврология. — 2012. — 420 (тематический номер).
4. Яременко О.Б. Нехирургическое лечение остеоартроза: тенденции последних лет // Новости медицины и фармации. Кардиология. — 2014. — 512 (тематический номер).
5. Appelboom T., Schuermans J., Verbruggen G., Henrotin Y., Reginster J.Y. Symptoms modifying effect of avocado/soybean unsaponifiables (ASU) in knee osteoarthritis. A double blind, prospective, placebo-controlled study // Scand. J. Rheumatol. — 2001. — 30 (4). — 242-7.
6. Carl H. Shin, MD; Chief Editor: Stephen Kishner. Lumbar Facet Arthropathy. http://emedicine.medscape.com/article/310069-overview
7. Debra G. Perina. Mechanical Back Pain. http://emedicine.medscape.com/article/822462
8. John K. Hsiang. Spinal Stenosis. http://emedicine.medscape.com/article/1913265-overview
9. Kinkade S. Evaluation and treatment of acute low back pain // Am. Fam. Physician. — Apr 15 2007. — 74 (8). — 1181-8 [Medline].
10. Laszlo Hodinka. Боль в нижней части спины / Национальный институт ревматологии и физиотерапии, Будапешт // Внутренняя медицина. — 2007. — 1 (1).
11. Maheu E., Mazières B., Valat J.P., Loyau G., Le Loët X., Bourgeois P., Grouin J.M., Rozenberg S. Symptomatic efficacy of avocado/soybean unsaponifiables in the treatment of osteoarthritis of the knee and hip: a prospective, randomized, double-blind, placebo-controlled, multicenter clinical trial with a six-month treatment period and a two-month followup demonstrating a persistent effect // Arthritis Rheum. — 1998 Jan. — 41 (1). — 81-91.
12. Podolecki T., Podolecki A., Hrycek A. Fibromyalgia: pathogenetic, diagnostic and therapeutic concerns // Pol. Arch. Med. Wewn. — 2009. — 119 (3). — 157-61
/137.jpg)
/138_2.jpg)

/137_2.jpg)
/138.jpg)