Статья опубликована на с. 112-117
Введение
Синдром грудного выхода (СГВ) — это совокупный термин, объединяющий группу нейрососудистых синдромов, возникающих при компрессии нейрососудистого пучка, в том числе стволов плечевого сплетения, подключичных сосудов, в области грудного выхода, обусловленных изменением соотношения между нейрососудистым пучком и окружающими костно-мышечным структурами.
Одной из главных причин СГВ в точке топографо-анатомических взаимоотношений костно-мышечных структур с нейрососудистым пучком являются изменения в передней лестничной мышце (синдром передней лестничной мышцы), обусловленные врожденными и приобретенными факторами [6].
При СГВ, вызванном компрессией ствола плечевого сплетения и подключичных сосудов, клиническая картина может иметь изолированную или смешанную форму, в зависимости от степени поражения элементов нейрососудистого пучка [9–11]. Болевой компонент, однако, присутствует при любой форме, независимо от поражения ствола плечевого сплетения и/или подключичных сосудов [7].
Задачей хирургического лечения СГВ является устранение анатомического конфликта между нейрососудистым пучком и окружающими костно-мышечными структурами. При данной ситуации, обусловленной изменениями в передней лестничной мышце, обязательно делать миотомию лестничных мышц (скаленотомия). Попытка осуществить скаленотомию у больного с СГВ была впервые предпринята в 1937 году Н.С. Naffzider, который сообщил о положительных результатах этой операции в раннем послеоперационном периоде. Однако в отдаленном послеоперационном периоде отмечалось возобновление симптоматики, особенно болевого синдрома [8].
На сегодняшний день стандартное оперативное вмешательство с целью лечения СГВ, обусловленного изменениями в передней лестничной мышце, включает невролиз плечевого сплетения, ангиолиз подключичных сосудов и скаленотомию в надключичной области, которые позволяют существенно улучшить состояние нервно-мышечного аппарата и трофические функции в верхних конечностях. Однако часто наблюдается возобновление болевого синдрома в послеоперационном периоде и актуальной также остается проблема длительности периода восстановления двигательной и чувствительной функции.
Целью исследования было улучшение результатов хирургического лечения больных с синдромом грудного выхода, обусловленным изменениями в передней лестничной мышце, путем усовершенствования методов длительной электростимуляции структур плечевого сплетения.
Материалы и методы
Проведено комплексное обследование 37 пациентов, которые находились на лечении в отделении восстановительной нейрохирургии ГУ «Институт нейрохирургии им. акад. А.П. Ромоданова НАМН Украины» с 1999 по 2014 г. В исследовании приняли участие 18 (48,6 %) женщин и 19 (51,4 %) мужчин. Возраст пациентов был от 9 до 74 лет. Преимущественно отмечалась односторонняя локализация процесса (89,2 % случаев). Двусторонняя локализация процесса наблюдалась у 4 пациентов. В сроки менее 6 месяцев до момента появления первых симптомов к специалисту обратились 15 (40,5 %) пациентов, от 6 до 12 месяцев — 9 (24,3 %), от 12 до 24 — 5 (13,5 %), спустя более 2 лет — 8 (21,6 %).
Диагностический комплекс у всех пациентов включал: клинико-неврологическое исследование и дополнительные инструментальные методы обследования, в том числе электронейромиографию (ЭНМГ), рентгенологическое исследование шейного отдела позвоночника и грудной клетки и ультразвуковую допплерографию (УЗДГ).
Для оценки выраженности болевого синдрома использовали стандартную визуально-аналоговую шкалу (ВАШ, в англоязычной литературе — Visual Analog Scale, VAS по E.C. Huskisson, 1982 г.): Р0 — отсутствие боли, Р1, P1–2 — легкая приступообразная боль, Р2, P2–3 — умеренная приступообразная боль, Р3, P3–4 — средняя приступообразная боль, Р4, P4–5 — сильная постоянная боль, Р5 и больше — сильная, нестерпимая постоянная боль. Исследование состояния чувствительности осуществлялось на основе схемы РНХИ им. проф. А.Л. Поленова S (0–4) [1–3]: S1 — выраженная гипестезия, S2 — умеренная гипестезия, S3 — легкая гипестезия, S4 — чувствительность сохранена. Оценка состояния мышц конечностей проводили на основе схемы РНХИ им. проф. А.Л. Поленова [1–3]: М0 — отсутствие активных движений, М1 — сокращение мышц без движения в суставах, М2 — слабые сокращения мышц, М3 — умеренное снижение силы, М4 — движения, достаточные по объему, легкое снижение силы, М5 — нормальная сила, движения в полном объеме; А0 — атрофия, А1 — выраженная гипотрофия, А2 — наличие гипотрофии, сниженный мышечный тонус, А3 — сниженный мышечный тонус, А4 — изменений нет. Исследование состояния трофических функций включало оценку степени хронической артериальной недостаточности по методике А.В. Покровского (1979) А (0–3) [4]: А0 — симптомы отсутствуют, А1 — незначительная бледность кожных покровов кисти, предплечья, А2 — постоянная бледность и похолодание кожных покровов в покое и на холоде, А3 — трофические изменения и язвы на пальцах, кисти; и оценка степени хронической венозной недостаточности (Савельев В.С. с соавт., 1972) V (0–3) [5]: V0 — симптомы отсутствуют, V1 — умеренный отек предплечья, V2 — отек, цианоз верхней конечности, V3 — выраженная варикозная сеть и отек на предплечье, плече и груди. Кроме этого, мы использовали специальные провокационные тесты, которые способствуют уточнению диагноза синдрома грудного выхода: тест Итона, тест Адсона (Боголепова), тест Окснер — Гаге и тест Райта.
При анализе результатов ЭНМГ принималось во внимание изменение следующих показателей: М-ответа и S-ответа. Тщательный анализ вышеуказанных показателей позволил нам определить как уровень, так и степень блока проведения по нервным стволам.
Рентгенологическое исследование шейного отдела позвоночника и грудной клетки в прямой проекции позволяло определить увеличение поперечных отростков позвоночника, возникающее при СГВ, а также наличие добавочного шейного ребра и определить его форму и размер.
С помощью ультразвукового допплерографического обследования определяли степень компрессии сосудистых компонентов и показатель линейной скорости кровотока (ЛCK).
Лечение больных с СГВ обычно начинают с комплексных консервативных методов, применяемых в течение 1–1,5 мес. У некоторых пациентов после курса консервативного лечения или во время его проведения наблюдается ухудшение качества жизни в виде грубых нарушений состояния нервно-мышечного аппарата, чувствительных, трофических функций и нестерпимой боли в пораженной конечности. В таких случаях, как правило, показано оперативное лечение.
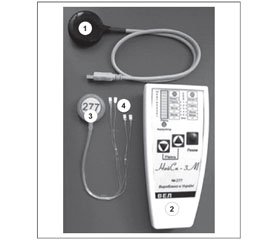
Всем 37 пациентам, наблюдаемым нами, было проведено хирургическое лечение, в том числе у 23 пациентов (первая группа) применяли лишь стандартные методы в виде невролиза структур плечевого сплетения, ангиолиза подключичных сосудов и скаленотомии в надключичной области с использованием классического переднего доступа; у 14 больных (вторая группа) дополнительно была установлена электростимулирующая система (ЭСС) «НейСи‑3М» (фирма «ВЭЛ», Украина) на структуру плечевого сплетения для продолжительной стимуляции в послеоперационном периоде (рис. 1, 2).
/114.jpg)
Установка ЭСС на структуру плечевого сплетения осуществлялась после устранения сдавления нейрососудистого пучка. Электростимуляцию обычно начинали на второй день после операции и проводили ее 3–4 раза в день в течение 10–15 минут с использованием параметров стимуляции, предварительно установленных в системе генератора импульсов «НейСи‑3М». Ранние результаты хирургического лечения оценивали на 1-й и 14-й день послеоперационного периода. При этом в качестве основных показателей рассматривали степень выраженности болевого синдрома и регресса трофических нарушений. Отдаленные результаты определяли не ранее чем через шесть месяцев после проведенного хирургического вмешательства. Эффективность лечения оценивали по состоянию нервно-мышечного аппарата, чувствительных и трофических функций, а также по степени выраженности болевого синдрома.
Результаты. Обсуждение
Анализ результатов хирургического лечения в 1-й день послеоперационного периода свидетельствует о наличии следующих положительных результатов: у 2 (8,7 %) из 23 пациентов первой группы отмечен регресс болевого синдрома от исходного уровня Р4 до уровня Р3–4, у одного пациента (4,3 %) — улучшение чувствительной функции от исходного уровня S1 до уровня S2 и у одного пациента (4,3 %) — улучшение трофической функции от исходного уровня V2 до уровня V1. У одного (7,1 %) из 14 пациентов второй группы — от Р3 до уровня Р2–3.
На 14-й день послеоперационного периода зафиксированы следующие положительные результаты: из 23 прооперированных больных из первой группы у 14 (60,9 %) пациентов отмечен регресс болевого синдрома: у двух (8,7 %) пациентов — от исходного уровня Р2 до уровня Р1–2; у 2 (8,7 %) пациентов — до уровня Р2 при исходном Р2–3. У 3 (13 %) больных с исходным уровнем Р3 виден регресс болевого синдрома до Р2; у 4 (17,4 %) пациентов с исходным уровнем Р3–4 отмечен регресс до Р2–3. При анализе 3 (13 %) тяжелых пациентов с постоянной сильной болью (Р4) в раннем послеоперационном периоде обнаружено снижение боли до уровня Р3. В ходе анализа результатов у пациентов с нарушением чувствительности нами отмечено наличие положительных результатов у двух (8,7 %) пациентов от исходного уровня S1 до уровня S2.
Со стороны улучшения трофической функции отмечено, что у 3 (13 %) больных наблюдалась полная нормализация функции артериального кровотока от исходного уровня А1. У 2 (8,7 %) пациентов с исходным уровнем А2 зафиксировано восстановление до уровня А1. Аналогичная картина видна и при нарушении венозного кровотока: у 4 (17,4 %) пациентов отмечено полное снятие отека верхней конечности от исходного уровня V1. У 3 (13 %) пациентов с исходным уровнем V2 наблюдалось снятие цианоза и наличие лишь незначительного отека (V1).
Из 14 больных второй группы у 11 (78,6 %) отмечен регресс болевого синдрома: у 4 (28,6 %) пациентов с исходным уровнем Р1–2 — до Р1; с исходным уровнем Р3 у 3 (21,4 %) виден регресс болевого синдрома до Р2; с исходным уровнем Р3–4 у 2 (14,3 %) больных отмечено регрессирование до уровня Р3, и у двух (14,3 %) больных отмечено регрессирование до уровня Р4 с исходным уровнем Р4–5. В ходе анализа результатов у пациентов с нарушением чувствительности нами отмечено наличие положительных результатов у 5 (35,7 %) пациентов: от исходного уровня S2 до уровня S3.
Также анализ результатов показал улучшение трофических функций: у 2 (14,3 %) пациентов наблюдалось полное восстановление артериального кровообращения от исходного уровня А1, и у 3 (21,4 %) пациентов с исходным уровнем А2 оно зафиксировано на уровне А1. Картина нормализации венозного кровотока: у 4 (28,6 %) пациентов отмечено полное снятие отека верхней конечности с исходным уровнем V1, и у 3 (21,4 %) пациентов с исходным уровнем V2 наблюдалось снятие цианоза и наличие лишь незначительного отека (V1).
В отдаленный послеоперационный период из 23 прооперированных (первая группа) у 17 (73,9 %) пациентов отмечен регресс болевого синдрома, в том числе в двух случаях двусторонней локализации: у одного (4,3 %) пациента с Р2 отмечено его снижение до уровня Р1 и у одного (4,3 %) пациента с Р2–3 отмечено его снижение до уровня Р1–2. При исходном уровне Р3 у 4 (17,4 %) виден регресс болевого синдрома до Р2, у 2 (8,7 %) пациентов — до Р1. У 6 (26,1 %) пациентов с Р3–4 отмечено его снижение до уровня Р2–3 и у 2 (8,7 %) тяжелых пациентов с Р4 показано снижение постоянной приступообразной боли до уровня Р3 и у одного (4,3 %) — до уровня Р2. В этой группе нами зафиксировано, что у 3 (13 %) пациентов наблюдалось возобновление болевого синдрома в отдаленном послеоперационном периоде и у 3 (13 %) пациентов не отмечены положительные результаты. Нормализация двигательной функции наблюдалась у 19 (82,6 %) пациентов в виде существенного регресса двигательного дефицита: при исходном уровне М1 у одного (4,3 %) больного — до М2, у 7 (30,4 %) пациентов с исходным уровнем M2 наблюдалось восстановление до M3 и у 8 (34,8 %) пациентов — от исходного уровня M3 до M4. При нарушении двигательной функции с исходным уровнем M4 у 3 (13 %) пациентов мы наблюдали ее полное восстановление до М5 и у троих (13 %) больных положительные результаты не были получены. Также у 14 (60,9 %) пациентов, принявших участие в исследовании, оперативное вмешательство позволило добиться регресса дегенеративных процессов в мышцах верхней конечности: при исходном уровне А1 у одного (4,3 %) пациента до А2, у 8 (34,8 %) пациентов с исходным уровнем А2 мышцы верхней конечности (преимущественно мышцы кисти) приобрели нормальную конфигурацию и объем, осталось только незначительное снижение мышечного тонуса (А3). У 5 (21,7 %) пациентов мышечный тонус полностью восстановился до нормального при исходном уровне А3. У четырех (17,4 %) больных мы не наблюдали положительных результатов, и у пяти (21,7 %) пациентов исходное состояние мышцы было в норме (А4). В ходе анализа результатов у пациентов с нарушением чувствительности нами отмечено наличие положительных результатов у 15 (65,2 %) больных: у 3 (13 %) пациентов с исходным уровнем S1 наблюдалось улучшение чувствительной функции до уровня S2, у 2 (8,7 %) пациентов — восстановление до S3. У 7 (30,4 %) пациентов чувствительные нарушения регрессировали от исходного уровня S2 до S3. У 3 (13 %) пациентов с исходным уровнем S3 после операции полностью восстановлена чувствительная функция до S4 и у 8 (34,8 %) она сохранилась на дооперационном уровне S3 в соответствующей зоне иннервации. Что касается нормализации артериального кровообращения, нами отмечено, что у 7 (30,4 %) пациентов при исходном уровне А1 и у одного (4,3 %) пациента — А2 наблюдалась полная нормализация функции артериального кровотока. У 12 (52,2 %) пациентов с исходным уровнем А2 зафиксировано восстановление до уровня А1. У 3 (13 %) больных положительные результаты не получены и сохранилась незначительная бледность кожных покровов кисти, предплечья. Что касается восстановления венозного кровотока, нами отмечено, что у 10 (43,5 %) пациентов с исходным уровнем V1 и у 3 (13 %) пациентов с V2 наблюдалось полное восстановление функции венозного кровотока. У 4 (17,4 %) пациентов с исходным уровнем V2 наблюдалось снятие цианоза и наличие лишь незначительного отека (V1), и у 6 (26,1 %) больных удовлетворительный эффект не отмечен. У 13 (92,9 %) пациентов второй группы отмечен регресс болевого синдрома, в том числе у одного (7,1 %) пациента с исходным уровнем болевого синдрома Р1–2 отмечено уменьшение до уровня Р1 и у 3 (21,4 %) пациентов — полное снятие болевого синдрома; у двух (14,3 %) пациентов с исходным уровнем Р3 виден регресс болевого синдрома до Р2 и у троих (21,4 %) больных — до Р1. У 2 (14,3 %) пациентов с исходным уровнем Р3–4 отмечено уменьшение проявления боли до уровня Р2–3. При анализе 2 (14,3 %) тяжелых пациентов с постоянной нестерпимой болью (Р4–5) в отдаленном послеоперационном периоде обнаружено снижение боли до уровня Р3.
При анализе результатов нормализации двигательной функции у 13 (92,9 %) больных отмечено достижение существенного регресса двигательного дефицита: при исходном уровне М1 у 3 (21,4 %) — до М2, у 2 (14,3 %) пациентов с исходным уровнем M2 наблюдалось восстановление до M3. У 5 (35,7 %) пациентов двигательный дефицит регрессировал от исходного уровня M3 до M4. У 3 (21,4 %) пациентов с исходным уровнем M4 мы наблюдали полное восстановление двигательной функции до М5, и у одного (7,1 %) пациента сохранялся периферический парез на уровне М4. Также путем анализа отдаленных результатов установлено, что у 8 (57,1 %) пациентов достигнут регресс дегенеративных процессов в мышцах верхней конечности: при исходном уровне А1 у 3 (21,4 %) — до А2, у 2 (14,3 %) пациентов с исходным уровнем А2 — восстановление до уровня А3. У 3 (21,4 %) пациентов мышечный тонус полностью восстановился от исходного уровня А3 до нормы (А4). У 2 (14,3 %) больных мы не наблюдали положительных результатов, и у 4 (28,6 %) пациентов исходный уровень был в норме. Со стороны чувствительной функции нами отмечено наличие положительных результатов у 12 (85,7 %) пациентов: у одного (7,1 %) пациента с исходным уровнем S1 — до уровня S2, у 10 (71,4 %) пациентов полностью восстановлена чувствительная функция до S4, в том числе у 5 (35,7 %) пациентов с уровнем S2 и у 5 (35,7 %) пациентов с исходным уровнем S3. Еще у одного (7,1 %) пациента наблюдалось улучшение чувствительности от исходного уровня S2 до S3, и у двух (14,3 %) больных сохранилась незначительная гипестезия в зоне автономной иннервации С8-Д1 корешков плечевого сплетения.
Что касается восстановления артериального кровотока, то у 7 (50 %) пациентов с исходным уровнем А1 и у троих (21,4 %) больных с А2 наблюдалась полная нормализация функции артериального кровотока. У 2 (14,3 %) пациентов с исходным уровнем А2 зафиксировано восстановление до уровня А1, и у 2 (14,3 %) больных мы не наблюдали положительной динамики. Также отмечен регресс нарушения венозного кровотока: у 8 (57,1 %) пациентов с исходным уровнем V1 и у двух (14,3 %) больных с V2 наблюдалось полное восстановление венозного кровотока. У 3 (21,4 %) пациентов с исходным уровнем V2 наблюдался регресс до V1, и у одного (7,1 %) пациента нами не отмечено положительных результатов.
Выводы
1. Использование стандартного оперативного вмешательства, включая невролиз структур плечевого сплетения, ангиолиз подключичных сосудов и скаленотомию в надключичной области, путем классического переднего доступа в случае неэффективности комплексного консервативного лечения больных с синдромом грудного выхода, обусловленным изменениями в передней лестничной мышце, позволяет эффективно улучшить неврологическое состояние и трофические функции у всех больных.
2. Дополнительная установка системы длительной электростимуляции плечевого сплетения в ходе стандартного оперативного вмешательства обеспечивает максимальное сокращение периода и больший объем восстановления функций чувствительности и нервно-мышечного аппарата верхней конечности при синдроме грудного выхода.
3. Длительная электростимуляция плечевого сплетения оказывает влияние на динамику болевого синдрома. Ее использование обеспечивает стабильный противоболевой эффект, особенно в отдаленном послеоперационном периоде, у всех пациентов с синдромом грудного выхода.
/114.jpg)
/114_2.jpg)