Статья опубликована на с. 11-14
Сформировавшийся в процессе эволюции специфический симбиоз человека с определенными группами микроорганизмов, заселившими нестерильные полости и кожные покровы его тела, преобразовался в единую микроэкологическую систему, гармонично функционирующую в пользу обеих составляющих симбиоза. С учетом наиболее высокой плотности микробных популяций в толстой кишке (около 60 % всей микробиоты человека) большинство исследований в области микробной экологии посвящено изучению микрофлоры желудочно-кишечного тракта, установлению причин развития кишечных дисбактериозов и разработке методов их коррекции. Однако нельзя не учитывать значимость микробных популяций, заселяющих другие органы, в первую очередь кожные покровы, ротоглотку и вагинальный отдел мочеполовой системы.
В организме женщины одним из важных аспектов, играющих значительную роль в поддержании физиологической нормы репродуктивного здоровья и всего организма в целом, является вагинальный биотоп, в котором обитает около 10 % аутофлоры. Влагалищная микрофлора строго индивидуальна и меняется в различные периоды развития женского организма. Понятие нормы различается не только в связи с возрастом, но и в связи с принадлежностью к разным этническим группам.
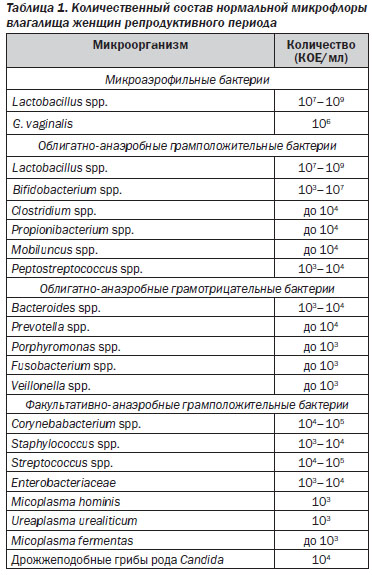
Особенностью нормальной микрофлоры половых путей здоровых женщин репродуктивного возраста является многообразие видового состава, представленного широким спектром микроаэрофилов, факультативных и облигатных анаэробных микроорганизмов (соотношение «анаэробы/аэробы» в репродуктивном периоде составляет 10 : 1). Ведущее место в вагинальном микробиоценозе — 95–98 % (107–109 КОЕ/мл) — занимают лактобациллы (палочки Додерлейна), чаще всего это микроаэрофильные, продуцирующие перекись водорода, реже анаэробные. Доля всех остальных многочисленных представителей влагалищного биоценоза в норме не превышает 3–4 %. Нормальный состав вагинального биоценоза женщин репродуктивного возраста приведен в табл. 1.
С момента первого описания в 1892 г. А. Doderlein лактобактерий как преобладающих микроорганизмов нормального влагалищного биоценоза их значимость в поддержании нормального биоценоза женского урогенитального тракта и до настоящего времени остается неоспоримой. Известно, что первым признаком вагинальных дисбиотических расстройств является снижение концентрации анаэробной молочнокислой флоры или потеря ею биологических свойств.
Основное место среди лактобактерий влагалища занимает род Lactobacillus. Во влагалище здоровой женщины обычно одновременно присутствуют несколько видов лактобацилл, что способствует расширению спектра защитных и других физиологических свойств биоценоза. Кроме того, установлено, что у здоровых женщин лактобациллы являются доминирующей микрофлорой не только влагалища, но и уретры, что предохраняет нижние отделы мочеполового тракта от колонизации уропатогенами и их восходящего инфицирования.
За счет способности активно размножаться в вагинальном секрете, адгезировать к эпителиоцитам, ферментировать гликоген с накоплением короткоцепочечных жирных кислот, синтезировать перекись водорода, лизоцим, стимулировать местный иммунитет данная группа молочнокислых бактерий в процессе эволюции оказалась наиболее приспособленной к колонизации влагалища и активному вытеснению из него других микроорганизмов. Об этом говорит высокая концентрация лактобацилл в вагинальном секрете здоровой женщины (до 109 КОЕ/мл).
Вначале предполагалось, что группу Doderlein составляют исключительно лактобациллы. Однако позже было установлено, что важными компонентами вагинальной микрофлоры являются также бифидобактерии. Во время беременности и особенно в предродовом периоде количество бифидобактерий во влагалище резко возрастает, что связано с эволюционно сформировавшейся функцией бифидофлоры матери как наиболее важного фактора защиты организма новорожденного от колонизации его потенциальными патогенами. Наиболее часто в вагинальной экосистеме встречаются виды B.bifidum, B.infantis, B.longum, B.breve и B.adolescentis. Бифидобактерии так же, как и лактобациллы, способны сбраживать гликоген с образованием органических кислот, адгезировать к эпителию, синтезировать антимикробные метаболиты и успешно конкурировать с факультативной и транзиторной микрофлорой. Установлено, что вагинальные бифидобактерии эффективно подавляют рост гарднерелл, стафилококков, эшерихий, клебсиелл, грибов и других условно-патогенных микроорганизмов.
Таким образом, физиологическую основу защитной микрофлоры влагалища составляют бактерии из родов Lactobacillus и Bifidobacterium. Помимо формирования в вагинальном биотопе условий, неблагоприятных для размножения условно-патогенной флоры, эти микроорганизмы способны стимулировать иммунитет и синтезировать метаболиты, улучшающие трофику эпителия урогенитального тракта и активизирующие процессы обновления эпителиальной ткани.
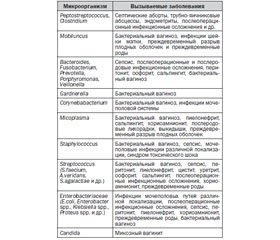
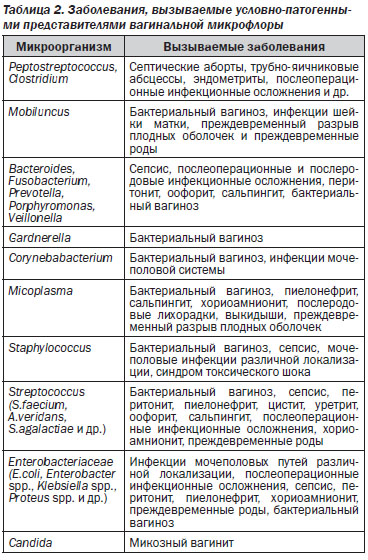
Помимо облигатной физиологической микрофлоры, во влагалище всегда присутствуют факультативные микроорганизмы, популяционный уровень которых в норме не превышает 3–4 %, хотя их видовой состав достаточно разнообразен (до 20 видов). Все эти микроорганизмы являются условно-патогенными и при снижении активности и популяционного уровня бактерий группы Doderlein, а также других факторов колонизационной резистентности женского организма могут вызывать различные заболевания (табл. 2).
Во влагалищном биотопе всегда присутствует в незначительной концентрации транзиторная (случайная) микрофлора, среди которой встречаются и патогенные виды. Однако эти микроорганизмы могут вызывать инфекционный процесс только при глубоком нарушении состава и функций вагинального микробиоценоза и значительном угнетении иммунной системы.
Современный уровень знаний в области микробиологии и физиологии позволяет заключить, что вагинальный микробиоценоз не является простой совокупностью микроорганизмов, случайно поселившихся во влагалище, а представляет собой эволюционно сформировавшуюся сложную микробную популяцию.
Одна из наиболее важных природных функций вагинальной экосистемы заключается в формировании микроэкологического здоровья новорожденных. Известно, что первыми микроорганизмами, контаминирующими плод после стерильного внутриутробного развития, является микрофлора родовых путей матери.
Ранее состояние вагинального биоценоза родильниц в основном рассматривалось как основной фактор, воздействующий на процесс заселения физиологической микрофлорой кишечника ребенка. Однако значимость вагинальной материнской микрофлоры для формирования здоровья ребенка намного шире. При естественном протекании родов происходит гарантированная контаминация вагинальными микроорганизмами не только желудочно-кишечного тракта, но и ротовой полости, верхних дыхательных путей, кожных покровов, мочеполового тракта. Микрофлора здоровой родильницы рационально дополняет несовершенные защитные факторы новорожденного и предупреждает колонизацию агрессивной микрофлорой не только естественных биотопов, но и стерильных органов и систем.
Характерно, что формирование вагинального биоценоза начинается сразу же после рождения девочки. Уже к концу первых суток после рождения стерильное влагалище новорожденной заселяется материнской вагинальной микрофлорой. При этом наряду с бактериями из группы Doderlein обнаруживаются условно-патогенные микроорганизмы, концентрация которых зависит от состояния микробной экологии родового пути матери. У здоровых новорожденных очень быстро во влагалищной экосистеме начинают преобладать лактобациллы и бифидобактерии. Это во многом обусловлено интранатальной передачей активных бактерий, индуцирующих синтез вагинальным эпителием гликогена, который, в свою очередь, стимулирует рост бактерий группы Doderlein.
Несмотря на то, что в дальнейшем микрофлора влагалища претерпевает закономерные изменения на разных этапах жизни, микроэкологические основы репродуктивного здоровья, заложенные в период новорожденности, играют существенную роль в его поддержании на протяжении всей дальнейшей жизни женщины.
Через 3–4 недели после рождения материнские эстрогены почти полностью исчезают из организма девочки, концентрация гликогена во влагалище также снижается, в результате чего рН влагалищного секрета повышается до нейтральной и слабощелочной реакции. Общее количество микроорганизмов во влагалище значительно снижается, и со второго месяца жизни до начала пубертатного периода микроорганизмы во влагалище здоровых девочек обнаруживаются лишь в незначительных концентрациях. С момента активизации функции яичников в связи с накоплением в организме девушки собственных эстрогенов наблюдается утолщение слоя вагинального эпителия и увеличение в нем концентрации гликогена. С этого времени бактерии группы Doderlein вновь занимают доминирующее положение и сохраняют его во время всего репродуктивного возраста здоровой женщины.
Наиболее благоприятные условия для поддержания высокого уровня активной микрофлоры влагалища наблюдаются во время беременности. Значительное увеличение в эпителии концентрации гликогена способствует интенсивному развитию бактерий группы Doderlein. Особо благоприятная микроэкологическая ситуация у здоровых беременных наблюдается начиная с III триместра беременности. При этом заметно снижается количество потенциальных патогенов и возрастает концентрация лактобацилл и бифидобактерий. Характерно, что уровень бифидофлоры повышается не только в вагинальном биотопе, но и в других микро-экосистемах (гастроинтестинальном тракте, ротовой полости, кожных покровах, особенно в области молочных желез). Микроэкологические изменения, происходящие у здоровых женщин во время беременности, являются одним из важнейших естественно сформировавшихся факторов защиты плода от перинатальных инфекций.
В послеродовом периоде, особенно первые 4–5 недель после родов, защитные свойства вагинальной микроэкосистемы минимальны. Это связано с травмированием родового канала, снижением уровня эстрогенов, уменьшением концентрации гликогена и др. Обычно в этот период на фоне снижения концентрации клеток бактерий Doderlein увеличивается уровень бактероидов, эшерихий, энтерококков и других потенциальных патогенов. Такие нарушения представляют высокий риск развития послеродовых инфекционных осложнений. У здоровых женщин послеродовые микроэкологические нарушения в генитальном тракте носят транзиторный характер и обычно восстанавливаются к 6-й неделе послеродового периода.
Стабильные изменения во влагалищном биотопе наступают в постменопаузальном возрасте. Происходящие в этом периоде возрастные гормональные и метаболические перестройки приводят к значительным морфологическим, функциональным и биохимическим изменениям в генитальном тракте. Влагалищная среда становится нейтральной или слабощелочной, снижается концентрация гликогена, создаются неблагоприятные условия для развития нормальной микрофлоры. На фоне снижения общего уровня микроорганизмов начинает доминировать условно-патогенная флора, количество которой контролируется собственными защитными механизмами организма женщины.
Таким образом, существует целый ряд эндогенных факторов, прямо или косвенно влияющих на состав вагинальной микрофлоры в организме женщины. В норме эти факторы компенсируются естественными защитными механизмами, и состав влагалищного биоценоза является относительно постоянным во время всего репродуктивного периода жизни. Однако при пониженной резистентности организма в различные, зависимые от гормональных или метаболических изменений периоды жизни женщины возможно развитие глубоких микроэкологических расстройств, которые могут стать причиной вторичных, серьезных патологических изменений.
Отрицательное влияние на состав и функции вагинальной микроэкосистемы оказывают и многие экзогенные факторы. Наиболее опасным является неадекватное применение медикаментозных средств, в частности антибактериальных, гормональных и иммунодепрессивных препаратов, цитостатиков, лучевой терапии.
Рациональная антибиотикотерапия гинекологических больных остается одним из самых сложных вопросов клинической медицины. В современных условиях этиология практически всех инфекционных заболеваний половых органов характеризуется наличием смешанной флоры. Даже в случае экзогенных урогенитальных инфекций к ним очень быстро присоединяется эндогенная условно-патогенная флора нижних отделов половых путей, отличающаяся большим разнообразием. Это вызывает необходимость использования комбинации антибактериальных препаратов, активных относительно широкого спектра возбудителей анаэробных и аэробных бактериальных инфекций, а также противогрибковых и противовирусных средств.
Массивная антимикробная терапия не только вызывает глубокие микроэкологические нарушения во всем организме, в том числе и в вагинальном биотопе, лишая мочеполовую систему естественной защиты, но и способствует формированию мультирезистентных популяций условно-патогенных микроорганизмов, а также искусственной селекции новых патогенов, которые все чаще вовлекаются в процесс развития инфекционно-воспалительных патологий.
Следует учитывать, что любое гинекологическое заболевание протекает в ассоциации с вагинальным дисбиозом, а интенсивная антибактериальная терапия с прессингом на анаэробную флору значительно усложняет дисбиотические расстройства во влагалище. За счет этого в организме происходит искусственное формирование резервуаров условно-патогенной флоры с множественной антибиотикорезистентностью.
Таким образом, традиционная этиотропная терапия, к сожалению, не всегда учитывает тесную связь между развитием инфекционно-воспалительных заболеваний в женской репродуктивной системе и вагинальными микроэкологическими нарушениями, значительно снижающими колонизационную резистентность урогенитального тракта и способствующими формированию эндогенного источника высоковирулентных инфекционных агентов.
В лечении гинекологических больных требуется комплексный подход, нацеленный не только на снижение популяционного уровня возбудителя заболевания, но и на восстановление нарушенной микроэкологической системы, причем не только в вагинальном биотопе, но и во всех других микробных экосистемах женского организма, особенно в пищеварительном тракте, микрофлора которого наиболее тесно связана с влагалищным биоценозом.
Анатомическая особенность расположения влагалища и ануса обеспечивает высокую частоту обмена микроорганизмами между кишечником и урогенитальным трактом. Установлено, что при вагинальных дисбиозах в урогенитальном тракте всегда резко возрастает концентрация кишечных микроорганизмов, чаще всего из родов Bacteroides, Fusobacterium, Peptostreptococcus, Clostridium, Eubacterium, Veillonella, Escherichia, Enterococcus и др. При этом в кишечном и в вагинальном биотопах заметно снижается популяционный уровень индигенных сахаролитических бактерий родов Bifidobacterium и Lactobacillus.
К сожалению, при лечении вагинальных дисбиозов очень редко учитывается тот факт, что нарушение в любом биотопе не протекает изолированно от других микробных экосистем и в первую очередь сочетается с дисбиозом пищеварительного тракта, который является основным резервуаром микрофлоры организма. Поэтому интравагинальная пробиотическая терапия не всегда приводит к стойкому клиническому эффекту без параллельной коррекции состава кишечного биоценоза.
Лакто® — инновационный комплексный пробиотик для быстрого и эффективного восстановления нормальной микрофлоры кишечника, купирования симптомов диареи различного генеза, ротавирусной инфекции, профилактики антибиотикассоциированных диарей.
Лакто® содержит наиболее важные для биоценоза организма микроорганизмы в клинически значимых концентрациях — Saccharomyces boulardii, Lactobacillus sporogenes, Lactobacillus rhamnosus, Bifidobacterium longum.
Сахаромицеты буларди (Saccharomyces boulardii) оказывают выраженное противодиарейное (антисекреторное) действие, обусловленное снижением цАМФ в энтероцитах, что приводит к уменьшению секреции воды и натрия в просвет кишечника. Способность Saccharomyces boulardii угнетать развитие патогенных и условно-патогенных бактерий и грибов, которые нарушают биоценоз кишечника, объясняет его антимикробное действие. Saccharomyces boulardii проявляют прямой антагонизм в отношении Clostridium difficile, Clostridium pneumoniae, Staphуlococcus aureus, Pseudomonas aeruginosa, Candida krusei, Candida pseudotropical, Candida albicans, Salmonella typhi, Salmonella enteritidis, Escherichia coli, Shigella dysenteriae, Shigella flexneri, Klebsiella, Proteus, Vibrio cholerae, а также Enthamoeba hystolitica, Lambliae, Enterovirus, Rotavirus.
Saccharomyces boulardii обладают также антитоксическим действием, обусловленным выработкой протеаз, которые расщепляют токсины А и В, вырабатываемые Clostridium difficile, и имеют рецептор энтероцита, с которым связывается токсин. Кроме того, Saccharomyces boulardii повышают выработку IgA энтероцитами тонкой кишки.
Лактобациллы (Lactobacillus sporogenes, Lactobacillus rhamnosus) и бифидобактерии (Bifidobacterium longum) являются представителями нормальной микрофлоры кишечника. Данные микроорганизмы проявляют антагонистическую активность в отношении патогенных и условно-патогенных микроорганизмов и создают благоприятные условия для развития полезной микрофлоры кишечника за счет ферментации глюкозы, маннозы, фруктозы и сахарозы до правовращающей (L+) молочной кислоты, которая не вызывает метаболический ацидоз; выработки бактериоцинов, которые ингибируют рост энтерококков, листерий и других условно-патогенных и патогенных микроорганизмов; нормализуют вагинальную микрофлору, восстанавливая природную кислую среду во влагалище (рН 3,8–4,5), и повышают стойкость слизистой оболочки к действию патогенных микроорганизмов. Кроме того, Bifidobacterium longum участвуют в синтезе витамина К, пантотеновой кислоты, витаминов группы В.
Поскольку Лакто® содержит только физиологичную микрофлору, рациональным является его использование в гинекологии и акушерстве.