Газета «Новости медицины и фармации» Неврология. Нейрохирургия. Психиатрия (579) 2016 (тематический номер)
Вернуться к номеру
Тактика ведения черепно-мозговой травмы в остром и восстановительном периодах
Авторы: Татьяна Чистик
Рубрики: Неврология, Хирургия, Психиатрия
Разделы: Медицинские форумы
Версия для печати
Статья опубликована на с. 21-24
Черепно-мозговая травма (ЧМТ) является одной из ведущих причин летальности и инвалидизации больных. По данным ВОЗ, ежегодно регистрируется около 1,4 млн черепно-мозговых травм. Среди лиц, выживших при этом виде патологии, только 10 % могут вернуться к прежней работе и только 2 % довольны качеством жизни. Поэтому совершенствование диагностики и поиски эффективных средств лечения ЧМТ входят в число важнейших задач современной науки и практики.
Тема оказания помощи пациентам с ЧМТ в остром и восстановительном периодах обсуждалась в рамках 10-й юбилейной конференции «Карпатские чтения», которая состоялась 9–11 июня в Ужгороде.
С докладом «Тактика ведения ЧМТ в остром периоде и прогноз течения» выступил президент Ассоциации нейрохирургов Украины д.м.н., профессор В.И. Смоланка (Ужгородский национальный университет).
Черепно-мозговая травма — широко распространенная патология во всех странах мира, нередко приводящая к инвалидности, а иногда и к смерти пациента. Оценка исходов ЧМТ осуществляется по шкале исходов, разработанной G. Jennet и В. Teasdale в 1974 году:
1 — смерть;
2— вегетативный статус;
3 — глубокая инвалидность — больной требует постоянного ухода;
4 — умеренная инвалидность — пациент не требует постоянной помощи, но ограниченна его трудоспособность;
5 — хорошее восстановление — возвращение к нормальной жизни;
6 — диффузное аксональное повреждение.
Анализ состояния пациентов осуществляется через 3, 6 и 12 месяцев. Так, в исследовании, в котором приняли участие 500 пациентов, перенесших черепно-мозговую травму, было показано, что удовлетворительного состояния к 3-му месяцу достигли лишь 2/3 пациентов, к 6-му — 90 %, и лишь у 5 % больных отмечалось значительное улучшение спустя 12 месяцев. Психологический и нейрофизиологический статусы после перенесенной ЧМТ могут улучшаться на протяжении нескольких лет (обычно до 2 лет). У больных со значительным дефицитом в последующие годы может происходить ухудшение состояния.
Среди прогнозов ЧМТ ведущим является развитие характерного посттравматического синдрома, характеризующегося головными болями, когнитивными нарушениями и изменениями личности. Лишь 10 % пациентов возвращаются к нормальной независимой жизни на протяжении первого года после перенесенной травмы. Более 90 % остаются в перманентном вегетативном состоянии. Причем прогноз заболевания тем хуже, чем больше патологических очагов повреждения возникло после ЧМТ.
К факторам, влияющим на прогноз данной патологии, относятся: состояние больного, его особенности и течение заболевания. Состояние больного при поступлении оценивается по характеру травмы, тяжести первичного повреждения: интракраниального либо экстракраниального, вторичным повреждениям и данным компьютерной томографии (КТ). Тяжесть интракраниального повреждения зависит от степени нарушения сознания, которое может изменяться уже в первые часы-дни после поступления и должно оцениваться как при поступлении больного, так и при стабилизации витальных функций по шкале комы Глазго (ШКГ). Согласно этому выделяют три степени тяжести ЧМТ:
— легкую (ШКГ 14–15 баллов), летальность составляет менее 1 %;
— среднюю (ШКГ 9–13 баллов), летальность — менее 10 %;
— тяжелую (ШКГ менее 8 баллов), летальность — около 30 %.
Тяжесть экстракраниального повреждения имеет большое значение при черепно-мозговой травме средней или легкой степени тяжести и в большей степени определяет раннюю летальность. К вторичным повреждениям мозга относятся гипоксия и артериальная гипо-/гипертензия как последствие повышения внутричерепного давления. К наиболее неблагоприятным КТ-данным — облитерация базальных цистерн, субарахноидальное кровоизлияние и дислокация мозга, определяемые по Роттердамской шкале или шкале Маршалла. Также проводится оценка лабораторных показателей, позволяющих выявить неблагоприятные прогностические признаки: высокий уровень сахара в крови, низкий гемоглобин, тромбоцитопению, нарушение коагуляции.
Кроме того, следует помнить, что наихудший прогностический признак при ЧМТ — это ухудшение состояния пациента, наиболее неблагоприятная комбинация — высокое внутричерепное давление и низкое перфузионное. Также не следует забывать, что развитие вторичных повреждений нередко возникает на фоне вполне благополучной картины КТ, что диктует необходимость постоянного наблюдения за состоянием пациента.
Артериальное давление и оксигенация требуют постоянного мониторинга: необходимо избегать артериальной гипотензии (артериальное давление ниже 90 мм рт.ст.), а сатурация кислорода должна быть не ниже 94 %.
Мониторинг интракраниального давления показан у всех пациентов с тяжелой ЧМТ (ШКГ до 8 баллов) и аномальной КТ (гематома, отек, очаг контузии, компрессия базальных цистерн). Также целесообразно его проведение у больных с тяжелой ЧМТ и одним из двух имеющихся признаков: возраст старше 40 лет и систолическое артериальное давление ниже 90 мм рт.ст. При этом используется наиболее эффективная интравентрикулярная методика мониторирования лечения.
Важным аспектом успешного лечения является контроль центрального перфузионного давления: необходимо избегать его падения ниже 50 мм рт.ст. Целевое значение должно быть в пределах 50–70 мм рт.ст.
Гиперосмолярная терапия включает обязательное назначение маннитола — эффективного средства контроля повышенного интракраниального давления, применяемого в дозе от 0,25 до 1 г/кг массы тела, преимущественно болюсным введением препарата. Лечение маннитолом должно начинаться при уровне внутричерепного давления более 20 мм рт.ст.
Должна осуществляться профилактика инфекционных осложнений. Возможно одноразовое введение антибиотика при интубации больного с ЧМТ с целью профилактики пневмонии. При вентрикулярном дренировании антибиотикотерапия не показана. Назначение барбитуратов в высоких дозах может быть рекомендовано у пациентов с повышенным внутричерепным давлением лишь в случае неэффективности другого медикаментозного и хирургического лечения. При тяжелой ЧМТ категорически не показаны гипервентиляция и назначение стероидов.
В качестве антиоксидантной терапии применяют Элфунат, введение которого осуществляется 3 раза в день, через каждые 8 часов. Минимальная доза Элфуната составляет 250 мг, максимальная суточная доза не должна превышать 800 мг. Препарат можно вводить внутривенно капельно с разведением его в 100–200 мл физиологического раствора. Лечение начинают с дозы 50–100 мг 1–3 раза в день, постепенно повышая ее до достижения терапевтического эффекта. Струйно Элфунат вводят в течение 5–7 минут со скоростью 40–60 капель в минуту (рис. 1).

Об астении и головной боли в восстановительном периоде ЧМТ рассказал зав. кафедрой неврологии, нейрохирургии и психиатрии медицинского факультета Ужгородского национального университета д.м.н., профессор М.М. Орос.
Практическое выздоровление или стойкая компенсация наблюдаются приблизительно у 30 % больных с последствиями черепно-мозговой травмы. У 15 % пациентов имеющиеся нарушения функций после легкой травмы проявляются в основном пост-коммоционным синдромом (ПКС). Согласно другим данным, прогрессирующее нарастание патологических явлений при легкой ЧМТ наблюдается у 50 % пострадавших, при среднетяжелой и тяжелой — у 90 %.
Наблюдаются парадоксальные диссоциации между неврологическим статусом в остром (практически нормализовавшемся) и отдаленном (насыщенном полиморфном) периодах легких ЧМТ, а также противоположная тенденция в развитии последствий травм разной тяжести:
— при среднетяжелых и тяжелых закрытых ЧМТ постепенное сглаживание очаговой симптоматики с годами уступает место нейродинамическим расстройствам с обилием неврозоподобных проявлений;
— после сотрясения мозга в отдаленные периоды возникают лептоменингиты, хориоэпендиматиты и другие органические изменения мозга.
О конечных последствиях можно говорить через 1 год после перенесенной ЧМТ, так как в дальнейшем каких-либо существенных изменений в состоянии больного не происходит. В Международной классификации болезней 10-го пересмотра состояния, возникающие после ЧМТ, обозначены термином «посткоммоционный (или постконтузионный) синдром», что указывает на наличие когнитивных, эмоциональных и поведенческих нарушений. Клинически ПКС характеризуется отсутствием корреляции между выраженностью жалоб и тяжестью сотрясения мозга, а также неврологического статуса. Обычно нарушенные функции восстанавливаются на протяжении 3 месяцев. Если этого не происходит в течение более 12 месяцев и по-прежнему сохраняются когнитивные нарушения и астенический синдром, то это свидетельствует о развитии хронического посткоммоционного синдрома, наличии психогенных факторов, стрессово-конфликтных ситуаций в связи с ЧМТ.
После ЧМТ возможно развитие посттравматической астении, проявляющейся слабостью, быстрой утомляемостью, снижением трудоспособности, апатией, эмоциональной лабильностью: от плаксивости до длительных бурных всплесков раздражительности с дальнейшим раскаянием, гиперестезией, вегетативными и вестибулярными расстройствами, нарушением сна.
Симптомокомплекс «астеническое состояние» обозначается как патологическое истощение после нормальной активности, снижения энергии при решении задач, требующих усилия и внимания, или генерализованного снижения способности к действию и состоит из трех составляющих:
1) проявлений собственно астении;
2) расстройств, обусловленных лежащим в основе астении патологическим состоянием;
3) расстройств, обусловленных реакцией личности на болезнь.
В основе патогенеза астении лежат гипоперфузия скелетной мускулатуры, в конечном итоге проявляющаяся мышечной утомляемостью, и центральная гипоперфузия, возникающая вследствие нейротранс-миттерных изменений, вызывающих вегетативную дисфункцию, депрессию, тревожные состояния, раздражительность и нарушение сна.
В зависимости от проявлений выделяют гиперстеническую и гипостеническую астению. Гиперстеническая астения сопровождается повышенным сенсорным возбуждением, в результате чего пациент становится крайне раздражительным, плохо переносит громкие звуки, шум, яркий свет. Гипостеническая астения обычно отличается снижением чувствительности более легкой формы, однако при нарастании астенического синдрома может переходить в гиперстеническую.
К основным критериям диагностики астении относят:
— когнитивные нарушения, проявляющиеся снижением памяти и внимания;
— болевые нарушения — миалгии, головную боль напряжения, кардиалгии, абдоминалгии, боли в спине;
— вегетативную дисфункцию — головокружение, диспепсию, тахикардию, гипервентиляцию, гипергидроз;
— эмоционально-внутреннее напряжение, тревогу, лабильность либо снижение настроения, раздражительность, страхи;
— мотивационные и обменно-эндокринные диссомнии, снижение либидо, изменение аппетита, похудение, отеки, дисменорею;
— гиперестезию — повышенную чувствительность к свету и звуку.
Одной из основных жалоб при астении является жалоба на усталость, не исчезающая даже после длительного отдыха. Наблюдаются общая слабость и нежелание выполнять обычную работу, ухудшение памяти, снижение внимания и сообразительности, трудности при формулировании собственных мыслей и их словесном выражении, нарушение концентрации: чтобы выполнить определенную работу, пациенты вынуждены делать перерыв, при решении поставленной задачи пытаются обдумывать ее не в целом, а разбив на части. Однако это не приносит желаемых результатов, а еще больше усиливает чувство усталости, увеличивает беспокойство и вызывает чувство собственной интеллектуальной несостоятельности.
Вегетативные расстройства проявляются тахикардией, лабильностью пульса, перепадами артериального давления, познабливанием или чувством жара в теле, генерализованным или локальным (ладони, подмышки, ступни) гипергидрозом, снижением аппетита, запорами, болевыми ощущениями в кишечнике и снижением потенции. Также при астении пациентов нередко беспокоит головная боль или чувство тяжести в голове.
Среди последствий ЧМТ головная боль занимает основное место, поскольку является самым частым симптомом при всех формах черепно-мозговой травмы и во всех периодах заболевания. Около 80–90 % людей, перенесших ЧМТ, впоследствии жалуются на головную боль.
В соответствии с Международной классификацией головной боли, посттравматическая головная боль (ПТГБ) разделяется на острую и хроническую. ПТГБ считается острой, если возникает в первые 14 дней после ЧМТ и длится не больше 8 недель после травмы. Для хронической ПТГБ также характерно возникновение головной боли в первые 14 дней после травмы, однако ее продолжительность составляет более 8 недель после ЧМТ.
Причинами острой головной боли, связанной с ЧМТ, могут быть: повреждение мягких тканей головы и шеи, изменения ликвородинамики, травматическое субарахноидальное кровоизлияние или внутричерепная гематома. Максимальная головная боль наблюдается в остром периоде, постепенно уменьшаясь. Если у больного со временем боль не регрессирует, то, исключив серьезную органическую патологию, следует искать психологические причины ее возникновения.
В отличие от симптоматической острой ПТГБ хроническая носит самостоятельный характер и не зависит от тяжести черепно-мозговой травмы и неврологических дефектов. Кроме головной боли, определяются снижение концентрации внимания, повышенная утомляемость, ухудшение памяти и эмоциональная лабильность. Обычно выделяют следующие клинические формы хронической ПТГБ: головная боль напряжения, мигренеподобные, невралгические и цервикогенные боли. Считается, что главная роль в возникновении хронической ПТГБ принадлежит психосоциальным факторам. У таких пациентов задолго до перенесенной травмы головные боли наблюдались в несколько раз чаще, чем в здоровой популяции. Травма лишь привлекает внимание к расстройствам, которые существовали раньше, но оставались незамеченными. Кроме того, сама травма может выступать не столько как травма мозга, сколько как психологическая травма. Также хроническая ПТГБ нередко наблюдается у лиц, склонных к ипохондрической интерпретации чувств с дистимическими и конверсионными реакциями. Кроме того, неблагоприятными факторами, способствующими хронизации ПТГБ, считаются: особенности структуры личности, злоупотребление анальгетиками, возраст старше 40–50 лет на момент травмы, слишком длительный постельный режим, ятрогенные влияния.
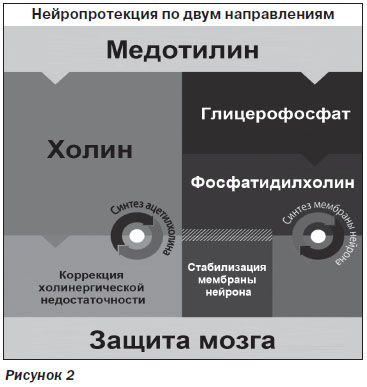
Для улучшения прогноза ЧМТ и увеличения вероятности полного выздоровления при данной патологии показано назначение Медотилина. Он улучшает передачу нервных импульсов в холинергических нейронах, позитивно влияет на пластичность нейрональных мембран и функцию рецепторов, улучшает церебральный кровоток, усиливает метаболические процессы в головном мозге, восстанавливает сознание при травматическом повреждении головного мозга (рис. 2).
Действующее вещество Медотилина холина альфосцерат. Эффективность и безопасность применения холина альфосцерата при ЧМТ имеют большую доказательную базу. Так, в исследовании Т. Mandat, А. Wilk et al., проведенном в клинике нейрохирургии центрального госпиталя Военной медицинской академии, Институте травматологии, ортопедии и нейрохирургии в Варшаве, при участии пациентов с ЧМТ было показано, что применение холина альфосцерата обеспечивает улучшение состояния в 96 % случаев, при этом полное восстановление неврологических функций наблюдалось у 61 % больных (рис. 3).

Лечение ПТГБ должно включать анальгетические средства, среди которых предпочтительнее использование нестероидных противовоспалительных препаратов. Важная роль в коррекции посттравматических цефалгий принадлежит рациональной терапии антидепрессантами и ноотропами.
К немедикаментозным методам терапии ПТГБ относятся:
— иглорефлексотерапия, массаж, лечебная физкультура;
— психотерапия: суггестивная (гипноз, плацебо-терапия) и аналитическая (транзактный анализ). Гипнотерапия — метод, основанный на лечебном настрое в состоянии гипнотического сна. Применяется в основном при наличии стойкого и/или интенсивного болевого синдрома, который отвечает объективным изменениям в неврологическом статусе, а также при наличии выраженной психопатологической симптоматики. Плацебо-терапия наиболее эффективна при наличии выраженной конверсионной симптоматики и ежедневном приеме анальгетических средств. Транзактный анализ — метод, основанный на перестройке отношений пациента с социальным окружением, с анализом внутриличностных проблем и принятием пациентом новых решений относительно собственной жизни.
От редакции
Недавно в арсенале украинских врачей появился препарат Элфунат, представляемый на фармацевтическом рынке Украины компанией World Medicine. Действующим веществом Элфуната является этилметилгидроксипиридина сукцинат (в 1 мл препарата содержится 50 мг действующего вещества).
Этилметилгидроксипиридина сукцинат относится к классу 3-оксипиридинов и является ингибитором свободнорадикальных процессов, мембранопротектором, оказывает антигипоксическое, стрессопротекторное, ноотропное, противосудорожное и анксиолитическое действие. Препарат повышает резистентность организма к действию вредных факторов, к кислородозависимым патологическим состояниям, улучшает мозговой метаболизм и кровоснабжение головного мозга, микроциркуляцию и реологические свойства крови, уменьшает агрегацию тромбоцитов, стабилизирует мембранные структуры клеток крови при гемолизе. Этилметилгидроксипиридина сукцинат ингибирует перекисное окисление липидов, повышает активность супероксиддисмутазы, повышает соотношение липид ― белок, уменьшает вязкость мембраны, увеличивает ее текучесть. Этилметилгидроксипиридина сукцинат повышает концентрацию дофамина в головном мозге. Вызывает усиление компенсаторной активации аэробного гликолиза и снижение степени угнетения окислительных процессов в цикле Кребса в условиях гипоксии с повышением содержания аденозинтрифосфата и креатинфосфата, активацию энергосинтезирующих функций митохондрий, стабилизацию клеточных мембран. Показанием к применению препарата этилметилгидроксипиридина сукцината Элфунат в неврологии является острая и хроническая церебральная недостаточность (черепно-мозговые травмы и их последствия, острые и хронические нарушения мозгового кровообращения, когнитивные нарушения).