Журнал "Гастроэнтерология" 4 (62) 2016
Вернуться к номеру
Применение эссенциальных фосфолипидов для лечения жировой болезни печени
Авторы: Степанов Ю.М. - ГУ «Институт гастроэнтерологии НАМН Украины», г. Днепр, Украина
Рубрики: Гастроэнтерология
Разделы: Справочник специалиста
Версия для печати
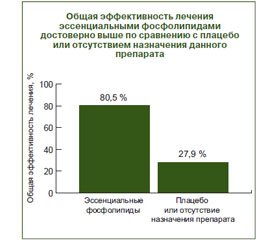
Передумови. З урахуванням схожості гістопатологічного патерну неалкогольної жирової хвороби печінки та алкогольної хвороби печінки було запропоновано обидва захворювання об’єднати в одну нозологічну форму під загальною назвою «жирова хвороба печінки». Методологія. При виконанні даного огляду був проведений повторний аналіз 25 досліджень, включених в огляд K.J. Gundermann зі співавт. (2016). У цих роботах вивчали ефективність і безпечність есенціальних фосфоліпідів, що були отримані з соєвих бобів і містили не менше 72 % фосфатидилхоліну. Результати. При аналізі 20 досліджень із неалкогольної жирової хвороби печінки було з’ясовано, що есенціальні фосфоліпіди зменшували вираженість симптомів, у тому числі загального нездужання, стомлюваності, нудоти, частоту болю в правому підребер’ї, здуття живота, закрепів, індекс ожиріння та товщину шкірної складки. Було відзначено позитивний вплив есенціальних фосфоліпідів на лабораторні показники плазми крові (функціональні тести печінки — аланінамінотрансфераза, аспартатамінотрансфераза, гамма-глутамілтранспептидаза, лужна фосфатаза; показники ліпідного обміну — загальний холестерин, тригліцериди, холестерин ліпопротеїнів низької щільності). Есенціальні фосфоліпіди покращували дані ультразвукового дослідження та комп’ютерної томографії печінки в 60–75 % пацієнтів. Одночасно спостерігалася ревертація гістопатологічних змін у печінці: зменшувалася вираженість стеатозу, балонування, інтраацинарного та портального запалення, що призводило до зниження стадії стеатогепатиту за класифікацією Brunt. Загальна ефективність лікування есенціальними фосфоліпідами становила 80,5 %, тоді як у групах плацебо або відсутності призначення препарату — 27,9 % (p < 0,05). При вивченні 5 досліджень з алкогольної хвороби печінки були зафіксовані подібні результати, однак для їх верифікації необхідно виконати більшу кількість досліджень. Дані всіх названих вище досліджень свідчать про те, що лікування есенціальними фосфоліпідами було безпечним. Висновки. У 25 клінічних дослідженнях були підтверджені ефективність і безпека есенціальних фосфоліпідів при лікуванні жирової хвороби печінки.
Предпосылки. С учетом сходства гистопатологического паттерна неалкогольной жировой болезни печени и алкогольной болезни печени было предложено оба заболевания объединить в одну нозологическую форму под общим названием «жировая болезнь печени». Методология. При выполнении данного обзора был проведен повторный анализ 25 исследований, включенных в обзор K.J. Gundermann и соавт. (2016). В этих работах изучали эффективность и безопасность эссенциальных фосфолипидов, полученных из соевых бобов и содержащих не менее 72 % фосфатидилхолина. Результаты. При анализе 20 исследований по неалкогольной жировой болезни печени было выявлено, что эссенциальные фосфолипиды уменьшали выраженность симптомов, в том числе общего недомогания, утомляемости, тошноты, частоту возникновения боли в правом подреберье, вздутия живота, запоров, индекс ожирения и толщину кожной складки. Было отмечено положительное влияние эссенциальных фосфолипидов на показатели плазмы крови (функциональные тесты печени — аланинаминотрансфераза, аспартатаминотрансфераза, γ-глутамилтранспептидаза, щелочная фосфатаза; показатели липидного обмена — общий холестерин, триглицериды, холестерин липопротеинов низкой плотности). Эссенциальные фосфолипиды улучшали данные ультразвукового исследования и компьютерной томографии печени у 60–75 % пациентов. Одновременно наблюдалась ревертация гистопатологических изменений в печени: уменьшалась выраженность стеатоза, баллонирования, интраацинарного и портального воспаления, что приводило к снижению стадии стеатогепатита по классификации Brunt. Общая эффективность лечения эссенциальными фосфолипидами составила 80,5 %, в то время как в группах плацебо или отсутствия назначения препарата — 27,9 % (p < 0,05). При изучении 5 исследований по алкогольной болезни печени были зафиксированы сходные результаты, однако для их верификации необходимо выполнить большее количество исследований. Данные всех вышеназванных исследований свидетельствуют о том, что лечение эссенциальными фосфолипидами было безопасным. Выводы. В 25 клинических исследованиях были подтверждены эффективность и безопасность эссенциальных фосфолипидов при лечении жировой болезни печени.
Background. Given the similarity of histopathological pattern of non-alcoholic fatty liver disease and alcoholic liver disease, it was proposed to combine these both diseases in one nosological form named «fatty liver disease». The purpose of this review was to evaluate the efficacy and safety of essential phospholipids for the treatment of fatty liver disease. Methodology. When performing this review, re-analysis of 25 studies included in the review K.J. Gundermann et al. (2016), has been made. In these studies, essential phospholipids were obtained from soybeans containing not less than 72 % phosphatidylcholine. Results. It was found that essential phospholipids reduce the severity of symptoms, including general malaise, fatigue, nausea, incidence of hepatic pain, abdominal distension, constipation, obesity index and skin-fold thickness when used in nonalcoholic fatty liver disease (20 studies). Essential phospholipids were found to improve biochemical blood plasma markers (liver function tests — alanine aminotransferase, serum glutamic oxalacetic transaminase, gamma-glutamyl transpeptidase, alkaline phosphatase, markers of lipid metabolism — total cholesterol, triglycerides, LDL cholesterol). Essential phospholipids improved the results of sonography and computed tomography of the liver in 60–75 % of patients. At the same time there observed the reverse of histopathological changes in the liver: decreased severity of steatosis, ballooning, intra-acinar and portal inflammation, leading to a decrease of the stage of steatohepatitis by Brunt classification. The total efficiency of the treatment with essential phospholipids was 80.5 %, while the total efficiency of the treatment in the placebo or «no treatment» groups was 27.9 % (p < 0.05). Similar results were obtained for the alcoholic liver disease (5 studies), but more researches are needed. Data from all the above cited studies suggest that the treatment of essential phospholipids was safe. Conclusion. In 25 clinical studies it was confirmed the effectiveness and safety of the essential phospholipids for the treatment of fatty liver disease.
есенціальні фосфоліпіди, жирова хвороба печінки.
эссенциальные фосфолипиды, жировая болезнь печени.
essential phospholipids, fatty liver disease.
Статья опубликована на с. 58-64
Жировая болезнь печени
Эссенциальные фосфолипиды
Методология обзора
Неалкогольная жировая болезнь печени
/60.jpg)
Ультразвуковое исследование и компьютерная томография
/60_2.jpg)
Гистологические изменения
Общая эффективность лечения
/62.jpg)
Алкогольная болезнь печени
Безопасность
Заключение
1. Sass D.A., Chang P., Chopra K.B. Nonalcoholic fatty liver disease: a clinical review // Dig. Dis. Sci. — 2005. — Vol. 50, № 1. — P. 171-180.
2. Nonalcoholic steatohepatitis: Mayo Clinic experiences with a hitherto unnamed disease / Ludwig J., Viggiano T.R., McGill D.B., Oh B.J. // Mayo Clin. Proc. — 1980. — Vol. 55, № 7. — P. 434-438.
3. Partha P., Sayantan R. Alcoholic liver disease: a comprehensive review // EMJ. — 2016. — Vol. 1, № 2. — P. 85-92.
4. Völzke H. Multicausality in fatty liver disease: is there a rationale to distinguish between alcoholic and non-alcoholic origin? // World J. Gastroenterol. — 2012. — Vol. 18, № 27. — P. 3492-3501.
5. Essential phospholipids // http://www.titanbiotechltd.com
6. PhosChol Prescribing Information // http://www.phoschol.com
7. Kidd P. Phosphatidylcholine: a superior protectant against liver damage // Alt. Med. Rev. — 1996. — Vol. 1, № 4. — P. 258-274.
8. Activity of essential phospholipids (EPL) from soybean in liver diseases / Gundermann K.J., Kuenker A., Kuntz E., Droździk M. // Pharmacol. Rep. — 2011. — Vol. 63, № 3. — P. 643-659.
9. Essential phospholipids in fatty liver: a scientific update / Gundermann K.J., Gundermann S., Drozdzik M., Mohan Prasad V.G. // Clin. Exp. Gastroenterol. — 2016. — Vol. 9. — P. 105-117.
10. Энерлив // http://compendium.com.ua
11. Multimodal treatment resulting in rapid improvement of fatty liver in obese patients / Watanabe A., Kobayashi M., Morishita N., Nagashima H. // Curr. Ther. Res. — 1988. — Vol. 43, № 2. — P. 239-246.
12. Randomised placebo-controlled double blind trial on «essential» phospholipids in the treatment of fatty liver associated with diabetes / Gonciarz Z., Besser P., Lelek E. et al. // Méd. Chir. Dig. — 1988. — Vol. 17, № 1. — P. 61-65.
13. Polyunsaturated phosphatidylcholine combined with vitamin B complex in the treatment of patients with disorders of the hepatobiliary function caused by unbalanced nutrition // Cairella M., Callisto F., Godi R., Marchini G. // Clin. Ter. — 1989. — Vol. 131, № 4. — P. 237-246.
14. Clinical progress of 51 fatty liver cases analyzed by liver function tests and ultrasonic screening and results of EPL administered cases / Koga S., Irisa T., Miyata Y. et al. // Prog. Med. — 1991. — Vol. 11, № 7. — P. 1891-1899.
15. A randomized controlled study of essential phospholipids (Essentiale capsules) in the treatment of fatty liver / Li J.H., Chen X.Y., Zhong C.F., Min J. // Infect. Dis. Info. — 2000. — Vol. 13, № 4. — P. 180-181.
16. Yin D., Kong L. Observation for curative effect of Essentiale in treatment of fatty liver caused by diabetes mellitus // Med. J.Q. Ilu. — 2000. — Vol. 15. — P. 277-278.
17. Ohbayashi H. Twelve-month chronic administration of polyenephosphatidylcholine (EPL®) for improving hepatic function of fatty liver patients // Prog. Med. — 2004. — Vol. 24, № 7. — P. 1751-1756.
18. Effect of essentiale in diabetic subjects with non-alcoholic fatty liver / Poongothai S., Karkuzhali K., Siva Prakash G. et al. // Int. J. Diab. Dev. Ctries. — 2005. — Vol. 25, № 1. — P. 12-19.
19. The therapeutic effect of polyenephosphatidylcholine (EPL) on NASH / Ohbayashi H., Fujimoto M., Yoshida M. et al. // Liver Bile Pancreas. — 2006. — Vol. 52, № 4. — P. 637-642.
20. Liang H. Treatment of fatty liver applying polyene phosphatidyl choline // Chin. Med. Factory Mine. — 2006. — Vol. 19, № 3. — P. 207-208.
21. Arvind N., Savaikar P., Rajkumar J.S. Therapy for NAFLD-comparative study of essential phospholipids vs ursodeoxycholic acid // Ind. J. Clin. Pract. — 2006. — Vol. 16, № 10. — P. 21-24.
22. Improvement of NASH with two-year treatment with oral polyenephosphatidylcholine / Ohbayashi H., Fujimoto M., Yamase H., Ito M. // J. Rural Med. — 2007. — Vol. 1. — P. 67-73.
23. Shen Z. Observation of efficacy in 100 patients with non-alcoholic fatty liver disease treated with Essentiale // Chin. J. Curr. Clin. Med. — 2007. — Vol. 5, № 8. — P. 693-694.
24. Application of essential phospholipids in complex therapy of steatohepatitis of the mixed origin / Buyeverov A.O., Yeshanu V.S., Mayevskaya M.V., Ivashkin V.T. // Klin. Persp. Gastroenterol. Hepatol. — 2008. — Vol. 1. — P. 17-22.
25. Clinical observation on polyene phosphatidyl choline and metformin in the treatment of type 2 diabetes and non-alcoholic fatty liver disease / Sun C., Zheng X., Tan Z. et al. // Clin. Focus. — 2008. — Vol. 23, № 17. — P. 1272-1273.
26. Zhuang X.S., Zhang Z.J. Study of ursodeoxycholic acid (UDCA) combined with polyene phosphatidylcholine in the treatment of non-alcoholic steatohepatitis // China Pract. Med. — 2009. — Vol. 4, № 10. — P. 11-12.
27. Zhou S.Y., Sun Z.Y. Therapeutic efficacy of polyunsaturated phosphatidylcholine on fatty liver disease // J. Clin. Hepatol. — 2010. — Vol. 26, № 3. — P. 286-287.
28. Effect of Xuezhikang capsule on serum tumor necrosis factor-α and interleukin‑6 in patients with nonalcoholic fatty liver disease and hyperlipidemia / Fan X., Deng Y., Ye L. et al. // Chin. J. Integr. Med. — 2010. — Vol. 16, № 2. — P. 119-123.
29. Guo X.L., Liang P.X., Xu Y.Q. Comparison of efficacies of diammonium glycyrrhizinate and polyene phosphatidylcholine on nonalcoholic steatohepatitis // Chin. J. New Drugs. — 2012. — Vol. 21, № 3. — P. 289-293.
30. Beneficial influence of polyunsaturated phosphatidylcholine enhances functional liver condition and liver structure in patients with nonalcoholic steatohepatitis accompanied by diabetes type 2. Results of prolonged randomized blinded prospective clinical study / Sas E., Grinevich V., Efimov O., Shcherbina N. // J. Hepatol. — 2013. — Vol. 58. — P. S549.
31. Knüchel F. Double-blind study in patients with alcoholic fatty liver. The influence of «essential» phospholipids on enzyme behaviour and lipid composition of the serum // Med. Welt. — 1979. — Vol. 30, № 11. — P. 411-416.
32. Schüller Pérez A., Gonzáles San Martin F. Placebo-controlled study with polyunsaturated phosphatidylcholine in alcoholic steatosis of the liver // Med. Welt. — 1985. — Vol. 36, № 16. — P. 517-521.
33. Polyunsaturated phosphatidyl choline for acute alcoholic hepatitis: a double-blind, randomized, placebo-controlled trial / Panos M.Z., Polson R., Johnson R. et al. // Eur. J. Gastroenterol. Hepatol. — 1990. — Vol. 2, № 5. — P. 351-355.
34. Veterans Affairs Cooperative Study 391 Group. II. Veterans affairs cooperative study of polyenylphosphatidylcholine in alcoholic liver disease / Lieber C.S., Weiss D.G., Grozmann R. et al. // Alcohol. Clin. Exp. Res. — 2003. — Vol. 27, № 11. — P. 1765-1772.
35. Polyunsaturated phosphatidylcholine reduces insulin resistance and hepatic fibrosis in patients with alcoholic liver disease: results of randomized blinded prospective clinical study / Sas E., Grinevich V., Kravchuk U., Efimov O. // J. Hepatol. — 2011. — Vol. 54. — P. S207.

/58.jpg)
/61.jpg)