Пациент, 1988 года рождения, направлен для проведения допплер-УЗИ почечной артерии трансплантированной почки в связи с подозрением на ее стеноз. Из анамнеза стало известно, что 20.04.2016 г. пациенту была успешно проведена трансплантация трупной почки. Последний месяц функция почки без видимой причины стала резко снижаться, проведена эффективная терапия по купированию криза отторжения. Однако сохраняется артериальная гипертензия 2-й степени, низкая рСКФб, соответствующая ХБП 3б–4-й стадии. Возникло предположение о стенозе почечной артерии, что подтвердилось при рутинном допплер-УЗИ. С целью экспертной оценки возникшего предположения пациент подвергнут данному исследованию.
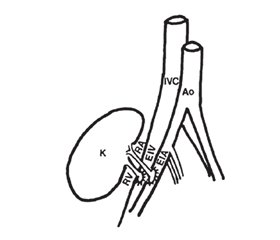
Анатомическая справка представлена на рис. 1.
Протокол допплер-УЗИ трансплантированной почки
В правой подвздошной области на уровне крыла ПВК визуализирована трансплантированная почка, расположенная в типичном для операций такого рода месте. Почка бобовидной формы 111 × 60 × 41 мм, объем 141,9 см3, контур четкий, ровный.
Паренхима однородна, без очаговых уплотнений, умеренно сниженной эхогенности, умеренно дольчатая, толщина 18–21 мм. Почечный синус не деформирован, в центральной части определяется колонка Бертини. Чашечки не расширены. Лоханка щелевидной формы, ее стенки умеренно утолщены (1–2 мм), феномен двухконтурности.
При ЦДК отмечается выраженная асимметрия кровотока по сегментам (рис. 2, 3).
От общей подвздошной артерии прослеживается два анастомоза: к воротам почки (основная артерия) и к нижнему сегменту (добавочная артерия). Обе артерии умеренно извиты, основная артерия несколько длиннее, чем добавочная. Кровоток прослеживается в обеих артериях.
В истоке в основной артерии в области анастомоза регистрируется скорость более 200 см/с, дистальнее отмечается снижение скорости и появление постстенотического спектра кровотока. Бассейн основной артерии занимает примерно 2/3 почки и распространяется на ее верхний и средний сегменты. В междольковых и стриарных артериях бассейна кровоток обеднен, спектры кровотока по типу «tardus-parvus», скорости низкие,
RI 0,32–0,42.
В добавочной артерии к нижнему полюсу кровоток прослеживается на всем протяжении, –спектры типичные, в истоке ПСС до 100 см/с, RI 0,77. Бассейн добавочной артерии занимает примерно 1/3 почки и распространяется на нижний сегмент. В междольковых и стриарных артериях бассейна кровоток хорошо прослеживается во всех отделах, спектры кровотока типичные, скорость в пределах нормы, RI 0,6.
С помощью сдвиговолновой эластографии была оценена жесткость (модуль Юнга — МЮ) паренхимы почки в различных сегментах. Всего было сделано 4 замера в бассейне добавочной артерии (нижний сегмент почки) и 4 замера в бассейне основной артерии (верхний и средний сегменты почки).
Отмечается существенная асимметрия жесткости паренхимы сегментов с сохраненным кровотоком (26,75 ± 5,31 кПа) и постстенотическим кровотоком (10,06 ± 3,19 кПа). Результаты представлены в табл. 1.
Исследование от 13 декабря 2016 г. после баллонной дилатации (17 ноября 2017 г.) стенозированной основной артерии
В правой подвздошной области на уровне крыла ПВК визуализирована трансплантированная почка, расположенная в месте, типичном для такого рода операций. Почка бобовидной формы, 112 × 54 × 40 мм, объем 128,6 см3, контур четкий, ровный. Паренхима однородна, без очаговых уплотнений, умеренно сниженной эхогенности, умеренно дольчатая, толщина 15–17 мм. Почечный синус не деформирован, в центральной части определяется колонка Бертини. Чашечки не расширены. Лоханка щелевидной формы, стенки умеренно утолщены (1–2 мм), феномен двухконтурности.
При ЦДК отмечаются аналогичный предыдущему исследованию кровоток в нижнем сегменте и улучшение перфузии в срединном и верхнем сегментах (рис. 5).
/95-1.gif)
От общей подвздошной артерии прослеживаются два анастомоза: к воротам почки (основная артерия) и к нижнему сегменту (добавочная артерия). Обе артерии умеренно извиты, основная артерия несколько длиннее, чем добавочная. Кровоток прослеживается в обеих артериях. В основной артерии к воротам на всем протяжении до ворот скорость около 180 см/с, RI 0,73. Бассейн основной артерии занимает примерно 2/3 почки и распространяется на ее верхний и средний сегменты. В междольковых и стриарных артериях бассейна кровоток определяется во всех отделах, спектры типичные, ПСС 24–35 см/с, RI 0,55–0,61, явное улучшение перфузии по сравнению с показателем при исследовании 15.11.16, но несколько ниже кровотока в нижнем полюсе из бассейна добавочной артерии. В артерии к нижнему полюсу кровоток прослеживается на всем протяжении, ПСС около 90 см/с, RI 0,67, бассейн занимает примерно 1/3 часть почки, в междольковых и стриарных артериях скорость 33–40 см/с, RI 0,61–0,66.
С помощью сдвиговолновой эластографии мы оценили жесткость (модуль Юнга) паренхимы почки в различных сегментах. Всего было сделано 4 замера в бассейне добавочной артерии (нижний сегмент почки) и 4 замера в бассейне основной артерии (верхний и средний сегменты почки). Результаты представлены в табл. 2.
После баллонной дилатации стенозированной артерии и восстановления перфузии почки жесткость составляла 30,4 ± 6,5 и 15,4 ± 2,4 кПа в нижнем и средне-верхнем сегментах соответственно.
Обсуждение
Методика, физические принципы, артефакты сдвиговолновой эластографии (SWE) подробно описаны многими авторами (Yang J.R. 2016; Дынник О.Б, 2014). В настоящее время методика хорошо зарекомендовала себя в оценке стадии фиброза печени или очаговой патологии печени, дифференциальной диагностике доброкачественных и злокачественных образований молочной и щитовидной желез. В литературе встречаются достаточно противоречивые сообщения о жесткости паренхимы как нормальных, так и патологически измененных почек, при этом значения жесткости (модуля Юнга) паренхимы почек у разных авторов существенно отличаются. Grenier с соавт. указывают, что у здоровых добровольцев жесткость кортикального слоя была 15,4 ± 2,5 кПа, а медуллярного — 10,8 ± 2,7 кПа. A.E. Samir с соавт. (2015) показали, что жесткость паренхимы нормальной почки составляла 4,40 (3,68–5,70) кПа, а паренхима у больных хроническими заболеваниями почек — 9,40 (5,55–22,35) кПа (p = 0,002) (Samir, 2015). По мнению Grenier с соавт. (2013), это связано с техническими ограничениями сдвиговолновой эластографии, точность измерения которой ограничена глубиной 5 см. Анатомическая локализация трансплантата дает возможность с высокой точностью оценить жесткость паренхимы почки. По данным S. Brocchi с соавт. (2014), жесткость паренхимы нормально работающей трансплантированной почки составляет 34,06 ± 10,72 кПа. Однако, по данным J.R. Yang (2016), в трансплантированных почках при нормальном функционировании жесткость достигает 24,41 кПа, при хронической нефропатии аллотрансплантата (CAN) она увеличивается до 36,9 кПа.
Наши данные в обоих наблюдениях для нижнего полюса с постоянно сохраненной перфузией демонстрируют сходные результаты. Нарушение кровотока в верхнем и срединном сегментах привело к существенному снижению жесткости паренхимы. Несмотря на то, что кровоток в основной артерии после баллонной дилатации практически нормализовался, жесткость паренхимы остается сниженной.
Теоретически считается, что чем больше выражен фиброз паренхимы при диффузных заболеваниях и чем активнее воспаление, тем выше должна быть скорость распространения волн сдвига и выше значение модуля Юнга (жесткости) ткани. Для печени этот критерий стал надежной мерой при оценке стадии фиброза при хронических гепатитах (Bota, 2014; Zaffanello, 2015). По-видимому, жесткость почечной паренхимы также существенно зависит от состояния перфузии кровью, артериального давления и других сердечно-сосудистых параметров (Zaffanello, 2015). Это приводит к тому, что жесткость паренхимы почки снижается с возрастом (Zaffanello, 2015).
Ввиду очень малого количества таких сообщений при описании данного клинического наблюдения мы приводим констатацию факта снижения жесткости при ишемии почки за счет стеноза приводящей артерии.
Вместе с тем технология сдвиговолновой эластографии в реальном времени может обеспечить представление количественных показателей состояния паренхимы почки, что позволяет избежать негативного влияния субъективных факторов в ходе диагностического процесса.
Сдвиговолновая эластография может отражать следующие гистологические комбинации: ишемическая болезнь почек (гломерулосклероз и т.п.), заболевания трансплантата (например, утолщение или истончение клубочковой базальной мембраны, увеличение мезангиальной матрицы и т.д.), интерстициальный фиброз, атрофия канальцев, атеросклероз, гиалиновая дегенерация артериол, фиброзное утолщение интимы артерии и отслаивание или разрушение капиллярной базальной мембраны, прогрессивный фиброз. Причем изменение жесткости может быть одним из критериев нормализации кровообращения при восстановительной сосудистой терапии/хирургии.
Принято считать, что почки становятся жесткими, а эластичность и податливость уменьшаются в ответ на развитие атрофии в клубочках петель, а также утолщение базальной мембраны, развитие гломерулосклероза и интерстициального фиброза. Однако сосудистый компонент также существенно влияет на механические свойства тканей.
Таким образом, эластография может быть рекомендована для выявления хронического отторжения трансплантата и нарушений метаболизма ткани почки при возникновении транзиторных нарушений.
Конфликт интересов. Получено информированное согласие пациента на публикацию истории его болезни.
Благодарности. Автор приносит искреннюю благодарность медицинским работникам г. Гомеля, проводившим биопсию и бесконтрастное исследование, сотрудникам отделений трансплантации, функциональной диагностики и сосудистой хирургии Института хирургии имени акад. А. Шалимова.
Комментарий специалиста
Иванов Д.Д.,
зав. кафедрой нефрологии и почечно-заместительной терапии НМАПО имени П.Л. Шупика
В представленном клиническом наблюдении экспертное заключение врача УЗ-диагностики потребовалось для подтверждения наличия стеноза почечной артерии и оценки увеличения плотности почечной ткани как возможного прогностического показателя выживаемости трансплантата. Данному исследованию предшествовали:
1. Развитие острого повреждения почки 3-й стадии непосредственно после трансплантации почки с последующим восстановлением ее функции до рСКФ 60–75 мл/мин.
2. Развитие криза отторжения спустя 6 месяцев после проведенной трансплантации, в связи с чем была выполнена биопсия почки, подтвердившая активное антителоопосредованное отторжение трансплантата.
3. Проведение консультации с проф. Л. Ростангом (Франция), после чего была успешно использована схема подавления отторжения, включавшая в себя плазмаферез 1,5 л № 7, синхронизированный с пульс-терапией метипредом, введением ритуксимаба и иммуноглобулина.
4. После подавления криза отторжения пациенту была прекращена диализная помощь, но сохранялась низкая рСКФ (18–22 мл/мин), возникло предположение о наличии стеноза почечной артерии. Проведение рентгеноконтрастной ангиографии было невозможным при такой скорости клубочковой фильтрации ввиду крайне высокого риска развития острого повреждения почек, в связи с чем выполнено допплер-УЗИ с эластографией (см. выше) и бесконтрастное исследование (г. Гомель) (рис. 1), при котором установлено два участка стеноза с –сужением более 75 %.
17.11.2016 пациенту выполнена баллонная дилатация участков стеноза в Институте хирургии им. акад. А. Шалимова, после которой отмечается стабилизация показателей АД, модифицированного кардосалом, моксогаммой и небилетом в пределах 135–144/85–90 мм рт.ст., рСКФ 30 мл/мин, альбуминурия 80–120 г/л.
Комментарий специалиста
Дядык Е.А.,
зав. кафедрой патологической и топографической анатомии НМАПО имени П.Л. Шупика, д.м.н., профессор
1. 19.11.2008 г. проведено первое морфологическое исследование почек, № 60999-6101/2008 г.
Заключение: мезангиокапиллярный гломерулонефрит с тенденцией к экстракапиллярному компоненту, с выраженными нарушениями тубулярного эпителия, с депозитами IgG, IgA, в меньшей степени — IgМ в базальной мембране и эндотелии капилляров клубочков, в меньшей степени — депозитами в мезангиуме, с депозитами IgG, IgA в эпителии канальцев и в строме между канальцами.
2. 31.10.2014 г. проведено повторное морфологическое исследование почек, № 14CSD18696.
Заключение: мезангиокапиллярный гломерулонефрит с умеренным тубулоинтерстициальным компонентом, признаками хронизации процесса (начальным гломерулосклерозом, атрофией эпителия, очаговым интерстициальным фиброзом), субэндотелиальными депозитами IgG, IgM, в меньшей степени — IgA, C3, мезангиальными депозитами иммуноглобулинов, выраженными депозитами иммуноглобулинов, в меньшей степени — комплемента С3 в эпителии канальцев и в строме.
Была проведена оценка лечебного патомор–фоза.
При сравнении морфологических изменений первичной и повторной биопсий отмечается нарастание признаков хронизации заболевания — начальный гломерулосклероз, атрофия эпителия канальцев, очаговый интерстициальный фиброз, однако не отмечен экстракапиллярный компонент как показатель активности. Наряду с признаками хронизации имеет место выраженная депозиция иммуноглобулинов, фракции комплемента С3 в эпителии канальцев, в строме между канальцами, что является проявлением активных изменений в тубулоинтерстициальном аппарате.
3. 15.08.2016 г. проведено морфологическое исследование почечного трансплантата. В биоптате до 18 клубочков, один гиалинизирован полностью, в двух клубочках — коллапс капиллярных петель (рис. 1); в просвете капсулы Боумена — экссудат (фибрин); в клубочках неравномерная, от слабой до умеренной степени выраженности (в некоторых клубочках), пролиферация мезангиальных клеток, набухание и — в части клубочков — пролиферация эндотелиальных клеток (рис. 2); часть капиллярных петель неравномерно утолщена (за счет фибриноидных изменений и фибриноидного некроза); в части капиллярных петель (от 25 до 50 %) отмечается расщепление базальных мембран (по типу двойного контура), в части капиллярных петель — склероз; в зоне мезангиума, в просвете капиллярных петель — очаговая инфильтрация моноцитами, реже — полиморфно-ядерными лейкоцитами, очаговое неравномерно выраженное увеличение мезангиального матрикса; в 2 клубочках — фиброклеточные полулуния, в одном занимающее 2/3 периметра, в одном — 1/3; в 6 клубочках — сращения периферических капиллярных петель с эпителием капсулы Боумена практически по всему периметру (рис. 1); неравномерно выраженное утолщение и очаговое расщепление базальной мембраны капсулы Боумена.
В канальцах дистрофические изменения (по типу вакуольной, очаговой баллонной дистрофии), некроз групп клеток, очаги атрофии эпителия канальцев с утолщением и очаговым расщеплением тубулярной базальной мембраны. В эпителии канальцев — мононуклеарная, лимфоцитарная инфильтрация (от слабой до умеренно выраженной), в просвете части канальцев встречаются лимфоциты, моноциты. Часть перитубулярных капилляров расширена, в некоторых из них — очаговое утолщение стенки, расщепление базальной мембраны, в части капилляров в просвете лимфоциты, моноциты. В просвете канальцев — гиалиновые цилиндры, слущенные клетки, белковые массы. В строме — отек, очаги начального интерстициального фиброза (рис. 2), в том числе и периваскулярного; очаговые разной распространенности, лимфогистиоцитарные с примесью моноцитов, единичных плазматических клеток перигломерулярные, интертубулярные, периваскулярные инфильтраты. В части сосудов мелкого калибра — утолщение стенки за счет дисмукоидоза, очаговая инфильтрация моноцитами, лимфоцитами, в некоторых сосудах среднего и более крупного калибра — утолщение стенки, отек клеток эндотелия, очаговая инфильтрация моноцитами, очаги фибриноидных изменений, дисмукоидоз в стенке, очаговый эластофиброз, явления спазма, в некоторых сосудах — склероз (рис. 3).
/101-1.gif)
/101-2.gif)
Иммуноморфологическое исследование:
D68: в клубочках единичные макрофаги, макрофаги между канальцами, в некоторых перитубулярных капиллярах, в клеточных инфильтратах, в интиме части сосудов.
С3: в клубочках разного размера гранулярные субэндотелиальные, мезангиальные очаговые депозиты от ++ до +++, в эндотелии части капиллярных петель депозитов от + до ++, очаговые депозиты в строме между канальцами, в перитубулярных капиллярах депозитов от ++ до +++, в эпителии канальцев депозиты в виде зернистости до +++.
CD3: в клубочках единичные Т-лимфоциты, много Т-лимфоцитов в клеточных инфильтратах, в эндотелии части сосудов, в эпителии некоторых канальцев — позитивное окрашивание.
CD20: в клубочках нет окраски, от небольшого до умеренного количества В-лимфоцитов в клеточных инфильтратах разной локализации.
Заключение: морфологические и иммуногистохимические данные свидетельствуют в пользу хронического активного антителоопосредованного отторжения трансплантата с проявлениями трансплантационной гломерулопатии, признаками хронического активного Т-клеточноопосредованного отторжения трансплантата, начальным интерстициальным фиброзом и атрофией эпителия канальцев (t2, v1-2, i1, g1, рtc1; сi1, ct2, сg2, mm1, cv1-2, ah1) (Banff Сlassification, 2007).
Список литературы
1. Динник О.Б. Ультразвукова еластографія: теорія і практика створення навчального тренажера / О.Б. Динник, М.М. Жайворонок, Н.М. Кобиляк [та ін.] // Променева діагностика, променева терапія. — 2014. — № 3. — С. 42-53.
2. Brown E.D. Complications of Renal Transplantation: Evaluation with US and Radionuclide Imaging / Elizabeth D. Brown, Michael Y.M. Chen, Neil T. Wolfman, David J. Ott, Nat E. Watson Jr // RG. — 2000. — Vol. 20, № 3. — Р. 607-622. — DOI: http://dx.doi.org/10.1148/radiographics.20.3.g00ma14607
3. Brocchi S. Shearwave elastography in kidney transplantation: a new diagnostic tool to assess chronic allograft fibrosis / S. Brocchi, C. Sportoletti, C. Serra, M. Zompatori // ECR. — 2014. — Scientific Exhibit. Poster No C‑1199. — DOI: 10.1594/ecr2014/C‑1199.
4. Yang J.R. Application value of shear wave elastography technique in diagnosis of chronic allograft nephropathy / Jin-Ru Yang, Fei-Qian Wang, Ning Li, Wen-Qian Pan, Hong Ai // Int. J. Clin. Exp. Med. — 2016. — 9(6). — Р. 9449-9454. — www.ijcem.com/files/ijcem0016272.pdf
5. Bota S., Sporea I., Sirli R. et al. Factors associated with the impossibility to obtain reliable liver stiffness measurements by means of acoustic radiation force impulse (ARFI) elastography — analysis of a cohort of 1,031 subjects // Eur. J. Radiol. — 2014. — 83. — Р. 268-272.
6. Zaffanello M. Renal Elasticity Quantification by Acoustic Radiation Force Impulse Applied to the Evaluation of Kidney Diseases: A Review / M. Zaffanello, G. Piacentini, C. Bruno, M. Brugnara, V. Fanos // Journal of Investigative Medicine. — 2015 April. — Vol. 63, № 4.
7. Wang L., Xia P., Lv K. et al. Assessment of renal tissue elasti–city by acoustic radiation force impulse quantification with histopathological correlation: preliminary experience in chronic kidney disease // Eur. Radiol. — 2014. — 24. — Р. 1694-1699.
8. Grenier N. Quantitative elastography of renal transplants using supersonic shear imaging: a pilot study / Nicolas Grenier, Séverine Poulain, Sébastien Lepreux, Jean-Luc Gennisson, Benjamin Dallaudière, Yann Lebras, Eric Bavu & Aude Servais, Vannary Meas-Yedid, Mathieu Piccoli, Thomas Bachelet, Mickaël Tanter, Pierre Merville, Lionel Couzi // Eur. Radiol. — 2012. — 22. — Р. 2138-2146. — DOI: 10.1007/s00330-012-2471-9.
9. Sohn B. Shear wave velocity measurements using acoustic radiation force impulse in young children with normal kidneys versus hydronephrotic kidneys / Beomseok Sohn, Myung-Joon Kim, Sang Won Han, Young Jae Im, Mi-Jung Lee // Ultrasonography. — 2014. — 33. — Р. 116-121. — http://dx.doi.org/10.14366/usg.14002
/101-1.gif)
/101-2.gif)

/94-1.gif)
/96-1.gif)
/95-1.gif)
/97-1.gif)
/99-1.gif)