Всемирная организация здравоохранения и Продовольственная сельскохозяйственная организация ООН (ФАО) в 2014 году опубликовали многокритериальный рейтинг риска заражения пищевыми паразитами. Экспертная группа провела огромное исследование, в котором учитывался риск заражения тем или иным гельминтом, тяжесть клинической картины, вызванной паразитом, прогноз для жизни человека после перенесенного заболевания. На основании этого ими был подготовлен рейтинг самых опасных пищевых паразитов. Мы на страницах журнала хотим показать вам десятку лидеров этого списка.
9-е место среди самых опасных пищевых паразитов
Аскаридоз
Шифр МКБ-10: В77
Аскаридоз — антропонозный геогельминтоз, вызываемый Ascaris lumbricoides, характеризующийся поражением дыхательных путей и аллергическими реакциями в фазе миграции личинок, а при паразитировании половозрелых гельминтов — хроническим поражением желудочно-кишечного тракта и осложнениями [1–3].
Возбудитель аскаридоза человека Ascaris lumbricoides относится к подотряду Ascaridate (Skrjabin, 1915), семейству Ascaridae (Baird, 1853), роду Ascaris (Lin–naeus, 1758).
История открытия
Аскаридоз известен с давних времен. Об этом свидетельствуют древние упоминания о паразитических червях в древнейших исторических памятниках — медицинских источниках. В знаменитом папирусе Эберса, относящемся к 1550 г. до н.э., имеются сведения о паразитических червях человека, в частности об аскариде. Египтологи, расшифровавшие иероглифы этого папируса, выяснили, что там имеется целый ряд указаний, как лечить глистные болезни и как убивать паразитических червей в теле человека [4]. Самое древнее лекарство для умерщвления червей было изобретено в XVI веке до н.э. Его рецепт содержится в знаменитом папирусе. Египтяне считали, что если смешать косточки фиников, дисарт (растение) и сладкое пиво, сварить все это и выпить, то гельминты покинут тело тотчас же [4].
Гиппократ (460–370 г. до н.э.) ввел термины helminthos и askaridos. Он придавал очень серьезное значение гельминтозам, говорил о распространенности аскарид у детей, об облегчении течения болезни после изгнания глистов и других нюансах.
Аристотель (384–342 г. до н.э.) знал 3 вида червей: аскариду, тению и острицу. Под словом «гельминты» он понимал червей и личинок насекомых [4].
В середине XVI века был описан возбудитель аскаридоза. А научная гельминтология начала развиваться во второй половине XVIII века.
Петербургский академик Даллас распознал в яйцах паразитических червей элементы их дальнейшего развития и тем самым нанес удар теории самопроизвольного зарождения глистов, которая, однако, держалась очень долго, окончательно исчезнув лишь во второй половине XIX века. Конец XVIII века и самое начало XIX века характеризуются работой целой плеяды гельминтологов (Muller, Goeze, Bloch, Zeder, Batsch), которые создали гельминтологическую науку.
В 1932 году ученый Леффлер впервые описал симптомокомплекс, который обнаруживается при рентгенологическом обследовании в виде причудливой формы затемнений легкого, которые в случае повторного исследования через 3–5 дней могут исчезнуть совсем или появиться в другом месте. Не имеющие устойчивости такие инфильтраты в легких сопровождались значительной эозинофилией крови. В типичных случаях могут появиться аллергические высыпания на коже. Как правило, заболевание заканчивается за 2–3 или за 7–14 дней. Описанный Леффлером симптомокомплекс иногда называют комплексом Леффлера [4].
Однако Леффлером не была определена этиология данной болезни. И лишь спустя несколько лет этиологию описал Muller — врач, работающий в Швейцарском туберкулезном санатории, проведя опыт с собственным заражением.
Строение
В живом состоянии гельминты веретенообразной формы, красноватого, после гибели — желтовато-белого цвета.
Самцы достигают 15–25 см в длину и 2–4 мм в ширину. Хвостовой конец в фиксированном состоянии крючковидно загнут. На вентральной стороне хвоста имеется до 70 пар преанальных и 7 пар постанальных сосочков — органов осязания. Две равные спикулы достигают 1,5–2 мм длины.
Самки значительно крупнее — 20–40 см в длину и до 6 мм в ширину. Задний конец их тел конически заострен. Вульва открывается в конце передней трети тела, где у половозрелых самок имеется кольцевидная перетяжка. Вблизи заднего конца на вентральной стороне открывается анальное отверстие [1, 3, 5].
Головной конец аскариды снабжен тремя губами, которые окружают ротовое отверстие. По боковым сторонам хорошо видны продольные боковые линии, в которых проходят канальцы выделительной системы.
Пищеварительная система представлена ротовым отверстием, длинным цилиндрическим пищеводом, кишечной трубкой, заканчивающейся анальным отверстием.
Половая система самки представлена парными яичниками, яйцеводами и двумя матками, переходящими в вагину, у самца — семенниками, семяпроводом, семяизвергательным каналом, который впадает в клоаку, и двумя спикулами длиной 1,5–2 мм.
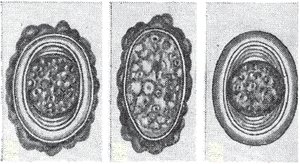
Плодовитость аскарид очень высока. Одномоментно в теле самок обнаруживается до 27 млн яиц на разных стадиях развития. За сутки взрослая самка откладывает около 240 тыс. яиц, в год аскарида выделяет 64 млн яиц. Во внешнюю среду выделяются как оплодотворенные, так и неоплодотворенные яйца. Оплодотворенные яйца чаще овальной, реже шаровидной формы, размером 50–70 на 40–50 мкм. Яйца покрыты толстой многослойной оболочкой, наружная — бугристая белковая, которая, будучи в половых органах самки бесцветной и прозрачной, при выходе в кишечник окрашивается пигментом фекалу в темно-желтый, коричневый цвет и становится непрозрачной. Белковая оболочка защищает яйцо от механических повреждений. Внутренняя оболочка — липоидная, многослойная, гладкая, бесцветная, прозрачная — защищает развивающийся зародыш химических веществ. Внутри яйца располагается мелкозернистый шаровидный бластомер (рис. 1) [1, 3].
/79-1.gif)
Иногда обнаруживаются яйца без белковой оболочки: гладкие, бесцветные, прозрачные, они трудны для диагностики.
Неоплодотворенные яйца могут иметь самую разнообразную форму: чаще они удлиненные, вытянутые, грушевидные, трехгранные. Их размеры колеблются в широких пределах — 50–100 × 40–45 мкм. Белковая оболочка таких яиц грубая, зубцы ее неровные, длинные чередуются с короткими. Все содержимое яйца заполнено крупными желточными клетками. Редко, но встречаются неоплодотворенные яйца без белковой наружной оболочки. Такие яйца особенно трудны для диагностики, их часто принимают за растительные клетки [1, 3].
Жизненный цикл
Аскарида — типичный геогельминт. Ее развитие проходит при участии одного хозяина и зависит от природно-климатических условий местности, определяющих возможность созревания яиц гельминта до инвазионной стадии во внешней среде (рис. 2).
Половозрелые гельминты паразитируют в тонкой кишке человека. При одновременном паразитировании особей обоих полов — самок и самцов — самки выделяют оплодотворенные яйца, способные дальше развиваться, завершать биологический цикл до стадии инвазионной личинки. Созревание яиц в почве происходит при температуре от +13 до +36 °С и влажности не ниже 48 %. В процессе развития зародыш в яйце проходит стадии бластомера, морулы, гаструлы, головастика и, наконец, личинки [1, 3, 5].
В случае неинтенсивной инвазии, когда паразитируют 1–2 самки, они выделяют неоплодотворенные яйца, обнаружение которых подтверждает наличие инвазии (это важно для клиники), но дальнейшего развития таких яиц не происходит.
В кишечнике человека скорлупа яиц разрушается, и личинки освобождаются. Далее они совершают сложный путь миграции: проникнув в слизистую оболочку, попадают в кровеносные капилляры кишечной стенки, затем по системе портальной вены заносятся в печень, откуда по нижней полой вене — в правую половину сердца и через легочную артерию — в легкие. Здесь через разорванные капилляры личинки выходят в просвет альвеол, при помощи мерцательного эпителия, выстилающего бронхиолы, бронхи, трахею, продвигаются по воздухоносным путям и попадают в глотку и в ротовую полость. При заглатывании слюны они попадают в желудок, затем — в кишечник, где происходит их созревание до взрослых особей.
Длительность миграционной фазы составляет 12–14 дней. Только прошедшая миграцию личинка способна созревать в кишечнике до состояния, когда половозрелые особи начинают выделять яйца. С момента заражения до появления яиц в фекалиях проходит 2,5 месяца. Продолжительность паразитирования взрослых особей в кишечнике не превышает одного года [1, 3, 5].
Патогенез
Заражение аскаридозом происходит пероральным путем. В процессе развития аскариды в организме проходят две фазы: миграционную и кишечную.
Патологической основой миграционной, или ранней, фазы является сенсибилизация организма продуктами обмена мигрирующих в крови и тканях личинок и распада погибших. Продукты метаболизма личинок аскарид — сильные паразитарные аллергены. Они вызывают аллергические реакции гиперчувствительности — как общие, так и местные; эозинофильные инфильтраты в легких, гранулематозный гепатит, кожные высыпания, гиперэозинофилию в крови и др. Имеет значение также травматизация личинками тканей во время миграции, образование геморрагии, иногда — обширных кровоизлияний [2, 3, 5].
В кишечной фазе аскаридоза аллергический фактор менее выражен, хотя явления аллерготоксикоза также имеют место.
Взрослые аскариды наносят механические травмы благодаря упругости тел и подвижности. В известной мере эти механизмы играют роль в рефлекторном нарушении функций желудка, кишечника, развитии спастической непроходимости кишечника, травмировании стенки тонкой кишки, вплоть до ее перфорации.
Своеобразие патологического процесса при аскаридозе определяется сенсибилизацией макроорганизма продуктами метаболизма, линькой личинок и распадом погибших гельминтов; воздействием мигрирующих личинок на ткани и кровеносные сосуды; нарушением процессов пищеварения; развитием гиповитаминозов (дефицит пиридоксина, ретинола, аскорбиновой кислоты); токсическим воздействием факторов агрессии гельминтов; присоединением бактериальной инфекции и другими осложнениями. После перенесенного аскаридоза формируется кратковременный, нестойкий иммунитет, который не защищает человека от повторных заражений. Только при частых повторных заражениях у человека может сформироваться иммунитет, который препятствует наступлению кишечной стадии аскаридоза [2].
Доказано иммуносупрессивное влияние аскарид, у детей ослаблена выработка антител к дифтерийному анатоксину.
Тяжелые хирургические последствия влечет за собой проникновение аскарид в печень, дыхательные пути. Наличие аскарид в кишечнике весьма осложняет течение и исход оперативных вмешательств при различных патологиях.
Классификация [2]
I. Международная классификация болезней 10-го пересмотра (МКБ-10):
B77.0 Аскаридоз с кишечными осложнениями.
B77.8 Аскаридоз с другими осложнениями.
B77.9 Аскаридоз неуточненный.
II. Клиническая классификация аскаридоза:
A. По типу:
1. Типичный (манифестный).
2. Атипичный (субклинический, бессимптомный).
В. По фазе болезни:
1. Ранняя.
2. Поздняя.
С. По тяжести:
1. Легкая форма.
2. Среднетяжелая форма.
3. Тяжелая форма.
D. По наличию осложнений:
1. Без осложнений.
2. С кишечными осложнениями (непроходимость кишечника, перитонит, аппендицит, холангиогепатит, механическая желтуха, панкреатит).
3. С внекишечными осложнениями (гнойный холангит, абсцессы печени, гнойный плеврит, сепсис, абсцессы брюшной полости, асфиксия и др.).
Клиническая картина
Клинические проявления аскаридоза зависят от интенсивности инвазии и фазы развития заболевания. Как правило, аскаридоз характеризуется желудочно-кишечными расстройствами, снижением аппетита, рвотой, тошнотой, болями в животе и неконтролируемым слюноотделением. Кроме того, нередко наблюдаются заболевания дыхательных органов, начиная от банальной простуды и заканчивая воспалением легких, также возможны нарушения в психике — от раздражительности, головокружений до эпилептических припадков [2, 3, 5, 6]. Выделяют две фазы: раннюю (миграционная, личиночная) и позднюю (кишечная, фаза паразитирования половозрелых аскарид).
Ранняя фаза обусловлена миграцией личинок гельминта. В первой фазе аскаридоза клинические проявления иногда неявно выражены, болезнь проходит без осложнений. Иногда начало заболевания сопряжено с обычным недомоганием, бывает сухой кашель или же с незначимой слизистой мокротой, реже — слизисто-гнойной. Мокрота порой имеет оранжевую окраску и содержит не очень большую примесь крови. Температура тела, как правило, обычная и субфебрильная, иногда поднимается до 38 °С. Основным показанием к обследованию в этой фазе является легочная симптоматика — кашель (сухой или с небольшим количеством мокроты, которая может содержать примесь крови), плевриты в сочетании с эозинофилией и возможными кожными проявлениями аллергических реакций, возможны симптомы бронхиальной астмы, атипичной бронхо–пневмонии. При инструментальном исследовании часто выявляются летучие инфильтраты (синдром Леффлера) в легких [2, 5, 6]. Иногда бывают сухие и мокроватые хрипы, у некоторых больных наблюдается укорочение перкуторного звука. Физикальные способы порой выявляют перемены в легких. При рентгенологическом исследовании в них отмечается присутствие круглых, округлых, звездчатых, фестончатых, многоугольных инфильтратов. Инфильтраты бывают как единичными, так и многочисленными, появляются в одной доле или по всему легкому [2, 5, 6]. Эозинофильные инфильтраты обнаруживаются около 2–3 недель; у отдельных пациентов, исчезнув, они бывают замечены опять спустя несколько месяцев и сохраняются месяцами. Число лейкоцитов, как правило, нормальное, время от времени наблюдается лейкоцитоз. Характерна эозинофилия, достигающая у пациентов 60–80 %; она бывает замечена в большинстве случаев в одно и то же время с инфильтратами в легких. СОЭ обычно в норме, повышение ее бывает нечасто. Патологической основой миграционной, или ранней, фазы является сенсибилизация организма продуктами обмена мигрирующих в крови и тканях личинок и распада погибших. Продукты метаболизма личинок аскарид — сильные паразитарные аллергены. Они вызывают аллергические реакции гиперчувствительности, как общие, так и местные, эозинофильные инфильтраты в легких, гранулематозный гепатит, кожные высыпания, гиперэозинофилию в крови и др. Имеет значение также травматизация личинками тканей во время миграции, образование геморрагии, иногда — обширных кровоизлияний [2, 5, 7].
Может развиться гранулематозный гепатит с нарушением пигментного обмена, признаками цитолиза. Спленомегалия и миокардиодистрофия. Присоединение бактериальной инфекции служит причиной развития пневмонии. В этих случаях отсутствие адекватной терапии у детей раннего возраста может привести к летальному исходу.
Поздняя фаза заболевания связана с пребыванием гельминтов в кишечнике. На этой стадии заболевание также может протекать по-разному, в том числе и без выраженных симптомов аскаридоза. Позднюю фазу с выраженной клиникой именуют кишечной, так как в это время в большинстве случаев превалируют нарушения желудочно-кишечного характера, часто сопровож–дающиеся астеническими явлениями. Пациенты жалуются на изменение аппетита — снижение, отсутствие, чрезмерную разборчивость в еде («капризный» аппетит, характерный при аскаридозе у детей). Также присутствует тошнота, обильное слюноотделение — особенно по утрам, пока желудок еще не наполнен [2, 7, 8].
При аскаридозе нередки запоры и поносы; наиболее часто наблюдается чередование этих явлений, но может отмечаться и преимущественное развитие энтерита. У пациентов детского возраста доминируют нарушения пищеварения на фоне достаточно сильных болей в области живота, часто имеющих схваткообразный характер и начинающихся без видимых причин либо при пальцевом осмотре. По результатам рентгенологических исследований выявляются патологии тонкого отдела кишечника, например измененный рельеф слизистой оболочки и т.п. Больные могут жаловаться на вздутый живот, неприятное чувство передвижения по кишечнику чего-то чужеродного [8].
И у детей, и у взрослых на поздней стадии часто наблюдается болевой синдром, возникающий при прощупывании (пальпации) области живота. Детям свойственна разлитая болезненность, взрослым — болезненность, локализованная вдоль средней линии вверх от пупочной зоны, а также правее этой линии. Также при глистной инвазии характерно пониженное выделение желудочной секреции.
У больных отмечаются функциональные нарушения со стороны нервной системы: головные боли, головокружения, повышенная утомляемость, нарушение сна, истерические припадки, эпилептиформные судороги, менингизм. В ряде случаев возможны проявления вегетососудистой (нейроциркуляторной) дисфункции по гипотоническому типу (снижение артериального давления, тошнота на фоне гипотонии и др.) [2, 9].
В некоторых случаях именно астенические симптомы аскаридоза являются наиболее выраженными [9].
Так же как и на ранней стадии, на втором этапе аскаридоза присутствуют различного рода аллергии: кожные высыпания по типу крапивницы, повышение количества эозинофилов (не в таких количествах, как на первом этапе). Довольно часто регистрируют умеренное понижение содержания гемоглобина в эритроцитах (гипохромная анемия); этот симптом особенно характерен для детей [10].
Осложнения
Выделяют кишечные и внекишечные осложнения аскаридоза.
Кишечные осложнения — это механическая непроходимость кишечника, прободение кишечной стенки с развитием перитонита, аппендицит.
Кишечная непроходимость может быть обусловлена обтурацией просвета кишечника клубком свернувшихся аскарид или результатом спазма кишечника. Основными признаками аскаридозной непроходимости являются схваткообразные резкие боли в животе и тошнота, задержка стула и газов, вздутие живота, видимая перистальтика кишечника, опухоль, прощупывающаяся в брюшной полости, чаще в подвздошной области. Согласно докладу научной группы ВОЗ, частота кишечной непроходимости и осложнений, вызываемых миграцией аскарид, в США составляет 10–15 % всех случаев острого живота. В юго-восточных районах США кишечная непроходимость у детей 1–5 лет регистрируется в 2 случаях на 1000 инвазированных. «Если принять показатель 6 на 100 000 населения угрожающих жизни осложнений (хирургических), это может составить тысячи случаев смерти при учете многих миллионов инвазированных лиц» (из серии технических докладов ВОЗ, № 666, 1983 г.).
Заползание аскарид в желчный пузырь и желчные протоки вызывает механическую желтуху, а в случае присоединения вторичной инфекции — гнойный холангит, множественные абсцессы печени, перитонит, сепсис.
Для аскаридоза печени и желчных протоков характерны такие симптомы, как сверлящие боли в правом подреберье, отсутствие или слабая выраженность желтушности кожи, рвота, увеличение печени, иногда — выделение аскарид с рвотными массами. В таких случаях необходима немедленная операция.
Миграция аскарид в протоки поджелудочной железы приводит к развитию острого панкреатита, заползание в червеобразный отросток — аппендицита.
Аскариды способны перфорировать кишечник в области операционных швов, что приводит к развитию перитонита.
При антиперистальтике и рвоте при выходе из нар–коза после операции аскариды могут попасть в пищевод, откуда проникают в глотку, достигая дыхательных путей и вызывая асфиксию.
Аскаридоз отягощает течение различных болезней, в том числе острых детских инфекций — кори, коклюша, дифтерии, скарлатины, дизентерии, брюшного тифа, болезни Боткина, способствуя более тяжелому и длительному их течению, развитию рецидивов, осложнений и более частому носительству. Подобное влияние аскаридоз оказывает на течение хронических болезней, осложняя течение туберкулеза, трахомы, трихофитии, конъюнктивитов, кожных заболеваний и др., что, возможно, связано с иммуносупрессивным действием аскарид. Это необходимо учитывать при проведении профилактических прививок, которые не достигают своей цели при наличии гельминтов в кишечнике. Освобождение от инвазии до проведения вакцинации является законом, не требующим объяс–нений [11, 12].
Аскаридозная инвазия в акушерской клинике также не остается без последствий. Доказано отрицательное влияние аскаридоза на течение беременности. У инвазированных беременных чаще регистрируются токсикозы, нарушения развития плода, осложняется течение родов и послеродового периода. Хотя врожденный аскаридоз принято считать казуистикой.
Диагностика
Основой диагностики ранней фазы аскаридоза являются клинико-эпидемиологические данные. Острые клинические симптомы бронхолегочной патологии (лихорадка, кашель, загрудинные боли, эозинофилия крови, летучие и фильтраты в легких и др.) в сезон года, не характерный для простудных заболеваний, пребывание в очагах аскаридоза, участие (особенно детей) в сборе клубники, ранних овощей являются основанием для предположительного диагноза [13, 14].
Безусловным подтверждением диагноза является обнаружение личинок в мокроте, однако это очень редкие находки, и поэтому они имеют малое практическое значение.
Предложены серологические методы диагностики: реакция преципитации на живых личинках аскарид (Е.С. Лейкина), реакция непрямой гемагглютинации, латекс-агглютинации, реакция ускорения оседания эритроцитов (по Кротову). Обнадежили методики, основанные на обнаружении летучих жирных кислот в слюне и моче по Н.Я. Сопруновой [14]. Однако, имея очень важное научное значение (изучение иммунитета, эпидемиологии, патогенеза), в широкую практику серологические методы не вошли. Поэтому при наличии предположительного диагноза необходимо через 3 месяца (когда аскариды достигнут половой зрелости и начнут выделять яйца) провести копрологическое исследование, используя методы толстого мазка по Като или метода обогащения (Фюллеборна, Калантарян и др.) [15].
Учитывая возможность паразитирования только самцов, что свидетельствует о неинтенсивной инвазии, когда копроовоскопия отрицательна, рекомендуется диагностическая дегельминтизация.
Дифференциальная диагностика
Рентгенологическая картина инфильтратов в легких в ранней фазе может симулировать туберкулез, пневмонию, опухоль легкого. Основное отличие инфильтратов при аскаридозе — их быстрое исчезновение без каких-либо остаточных явлений. Подобные инфильтраты могут обнаруживаться и при других гельминтозах — анкилостомидозах и стронгилоидозе. В поздней фазе дифференциальная диагностика в первую очередь требуется с дуоденитом, энтеритом, холециститом и другими заболеваниями пищеварительной системы.
Обоснование и формулировка диагноза
При формулировке диагноза аскаридоза учитывают особенности клинического течения заболевания (нозологическая форма, клиническая форма, степень тяжести, период болезни) и приводят его обоснование.
При наличии осложнений и сопутствующих заболеваний запись делается отдельной строкой:
— осложнение;
— сопутствующее заболевание.
При обосновании диагноза следует указать эпидемиологические, клинические, лабораторные, инструментальные данные и результаты специальных методов исследования, на основании которых подтвержден диагноз аскаридоза [2].
Лечение
Лечение аскаридоза проводится под контролем инфекциониста (детского инфекциониста или педиатра) и состоит из организационно-режимных мероприятий, дегельминтизации, диспансерного наблюдения и профилактики повторного заражения [5].
Принципы лечения больных аскаридозом преду–сматривают одновременное решение нескольких задач:
— предупреждение дальнейшего развития патологического процесса, обусловленного заболеванием;
— предупреждение развития и купирование патологических процессов осложнений;
— предупреждение формирования остаточных явлений, рецидивирующего и хронического течения.
Общие рекомендации касаются главным образом соблюдения диеты с повышенным содержанием витаминов, животных белков и ограничением углеводов.
Медикаментозная терапия проводится противогельминтными препаратами, из которых в ранней фазе аскаридоза назначаются альбендозол или мебендазол, а в кишечной — левомизол, пирантел и др. [16]. Для снижения аллергизации одновременно с противогельминтными препаратами рекомендуется короткий курс приема антигистаминных средств. С целью нормализации пищеварительной функции используются ферменты (панкреатин). Коррекция микрофлоры кишечника проводится с помощью пробиотических препаратов [11, 12].
Контроль эффективности противогельминтной терапии осуществляется через 2 недели и 1 месяц после курса лечения трехкратно.
Диспансерное наблюдение
За переболевшим аскаридозом пациентом устанавливается диспансерное наблюдение сроком на 3 года с ежегодной копроовоскопией.
Профилактика
Профилактика аскаридоза должна быть направлена на своевременное выявление и дегельминтизацию больных, гигиеническое воспитание детей, повышение уровня санитарной культуры среди взрослых [11]. Избежать заражения аскаридозом поможет соблюдение элементарных норм гигиены: мытье рук перед едой, после улицы, посещения туалета; тщательное промывание под проточной водой ягод, фруктов, овощей перед подачей на стол. При неосложненном течении аскаридоза прогноз благоприятный. В случае отсутствия повторной инвазии примерно через год происходит самоизлечение вследствие естественной гибели аскарид. Осложнения развиваются сравнительно редко, главным образом у детей и ослабленных пациентов.
10-е место среди самых опасных пищевых паразитов
Трипаносомозы
Шифр МКБ-10: B56 — африканский трипаносомоз; B57 — болезнь Шагаса.
Трипаносомозы — тропические трансмиссивные заболевания, вызываемые трипаносомами — простейшими класса жгутиковых. Различают трипаносомоз африканский — сонную болезнь (morbus dormitivus, sleeping sickness) и американский — болезнь Шагаса (morbus Shagasy) [1, 3, 17].
Возбудители относятся к типу простейших, классу жгутиковых, семейству Trypanosomatidae. Африканский трипаносомоз вызывают Tr.gambiense и Tr.rhodesiense, американский — Tr.сruzi. Морфологические различия возбудителей несущественны.
В список десяти самых распространенных пищевых паразитов входят Tr.сruzi. Несмотря на то, что эта инфекция передается через фекалии триатомовых клопов (также известных как поцелуйные клопы), недавно было доказано, что заразиться можно просто употребляя еду, загрязненную фекалиями этих клопов. Несколько последних вспышек заболеваемости были связаны с зараженными фруктовыми соками. Это делает возможным превращение трипаносом в мировой возбудитель заболеваемости.
Болезнь Шагаса (B57; американский трипаносомоз) — протозооз, вызываемый внутриклеточным простейшим паразитом рода трипаносом (T.cruzi), приводящий к воспалительно-дегенеративным изменениям со стороны сердца, нервной системы, ЖКТ [3, 17].
Болезнь Шагаса относится к природно-очаговым заболеваниям и широко распространена практически во всех странах Американского континента: эндемичными по трипаносомозу районами являются Центральная и Южная Америка. В сельской местности большинство населения заражается трипаносомозом еще в детском возрасте, часто инвазия протекает бессимптомно. Среди зараженных болезнью Шагаса преобладают лица мужского пола [17].
История открытия
Бразильский врач Карлос Шагас назвал своим именем болезнь, которая сегодня известна как американский трипаносомоз.
Карлос Шагас окончил медицинский институт в Рио-де-Жанейро (1902), специализировался в изучении малярии. По завершении образования поступил на работу в портовую администрацию города Сантус для борьбы с малярией у портовых рабочих и добился в этом направлении существенных успехов, направив свои усилия на профилактику заболеваемости (Шагас предложил программу опрыскивания инсектицидами районов проживания рабочих).
В 1906 г. Шагас перешел на работу в Научно-медицинский институт Освальдо Круса. Институт командировал его для борьбы с малярией в район реки Сан-Франсиску, где Шагас провел два года. Здесь Шагас обратил внимание на кровососущего жука Triatoma из семейства Reduviidae и в 1909 г. обнаружил, что этот жук является носителем ранее неизвестного простейшего-паразита рода Trypanosoma. Шагас назвал его Trypanosoma cruzi в честь Освальдо Круса. Далее Шагас выяснил, что жук передает трипаносому укушенному им человеку. Обследовав обезьян, зараженных трипаносомой, Шагас выявил симптомы заболевания, вызываемого этим простейшим, и обнаружил их у местного населения. В результате всех своих исследований Шагас единолично полностью описал новую найденную инфекцию (ее возбудителя, переносчика, способ заражения, клинические проявления и эпидемиологию), что стало уникальным случаем в истории медицины. Попутно Шагас описал также новый грибок, обнаруженный в легких у больных, первоначально приняв его за особую форму жизненного цикла трипаносомы; этот грибок был описан годом позже, в 1910 г., другим бразильским специалистом, Антонио Карини, как отдельная форма жизни и стал первым исследованным представителем рода Pneumocystis, значительно позже попавшего в поле зрения многих специалистов в связи с тем, что другой вид этого грибка вызывает пневмоцистную пневмонию.
Открытие Шагаса получило широкое признание. Он был избран в бразильскую Национальную медицинскую академию, дважды номинирован на Нобелевскую премию по медицине. В 1917–1934 гг. Шагас возглавлял Институт Освальдо Круса.
Строение
Возбудителем болезни Шагаса является жгутиковое простейшее Trypanosoma cruzi, сложный цикл развития которого включает смену хозяев — позвоночных животных и человека, а специфическим переносчиком служат кровососущие клопы подсемейства Triatominae (триатомовые). Строение трипаносомы, то есть ее морфологическая структура, в течение взрослой, трипаносомной стадии развития имеет форму трипомастиготы. Тело трипаносомы длиной от 12 до 40–70 мкм и имеет продольную форму сильно вытянутого овала с заостренными концами, напоминающую веретено [18, 19].
Оно состоит из одной клетки — митохондрии с цитоплазмой и единственным ядром; клетка имеет плотную гликопротеиновую оболочку (перипласт). Также в клетке трипаносомы имеется дисковидный органоид кинетонуклеус (или кинетопласт), содержащий ДНК, и меньшее по размеру тельце (кинетосома или блефаропласт), от которого начинается наружный вырост клетки трипаносомы флагеллоподий. Этот органоид движения паразита попросту именуется жгутиком. Он тянется вдоль тела клетки и приподнимает образованную перипластом пластинчатую перепонку, которая также расположена вдоль всей клетки (с одной стороны). Специалисты называют ее ундулирующей мембраной (от лат. undulatus — волнообразный), и ее функция — извиваясь, продвигать трипаносому в нужном направлении. Такое строение трипаносомы присуще паразиту, когда он находится в организме окончательного хозяина [4, 20].
Кроме того, находясь там, трипаносома может быть и в форме амастиготы (овальной, меньшего размера и без жгутика). А вот на критидиальной стадии, пребывая в организме насекомого-переносчика, морфологическая структура клетки приобретает вид эпимастиготы: клетка удлиненная, но жгутик короткий и волнообразная мембрана сильно недоразвита.
Trypanosoma cruzi имеет C- или S-образную форму тела, а также более длинный жгутик и зауженную волнообразную мембрану.
Жизненный цикл
Паразит проходит несколько фаз жизненного цикла: амастигота, обитающая в тканевых клетках человека; эпимастигота, растущая в кишечнике переносчиков; и трипомастигота, находящаяся в крови животных и человека. Основным хозяином T.cruzi является человек, дополнительными — броненосцы, муравьеды, обезьяны и домашние животные (собаки, кошки, свиньи). Инвазионной стадией для переносчиков и хозяев являются трипомастиготные формы. Заражение клопов происходит в процессе питания кровью человека или животных, содержащей трипомастиготы. В организм человека возбудитель болезни Шагаса заносится вместе с инфицированными фекалиями клопов при расчесывании ранок после их укусов на коже и слизистых губ, носа, конъюнктивы [17, 20].
Характерной особенностью T.cruzi является способность к внутриклеточному паразитизму в макрофагах кожи и слизистых оболочек, в клетках миокарда, эндотелия лимфатических узлов, селезенки, печени, легких, нейроглии. После разрыва пораженных клеток, переполненных размножившимися амастиготами, происходит заражение новых клеток. Паразитирование трипаносом приводит к воспалительно-дистрофическому и дегенеративному поражению внутренних органов. Для T.cruzi характерна персистенция в организме хозяина в течение всей жизни.
Человек инфицируется T.cruzi несколькими путями:
— люди могут переносить паразита на глаза, рот или порезы, если до этого коснулись фекалий инфицированного триатомового клопа;
— фекалии клопа могут попадать людям в глаза прямым путем;
— при употреблении не прошедшей тепловую обработку пищи, зараженной фекалиями клопа, паразит может попадать в пищевод;
— матери могут передавать T.cruzi детям во время беременности или при рождении;
— паразит может передаваться через зараженную кровь при переливании крови или трансплантации органов.
Риск инфекции T.cruzi непосредственно обусловлен нищетой. Миграция сельского населения в города, имевшая место в Латинской Америке в 1970-х и в 1980-х годах, изменила традиционную эпидемиологическую картину болезни Шагаса, ставшую городской инфекцией, которая передается при переливании крови. Степень зараженности банков крови в некоторых городах американского континента может составлять от 3 до 53 %, указывая на тот факт, что в запасах крови распространенность крови, инфицированной T.cruzi, может превышать распространенность вирусов гепатитов В и С и ВИЧ [17, 20].
Естественная восприимчивость у людей высокая; среди механизмов передачи — переливание зараженной крови, врожденная форма или молоко инфицированной матери.
Клиническая картина
Инкубационный период заболевания продолжается 1–3 недели. Затем в месте проникновения трипаносом может развиться местная воспалительная реакция (шагома) в виде эритематозного узла с припухлостью и покраснением либо одностороннего багрового отека века (симптом Роминьи) с конъюнктивитом, сопровождающаяся увеличением регионарных лимфоузлов (рис. 3).
Болезнь Шагаса проходит в 2 стадии: острую (первые 2 месяца) с циркуляцией большого количества паразитов в крови и хроническую — с концентрацией трипаносом во внутренних органах [3, 20, 21].
В острой стадии болезни Шагаса симптомы в большинстве случаев отсутствуют, у части больных проявляются в легкой форме. У детей до 5 лет развивается наиболее тяжелая форма с системными проявлениями и летальностью до 10–14 %. Среди общих симптомов болезни Шагаса может отмечаться недомогание, постоянная или ремиттирующая лихорадка (до 39–40 °С), головная и мышечная боль, отеки на ногах, одутловатость лица, мелкая макулезная сыпь. Характерен шейный, паховый и подмышечный лимфаденит, гепатоспленомегалия. Могут возникать вторичные шагомы — плотные узлы в подкожной клетчатке. Отмечается преимущественное поражение сердца, ЦНС и периферических ганглиев, органов ретикулоэндотелиальной системы. Развивается острое воспаление и расширение всех камер сердца (кардиомегалия), диффузный миокардит, нарушение сердечной деятельности. У некоторых больных (особенно у детей раннего возраста) может возникнуть острый специфический менингоэнцефалит, кровоизлияние в мозговые оболочки. Врожденная болезнь Шагаса может приводить к спонтанному аборту или преждевременным родам; у новорожденных сопровождается тяжелой анемией, гепатоспленомегалией, желтухой, судорогами, нередко — летальным исходом.
При хронической форме болезни Шагаса симптомы могут долго отсутствовать, пока не произойдут необратимые повреждения внутренних органов. Чаще всего развивается кардиомиопатия, выражающаяся сердечной недостаточностью, аритмией, тромбоэмболией. Со стороны ЖКТ характерны патологическое расширение пищевода (мегаэзофагус), проявляющееся дисфагией, болью при глотании, и расширение толстой кишки (мегаколон), сопровождающееся кишечной непроходимостью, скоплением каловых камней. Возникают вегетативные нарушения и периферическая нейропатия. С течением времени болезнь Шагаса может приводить к внезапной смерти вследствие прогрессирующего разрушения сердечной мышцы [21, 22].
Диагностика
Диагностика болезни Шагаса включает тщательный сбор анамнеза (с учетом места рождения больного, поездок в эндемичные по заболеванию районы), анализ данных клинической картины и лабораторных исследований (микроскопического и культурального методов, серологических анализов и ПЦР).
В качестве исследуемого материала используется кровь, спинномозговая жидкость, пунктаты из первичных мест поражения, лимфоузлов, селезенки, костного мозга. В острой стадии болезни Шагаса (первые 6–12 недель) паразитов можно обнаружить при микроскопии толстой капли крови или фиксированных окрашенных препаратов. Бактериологический посев крови больного помогает выявить чистую культуру T.cruzi. При болезни Шагаса применяется ксенодиагностика, включающая исследование содержимого кишечника неинвазированного триатомового клопа после насыщения его кровью больного. Возможно проведение биологической пробы с введением крови пациента морским свинкам или белым мышам и последующим изучением образцов тканей [13, 14].
При хронической болезни Шагаса более эффективна серодиагностика: реакция связывания комплемента, реакция непрямой флюоресценции, реакция непрямой гемагглютинации, ИФА.
Наличие специфических IgM говорит об острой стадии болезни Шагаса, при хронической присутствуют только IgG. Некоторые инфекции, например, малярия, сифилис, лейшманиоз, могут давать ложноположительные результаты на трипаносомоз, поэтому рекомендуется применять не менее двух независимых методов серодиагностики. Необходима дифференциальная диагностика патогенных трипаносом от непатогенных видов, способных находиться в организме человека, не вызывая развитие заболевания.
Лечение
На сегодняшний день лечение болезни Шагаса малоэффективно; терапия позволяет снизить летальность среди больных, но не дает уверенности в полной эрадикации внутриклеточных форм T.cruzi. В лечении болезни Шагаса применяются два антипаразитарных препарата: нифуртимокс и бензнидазол, прием которых более эффективен в острой стадии заболевания. В хронической стадии инфекции лечение направлено на облегчение симптомов развившихся осложнений болезни Шагаса. При сердечной недостаточности и аритмии, для профилактики тромбоэмболических состояний назначаются ингибиторы АПФ, сердечные гликозиды, антиаритмические средства, антикоагулянты, в тяжелых случаях показаны аортокоронарное шунтирование, имплантация кардиостимулятора, трансплантация сердца. Лечение менингоэнцефалита — симптоматическое; при поражении ЖКТ могут использоваться кортикостероиды; при мегаколоне возможно хирургическое вмешательство: наложение колостомы, резекция толстой кишки.
Прогноз
Прогноз болезни Шагаса зависит от стадии заболевания, остроты развития и обратимости воспалительно-дегенеративных поражений внутренних органов, возраста больного. Пациенты с поздней стадией болезни Шагаса часто умирают от острой сердечной недостаточности, инфаркта, инсульта, дети раннего возраста — от стремительно развившегося острого менингоэнцефалита.
Профилактика
Профилактика болезни Шагаса включает инсектицидную обработку жилья человека, птичников, свинарников — основных мест обитания клопов — переносчиков паразитов, благоустройство жилища; отбор и обследование на трипаносомоз потенциальных доноров крови и органов, санитарное просвещение населения.
Конфликт интересов. Автор заявляет об отсутствии какого-либо конфликта интересов при подготовке данной статьи.

/79-1.gif)
/80-1.gif)
/85-1.gif)