Резюме
У статті наведено літературні дані щодо основних клінічних проявів, частоти, сучасних методів пренатальної і постнатальної діагностики, лікування та прогнозу відкритої артеріальної протоки — природженої аномалії серцево-судинної системи в дітей. Згідно з міжнародною класифікацією хвороб 10-го перегляду, виділяють Q25.0. Відкрита артеріальна протока. Відкрита боталлова протока. Незарощування артеріальної протоки. Частота відкритої артеріальної протоки в доношених новонароджених становить 0,006–0,02 %, у недоношених новонароджених — 15–80 %. Клініка відкритої артеріальної протоки залежить від її величини, рівня тиску в легеневій артерії і співвідношення опору малого і великого кола кровообігу. Одна з основних клінічних ознак відкритої артеріальної протоки — безперервний «машинний» систолодіастолічний шум у II–III міжребер’ї уздовж лівого краю грудини. У новонароджених, дітей перших місяців життя, а також за наявності високої легеневої гіпертензії діастолічний компонент шуму може бути відсутнім, вислуховуються тільки систолічний шум і посилений другий тон на легеневій артерії, визначаються високий і швидкий пульси, збільшення пульсового тиску. У недоношених дітей, які мають малу вагу, відкрита артеріальна протока аускультативно не виявляється. На електрокардіограмі — ознаки перевантаження лівого шлуночка. За допомогою ехокардіографії можливі безпосередня візуалізація протоки, діагностика збільшення розміру лівого шлуночка, визначення ознак об’ємного перевантаження лівого шлуночка. Рентгенологічно — посилення судинного рисунка легенів, збільшення діаметра серця за рахунок гіпертрофії лівого шлуночка. Метод медикаментозної облітерації з використанням індометацину ефективний у новонароджених в перші два тижні життя. Показанням до хірургічної корекції є встановлення пороку серця в дитини після 6–12 міс. життя. Оптимальний для операції вік хворих — від 2 до 5 років.
В статье представлены литературные данные об основных клинических проявлениях, о частоте встречаемости, современных методах ранней неонатальной и постнатальной диагностики, лечении и прогнозе открытого артериального протока — врожденного порока сердечно-сосудистой системы у детей. Согласно международной классификации болезней 10-го пересмотра, выделяют Q25.0. Открытый артериальный проток. Открытый боталлов проток. Незаращение артериального протока. Частота открытого артериального протока у доношенных новорожденных составляет 0,006–0,02 %, у недоношенных новорожденных — 15–80 %. Клиника открытого артериального протока зависит от его величины, уровня давления в легочной артерии и соотношения сопротивления малого и большого кругов кровообращения. Один из основных клинических признаков открытого артериального протока — непрерывный «машинный» систолодиастолический шум во II–III межреберьях вдоль левого края грудины. У новорожденных, детей первых месяцев жизни, а также при наличии высокой легочной гипертензии диастолический компонент шума может отсутствовать, выслушиваются только систолический шум и усиленный второй тон на легочной артерии, определяются высокий и скорый пульсы, увеличение пульсового давления. У маловесных недоношенных детей открытый артериальный проток аускультативно не выявляется. На электрокардиограмме — признаки перегрузки левого желудочка. С помощью эхокардиографии возможны непосредственная визуализация протока, диагностика увеличения размера левого желудочка, определение признаков объемной перегрузки левого желудочка. Рентгенологически — усиление сосудистого рисунка легких, увеличение поперечника сердца за счет гипертрофии левого желудочка. Метод медикаментозной облитерации с использованием индометацина эффективен у новорожденных в первые две недели жизни. Показанием к хирургической коррекции является установление порока сердца у ребенка после 6–12 мес. жизни. Оптимальный для операции возраст больных — от 2 до 5 лет.
The article presents the published data on the prevalence, the main clinical manifestations, and modern methods of early neonatal and postnatal diagnosis, treatment and prognosis of patent ductus arteriosus — the congenital malformation of cardiovascular system. The International Statistical Classification of Diseases version10 defines it Q25.0 Patent ductus arteriosus. Patent ductus Botalli. Botallo’s duct patency. The pre-valence of the patent ductus arteriosus is from 0.006 to 0.02 % in mature newborns, in premature newborns — from 15 to 80 %. Clinical manifestation of the malformation depends on its size, pulmonary pressure, and proportion of pulmonary and syste-mic circulation. One of the basic clinical signs of patent ductus arteriosus is permanent eddy murmur in II–III space along left sternal border. In newborns and infants and if severe pulmonary hypertension diastolic murmur can be absent while systolic and forced second sound on pulmonary artery, collapsing magnus pulse, increased pulse pressure are determined. Open ductus arteriosus is not determined auscultatory in low-weight premature children. The electrocardiograph reveals downloaded left ventricular. Echo-cardiograph images ductus arteriosis, increased left ventriclular, volume overload of left ventricular. Chest roentgenograms may reveal prominent pulmonary arterial markings, increased heart breadth due to hypertrophic left ventricular. Drug obliteration with indometacin is effective in newborns aged 2 weeks. The surgical indication is verified heart disease aged 6–12 months old. The appropriate age for surgical intervention is 2–5 years old.
Публикация не имеет связи с плановыми научно-исследовательскими работами, фондами, грантами.
Открытый артериальный (боталлов) проток (ОАП) — наличие аномального сосудистого сообщения (канала) между аортой и легочной артерией (рис. 1).
Согласно Международной классификации болезней 10-го пересмотра, выделяют Q25.0. Открытый артериальный проток (ОАП). Открытый боталлов проток. Незаращение артериального протока.
Первые анатомические описания ОАП принадлежат Галену (130–200 гг. н.э.) [1]. Также о данной аномалии сообщает G. Аrаnzio (1564). Несколько позже итальянский врач Леонардо Боталлио (1530–1600) описал сосуд, соединяющий аорту и легочную артерию, и, согласно Базельской классификации 1895 г., этому сосуду было присвоено имя Л. Боталлио. Объяснение функционального значения протока, кровообращения плода стало возможным с открытием кровообращения Гарвеем.
Частота ОАП у доношенных новорожденных составляет 0,006–0,02 %, у недоношенных новорожденных — 15–80 %, причем при массе менее 1000 г максимальная частота — 80 %, при 1500–2000 г — 10–15 %. Согласно клиническим данным, ОАП выявляется в 5–34 % случаев [2], а по патологоанатомическим — в 3–9,8 % случаев среди всех врожденных пороков сердца. Изолированный открытый артериальный проток среди всех врожденных пороков сердца составляет 10–24 % [3]. Соотношение детей мужского и женского полов — 1 : 2.
Врожденные пороки сердечно-сосудистой системы антенатально диагностируются у 62,2 % детей [4].
Сочетание с другими пороками. У 5–12 % больных ОАП сочетается с другими врожденными пороками.
Клиника
Функционирование артериального протока может рассматриваться как нормальное до 10 дней — 3 мес. жизни у доношенных новорожденных [5]. Проток может быть различной длины (от 3 до 25 мм) и ширины (от 2 до 30 мм в диаметре). Клиника ОАП зависит от величины артериального протока, уровня давления в легочной артерии и соотношения сопротивления малого и большого кругов крово-
обращения. Гемодинамические нарушения заключаются в сбросе крови из аорты в легочную артерию, что приводит к переполнению малого круга кровообращения и перегрузке левых отделов сердца. При развитии легочной гипертензии наблюдается перегрузка и правого желудочка. У большинства детей ОАП клинически проявляется в конце первого или на втором-третьем году жизни. С рождения или в первые недели жизни клинически проявляются ОАП большого диаметра.
Ранняя неонатальная и постнатальная диагностика
Один из основных клинических признаков ОАП — непрерывный «машинный» систолодиастолический шум во II–III межреберьях вдоль левого края грудины. У новорожденных, детей первых месяцев жизни, а также при наличии высокой легочной гипертензии диастолический компонент шума может отсутствовать, выслушиваются только систолический шум и усиленный второй тон на легочной артерии, определяются высокий и скорый пульс, увеличение пульсового давления. У маловесных недоношенных детей ОАП аускультативно не выявляется. Для новорожденных с ОАП характерны трудности грудного вскармливания, отказ от еды, быстрая утомляемость, развитие гипотрофии и наличие в анамнезе частых бронхолегочных заболеваний. При плаче и кормлении младенца бледность кожных покровов сменяется преходящим цианозом из-за появления венозно-артериального сброса крови. У новорожденных не отмечаются систолическое дрожание и усиление верхушечного толчка, характерные для детей старшего возраста.
Выявляется систолодиастолический шум над всей сердечной областью с максимальной регистрацией во II межреберье слева у грудины (при нормальных показателях величины систолического давления в легочной артерии). В случае увеличения давления в легочной артерии может выявляться лишь систолический шум, а при высоких цифрах — шум недостаточности клапанов легочной артерии (шум Грэхема — Стилла).
На электрокардиограмме — признаки перегрузки левого желудочка.
С помощью эхокардиографии [6] возможны непосредственная визуализация протока, диагностика увеличения размера левого желудочка, определение признаков объемной перегрузки левого желудочка (увеличение амплитуды движения межжелудочковой перегородки и миокарда задней стенки левого желудочка, увеличение левого предсердия; возрастание отношения размеров левого предсердия к диаметру аорты на уровне клапанного кольца > 1,1; уменьшение отношения периода напряжения к периоду изгнания левого желудочка < 0,25; снижение диастолических скоростей кровотока в магистральных церебральных артериях с увеличением индекса их сосудистой резистентности) [7–11].
Критерии постнатальной диагностики следующие:
І. Анамнестические: наличие в генеалогическом анамнезе врожденных либо приобретенных заболеваний сердечно-сосудистой системы, заболевания матери во время беременности, особенно в первом триместре, воздействие на беременную токсических, химических и других факторов, радиоактивного излучения; неблагоприятный акушерский анамнез (аборты, выкидыши), ранняя либо поздняя беременность, большая разница в возрасте родителей, кровнородственные браки; приступы цианоза, асфиксии в периоде новорожденности, отставание в физическом развитии, частые пневмонии, бронхиты у ребенка.
ІІ. Клинические: быстрая утомляемость, одышка, бледность кожи и видимых слизистых оболочек; систолодиастолическое дрожание над областью сердца, максимально выраженное во II межреберье слева от грудины; верхушечный толчок усиленный, разлитой, смещен влево и вниз; смещение границ относительной сердечной тупости влево (за счет гипертрофии левого желудочка в IV–V межреберьях, расширения ствола легочной артерии и гипертрофии левого предсердия в I–II межреберьях); грубый «машинный» непрерывный систолодиастолический шум с максимальным выслушиванием во II межреберье слева от грудины (над легочной артерией), проводящийся в межлопаточное пространство и на сосуды шеи; акцент и расщепление второго тона на легочной артерии. Систолическое артериальное давление нормальное или умеренно повышено за счет большого систолического выброса в аорту, а диастолическое артериальное давление значительно снижено (иногда до 0), существенное увеличение пульсового давления.
В терминальной стадии порока у детей старшего возраста развиваются постоянная одышка, цианоз, более выраженный на нижних конечностях, тахикардия в покое, нарушения сердечного ритма, кардиомегалия, признаки систолической перегрузки и декомпенсация правых отделов сердца: гепатомегалия, отеки на нижних конечностях, пульсация яремных вен.
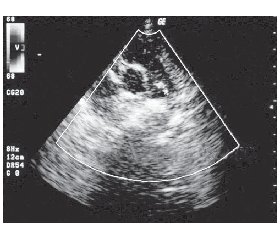
III. Параклинические. 1. Электрокардиограмма: признаки перегрузки левого желудочка, позднее, при развитии легочной гипертензии — обоих желудочков; с уменьшением артериовенозного сброса крови более выражена гипертрофия правого желудочка, появляются нарушения сердечного ритма и проводимости. 2. Эхокардиограмма: увеличение размеров полостей левого предсердия (рис. 2) и левого желудочка, увеличение амплитуды движения митрального клапана. 3. Рентгенологические: усиление сосудистого рисунка легких, увеличение поперечника сердца за счет гипертрофии левого желудочка (кардиоторакальный индекс больше 55–60 %) и сглаженность талии за счет увеличения размеров левого предсердия. Позже, при развитии легочной гипертензии, определяются обеднение периферического рисунка на фоне расширения центральных стволов (форма «обрубленного дерева»), расширение и выбухание ствола легочной артерии по левому контуру сердца, расширение восходящей аорты.
Дифференциальную диагностику следует проводить с функциональным систолодиастолическим шумом «волчка» на сосудах шеи, вызывающим особые трудности в распознавании порока при локализации слева; в таких случаях интенсивность функционального шума меняется при перемене положения тела и при дыхании. В ряде случаев имеются определенные трудности при исключении легочной артериовенозной фистулы, аортолегочного свища, разрыва аневризмы синуса Вальсальвы, коронарной фистулы.
Лечение
Для коррекции гемодинамически значимого функционирующего артериального протока используют консервативное ведение (ограничение объема вводимой жидкости и наблюдение), медикаментозную терапию и хирургическое лечение [12–29]. Метод медикаментозной облитерации с использованием нестероидных противовоспалительных препаратов: индометацина, ибупрофена, парацетамола [30–39] — эффективен у новорожденных в первые две недели жизни. Индометацин вводят внутривенно из расчета 0,1–0,2 мг/кг массы 1–2 раза в сутки в течение 1–3 дней под эхокардиографическим контролем. Курсовая доза — не более 0,6 мг/кг массы тела. Возможны побочные действия: внутричерепные и желудочно-кишечные кровотечения, гипонатриемия, транзиторные ренальные дисфункции. Лечение нестероидными противовоспалительными препаратами противопоказано при почечной недостаточности, энтероколите, нарушениях свертывающей системы крови, билирубинемии выше 0,1 г/л.
Показанием к хирургической коррекции ОАП является установление порока сердца у ребенка после 6–12 мес. жизни. Оптимальный для операции возраст больных — от 2 до 5 лет. При ОАП с синдромом дыхательных расстройств оптимальным возрастом для хирургического лечения является первый месяц жизни ребенка. Метод закрытия ОАП путем перевязки протока либо пересечения с ушиванием обоих концов дает хорошие результаты у 97–98 % оперированных больных, особенно у детей первых лет жизни, при отсутствии развившейся легочной гипертензии.
Прогноз
Узкий ОАП в целом не влияет на продолжительность жизни, но увеличивает риск инфекционного эндокардита. Средний и широкий ОАП практически никогда не закрываются самостоятельно, самопроизвольное закрытие после 3 мес. происходит редко [40]. Эффективность консервативного лечения узких ОАП достигает 90 %. При ОАП летальность в течение первого года жизни составляет 20 %. Синдром Эйзенменгера у детей старшего возраста наблюдают в 14 % случаев, инфекционный эндокардит и эндартериит — в 9 %. Аневризма протока и ее разрывы — единичные случаи. Средняя продолжительность жизни при средних ОАП — 40 лет, при широких — 25 лет. Послеоперационная летальность — 3 %. Клиническая реабилитация в зависимости от гемодинамических нарушений проходит в течение 1–5 лет.
После закрытия артериального протока у детей реканализация обычно не наблюдается, в дальнейшем эти дети нормально развиваются. У недоношенных детей с большим ОАП отмечается формирование бронхолегочных дисплазий, некротизирующего энтероколита, патологии центральной нервной системы (внутрижелудочковые кровоизлияния и гипоксически-ишемическое поражение головного мозга), ретинопатии [41, 42].
Конфликт интересов. Авторы заявляют об отсутствии какого-либо конфликта интересов при подготовке данной статьи.
Список литературы
1. Benson L.N. The Arterial Duct: Its Persistence and Its Patency / L.N. Benson // Paediatric Cardiology. — Philadelphia: Churchill Livingstone, 2010. — P. 875-893. — doi: org/10.1016/B978-0-7020-3064-2.00045-х.
2. Сеидбекова Ф.О. Частота встречаемости врожденных пороков сердца среди новорожденных г. Баку // Вісник проблем біології і медицини. — 2013. — Т. 2, № 1. — С. 158-160.
3. Patent ductus arteriosus — not only a paediatric issue / M. Jędrzejek, J. Sarbinowska, K. Wiślińska, W. Błaż // Paediatrics & Family Medicine. — 2014. — Vol. 1, № 2. — P. 197-211. — DOI: 10.15557/PFM.2014.0018.
4. Доронина Т.Н. Особенности эпидемиологии врожденных пороков сердца у детей раннего возраста / Т.Н. Доронина, Н.С. Черкасов // Медицинский альманах. — 2012. — № 3(22). — С. 175-176.
5. Time to spontaneous ductus arteriosus closure in full-term neonates / H. Nagasawa, C. Hamada, M. Wakabayashi [et al.] // Open Heart. — 2016. — Vol. 3, № 1. — e000413. — DOI: 10.1136/openhrt-2016-000413.
6. Филюшкина М.Н. Фетальные коммуникации у недоношенных детей в течение первого года жизни / М.Н. Филюшкина, А.А. Тарасова, М.С. Ефимов // Ультразвуковая и функциональная диагностика. — 2013. — № 3. — С. 120.
7. Nagasawa H. Evaluation of left ventricular volumes in the early neonatal period using three-dimensional echocardiography / H. Nagasawa // Cardiology in the Young. — 2014. — Vol. 24, Is. 4. — P. 685-693. — DOI: https://doi.org/10.1017/S1047951113000954.
8. Критерії діагностики гемодинамічно значущої відкритої артеріальної протоки у недоношених новонароджених / А.Д. Бойченко, М.О. Гончарь, І.Ю. Кондратова, А.В. Сенаторова // Неонатологія, хірургія та перинатальна медицина. — 2015. — Т. 5, № 1. — С. 24-27.
9. Спивак Е.М. Особенности клинических проявлений открытого артериального протока у глубоконедоношенных детей / Е.М. Спивак, Т.Н. Николаева, А.М. Климачев // Российский вестник перинатологии и педиатрии. — 2016. — Т. 61, № 1. — С. 51-55.
10. Гемодинамічно значуща відкрита артеріальна протока у недоношених новонароджених. Проблема чи ні? / Г.С. Сенаторова, А.Д. Бойченко, М.О. Гончарь [та ін.] // Международный журнал педиатрии, акушерства и гинекологии. — 2015. — Т. 8, № 1. — С. 87.
11. Современные представления об открытом артериальном протоке у новорожденных / Д.С. Крючко, А.Г. Антонов, А.А. Ленюшкина [и др.] // Педиатрия. Журнал им. Г.Н. Сперанского. — 2011. — Т. 90, № 1. — С. 130-136.
12. Patent ductus arteriosus / M.A. Mumtaz, A. Qureshi, C. Mavroudis, C.L. Backer // Pediatric Cardiac Surgery. — Oxford: Blackwell Publishing Ltd, 2013. — P. 225-233. — DOI: 10.1002/9781118320754.ch12.
13. Schneider D.J. The patent ductus arteriosus in term infants, children, and adults // Seminars in perinatology. — 2012. — Vol. 36, № 2. — P. 146-153. — DOI: 10.1053/j.semperi.2011.09.025.
14. Slater B.J. Thoracoscopic Management of Patent Ductus Arteriosus and Vascular Rings in Infants and Children / B.J. Slater, S.S. Rothenberg // Journal of laparoendoscopic & advanced surgical techniques. Part A. — 2016. — Vol. 26, № 1. — P. 66-69. — DOI: 10.1089/lap.2015.0126.
15. Стентування відкритої артеріальної протоки, як етап паліативного лікування, при вроджених вадах серця з дуктус-залежним легеневим кровотоком / A.B. Максименко, Ю.Л. Кузьменко, О.О. Мотречко [та ін.] // Современная педиатрия. — 2014. — № 6. — С. 74-79.
16. Хирургические операции у новорожденных в условиях палаты интенсивной терапии / Ю.А. Козлов, В.А. Новожилов, А.А. Распутин [и др.] // Детская хирургия. — 2016. — № 2. — С. 77-82.
17. Разумовский А.Ю. Минимально-инвазивные способы хирургического лечения открытого артериального протока у детей / А.Ю. Разумовский, Ю.В. Нагорная // Детская хирургия. — 2016. — № 3. — С. 149-155.
18. Nelson Textbook of pediatrics / R.M. Kliegman, B.F. Stanton, J.W. St Geme III, N.F. Schor; ed. by R.E. Behrman. — 20th ed. — Canada: ELSEVIR, 2016. — 5315 p.
19. Patent ductus arteriosus in premature infants: to treat or not to treat? / M.A. Mohamed, M. El-Dib, S. Algahtani [et al.] // Journal of perinatology: official journal of the California Perinatal Association. — 2017, Feb 16. — DOI: 10.1038/jp.2017.4.
20. Transcatheter Closure of Patent Ductus Arteriosus in Adolescents and Adults: A Case Series / S.T. Putra, M.M. Djer, N.S. Idris, S. Sastroasmoro // Acta medica Indonesiana. — 2016. — Vol. 48, № 4. — P. 314-319. — PMID: 28143993.
21. Patent Ductus Arteriosus Treatment in Very Preterm Infants: A European Population-Based Cohort Study (EPICE) on Variation and Outcomes / A.K. Edstedt Bonamy, A. Gudmundsdottir, R.F. Maier [et al.] // Neonatology. — 2017. — Vol. 111, № 4. — P. 367-375. — DOI: 10.1159/000454798.
22. Percutaneous Patent Ductus Arteriosus (PDA) Closure Du-ring Infancy: A Meta-analysis / C.H. Backes, B.K. Rivera, J.A. Bridge [et al.] // Pediatrics. — 2017. — Vol. 139, № 2. — PII: e20162927. — DOI: 10.1542/peds.2016-2927.
23. Lung function in very low birth weight infants after pharmacological and surgical treatment of patent ductus arteriosus — a retrospective analysis / P. Barikbin, H. Sallmon, S. Wilitzki [et al.] // BioMed Central pediatrics. — 2017. — Vol. 17, № 1. — P. 5. — DOI: 10.1186/s12887-016-0762-z.
24. Schranz D. ’End-stage’ heart failure therapy: potential lessons from congenital heart disease: from pulmonary artery banding and interatrial communication to parallel circulation / D. Schranz, H. Akintuerk, N.F. Voelkel // Heart. — 2017. — Vol. 103, № 4. — P. 262-267. — DOI: 10.1136/heartjnl-2015-309110.
25. Patent ductus arteriosus with persistent pulmonary artery hypertension after transcatheter closure / J. Feng, X. Kong, Y. Sheng, R. Yang // Therapeutics and clinical risk management. — 2016. — Vol. 12. — P. 1609-1613. — DOI: 10.2147/TCRM.
S112400.
26. Prescott S. Patent Ductus Arteriosus in the Preterm Infant: Diagnostic and Treatment Options / S. Prescott, J. Keim-Malpass // Advances in neonatal care. — 2017. — Vol. 17, № 1. — P. 10-18. — DOI: 10.1097/ANC.0000000000000340.
27. Организация хирургической помощи преждевременно рожденным детям с функционирующим артериальным протоком в перинатальном центре Автономной Республики Крым / И.А. Аксенова, А.И. Кваша, Б.М. Тодуров [и др.] // Таврический медико-биологический вестник. — 2013. — Т. 16, № 3. — Ч. 1. — С. 36-38.
28. Снісарь В.І. Ефективність способів лікування відкритої артеріальної протоки у недоношених новонароджених з низькою вагою / В.І. Снісарь, І.О. Анікін // Біль, знеболювання і інтенсивна терапія. — 2013. — № 2 (додаток). — С. 454-457.
29. Транскатетерне закриття відкритої артеріальної протоки / Ю.В. Панічкін, І.О. Дітківський, Б.В. Черпак [та ін.] // Серце і судини. — 2011. — № 1. — С. 43-49.
30. Спивак Е.М. Центральная гемодинамика при открытом артериальном протоке у недоношенных новорожденных детей / Е.М. Спивак, А.М. Климачев, И.В. Майден // Ярославский педагогический вестник. — 2013. — Т. 3, № 1. — С. 127-130. — Импакт-фактор журнала в РИНЦ: 0,165.
31. The Effects of Oral Ibuprofen on Medicinal Closure of Pa-tent Ductus Arteriosus in Full-Term Neonates in the Second Postnatal Week / M.R. Alipour, Shamsi M. Mozaffari, S.M. Namayandeh [et al.] // Iranian journal of pediatrics. — 2016. — Vol. 26, № 4. — e5807. — DOI: 10.5812/ijp.5807.
32. Effectiveness and safety of treatments used for the management of patent ductus arteriosus (PDA) in preterm infants: a protocol for a systematic review and network meta-analysis / S. Mitra, I.D. Florez, M.E. Tamayo [et al.] // BMJ Open. — 2016. — Vol. 6, № 7. — e011271. — DOI: 10.1136/bmjopen-2016-011271.
33. Современные стратегии выхаживания недоношенных детей / Д.Н. Сурков, Д.О. Иванов, А.И. Оболонский [и др.] // Детская медицина Северо-Запада. — 2012. — Т. 3, № 1. — С. 4-9.
34. Yen T.A. Efficacy of Repeated Courses of Ibuprofen in the Closure of Patent Ductus Arteriosus in Premature Infants / T.A. Yen, C.C. Wang // Pediatrics and neonatology. — 2017, Jan 19. — PII: S1875-9572(17)30022-0. — DOI: 10.1016/j.pedneo. 2016.12.003.
35. Efficacy and safety of rectal ibuprofen for patent ductus arteriosus closure in very low birth weight preterm infants / N. Demir, E. Peker, İ. Ece [et al.] // Journal of maternal-fetal and neonatal medicine. — 2017, Jan 25. — P. 1-10. — DOI: 10.1080/14767058.2016.1238897.
36. Bancalari E. Management of Patent Ductus Arteriosus: Are We Looking at the Right Outcomes? / E. Bancalari, D. Jain // The Journal of pediatrics. — 2016, Dec 29. — PII: S0022-3476(16)31432-9. — DOI: 10.1016/j.jpeds.2016.12.033.
37. Comparative study of the efficacy and safety of paracetamol, ibuprofen, and indomethacin in closure of patent ductus arteriosus in preterm neonates / A.E. El-Mashad, H. El-Mahdy, D. El-Amrousy, M. Elgendy // European journal of pediatrics. — 2017. — Vol. 176, № 2. — P. 233-240. — DOI: 10.1007/s00431-016-2830-7.
38. The Role of Paracetamol for Closing Patent Ductus Arteriosus. A Challenging Alternative for Ductal Closure? / I. Tofé Valera, M.P. Jaraba Caballero, M.D. Ruiz González [et al.] // Revista española de cardiología (Engl. еd). — 2016. — Vol. 69, № 11. — P. 1103-1104. — DOI: 10.1016/j.rec.2016.05.013.
39. Єсипчук К.В. Медикаментозне лікування відкритої артеріальної протоки / К.В. Єсипчук // Український науково-медичний молодіжний журнал. — 2015. — Спец. вип. 2. — С. 47-48.
40. Шарыкин А.С. Спонтанное закрытие открытого артериального протока у пациента в возрасте 15 лет / А.С. Шарыкин, Е.В. Шилыковская // Педиатрия. Журнал им. Г.Н. Сперанского. — 2012. — Т. 91, № 2. — С. 156-158.
41. Открытый артериальный проток у недоношенного новорожденного: тактика неонатолога / Д.С. Крючко, Е.Н. Байбарина, А.А. Рудакова // Вопросы современной педиатрии. — 2011. — Т. 10, № 1. — С. 58-65.
42. Анікін І.О. Відкрита артеріальна протока у недоношених новонароджених з критичною вагою: сучасний погляд на проблему / І.О. Анікін, B.I. Снісарь // Запорожский медицинский журнал. — 2011. — Т. 13, № 6. — С. 76-80.