Резюме
У статті наведено дані лікування 90 пацієнтів з коінфекцією ВІЛ/ВГС, які отримували противірусне лікування хронічного вірусного гепатиту С (ХВГС). Лікування пег-інтерфероном (Peg-IFN) у комбінації з лікарськими засобами прямої дії, такими як софосбувір та рибавірин, отримували 53 (59 %) пацієнти на тлі прийому антиретровірусної терапії (АРТ), інші хворі були на безінтерферонових схемах терапії. У результаті моніторингу терапії з’ясовано, що мали місце деякі інтерферон- або рибавіринзалежні побічні ефекти в пацієнтів, що потребує мультидисциплінарного підходу до менеджменту пацієнтів для своєчасної корекції несприятливих подій, пов’язаних як зі схемою лікування ХВГС, так і з лікарськими взаємодіями АРТ. Стійку вірусологічну відповідь (СВВ12) отримали 86 (96,6 %) хворих.
В статье приведены данные лечения 90 пациентов с коинфекцией ВИЧ/ВГС, получавших противовирусное лечение хронического вирусного гепатита С (ХВГС). Лечение пег-интерфероном в комбинации с препаратами прямого действия, такими как софосбувир и рибавирин, получали 53 (59 %) пациента на фоне приема антиретровирусной терапии (АРТ), остальные больные были на безынтерфероновых схемах терапии. В результате мониторинга терапии установлено, что имели место некоторые интерферон- или рибавиринзависимые побочные эффекты у пациентов, что требует мультидисциплинарного подхода к менеджменту пациентов для своевременной коррекции неблагоприятных событий, связанных как со схемой лечения ХВГС, так и с лекарственными взаимодействиями АРТ. Стойкий вирусологический ответ (СВВ12) получили 86 (96,6 %) больных.
The article presents data on the treatment of 90 patients with HIV/HCV (human immunodeficiency virus/hepatitis С virus) co-infection who received antiviral treatment against chronic viral hepatitis C (HVHC). Treatment using peginterferon in combination with direct acting drugs such as sofosbuvir and ribavirin was administered to 53 (59 %) patients on the background of antiretroviral therapy (ART), and other patients received non-interferon therapy. As a result of therapy monitoring, it has been found that some interferon- or ribavirin-dependent side effects occurred that required multi-disciplinary approach to patients’ management for timely correction of adverse events associated with both treatment regimen in HVHC and drug interactions in ART. Sustained virologic response (SVR12) was obtained in 86 (96.6 %) patients.
Вступ
Коінфекція ВІЛ/ВГС є досить поширеною серед людей, які живуть із ВІЛ. Так, наприклад, у 2015 році в Україні серед уперше виявлених хворих на ВІЛ-інфекцію HCV-інфекцію мали близько 36 % пацієнтів, а у 2016 році офіційно було зареєстровано 29 980 осіб з коінфекцією ВІЛ/ВГС [1]. Лікування пацієнтів із коінфекцією ВІЛ/ВГС, як і раніше, залишається складним питанням в Україні. HCV-інфекція негативно впливає на перебіг ВІЛ-інфекції, прискорює зниження рівня CD4+-клітин, підвищує ризик летальності внаслідок прогресування стадій ВІЛ-інфекції та розвитку СНІДу. Сама пандемія гемоконтактних вірусних гепатитів за кількістю інфікованих у 4–5 разів перевищує поширеність ВІЛ-інфекції у світі [2]. Також соціальні ризики поширення хвороби ускладнюються тим, що на сьогодні ми не маємо специфічної профілактики гепатиту С та ВІЛ-інфекції. Перебіг HCV-інфекції, як і раніше, має приховану клінічну картину без гострої, яскравої симптоматики та виявляється вже на більш пізніх, хронічних стадіях хвороби, що утруднює своєчасне призначення необхідного лікування хворому та негативно впливає на прогноз і наслідки хвороби [3]. Тож прихований перебіг HCV-інфекції сприяє подальшому поширенню хвороби та спричинює прихований епідемічний процес.
Завдяки прориву в лікуванні хронічного вірусного гепатиту С (ХВГС), появі нових противірусних препаратів прямої дії хворі отримали можливість повністю вилікувати HCV-інфекцію. Але зараз, у перехідний період, застосовуються нові й старі схеми лікування, оскільки безінтерферонова терапія ще недоступна всім хворим через високу вартість [4]. Оскільки Україна належить до країн із високим рівнем поширення ХВГС та обмеженими ресурсами, в Україні ще застосовують схеми, що містять пег-інтерферон у комбінації з лікарськими засобами прямої дії, такими як софосбувір [5].
Мета дослідження: провести моніторинг противірусної терапії хронічного вірусного гепатиту С у хворих із коінфекцією ВІЛ/ВГС, які перебували під наглядом у КЗ «Дніпропетровський обласний центр з профілактики та боротьби зі СНІДом».
Матеріали та методи
У дослідженні проведено ретроспективний аналіз та моніторинг лікування 90 пацієнтів з коінфекцією ВІЛ/ВГС, які отримували лікування хронічного вірусного гепатиту С. Пацієнти були розподілені за статтю та віком (рис. 1).
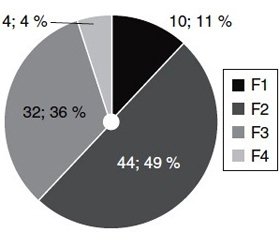
Як видно з рис. 1, хворі розподілились таким чином: чоловіки — 60 (67,7 %), жінки — 30 (33,3 %). Середній вік (М ± SD) становив 42,04 ± 6,10 року. Близько половини хворих (55 %) були у віковому діапазоні 40–49 років, і 49 % хворих мали помірний рівень фіброзу (рис. 2). Зокрема, фіброз F1 мали 10 пацієнтів (11,11 %); F2 — 44 пацієнти (48,89 %); F3 — 32 пацієнти (35,56 %); F4 — 4 пацієнти (4,44 %).
За генотипом HCV хворі розподілились таким чином (рис. 3): 1-й генотип — 51 (56,67 %); 2-й генотип — 3 (3,33 %); 3-й генотип — 36 (40 %) хворих та коінфекція В + С була у 2 пацієнтів (2,2 %). HCV-РНК навантаження > 106 МО/мл було в 38 пацієнтів (42,22 %).
/50-1.jpg)
Лікування гепатиту С було призначене 92,22 % наївних пацієнтів (83 хворі). У 85 (94,4 %) пацієнтів лікування гепатиту С проводилось на тлі прийому антиретровірусної терапії (АРТ). У всіх пацієнтів рівень ВІЛ-РНК був на рівні ≤ 40 копій/мл. Хворі були зі стадією А та В (за CDC). Туберкульоз в анамнезі перенесли 20 осіб (30,3 %). Кількість CD4+ > 200 клітин/мкл — у 42 (46,6 %) і > 500 клітин/мкл — у 48 (53,3 %) пацієнтів. Також у хворих проводився моніторинг загальноклінічних та біохімічних показників крові, враховувались наявність анемії, зміни печінкового комплексу й інші несприятливі події або побічні явища. Проводилось опитування хворих у вигляді анкетування для оцінки тривоги, депресії. Була використана адаптована госпітальна шкала тривоги й депресії (HADS) (Zigmond and Snaith, 1983). Дослідний інструмент p < 0,05 було визначено як статистично значимий.
Хворі отримували противірусну терапію ВГС із застосуванням препаратів прямої дії та інтерферонів. Схеми терапії призначались згідно з протоколами та рекомендаціями залежно від генотипу HCV. Розподіл хворих у групах залежно від схеми терапії поданий на рис. 4.
Як видно з рис. 4, такі схеми призначались хворим протягом 12 або 24 тижнів: SOF + Peg-IFN + RBV12W — 53 (59 %); SOF + DCV12W — 18 (20 %); SOF + RBV24W — 8 (9 %); SOF + RBV12W — 2 (2 %); SOF + DCV + RBV12W — 6 (7 %); SOF + DCV + RBV24W — 1 (1 %); SOF/LDV + RBV12W — 1 (1 %); SOF/LDV12W — 1 (1 %). Пацієнтам, які отримували АРТ, корегували дози противірусної терапії, враховуючі взаємодію ліків. При призначенні рибавірину азидотимідин замінювали на тенофовір або абакавір перед початком терапії. З використанням ефавіренцу доза даклатасвіру збільшувалася до 90 мг.
Результати та обговорення
Аналіз отриманих даних показав, що застосування схем, що містять пег-інтерферон у комбінації з лікарськими засобами прямої дії, виявилось ефективним порівняно з попередніми дослідженнями, у яких застосовувались лише пегільований інтерферон та рибавірин. Один пацієнт припинив лікування через низьку прихильність, три пацієнти мали рецидив на 12-му тижні після закінчення лікування. Отже, загалом стійку вірусологічну відповідь (СВВ12) мали 86 (96,6 %) хворих.
Також аналіз показав наявність деяких побічних явищ у дослідній групі пацієнтів, що залежали від схеми терапії. Так, у ході лікування пацієнти, які отримували рибавірин або пег-інтерферон, мали такі побічні реакції: анемія — 46 (51,1 %), нейтропенія — 11 (12,2 %).
При оцінці за госпітальною шкалою тривоги та депресії в динаміці виявилось, що на початку терапії серед хворих, які отримували пег-інтерферон, легкий ступінь тривоги через два місяці лікування фіксувався в 50 осіб (55,5 %), а субклінічна депресія реєструвалась у 13 (14,4 %) хворих. У разі необхідності проводилась корекція лікування. Пацієнти були консультовані психіатром та отримували необхідне лікування, включаючи за необхідності застосування трициклічних антидепресантів на короткий час. Інші побічні ефекти спостерігалися в 5–10 % пацієнтів: нудота, дратівливість, міалгія, сухість шкіри, порушення сну. Усі описані побічні ефекти були переважно м’якими, підлягали корегуванню й не потребували припинення терапії.
Висновки
Результати показали, що один пацієнт припинив лікування через низьку прихильність, СВВ12 мали 86 (96,6 %) хворих із коінфекцією ВІЛ/ВГС. Незважаючи на більш короткий курс лікування при призначенні препаратів прямої дії для лікування ХВГС, продовження застосування у схемах пегільованого інтерферону та рибавірину в пацієнтів із коінфекцією ВІЛ/ВГС призводить до небезпеки виникнення деяких інтерферон- або рибавіринзалежних побічних ефектів у пацієнтів. Тому потрібен мультидисциплінарний підхід до ведення пацієнтів для своєчасної корекції несприятливих подій, що пов’язані як із схемою лікування ХВГС, так і з лікарськими взаємодіями АРТ.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.

/50-1.jpg)
/50-2.jpg)