Резюме
Актуальність. Відношення між хронічною хворобою нирок (ХХН) і кардіоваскулярними захворюваннями (КВЗ) є важливими та комплексними і характеризуються наявністю численних несприятливих чинників порівняно з хворими з самостійними КВЗ. Мета дослідження: оцінити частоту факторів кардіоваскулярного ризику серцево-судинних ускладнень, нефрологічних факторів ризику та їх комбінацію у пацієнтів з ХХН IV–V ст., які дожили до етапу замісної ниркової терапії. Матеріали та методи. Ретроспективно проаналізовано медичну документацію (упродовж 2 років) 42 хворих (чоловіків — 12 (28,6 %), жінок — 30 (71,4 %)) на ХХН IV–V стадії, які на час проведення аналізу медичної документації не отримували замісну ниркову терапію. Усім хворим розраховували індекс маси тіла (ІМТ), визначали артеріальний тиск (АТ), частоту серцевих скорочень (ЧСС), оцінювали показники загального та біохімічного аналізу крові та сечі, визначали рівень залишкового діурезу. У всіх хворих обчислено швидкість клубочкової фільтрації (ШКФ) за формулою CKD-EPI. Статистична обробка матеріалів дослідження — пакет програм Statistica v.6.1 (Statsoft Inc., США). Результати. Середній вік пацієнтів становив 47,6 ± 11,6 року. Отримані дані засвідчили, що хворі на ХХН, які дожили до замісної ниркової терапії, мали добовий діурез понад 500 мл, ЧСС менше 90 уд/хв, рівень систолічного АТ у таких пацієнтів підтримувався медикаментозно на рівні менше 160 мм рт.ст., також характерною ознакою був рівень загального холестерину (ЗХС) крові ≥ 4,5 ммоль/л та ІМТ понад 25 кг/м2. Нами був виявлений прямий кореляційний зв’язок між рівнем ШКФ та рівнем ЗХС крові (r = 0,32, р = 0,04); між ШКФ та рівнем гемоглобіну крові (r = 0,39, р = 0,01) і прямий кореляційний зв’язок між ШКФ і кількістю залишкової сечі у обстежених хворих (r = 0,32, р = 0,04). Висновки. Найбільш вагомими чинниками доживання хворого на ХХН до замісної ниркової терапії є молодий вік (до 40 років), наявність залишкової сечі (добовий діурез понад 500 мл/добу), відсутність цукрового діабету. Велику роль відіграє контроль систолічного АТ < 160 мм рт.ст. та анемії.
Актуальность. Взаимосвязи между хронической болезнью почек (ХБП) и кардиоваскулярными заболеваниями (КВЗ) являются важными и комплексными, характеризуются наличием многочисленных неблагоприятных факторов по сравнению с больными с самостоятельными КВЗ. Цель исследования: оценить частоту факторов кардиоваскулярного риска сердечно-сосудистых осложнений, нефрологических факторов риска и их комбинацию у пациентов с ХБП IV–V ст., которые дожили до этапа заместительной почечной терапии. Материалы и методы. Ретроспективно проанализирована медицинская документация (в течение 2 лет) 42 пациентов (мужчин — 12 (28,6 %), женщин — 30 (71,4 %)) с ХБП IV–V стадией, которые на время проведения анализа медицинской документации не получали заместительную почечную терапию. Всем больным рассчитывали индекс массы тела (ИМТ), определяли артериальное давление (АД), частоту сердечных сокращений (ЧСС), оценивали показатели общего и биохимического анализа крови, мочи, определяли уровень остаточного диуреза. У всех больных вычислялась скорость клубочковой фильтрации (СКФ) по формуле CKD-EPI. Статистическая обработка материалов исследования — пакет программ Statistica v.6.1 (Statsoft Inc., США). Результаты. Средний возраст пациентов составил 47,6 ± 11,6 года. Полученные данные показали, что больные ХБП, которые дожили до заместительной почечной терапии, имели суточный диурез более 500 мл, ЧСС менее 90 уд/мин, уровень САД у таких пациентов поддерживался медикаментозно на уровне менее 160 мм рт.ст., также характерным признаком был уровень общего холестерина (ОХС) крови ≥ 4,5 ммоль/л и ИМТ более 25 кг/м2. Нами была обнаружена прямая корреляционная связь между уровнем СКФ и уровнем ОХС крови (r = 0,32, р = 0,04); между СКФ и уровнем гемоглобина крови (r = 0,39, р = 0,01) и прямая корреляционная связь между СКФ и количеством остаточной мочи у обследованных больных (r = 0,32, р = 0,04). Выводы. Наиболее значимыми факторами дожития больного ХБП до заместительной почечной терапии являются молодой возраст (до 40 лет), наличие остаточной мочи (суточный диурез более 500 мл/сут), отсутствие сахарного диабета. Большую роль играет контроль систолического АД < 160 мм рт.ст. и анемии.
Background. The relationship between chronic kidney disease (CKD) and cardiovascular diseases is important and is characterized by the presence of numerous adverse factors compared with patients with cardiovascular disease alone. The purpose of the study is to evaluate the incidence of risk factors for cardiovascular complications, nephrological risk factors and their combination in patients with CKD stage IV–V, who survived to the stage of renal replacement therapy. Materials and methods. Retrospectively, we have analyzed medical records (for 2 years) of 42 patients (12 (28.6 %) men, 30 (71.4 %) women) with CKD stage IV–V, who by the time of medical records analysis did not receive renal replacement therapy. All patients underwent the following measurements: body mass index, blood pressure, heart rate, complete blood count and biochemical blood test, the level of residual diuresis. To determine glomerular filtration rate (GFR), we used Chronic Kidney Disease Epidemiology Collaboration equation. Statistical processing of research materials was performed by means of Statistica v. 6.1 software package (Statsoft Inc., USA). Results. The mean age of patients was 47.6 ± 11.6 years. The study showed that patients with CKD, who survived to renal replacement therapy, had daily diuresis more than 500 ml, heart rate less than 90 bpm. Systolic blood pressure in such patients was maintained with drugs at the level of not less than 160 mmHg. The level of total cholesterol more than 4.5 mmol/l and body mass index more than 25 kg/m2 were also characteristic features. We found a direct correlation between GFR and total cholesterol (r = 0.32, p = 0.04), GFR and hemoglobin (r = 0.39, p = 0.01) and a direct correlation between GFR and the amount of residual urine (r = 0.32, p = 0.04). Conclusions. The most significant factors of survival of a patient with CKD before renal replacement therapy are: young age (under 40 years), presence of residual urine (daily diuresis more than 500 ml/day), absence of diabetes mellitus. The control of anemia and systolic blood pressure < 160 mmHg are of particular importance.
Вступ
Хронічна хвороба нирок (ХХН) на сучасному етапі розглядається як актуальна проблема не тільки нефрології, а й усієї внутрішньої медицини. Невпинне зростання захворюваності на ХХН у світі досягає розмірів епідемії. Поширеність ХХН, за різними даними, коливається від 10 до 30 % від загального населення [1–3]. Щорічно збільшується частота виявлення ниркової недостатності, що потребує великих затрат на лікування. Слід зазначити, що пізня діагностика суттєво погіршує подальший прогноз.
На всіх стадіях прогресування ХХН у пацієнтів зростає ризик розвитку кардіоваскулярних захворювань (КВЗ) та ймовірність смерті від кардіоваскулярних ускладнень (КВУ) [2]. За літературними даними, кардіоваскулярний ризик (КВР) при ХХН IV–V ст., що відповідає зниженню швидкості клубочкової фільтрації (ШКФ) < 30 мл/хв, переважає такий при збереженій функції нирок в 5,5 раза [4].
Серед факторів ризику розвитку КВУ при ХХН виділяють як традиційні кардіологічні (діабет, гіпертензія, паління та дисліпідемія), так і нефрологічні фактори ризику (анемія, протеїнурія, рівень залишкового діурезу, гіпоальбумінемія). Наявність у хворого ХХН, згідно з теорією кардіоренального континууму, вже вказує на високий ризик КВЗ, а додаткові фактори ризику, залучені до порочного кола, лише погіршують прогноз пацієнтів [5–7].
Найчастішими причинами смерті хворих на ХХН є гострі серцево-судинні події: їх частка становить 30–52 %, що в 5–20 разів вище, ніж в інший популяції [8].
Між початком захворювання на ХХН і потребою в замісній нирковій терапії проходять роки поступового, але прогресуючого погіршення стану пацієнта [9]. На різних стадіях ХХН превалює різна симптоматика, із якої досить тяжко відокремити суто нефрологічні та суто кардіологічні симптоми. Тривалий час патологія нирок розглядалась ізольовано від кардіологічних ризиків.
На початкових стадіях розвитку ниркової недостатності ризик розвитку КВЗ вищий, ніж в іншій популяції (30,1 проти 13,2 %), а у пацієнтів, які знаходяться на гемодіалізі, ризик розвитку КВЗ і смертності від КВЗ в 10–30 разів вище, ніж в іншій популяції людей [2].
Відношення між ХХН і КВЗ є важливими і комплексними та характеризуються наявністю численних несприятливих чинників порівняно з хворими з самостійними КВЗ (рис. 1).
Виявлення та корекція факторів ризику КВЗ — відомий золотий стандарт профілактики в кардіології, в той час як розкриття ролі спільних факторів ризику для КВЗ та ХХН, їх модифікація дозволить суттєво зменшити смертність серед хворих на ХХН та збільшити відсоток тих, хто дожив до етапу замісної ниркової терапії.
Оскільки фактори ризику КВЗ прямо впливають на прогноз для життя хворого з ХХН, саме вони призводять до зниження не тільки відсотка пацієнтів, що дожили до діалізу, але й віку пацієнтів, що знаходяться на діалізі в Україні порівняно з Європою. Так, середній вік пацієнтів на діалізі в Європі становить 64 роки, до 20 % пацієнтів мають вік понад 75 років [2]. На жаль, в Україні середній вік пацієнта на діалізі значно менший, що може свідчити про пізню діагностику та несвоєчасне лікування станів, які призводять до розвитку ХХН.
Наведені літературні дані вказують на важливість виявлення та корекцію факторів ризику розвитку КВЗ та КВУ у хворих на ХХН.
Таким чином, частота і різноманітність факторів ризику КВУ, а також їх комбінації або наявність КВЗ в анамнезі у конкретного хворого істотно впливають на подальший прогноз для його життя і є визначальними в доживанні пацієнтів до етапу замісної ниркової терапії.
Мета роботи: оцінити частоту факторів кардіо–васкулярного ризику серцево-судинних ускладнень, нефрологічних факторів ризику та їх комбінацію у пацієнтів з ХХН IV–V ст., які дожили до етапу замісної ниркової терапії.
Матеріали та методи
Відповідно до мети й завдань дослідження було ретроспективно проаналізовано медичну документацію (упродовж 2 років) 42 хворих на ХХН IV–V стадії (табл. 1).
Критерії включення до дослідження: хворі на ХХН IV–V ст. (ШКФ ≤ 29 мл/хв/1,73 м2), які на момент проведення аналізу не отримували замісної ниркової терапії.
Критерії виключення: гострий інфаркт міокарда менше 3 місяців; гостре порушення мозкового кровообігу менше 3 місяців; порушення ритму, що вимагали медикаментозного лікування; хронічна серцева недостатність IІІ ст.; тромбоемболія легеневої артерії; анемії, обумовлені іншими факторами; патологія щитоподібної залози; гостре пошкодження нирки.
Діагноз ХХН було встановлено відповідно до клінічних протоколів, рекомендованих МОЗ України та Європейським товариством нефрологів.
Лікування хворих проводилося згідно з Наказом МОЗ України від 11 травня 2011 року № 280/44 «Про затвердження стандарту та уніфікованих клінічних протоколів надання медичної допомоги зі спеціальності «нефрологія» [10].
Усім хворим за антропометричними даними розраховували індекс маси тіла (ІМТ) за формулою: маса тіла (кг) / зріст (м2). У групу з надмірною масою тіла були віднесені хворі зі значенням ІМТ від 25,0 до 29,9 кг/м2, а ожиріння діагностували при значенні ІМТ 30 кг/м2 і більше. Артеріальний тиск (АТ) визначали методом аускультації тонів М.С. Короткова з використанням тонометра після 5-хвилинного відпочинку пацієнта. У всіх пацієнтів оцінювали показники загального та біохімічного аналізу крові та сечі за загальноприйнятими методиками, визначали рівень залишкового діурезу. Для виявлення наявності та характеру ураження нирок у всіх пацієнтів обчислено ШКФ за формулою CKD-EPI [11].
Усім хворим проводили електрокардіографічне дослідження (ЕКГ) за допомогою електрокардіографа ЮКАРД-200 фірми UTAS (Україна) в 12 стандартних відведеннях з реєстрацією не менше 4 передсердно-шлуночкових комплексів. При ЕКГ у 12 відведеннях відмічали ознаки порушення ритму та провідності, гіпертрофії лівого шлуночка (ЛШ) та правого шлуночка, рубцеві зміни. Гіпертрофію ЛШ діагностували згідно з загальноприйнятими критеріями, розробленими M. Sokolov, T. Lyon: сума амплітуд зубців Sv1 + Rv5 більше 35 мм в осіб старше 40 років, більше 45 мм — в осіб молодше 40 років.
Статистичну обробку матеріалів дослідження проводили з використанням методів біостатистики, реалізованих у пакеті програм Statistica v.6.1 (Statsoft Inc., США) (ліцензійний номер AJAR909E415822FA). Первинна обробка отриманих даних проводилася методами описової статистики з поданням результатів для кількісних ознак (з урахуванням закону розподілу) у вигляді: кількості спостережень (n), середньої арифметичної (M), стандартної похибки середньої величини (m), стандартного відхилення (SD). Оцінка вірогідності відмінностей середніх для незв’язаних та зв’язаних вибірок проводилась за критеріями Стьюдента (t). Критичне значення рівня значимості (р) приймалося ≤ 0,05. Для оцінки взаємозв’язку між ознаками виконувався кореляційний аналіз з розрахунком коефіцієнтів рангової кореляції Спірмена (r).
Результати та обговорення
За результатами дослідження спостерігалося, що в співвідношенні чоловіків і жінок в обстеженій групі переважали жінки (табл. 1). Спостерігався більш молодший (47,6 ± 11,6 року) середній вік пацієнтів порівняно з Європою, що свідчить про те, що пацієнти більш старшого віку, в яких апріорі зростає ризик розвитку КВУ, не доживають до етапу замісної ниркової терапії.
Усі пацієнти в дослідженні мали артеріальну гіпертензію (табл. 2) на тлі прийому антигіпертензивної терапії. Лікування артеріальної гіпертензії проводили згідно з клінічними протоколами, затвердженими МОЗ України. В середньому пацієнти отримували 3 антигіпертензивних препарати. Середній рівень систолічного артеріального тиску у обстежених хворих — 162,2 ± 22,8 мм рт.ст., діастолічного артеріального тиску — 97,6 ± 12,1 мм рт.ст.
Таким чином, серед проаналізованих історій хвороби хворих на ХХН лише в 11,9 % хворих було досягнуто медикаментозно цільових значень АТ.
Керуючись ЕКГ-критерієм — індексом Соколова — Лайона, гіпертрофія лівого шлуночка визначено у 38 (90,5 %) хворих.
При оцінці частоти серцевих скорочень (ЧСС) виявлено, що лише 9 (21,4 %) хворих на ХХН мали рівень ЧСС ≥ 90 уд/хв. Середній рівень ЧСС серед обстежених хворих — 82,1 ± 4,7 уд/хв. Таким чином, виявлена тахікардія (ЧСС понад 90 уд/хв) є несприятливим додатковим кардіоваскулярним фактором ризику у хворих на ХХН.
Одним із найважливіших факторів ризику розвитку КВЗ є рівень загального холестерину (ЗХС) [12, 13]. За результатами обстеження було отримано наступні показники ЗХС (табл. 3).
Згідно з розрахунком і оцінкою ІМТ у обстежених хворих (табл. 4), превалювали надлишкова маса тіла та ожиріння 1–2-го ст., що в контексті кардіологічної патології було б розцінено як негативний чинник прогнозу [12]. Отже, у хворих на ХХН такі показники, ймовірно, позитивно впливають на виживання хворих і свідчать про відсутність синдрому білково-енергетичної недостатності. У той же час серед обстежених хворих відсутні пацієнти з ІМТ ≥ 40 кг/м2, що дало змогу оцінити це як негативний прогностичний чинник.
На жаль, оцінити тютюнопаління як один з вагомих кардіоваскулярних факторів ризику КВУ не вдалося через недостатню кількість даних у медичній документації.
Таким чином, можна розглянути частоту комбінації кардіоваскулярних факторів ризику КВУ у хворих на ХХН (рис. 3).
Серед найбільш значущих нефрологічних факторів ризику виділяють анемію [15]. Анемія у хворих на ХХН є не тільки значно поширеною проблемою при уремії, але й розглядається як незалежний фактор ризику КВУ і смертності [15, 16]. Разом із ретенцією рідини у хворих на ХХН анемія відіграє роль в перевантаженні серця об’ємом і, як наслідок, призводить до ремоделювання лівого шлуночка за ексцентричним типом гіпертрофії. Анемія погіршує оксигенацію тканин, обмежує фізичну активність пацієнтів і знижує якість життя.
За нашими даними, спостерігалися наступні показники гемоглобіну у обстежених хворих (табл. 5).
Таким чином, у 64,3 % обстежених хворих спостерігався показник Нb ≤ 90 г/л, що є значно нижче оптимального, описаного у світовій літературі рівня Нb, що може бути пояснено значно нижчою забезпеченістю хворих на ХХН ІV–V ст. препаратами, стимулюючими еритропоез у додіалізному періоді.
Нами було виявлено прямий кореляційний зв’язок між ШКФ та рівнем Нb крові (рис. 4).
Рівень альбумінів крові у обстежених хворих наведено у табл. 6.
Велику роль, за даними літератури, в процесі доживання хворих на ХХН відіграє наявність залишкової сечі. Так, 40 пацієнтів (95,2 % обстежених) мали добовий діурез понад 500 мл. Лише у 2 хворих добова кількість сечі становила менше 500 мл, що асоціювалось з гіршим прогнозом.
Нами був виявлений прямий кореляційний зв’язок між ШКФ та кількістю залишкової сечі у обстежених хворих (рис. 5).
За показниками добового аналізу сечі оцінювалась наявність протеїнурії. За нашими даними, у 34 хворих (80,9 % обстежених) було виявлено протеїн–урію помірного ступеня (≤ 1,5 г/добу).
Згідно з даними реєстру Європейської асоціації нефрологів, кількість хворих з термінальною ХНН, обумовленою ЦД (цукровий діабет) 1-го та 2-го типів, які перебувають на діалізі, становить 26 %. Серед обстежених нами хворих ЦД мав місце у 8 (19 %) хворих, серед яких ЦД 1-го типу становив 62,5 %, а ЦД 2-го типу —37,5 %. Цей показник є маркером того, яка кількість хворих з тяжким перебігом ЦД та діабетичною нефропатією доживає до етапу замісної ниркової терапії [17].
Частота комбінації нефрологічних факторів ризику у хворих на ХХН наведено на рис. 6.
Для об’єктивної оцінки впливу комбінації факторів ризику на дожиття хворих до замісної ниркової терапії було проаналізовано частоту комбінації кардіоваскулярних та нефрологічних факторів ризику (рис. 7).
Отримані результати засвідчили обернену залежність між кількістю факторів ризику і кількістю хворих, що дожили до етапу замісної ниркової терапії.
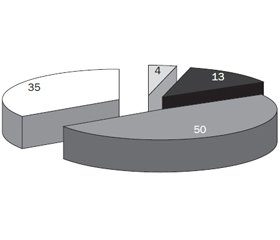
З метою виявлення найбільш вагомих чинників доживання хворих до замісної ниркової терапії було розглянуто частоту виявлення кожного окремо взятого фактора ризику (рис. 8).
Отримані дані свідчать, що хворі на ХХН, які дожили до замісної ниркової терапії, мали добовий діурез понад 500 мл, ЧСС менше 90 уд/хв, рівень САТ у таких пацієнтів підтримувався медикаментозно на рівні менше 160 мм рт.ст., також характерною ознакою є рівень ЗХС крові ≥ 4,5 ммоль/л та ІМТ понад 25 кг/м2. Даний аспект слід оцінювати з точку зору необхідності жорсткого контролю заходів щодо ренопротекції та вторинної профілактики КВЗ.
Результати, отримані у дослідженні, можуть бути перспективними при розробці профілактичних заходів у хворих на ХХН з метою зменшення кардіоваскулярних ускладнень і збільшення відсотка хворих, що доживуть до замісної ниркової терапії.
Висновки
1. Серед кардіоваскулярних факторів ризику у хворих на ХХН IV–V ст. до несприятливих пре–дикторів КВУ слід віднести: вік хворого та рівень ЗХС понад 4,5 ммоль/л, резистентну артеріальну гіпертензію на тлі прийому ≥ 3 антигіпертензивних засобів. Вкрай несприятливими кардіоваскулярними факторами ризику для хворих на ХХН є тахікардія (ЧСС понад 90 уд/хв) та рівень САТ понад 160 мм рт.ст. на тлі прийому антигіпертензивних препаратів.
2. Серед нефрологічних факторів ризику для хворих на ХХН найнесприятливішим є зниження добового діурезу менше 500 мл/добу. Наявність ЦД та тяжкої діабетичної нефропатії на тлі білково-енергетичної недостатності (гіпоальбумінемія < 35 г/л та ІМТ ≤ 18,5 кг/м2) асоціюється з гіршим прогнозом для виживанням.
3. Серед комбінації кардіоваскулярних і нефрологічних факторів ризику у хворих на ХХН найчастіше зустрічалось поєднання 5 факторів ризику (30 %) хворих, комбінація більшої кількості факторів ризику є прогностично несприятливою.
4. Найбільш вагомі чинники доживання хворого до замісної ниркової терапії: молодий вік (до 40 років), наявність залишкової сечі (добовий діурез понад 500 мл/добу), відсутність ЦД, велику роль відіграє контроль САТ < 160 мм рт.ст. та анемії.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
Інформація про внесок кожного автора
Курята О.В. — концепція і дизайн дослідження; Фролова Є.О. — збирання й обробка матеріалів, аналіз отриманих даних, написання тексту; Ященко Т.Д. — збирання матеріалів.
Рецензенти: д.м.н, проф. И.М. Фуштей, д.м.н., ст.н.с. І.В. Дроздова.
Список литературы
1. Chronic kidney disease as a global public health problem: approaches and initiatives — a position statement from Kidney Disease Improving Global Outcomes / A.S. Levey, R. Atkins, J. Coresh et al. // Kidney Int. — 2007. — 72. — Р. 247-59. — doi: 10.1038/sj.ki.5002343.
2. Курята О.В. Ліпідний обмін і кардіоваскулярний ризик у хворих на хронічну хворобу нирок: монографія / О.В. Курята, Є.О. Фролова. — Дніпропетровськ: Герда, 2013. — 112 с.
3. Couser W.G. The contribution of chronic kidney desease to the global burden of major noncommunicable disease / W.G. Couser, G. Remuzzi, S. Mendis, M. Tonelli // Kidney Int. — 2011. — 80(12). — Р. 1258-70. — doi: 10.1038/ki.2011.368.
4. Ene-Iordache B. Chronic kidney disease and cardiovascular risk in six regions of the world (ISN-KDDC): a cross-sectional study / B. Ene-Iordache // The Lancet Global Health. — 2016. — V. 4, № 5. — P. e307-e319. — doi: 10.1016/S2214-109X(16)00071-1.
5. Мельник А.А. Кардиоренальный синдром: диагностика, лечение / А.А. Мельник // Почки. — 2017. — Т. 6, № 1. — С. 10-22. — doi: 10.22141/2307-1257.6.1.2017.93777.
6. Визир В.А. Кардиоренальный синдром / В.А. Визир, А.Е. Березин // Артериальная гипертензия. — 2011. — № 2(16). — С. 100-109.
7. Ronco C. Cardiorenal syndrome in Critical Care / C. Ronco, R. Bellomo, P.A. McCullough // Contr. Nephrol. —
2010. — 165.
8. Колесник М.О. Кардіоваскулярні ускладнення у хворих на хронічну хворобу нирок / М.О. Колесник, І.І. Лапчинська, В.К. Тащук [та ін.] — К.: Поліграф плюс, 2010. — 224 с.
9. Jala D.I. Uric acid as a target of therapy in CKD / D.I. Jala, M. Chronhol, W. Chen, G. Targher // Am. J. Kidney Dis. — 2013. — № 61(1). — P. 134-146. — doi: 10.1053/j.ajkd.2012.07.021.
10. Наказ МОЗ України від 11 травня 2011 року № 280/44 «Про затвердження стандарту та уніфікованих клінічних протоколів надання медичної допомоги зі спеціальності «нефрологія». — Режим доступу: http://moz.gov.ua.
11. Kidney Disease: Improving Global Outcomes (KDIGO) 2012: Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease // Kidney Int. — 2013. — V. 3. — Р. 1-150.
12. Мельник А.А. Метаболический синдром и риск хронической болезни почек / А.А. Мельник // Почки. — 2017. — Т. 6, № 2. — С. 11-21. — doi: 10.22141/2307-1257.6.2.2017.102785.
13. Мельник А.А. Нарушение липидного обмена и его коррекция при хронической болезни почек / А.А. Мельник // Почки. — 2016. — № 2(16). — С. 85-95.
14. Vazini N.D. Lipid disorders and their relevance to outcomes in chronic kidney disease / N.D. Vazini, K. Norris // Blood Purif. — 2011. — № 31(1–3). — P. 433-446.
15. Kidney Disease: Improving Global Outcomes (KDIGO) Anemia Work Group. KDIGO Clinical Practice Guideline for Anemia in Chronic Kidney Disease // Kidney Int. — 2012. — Suppl. 2. — P. 279-335.
16. Курята А.В. Морфофункциональное состояние мио–карда и его изменение под влиянием коррекции анемии средствами, стимулирующими эритропоэз у пациентов на программном гемодиализе / А.В. Курята, Е.А. Фролова // Український журнал нефрології та діалізу. — 2011. — № 4(32). — С. 39-48.
17. Скалій Н.М. Медикаментозна корекція діабетичної нефропатії на стадії гіперфільтрації / Н.М. Скалій // Нирки. — 2016. — № 1(15). — С. 71-73.

/10-1.jpg)
/11-1.jpg)
/12-1.jpg)
/13-1.jpg)
/13-3.jpg)
/13-2.jpg)
/14-1.jpg)
/14-2.jpg)