Резюме
Актуальність. Практично постійним проявом подагри є ураження нирок, яке визначає прогноз хвороби. Гіперурикемія при подагричній нефропатії належить до незалежних чинників ризику зниження азото- й електролітовидільної функції нирок. Метою дослідження стала порівняльна оцінка впливу урикодепресантів алопуринолу і фебуксостату на функціональний стан нирок у хворих на подагру. Матеріали та методи. Під наглядом перебували 73 хворі на первинну подагру (чоловіки із середнім віком 49 років та тривалістю захворювання 10 років). Хронічну форму артриту встановлено в 71 % від числа хворих, інтермітовану — в 29 %, периферійні тофуси виявлено в 53 % випадків. Хронічну хворобу нирок I, II, III і IV стадії виявлено у співвідношенні 56 : 12 : 2 : 1, латентний, уролітіазний і протеїнуричний типи подагричної нефропатії — у 53, 37, 10 %, артеріальну гіпертензію — у 47 %. Гіперурикемію на момент обстеження констатовано у 84 % хворих, гіперурикурію — у 52 %, метаболічний, нирковий і змішаний типи гіперурикемії мали місце відповідно в 57, 3 і 40 % випадків. Результати. При порівняльній оцінці інгібіторів ксантиноксидази алопуринолу й ксантиноксиредуктази фебуксостату відносно функції нирок у хворих на подагричну нефропатію перевагу слід віддати другому препарату, хоча гіпоурикемічна дія обох урикодепресантів приблизно однакова, а прогностичними критеріями ефективності алопуринол- та фебуксостат-терапії відповідно є початкові показники в’язкоеластичності сечі і β2-мікроглобулінурії. Висновки. У перспективі буде корисним визначення морфологічних змін з боку нирок при експериментальній подагричній нефропатії під впливом алопуринолу й фебуксостату, а також доцільна оцінка результатів комбінованого застосування урикодепресантів з іншими групами гіпоурикемічних засобів (урикозуриками, ферментом пеглотиказой тощо).
Актуальность. Практически постоянным проявлением подагры является поражение почек, которое определяет прогноз болезни. Гиперурикемия при подагрической нефропатии относится к независимым факторам риска снижения азото- и электролитовыделительной функции почек. Целью исследования стала сравнительная оценка влияния урикодепрессантов аллопуринола и фебуксостата на функциональное состояние почек у больных подагрой. Материалы и методы. Под наблюдением находилось 73 больных первичной подагрой (мужчины со средним возрастом 49 лет и длительностью заболевания 10 лет). Хроническая форма артрита установлена в 71 % от числа больных, интермиттирующая — в 29 %, периферические тофусы обнаружены в 53 % случаев. Хроническая болезнь почек I, II, III и IV стадии выявлена в соотношении 56 : 12 : 2 : 1, латентный, уролитиазный и протеинурический типы подагрической нефропатии — в 53, 37, 10 %, артериальная гипертензия — в 47 %. Гиперурикемия на момент обследования констатирована у 84 % больных, гиперурикурия — у 52 %, метаболический, почечный и смешанный типы гиперурикемии имели место соответственно в 57,3 и 40 % случаев. Результаты. При сравнительной оценке ингибиторов ксантиноксидазы аллопуринола и ксантиноксиредуктазы фебуксостата в отношении функции почек у больных подагрической нефропатией предпочтение следует отдать второму препарату, хотя гипоурикемическое действие обоих урикодепрессантов примерно одинаково, а прогностическими критериями эффективности аллопуринол- и фебуксостат-терапии соответственно являются исходные показатели вязкоэластичности мочи и β2-микроглобулинурии. Выводы. В перспективе будет полезным определение морфологических изменений со стороны почек при экспериментальной подагрической нефропатии под влиянием аллопуринола и фебуксостата, а также целесообразна оценка результатов комбинированного применения урикодепрессантов с другими группами гипоурикемических средств (урикозуриками, ферментом пеглотиказой и пр.).
Background. Renal damage is an almost constant symptom of gout, which determines the prognosis of the disease. Hyperuricemia in gouty nephropathy belongs to independent risk factors for deterioration of the nitrogen and electrolyte excretory function of the kidneys. The purpose of the study was a comparative evaluation of the effect of uricodepressants allopurinol and febuxostat on the functional state of the kidneys in patients with gout. Materials and methods. Seventy three patients with primary gout (men with an average age of 49 years and disease duration of 10 years) were examined. The chronic form of arthritis was diagnosed in 71 % of cases, the intermittent one — in 29 %, peripheral tofi were detected in 53 % of patients. Chronic kidney disease stage I, II, III and IV was diagnosed at a ratio of 56 : 12 : 2 : 1, latent, urolytic and proteinuric types of gouty nephropathy — in 53, 37, 10 % of cases, arterial hypertension — in 47 %. Hyperuricemia at the time of examination was found in 84 % of patients, hyperuricuria — in 52 %, metabolic, renal and mixed types of hyperuricemia occurred in 57; 3 and 40 % of cases, respectively. Results. Comparative evaluation of allopurinol, a xanthine oxidase inhibitor, and febuxostat, a xanthine oxidoreductase inhibitor, in terms of kidney function in patients with gouty nephropathy, showed that the latter should be preferred, although the hypouricemic effect of both uricodepressants is approximately the same, and the initial indices of viscoelasticity of urine and β2-microglobulinuria are prognostic criteria for the efficacy of allopurinol and febuxostat therapy, respectively. Conclusions. In the future, it will be useful to determine the morphological changes in the kidneys in experimental gouty nephropathy under the influence of allopurinol and febuxostat, and it is also advisable to evaluate the results of combined use of uricodepressants with other groups of hypouricemic agents (uricosuric drugs, pegloticase enzyme, etc.).
Введение
Подагра относится к наиболее частым ревматическим заболеваниям и занимает лидирующую позицию среди всех артр итов у мужчин [26], причем распространенность ее повсеместно растет (за 20–25 лет на 30–50 % [14]), достигая сейчас в популяции 6 % и более [17]. Практически постоянным проявлением подагры является поражение почек, которое определяет прогноз болезни [9, 11, 27]. Гиперурикемия при подагрической нефропатии относится к независимым факторам риска снижения азото- и электролитовыделительной функции почек, а урикодепрессивная терапия может в этих ситуациях быть весьма успешной [22, 33].
Лечение подагрической нефропатии вызывает немалые трудности [2, 26, 29], при этом, к сожалению, за последние годы наметилась резистентность многих больных к применению уриконормализующих препаратов [25]. Наиболее распространенными медикаментозными средствами для патогенетической терапии подагры являются урикодепрессанты аллопуринол (ингибитор ксантиноксидазы) и фебуксостат (ингибитор ксантиноксиредуктазы) [4, 6, 36]. Двойное слепое контролируемое исследование показало возможность торможения темпов прогрессирования почечной недостаточности у таких больных [12].
В отличие от аллопуринола применение непуринового урикодепрессанта фебуксостата (аденурика, улорика) возможно у пациентов со сниженной функцией почек [8, 13], причем иногда регистрируется ее восстановление [34]. Как считают Y.H. Lien, J.L. Logan [18], E. Paschou et al. [21], существует настоятельная необходимость сравнительной оценки влияния аллопуринола и фебуксостата на функцию почек у больных подагрой. Это и стало целью данного исследования.
Материалы и методы
Под наблюдением находилось 73 больных первичной подагрой (мужчины со средним возрастом 49,40 ± 0,86 года и длительностью заболевания 10,30 ± 0,92 года). Критерии диагностики заболевания базировались на проявлениях суставного и почечного синдромов, характера гиперурикемии и наличия тофусов [3, 24]. Хроническая форма артрита установлена в 71,2 % от числа больных, интермиттирующая — в 28,8 %, периферические тофусы обнаружены в 53,4 % случаев. Хроническая болезнь почек I, II, III и IV стадии выявлена в соотношении 56 : 12 : 2 : 1 или соответственно в 78,1, 16,4, 2,7 и 1,4 % наблюдений, латентный, уролитиазный и протеинурический тип подагрической нефропатии — в 53,4, 37, 9,6 %, артериальная гипертензия (среднее давление > 115 мм рт.ст.) — в 46,6 % (119,90 ± 2,52 мм рт.ст.).
Гиперурикемия (> 420 мкмоль/л) на момент обследования констатирована у 83,6 % больных, гиперурикурия (> 800 мг/сут) — у 52,1 %, метаболический, почечный и смешанный типы гипер–урикемии имели место соответственно в 57,5, 2,7 и 39,7 %. Исходный уровень мочевой кислоты в крови составил 590,60 ± 17,37 мкмоль/л, в моче — 873,2 ± 44,6 мг/сут, клиренс мочевой кислоты — 8,40 ± 0,49 мл/мин, показатели сывороточного оксипуринола — 56,80 ± 7,94 мкмоль/л, активности ксантиноксидазы — 7,70 ± 0,21 нмоль/мл/мин, аденозиндезаминазы — 9,10 ± 0,28 нмоль/мл/мин, 5-нуклеотидазы — 8,8 ± 0,3 нмоль/мл/мин.
Протеинурия обнаружена у 38,4 % от числа больных (в 4,1 % случаев был нефротический синдром), лейкоцитурия (> 2 × 103/мкл) — у 26 %, эритроцитурия (> 1 × 103/мкл) — у 35,6 %, урат–урия — у 19,2 %, оксалатурия — у 27,4 %. Показатели фибронектинурии составили 527,10 ± 13,47 мг/л, β2-микроглобулинурии — 51,30 ± 2,26 мг/л, нитритурии — 5,70 ± 0,17 мкмоль/л, поверхностного натяжения мочи — 51,10 ± 0,35 Н/м, вязкоэластичности — 16,90 ± 0,68 мН/м, релаксации — 170,60 ± 5,82 с. Креатинин крови был равен 110,90 ± 6,55 мкмоль/л, мочевина — 8,20 ± 0,37 ммоль/л, клиренс креатинина — 101,10 ± 2,71 мл/мин, калия — 21,9 ± 0,4 мл/мин, натрия — 2,40 ± 0,05 мл/мин, кальция — 3,90 ± 0,06 мл/мин, магния — 2,90 ± 0,04 мл/мин, хлора — 3,40 ± 0,07 мл/мин, фосфора — 28,40 ± 0,22 мл/мин.
Статистическая обработка полученных результатов исследований проведена с помощью компьютерного вариационного, корреляционного, непараметрического, одно- (ANOVA) и многофакторного (ANOVA/MANOVA) дисперсионного анализа (программы Microsoft Excel и Statistica Stat-Soft, США). Оценивали средние значения (M), их стандартные отклонения (SD) и ошибки, коэффициенты параметрической корреляции Пирсона и непараметрической Кендалла (t), критерии дисперсии Брауна — Форсайта (BF) и Уилкоксона — Рао (WR), различий Стьюдента (t) и Макнемара — Фишера (x2), а также достоверность статистических показателей (p).
Методом слепого отбора больные были распределены на две группы: 1-ю составили 45 (61,6 %) пациентов, которым назначали урикодепрессор аллопуринол (200–700 мг/сут), во 2-ю группу вошли 28 (38,4 %) человек, у которых применяли фебуксостат (80–200 мг/сут). Дозы препаратов определялись уровнем урикемии, назначение гипоурекемических препаратов начинали с уровня выше 420 мкмоль/л у мужчин и 360 мкмоль/л — у женщин. Дозу повышали ступенчато по инструкции через неделю после последнего обострения артрита. Представители 1-й и 2-й группы не отличались между собой по возрасту, длительности заболевания, форме артрита, наличию тофусов, артериальной гипертензии, уровню среднего артериального давления и других средств патогенетической терапии (по показаниям использовали статины, фибраты, сартаны, ингибиторы ангиотензинпревращающего фермента, антиагреганты, L-аргинин, кверцетин). Пациенты получали нестероидные противовоспалительные препараты, глюкокортикоиды и колхицин в зависимости от клинической ситуации.
Результаты
В группе с аллопуринолом на 19,3 % чаще отмечали латентный тип подагрической нефропатии, а при использовании фебуксостата — на 17,5 % уролитиазный (x2 = 15,59, p < 0,001). На фоне фебуксостата отмечена большая стадийность хронической болезни почек (x2 = 8,41, р = 0,038), а в 1-й и 2-й группах соотношение I, II, III и IV стадий соответственно составило 38 : 5 : 1 : 1 и 20 : 6 : 1 : 1.
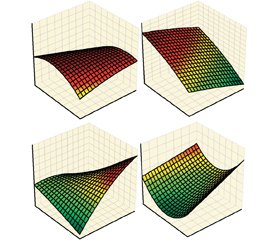
Как видно из рис. 1–4, больные, получавшие аллопуринол и фебуксостат, отличались по трехмерным интегральным гистограммам уровней в организме мочевой кислоты (урикемия + урикурия + клиренс мочевой кислоты), активности ферментов пуринового обмена (ксантиноксидаза + аденозиндезаминаза + 5-нуклеотидаза), показателей в моче белков (общая протеинурия + фибронектинурия + β2-микроглобулинурия) и физико-химических свойств мочи (поверхностное натяжение + вязко–эластичность + релаксация), хотя средние значения перечисленных значений были примерно равны, что позволяло проводить оценку эффективности лечебных мероприятий в обеих группах. Необходимо отметить, что если в 1-й группе исходный показатель скорости клубочковой фильтрации составил 107,00 ± 4,37 мл/мин, то во 2-й он был достоверно меньшим на 13,6 %, составляя 92,4 ± 5,4 мл/мин (t = 2,09, p = 0,040). При этом соотношение клиренса мочевой кислоты с эндогенным креатинином в 1-й и 2-й группах оказалось примерно одинаковым (соответственно 10,10 ± 2,96 и 11,50 ± 2,64 %).
/70-1.jpg)
/71-1.jpg)
Для дальнейшего анализа результатов применения аллопуринола и фебуксостата при подагрической нефропатии мы отобрали пациентов со скоростью клубочковой фильтрации < 100 мл/мин. Их соответственно оказалось в 1-й и 2-й группах 15 и 17 человек. По данным критерия Уилкоксона — Рао, характер урикодепрессивной терапии влияет на интегральную динамику показателей функции почек (WR = 6,42, p < 0,001). Рис. 5 свидетельствует, что спустя 2–3 месяца от начала применения аллопуринола было констатировано улучшение почечной функции в 33,3 % случаев, а восстановление — в 6,7 %, тогда как на фоне фебуксостата эти показатели соответственно составили по 35,3 %. Более того, во 2-й группе отсутствовали случаи ухудшения (уменьшения) параметров клиренса креатинина к окончанию сроков наблюдения за больными. Если в 1-й группе значения скорости клубочковой фильтрации до и после лечения аллопуринолом мало отличались, составляя 75,50 ± 6,51 и 74,10 ± 7,88 мл/мин, то во 2-й группе констатировано достоверное увеличение показателя на 1/4, соответственно с 76,10 ± 6,23 до 94,5 ± 5,5 мл/мин (t = 2,22, p = 0,034).
Мы выделили факторы, обладающие определенной прогностической значимостью при подагрической нефропатии. Для этого отобрали средние значения показателей и их стандартные отклонения (< M ± SD >), которые одновременно имели дисперсионные связи Брауна — Форсайта и корреляционные Кендалла с динамикой функции почек в 1-й и 2-й группах. Оказалось, что при использовании аллопуринола такие связи налицо в отношении модуля вязкоэластичности мочи (BF = 8,99, p = 0,030; t = –0,781, p = 0,048), а при назначении фебуксостата — показателя β2-микроглобулинурии (BF = 13,13, p = 0,018; t = –0,477, p = 0,046). По нашему мнению, прогнозпозитивными критериями в контексте дальнейшей функции почек у пациентов на фоне применения аллопуринола являются параметры вязкоэластичности мочи < 14 мН/м (< M-SD исходных значений 1-й группы), а при назначении фебуксостата — уровень β2-микроглобулинурии < 39 мг/л (< M-SD исходных значений 2-й группы).
Обсуждение
Как видно на рис. 6, при динамическом наблюдении за больными с подагрической нефропатией на уровни урикемии аллопуринол и фебуксостат воздействуют примерно одинаково, однако по содержанию в крови мочевины и креатинина, отражающих азотовыделительную функцию почек, преимущество, по нашему мнению, следует отдать фебуксостату. Принято считать, что общая эффективность 100–300 мг/сут аллопуринола примерно соответствует 40–120 мг/сут фебуксостата [35]. Между тем длительное применение аллопуринола и фебуксостата в таких дозах позволило нормализовать уровень урикемии соответственно в 21 и 62 % случаев подагры, при этом уменьшение или исчезновение периферических тофусов достигнуто в 50 % наблюдений использования аллопуринола и в 70 % — в процессе фебуксостат-терапии [1].
/72-1.jpg)
Ранее считалось, что аллопуринол противопоказан больным со снижением функции почек либо его использование в таких наблюдениях подагрической нефропатии должно осуществляться в значительно уменьшенных дозах [32]. В настоящее время подобные ограничения касаются только случаев заболевания со скоростью клубочковой фильтрации менее 30 мл/мин/1,73 м2 [30]. Существуют сведения, что в отличие от аллопуринола фебуксостат не предупреждает обострения подагрического артрита, хотя сильнее подавляет уровень урикемии [7, 31]. Мы на фоне урикодепрессивной терапии обоими препаратами в течение наблюдения за больными обострений суставного синдрома не отметили.
По данным литературы, фебуксостат при сопоставлении с аллопуринолом угнетает уровень креатининемии в большей степени [19]. S. Kim et al. [15] у больных подагрой провели сравнительную оценку ренопротекторного действия аллопуринола и фебуксостата, и, в конце концов, значимость в этом плане последнего урикодепрессанта оказалась выше. В свою очередь, как считают J.A. Singh и J.D. Cleveland [28], при обследовании пожилых больных с подагрической нефропатией пальму первенства как нефропротекторный препарат завоевал аллопуринол. Высказано мнение, что в случаях хронической болезни почек выраженных стадий патологического процесса к средствам выбора относится фебуксостат, тогда как на более ранних этапах развития подагрической нефропатии равнозначно применение аллопуринола [10]. Безусловно, отказываться от аллопуринола нецелесообразно, что доказано многолетней практикой, а длительное применение данного урикодепрессанта у больных подагрой является позитивной составляющей факторов в отношении дальнейшего сохранения функции почек [23].
По данным литературы, частота побочных действий фебуксостата примерно такая же, как и аллопуринола, но обычно отсутствует синдром гиперсенситивного васкулита [5]. При этом гепатотоксические и кожные побочные проявления аллопуринола во многом определяет высокий уровень в крови его метаболита оксипуринола [20]. Среди нежелательных эффектов фебуксостата чаще отмечаются незначительная кратковременная диарея [1] и преходящая нейтропения [16]. В течение наблюдения за больными подагрической нефропатией мы не констатировали каких бы то ни было побочных действий ни аллопуринола, ни фебуксостата.
Выводы
При сравнительной оценке ингибиторов ксантин–оксидазы аллопуринола и ксантиноксиредуктазы фебуксостата в отношении функции почек у больных подагрической нефропатией предпочтение следует отдать второму препарату, хотя гипоурикемическое действие обоих урикодепрессантов примерно одинаково, а прогностическими критериями эффективности аллопуринол- и фебуксостат-терапии соответственно являются исходные показатели вязкоэластичности мочи и β2-микроглобулинурии. В перспективе будет полезным определение морфологических изменений со стороны почек при экспериментальной подагрической нефропатии под влиянием аллопуринола и фебуксостата (этому вопросу будет посвящено сообщение 2), а также целесообразна оценка результатов комбинированного применения урикодепрессантов с другими группами гипоурикемических средств (урикозуриками, ферментом пеглотиказой и пр.).
Конфликт интересов. Авторы заявляют об отсутствии какого-либо конфликта интересов при подготовке данной статьи.
Рецензент: д.м.н., проф. О.Б. Яременко.
Список литературы
1. Becker M.A., MacDonald P.A., Hunt B., Gunawardhana L. Treating hyperuricemia of gout: safety and efficacy of febuxostat and allopurinol in older versus younger subjects // Nucleosides Nucleotides Nucleic Acids. — 2011. — № 30(12). — Р. 1011-7. — doi: 10.1080/15257770.2011.603715.
2. Crittenden D.B., Pillinger M.H. New therapies for gout // Ann. Rev. Med. — 2013. — № 64(1). — Р. 325-37. — doi: 10.1146/annurev-med-080911-105830.
3. Dalbeth N., Fransen J., Jansen T.L., Neogi T., Schuma–cher H.R., Taylor W.J. New classification criteria for gout: a framework for progress // Rheumatology. — 2013. — 52(10). — Р. 1748-53. — doi: 10.1093/rheumatology/ket154.
4. Dubreuil M., Neogi T., Chen C.A., Choi H.K., Chaisson C.E., Hunter D.J., Zhang Y. Increased risk of recurrent gout attacks with hospitalization // Am. J. Med. — 2013. — № 126(12). — Р. 1138-41. — doi: 10.1016/j.amjmed.2013.06.026.
5. Edwards N.L. Febuxostat: a new treatment for hyperuricaemia in gout // Rheumatology. — 2009. — № 48(2). — Р. 15-9. — doi: 10.1136/bcr-2017-222845.
6. Fang Z.H., Waizy H. Current concepts in the treatment of gouty arthritis // Orthop. Surg. — 2013. — № 5(1). — Р. 6-12. — doi: 10.1111/os.12024.
7. Faruque L.I., Ehteshami-Afshar A., Wiebe N., Tjosvold L., Homik J., Tonelli M. A systematic review and meta-analysis on the safety and efficacy of febuxostat versus allopurinol in chronic gout // Semin. Arthritis. Rheum. — 2013. — № 43(3). — Р. 367-75. — doi: 10.1016/j.semarthrit.2013.05.004.
8. Hiramitsu S., Ishiguro Y., Matsuyama H., Yamada K., Kato K., Noba M. et al. Febuxostat (Feburic tablet) in the mana–gement of hyperuricemia in a general practice cohort of Japanese patients with a high prevalence of cardiovascular problems // Clin. Exp. Hypertens. — 2013. — № 28(10). — Р. 183-8. — doi: 10.3109/10641963.2013.846358.
9. Humbert A., Stucker F. Acid uric : key player in a recently recognized devastating nephropathy and in the development of chronic kidney disease // Rev. Med. Suisse. — 2018. — № 14(595). — Р. 414-7.
10. Juge P.A., Truchetet M.E., Pillebout E., Ottaviani S., Vigneau C., Loustau C. et al. Efficacy and safety of febuxostat in 73 gouty patients with stage 4/5 chronic kidney disease: A retrospective study of 10 centers // Joint Bone Spine. — 2017. — № 84(5). — Р. 595-8. — doi: 10.1016/j.jbspin.2016.09.020.
11. Juraschek S.P., Kovell L.C., Miller E.R., Gelber A.C. Association of kidney disease with prevalent gout in the United States in 1988–1994 and 2007–2010 // Semin. Arthritis. Rheum. — 2013. — № 42(6). — Р. 551-61. — doi: 10.1016/j.semarthrit.2012.09.009.
12. Kabul S., Shepler B. A review investigating the effect of allopurinol on the progression of kidney disease in hyperuricemic patients with chronic kidney disease // Clin. Ther. — 2012. — № 34(12). — Р. 2293-6. — doi: 10.1016/j.clinthera.2012.10.008.
13. Kamatani N., Fujimori S., Hada T., Hosoya T., Kohri K., Nakamura T. et al. Multicenter, open-label study of long-term administration of febuxostat (TMX-67) in Japanese patients with hyperuricemia including gout // J. Clin. Rheumatol. — 2011. — № 17(4). — Р. 50-6. — doi: 10.1097/RHU.0b013e31822541d0.
14. Kiadaliri A.A., Uhlig T., Englund M. Burden of gout in the Nordic region, 1990–2015: findings from the Global Burden of Disease Study 2015 // Scand. J. Rheumatol. — 2018. — № 29(1). — Р. 1-8. — doi: 10.1080/03009742.2017.1405461.
15. Kim S., Kim H.J., Ahn H.S., Oh S.W., Han K.H., Um T.H. et al. Renoprotective effects of febuxostat compared with allopurinol in patients with hyperuricemia: A systematic review and meta-analysis // Kidney Res. Clin. Pract. — 2017. — № 36(3). — Р. 274-81. — doi: 10.23876/j.krcp.2017.36.3.274.
16. Kobayashi S., Ogura M., Hosoya T. Acute neutropenia associated with initiation of febuxostat therapy for hyperuricaemia in patients with chronic kidney disease // J. Clin. Pharm. Ther. — 2013. — Vol. 38, № 3. — P. 258-261.
17. Kuo C.F., Grainge M.J., See L.C., Yu K.H., Luo S.F., Zhang W., Doherty M. Epidemiology and management of gout in Taiwan: a nationwide population study // Arthritis. Res. Ther. — 2016. — № 23(17). — Р. 13-9. — doi: 10.1186/s13075-015-0522-8.
18. Lien Y.H., Logan J.L. Cross-reactions between allopurinol and febuxostat // Am. J. Med. — 2017. — № 130(2). — Р. 67-8. — doi: 10.1016/j.amjmed.2016.08.042.
19. Luo H., Fang W.G., Zuo X.X., Wu R., Li X.X., Chen J.W. et al. The clinical characteristics, diagnosis and treatment of patients with gout in China // Zhonghua Nei Ke Za Zhi. — 2018. — № 57(1). — Р. 27-31. — doi: 10.3760/cma.j.issn.0578-1426.2018.01.005.
20. Nakamura M., Fujita K., Toyoda Y., Takada T., Hasegawa H., Ichida K. Investigation of the transport of xanthine dehydrogenase inhibitors by the urate transporter ABCG2 // Drug. Metab. Pharmacokinet. — 2018. — № 33(1). — Р. 77-81. — doi: 10.1016/j.dmpk.2017.11.002.
21. Pascual E., Sivera F., Yasothan U., Kirkpatrick P. Febu–xostat // Nat. Rev. Drug. Discov. — 2009. — № 8(3). — Р. 191-2. — doi: 10.1038/nrd2831.
22. Pascual E., Sivera F., Andrés M. Managing gout in the patient with renal impairment // Drugs Aging. — 2018. — № 13(2). — doi: 10.1007/s40266-018-0517-7.
23. Perez-Ruiz F. Treatment with allopurinol is associated with lower risk of acute kidney injury in patients with gout: a retrospective analysis of a nested cohort // Rheumatol. Ther. — 2017. — № 4(2). — Р. 419-25. — doi: 10.1007/s40744-017-0082-2.
24. Radak-Perovic M., Zlatkovic-Svenda M. Novelties in gout // Srp. Arh. Celok. Lek. — 2013. — № 141(1–2). — Р. 109-15.
25. Richette P., Garay R. Novel drug discovery strategies for gout // Expert Opin. Drug Discov. — 2013. — № 8(2). — Р. 183-9. — doi: 10.1517/17460441.2013.742061.
26. Roddy E., Choi H.K. Epidemiology of gout // Rheum. Dis. Clin. North Am. — 2014. — № 40(2). — Р. 155-75. — doi: 10.1016/j.rdc.2014.01.001.
27. Ruilope L.M., Pontremoli R. Serum uric acid and cardio-renal diseases // Curr. Med. Res. Opin. — 2013. — № 29(3). — Р. 25-31. — doi: 10.1185/03007995.2013.790803.
28. Singh J.A., Cleveland J.D. Comparative effectiveness of allopurinol versus febuxostat for preventing incident renal disease in older adults: an analysis of Medicare claims data // Ann. Rheum. Dis. — 2017. — № 76(10). — Р. 1669-78. — doi: 10.1136/annrheumdis-2017-211210.
29. Sivera F., Andres M., Carmona L., Kydd A.S., Moi J., Seth R., Sriranganathan M. Multinational evidence-based recom–mendations for the diagnosis and management of gout: integrating systematic literature review and expert opinion of a broad panel of rheumatologists in the 3e initiative // Ann. Rheum. Dis. — 2014. — № 73(2). — Р. 328-35. — doi: 10.1136/annrheumdis-2013-203325.
30. Stamp L.K., Chapman P.T., Barclay M., Horne A., Frampton C., Tan P. et al. The effect of kidney function on the urate lowering effect and safety of increasing allopurinol above doses based on creatinine clearance: a post hoc analysis of a randomized controlled trial // Arthritis Res. Ther. — 2017. — № 19(1). — Р. 283-9. — doi: 10.1186/s13075-017-1491-x.
31. Tayar J.H., Lopez-Olivo M.A., Suarez-Almazor M.E. Febuxostat for treating chronic gout // Cochrane Database Syst. Rev. — 2012. — № 14(11). — Р. 177-83. — doi: 10.1002/14651858.CD008653.pub2.
32. Thurston M.M., Phillips B.B., Bourg C.A. Safety and efficacy of allopurinol in chronic kidney disease // Ann. Pharmacother. — 2013. — № 47(11). — Р. 1507-16. — doi: 10.1177/1060028013504740.
33. Treviño-Becerra A. Uric Acid: The unknown uremic to–xin // Contrib. Nephrol. — 2018. — № 192(1). — Р. 25-33. — doi: 10.1159/000484275.
34. Whelton A., Macdonald P.A., Zhao L., Hunt B., Gunawardhana L. Renal function in gout: long-term treatment effects of febuxostat // J. Clin. Rheumatol. — 2011. — № 17(1). — Р. 7-13. — doi: 10.1097/RHU.0b013e318204aab4.
35. Ye P., Yang S., Zhang W., Lv Q., Cheng Q., Mei M. et al. Efficacy and tolerability of febuxostat in hyperuricemic patients with or without gout: a systematic review and meta-analysis // Clin. Ther. — 2013. — № 35(2). — Р. 180-9. — doi: 10.1016/j.clinthera.2012.12.011.
36. Zarowitz B.J., O’Shea T.E. Demographic and clinical profile of nursing facility residents with gout // Consult. Pharm. — 2013. — № 28(6). — Р. 370-82. — doi: 10.4140/TCP.n.2013.370.

/70-1.jpg)
/71-1.jpg)
/72-1.jpg)