Введение
Боль пояснично-крестцового отдела позвоночника, несмотря на значительный технологический прогресс в медицине, остается одной из наиболее актуальных медицинских и социальных проблем. Дегенеративные поражения поясничного отдела позвоночника и связанные с ними клинико-неврологические проявления являются одной из наиболее важных проблем современной ортопедии. Дегенеративные изменения в позвоночнике диагностируются у 57 % людей уже в возрасте 20–29 лет. Частота их быстро прогрессирует, достигая в возрасте 40–49 лет 90–95 %, а у людей старше 60 лет — 100 % [1, 2].
Оценивая распространенность вертеброгенной патологии в общей структуре заболеваемости с временной утратой трудоспособности, необходимо отметить, что в нашей стране она занимает второе место, уступая только респираторным инфекциям, и составляет до 20–30 % в структуре неврологических заболеваний [2].
Нейрокомпрессионный болевой синдром пояснично-крестцового отдела позвоночника может быть вызван следующими состояниями: протрузией и грыжами межпозвонковых дисков, гипертрофией суставных отростков на фоне спондилоартроза, дегенеративным поясничным спинальным стенозом, дегенеративными деформациями позвоночника [3, 4].
Несмотря на очевидные успехи использования новых технологий хирургического лечения пациентов с дегенеративными заболеваниями позвоночника, консервативное лечение по праву остается основной медицинской помощью и используется у подавляющего большинства больных. Консервативное лечение ставит перед собой задачу купирования болевого синдрома в острый период болезни, а по его окончании — предотвращения рецидива болезни. Как показывают исследования, более 70–80 % пациентов в течение 12 недель лечения испытывают существенное улучшение состояния и обходятся без хирургического вмешательства [5–7].
Важнейшей задачей консервативного лечения является эффективное и быстрое устранение болевого синдрома и неврологических нарушений в ранние сроки. Как отмечает А.И. Продан [7], многочисленные статистические исследования показали, что если обострение длится не более 2–3 месяцев, то при любом виде консервативного лечения шансы на полное выздоровление составляют 95 %, при длительности болевого синдрома более 6 месяцев — 40 %, а если болевой синдром продолжается более года, то возможность выздоровления не превышает 15 %. Поэтому своевременное устранение боли на первоначальных этапах ее проявления — основа успешного выздоровления пациента.
Наличие различных механизмов развития нейрокомпрессионных болевых синдромов пояснично-крестцового отдела позвоночника при дегенеративно-дистрофических заболеваниях определяет использование комплексного фармакологического подхода к лечению. Он основан на устранении боли в соответствии с наличием асептического воспаления и иррадиирущих болевых синдромов, сопровождающих дегенеративные процессы в структурах позвоночника.
Золотым стандартом лечения болевых синдромов в области позвоночника являются нестероидные противовоспалительные препараты (НПВП). И хотя не всегда с помощью НПВП удается полностью избавиться от болевого синдрома, их эффективность не вызывает сомнений.
Нестероидные противовоспалительные препараты представляют собой обширную группу средств, ингибирующих различные химические механизмы воспаления. Существует мнение, что НПВП неэффективны при вертеброгенных радикулопатиях, но в экспериментальных исследованиях ряда авторов [6] показано выраженное уменьшение пери- и интраневрального воспаления при использовании, например, диклофенака натрия и отсутствие или уменьшение эффекта при введении, например, кетопрофена.
С учетом формирования защитного напряжения мышц спины в ответ на боль не менее важным компонентом лечения является купирование мышечного спазма [8, 9]. Применение миорелаксантов в комплексе с НПВП обусловлено их фармакологическим действием, поскольку они устраняют или уменьшают выраженность мышечного спазма как одного из важных компонентов боли. Применение миорелаксантов способствует уменьшению боли, увеличению объема движений, предотвращению образования контрактур, улучшению функциональной способности опорно-двигательного аппарата.
Важным аспектом использования миорелаксантов является то, что уменьшение мышечного спазма дает пациенту возможность полноценно выполнять программу физической реабилитации, тем самым ускоряя процесс выздоровления. Кроме того, использование миорелаксантов позволяет уменьшить дозу НПВП, что снижает риск возникновения побочных реакций [3].
M. van Tulder и соавт. провели систематический обзор препаратов для лечения болей в спине [10]. Ими найдено 19 рандомизированных исследований, связанных с использованием НПВП при болях в позвоночнике, 10 из которых имели высокую степень доказательности. В результате исследований авторами проведен обзор эффективности препаратов с определением уровня доказательности исследований (уровень 1):
— НПВП более эффективны, чем плацебо, у пациентов с острой болью в позвоночнике;
— эффективность различных НПВП ненамного выше эффективности парацетамола;
— действие различных НПВП фактически одинаково по эффективности для лечения острых болей в позвоночнике.
В Кокрановском обзоре лечения хронических болей в позвоночнике с помощью НПВП M. van Tulder et al. [10] нашли лишь умеренные доказательства их эффективности (уровень 2).
Примерно одной трети пациентов с жалобами на боли в позвоночнике назначаются миорелаксанты в рамках оказания первичной медицинской помощи. Назначение миорелаксантов при неспецифических болях в позвоночнике является спорным, в основном из-за наличия множества побочных эффектов. В дополнение к седативным свойствам препаратов, головным болям, тошноте и рвоте сообщается о потенциальном злоупотреблении и зависимости от них. В ряде исследований обнаружены убедительные научные доказательства того, что безбензодиазепиновые миорелаксанты являются эффективными для лечения острой боли в позвоночнике, в то время как в доступной литературе нами не найдено никаких доказательств их эффективности при хроническом болевом синдроме [12].
Цель исследования: оценить эффективность применения НПВП и миорелаксантов в лечении болевого синдрома у пациентов с дегенеративно-дистрофическими поражениями позвоночника.
Материалы и методы
Нами был проведен ретроспективный анализ данных историй болезни 120 пациентов (78 женщин и 42 мужчин) в возрасте 39,7 ± 5,2 года с диагнозом остео-хондроза, протрузии или грыжи межпозвонкового диска пояснично-крестцового отдела позвоночника, проходивших стационарное консервативное лечение в отделении реабилитации ГУ «Институт травматологии и ортопедии НАМНУ». Средний показатель продолжительности болевого синдрома до госпитализации составил 3,1 ± 0,8 месяца. Все пациенты были клинически обследованы (исследование неврологического статуса), количественная и качественная оценка болевого синдрома проводилась на основании визуальной аналоговой шкалы (ВАШ) боли.
Для оценки степени нарушения жизнедеятельности, обусловленного патологией позвоночника, использовали анкетирование Оswestry Disability Index (ODI) и анкетирование Роланда — Морриса (Roland-Morris Disability Questionary, RDQ). Индекс выздоровления (ИВ), указывающий на степень восстановления после консервативного лечения, был рассчитан при выписке из стационара и при заключительной оценке через 6 месяцев после лечения по K. Hirabayashi et al. [13].
ИВ = (ODI до лечения — ODI после лечения)/(ODI до лечения) × 100 %.
Изменения в субъективных симптомах между выпиской и заключительной оценкой были классифицированы:
— как отличные (ИВ > 40 %);
— хорошие (ИВ = 21–40 %);
— удовлетворительные (ИВ < 20 %).
Морфологические изменения оценивали по данным МРТ. По данным рентгенографии поясничного отдела позвоночника определяли наличие сколиотической деформации. По функциональным рентгенограммам определяли наличие спондилолистеза и нестабильности в поясничном отделе позвоночника.
Срок пребывания в стационаре составлял 10–12 дней. Пациентов наблюдали в динамике после выписки. Отдаленные результаты лечения оценивали на протяжении 6 месяцев. Средний срок составил 6,8 ± 1,2 месяца.
По протоколу лечения пациентам назначали НПВП и миорелаксанты. Также пациентам рекомендовали ношение полужесткого фиксирующего корсета (3–5 часов в день).
Результаты и обсуждение
Динамика болевого синдрома по ВАШ
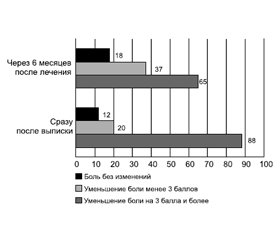
Регресс болевого синдрома на 3 и более балла на момент окончания лечения отмечали 88 (73,4 %) пациентов, менее 3 баллов — 20 (16,7 %) пациентов, без изменений — 12 (9,8 %). Через 6 месяцев после лечения по результатам анкетирования ВАШ наблюдалась следующая динамика: у 65 (54,1 %) пациентов отмечали регресс болевого синдрома более чем на 3 балла, у 37 (30,8 %) — менее 3 баллов, у 18 (15,1 %) пациентов — без изменений (рис. 1).
Оценка результатов лечения по данным анкетирования Роланда — Морриса
Оценивая возможности пациентов к самообслуживанию по опроснику Роланда — Морриса после применения НПВП получены следующие результаты: до лечения средний показатель у пациентов составил 17,7 ± 0,6 (из 24 возможных) балла, сразу после лечения — 12,9 ± 0,7 балла (регресс на 27,1 %), через 6 месяцев — 11,9 ± 0,8 балла (регресс на 32,7 %) в среднем по группе.
Оценка результатов лечения по показателям анкетирования Oswestry Disability Index
Оценка влияния боли в поясничном отделе позвоночника на нарушение жизнедеятельности посредством опросника Оswestry Disability Index (ODI): до лечения средний показатель у наших пациентов составил 71,4 ± 1,5 (из 100 возможных) балла, сразу после лечения — 49,6 ± 2,3 балла (регресс на 30,5 %), через 6 месяцев — 46,2 ± 3,2 балла (регресс на 35,2 %).
При оценке корреляции между показателями оценки анкетирования Роланда — Морриса и ODI нами отмечена сильная и достоверная связь, которая наблюдалась при исходном наблюдении (r = 0,73 (p < 0,05)) и усиливалась, достигая значения r = 0,9 (p < 0,05) при последующих наблюдениях после лечения и через 6 месяцев. Результаты собственных исследований подтверждают результаты исследований, проведенных A. Fujiwara et al. (2003), об относительной корреляционной взаимосвязи индексов Роланда — Морриса и Освестри [11].
Оценка показателей по индексу выздоровления
Оценка состояния пациентов на основании индекса выздоровления показала, что отличный результат лечения на момент выписки (ИВ1) отмечали у 80 (66,7 %) пациентов, хороший — у 29 (24,1 %), удовлетворительный — у 11 (9,2 %). На момент контрольного исследования через 6 месяцев (ИВ2) отличный результат лечения был отмечен у 67 (55,9 %) пациентов, хороший — у 37 (30,8 %), удовлетворительный — у 16 (13,3 %). Негативных показателей ИВ нами отмечено не было (рис. 2).
Оценка неврологического статуса
Анализ неврологических проявлений нейрокомпрессионных болевых синдромов пояснично-крестцового отдела позвоночника подтвердил регресс неврологической симптоматики в сравнении с исходными показателями, а именно: регресс на 75–100 % был отмечен у 69 (57,5 %) больных, на 50–74 % — у 33 (27,5 %), менее 50 % — у 18 (15 %).
Влияние сопутствующих патологий на результаты лечения
Анализ результатов лечения показал, что наличие в диагнозе сколиоза (у 13 пациентов) по данным рентгенографии не сразу сказывается на результатах лечения. Так, на момент выписки ИВ1 в группе пациентов со сколиозом не отличался от такового в группе пациентов без сколиозов (31 % и 30,3 % соответственно; p = 0,033). Однако через 6 месяцев в группе пациентов со сколиозом наблюдали уменьшение показателя ИВ2 до 11,2 %, в то время как средний показатель по остальной группе составлял 37,9 % (р = 0,079).
Наличие спондилолистеза (16 пациентов) по данным рентгенографии сказывается как на ближайших, так и на отдаленных результатах лечения. ИВ1 в группе со спондилолистезом составлял 19,6 % (средней показатель остальной группы — 33,1 %) (р = 0,015). Через 6 месяцев в группе со спондилолистезом показатель ИВ2 снизился до 11,1 %, в то время как в остальной группе данный показатель составил 40,4 % (р = 0,14).
Отсутствие нестабильности (у 101 пациента) является хорошим прогностическим признаком, что соответствует как хорошему результату сразу после лечения (ИВ1 — 34,8 %), так и отличному на момент контрольного исследования (ИВ2 — 44,2 %).
Наличие нестабильности L4-L5 (8 пациентов) достоверно снижает результаты лечения до уровня «хороший» (ИВ1 — 27,2 %) в ближайшие сроки исследований (р = 0,032). Негативная динамика отмечается и при контрольном исследовании через 6 месяцев (ИВ2 — 19,2 %) (р = 0,16).
Нестабильность же L5-S1 (5 пациентов) достоверно снижает результаты лечения до уровня «удовлетворительный» сразу после выписки (ИВ1 — 19,3 %) (р = 0,043). Через 6 месяцев показатель ИВ2 достоверно снижается до 5,4 % (р = 0,085).
Наличие нестабильности на 2 сегментах, L4-L5 и L5-S1, было нами отмечено у 6 пациентов. Индекс выздоровления сразу после проведенного лечения у них соответствовал хорошему результату лечения (ИВ1 — 27,8 %) (р = 0,014). Однако при повторном исследовании через 6 месяцев наблюдали достоверное его снижение до уровня «удовлетворительный» (ИВ2 — 13,7 %) (р = 0,13).
Наличие деформирующего артроза коленных суставов (16 пациентов) по данным рентгенографии сказывается как на ближайших, так и на отдаленных результатах лечения. ИВ1 в группе с гонартрозом составлял 22,8 % (средний показатель остальной группы — 31,4 %) (р = 0,62). Через 6 месяцев в группе с гонартрозом показатель ИВ2 несколько увеличился — до 27,1 %, в то время как в остальной группе он составил 36,3 % (р = 0,66).
Наличие деформирующего артроза тазобедренных суставов (22 пациентов) по данным рентгенографии незначительно сказывается на ближайших и значительно усугубляет отдаленные результаты лечения. ИВ1 в группе с коксартрозом составлял 23,8 % (средней показатель остальной группы — 31,4 %) (р = 0,091). Через 6 месяцев в группе с коксартрозом показатель ИВ2 снизился до 2,4 %, в то время как в остальной группе данный показатель составил 37,7 % (р = 0,161).
При оценке степени взаимосвязи между показателями ИВ1 и неврологической симптоматикой был получен следующий результат: корреляция одновременных показателей (сразу после лечения) отсутствует (r = –0,04, p > 0,05). Однако динамика неврологических проявлений может служить ориентировочным прогностическим показателем на период повторных исследований через 6 месяцев (r = 0,45, p < 0,004). Представленные данные позволяют сделать следующее заключение: хорошая динамика (регресс 75–100 %) неврологических проявлений сразу после проведенного лечения увеличивает показатель ИВ2 на 46 %.
Показатели неврологического статуса до и после проведенного лечения, а также его динамика продемонстрировали сильную степень (r > 0,7) корреляции с показателями анкетирования Роланда — Морриса через 6 месяцев, ODI после лечения, ODI через 6 месяцев и ИВ2. Данное заключение позволяет сделать вывод, что показатель неврологического статуса до лечения может быть использован как прогностический для перечисленных вышеуказанных показателей.
Однофакторный дисперсионный анализ показал, что наличие сколиоза по данным рентгенографии достоверно (p = 0,037) влияет на изменения в неврологическом статусе. То есть при отсутствии сколиоза позитивная динамика в неврологическом статусе отмечена у 69 % пациентов, а при его наличии — лишь у 29 %. Аналогичная картина наблюдается и при спондилолистезе: при отсутствии сколиоза позитивная динамика в неврологическом статусе отмечена у 72 % пациентов, а при наличии — лишь у 37 % (p < 0,015).
Выводы
Применение НПВП в комбинации с миорелаксантами дает позитивный эффект: снижает болевой синдром, улучшает показатели нарушения жизнедеятельности как в ближайшем, так и в отдаленном после лечения периоде. Наличие же сколиоза, спондилолистеза, нестабильности L4-L5 и деформирующего артроза тазобедренных суставов являлось негативным прогностическим признаком эффективности лечения.
Конфликт интересов. Авторы заявляют об отсутствии какого-либо конфликта интересов при подготовке данной статьи.
Список литературы
1. Ананьева Л.П. Проблема боли при заболеваниях опорно-двигательного аппарата. Обозрение мат-лов 12-го Всемирного конгресса по боли / Л.П. Ананьева // Боль. — 2009. — № 1(22). — С. 39-43.
2. Зозуля Ю.А. Хирургическое лечение нейро-компрессионных пояснично-крестцовых болевых синдромов / Ю.А. Зозуля, Е.Г. Педаченко, Е.Н. Слынько — К.: УИПК «Екс. Об.», 2006. — 348 с.
3. Кавалерский Г.М. Применение Цель Т в ортопедии для лечения дегенеративных заболеваний (аналитический обзор) / Г.М. Кавалерский, Л.Л. Силин // Русский медицинский журнал. Ортопедия. — 2014. — № 18. — С. 1377.
4. Луцик А.А. Пункционная диагностика и лечение вертеброгенного рефлекторного синдрома позвоночных артерий / А.А. Луцик, Е.В. Череватенко, Г.Ю. Бондаренко, А.И. Пеганов // Хирургия позвоночника. — 2014. —№ 1. — С. 78-85.
5. Луцик А.А. Сочетание оперативных и пункционных методов лечения дегенеративных заболеваний шейного отдела позвоночника / А.А. Луцик, Г.Ю. Бондаренко, Е.В. Череватенко // Мат-лы III съезда травматологов-ортопедов Сибирского федерального округа. — Горно-Алтайск, 2014. — С. 50-55.
6. Павленко С.С. О необходимости стандартизации оказания медицинской помощи больным с поясничными болями / С.С. Павленко // Боль. — 2009. — № 1(22). — С. 22-25.
7. Продан А.И. Дегенеративные заболевания позвоночника: Семиотика. Классификация. Диагностика / А.И. Продан, В.А. Радченко, Н.А. Корж. — Харьков: ИПП «Контракт», 2007. — Т. 1. — 242 с.
8. Ульянич А.Г. Хирургическое лечение вертебрально-базилярной сосудистой недостаточности, обусловленной сочетанием дискогенных и недискогенных поражений позвоночных артерий / А.Г. Ульянич, Е.В. Череватенко, А.И. Пеганов, В.В. Казанцев // Мат-лы III научно-практической конференции молодых ученых «Медицина XXI века». — Новокузнецк, 2013. — С. 114-116.
9. Череватенко Е.В. Пункционное лечение рефлекторного синдрома позвоночных артерий / Е.В. Череватенко, Е.И. Нечаева, Г.Ю. Бондаренко, А.И. Пеганов // Мат-лы IV научно-практической конференции молодых ученых «Медицина XXI века». — Новокузнецк, 2014. — С. 98-100.
10. Van Tulder M.W. Conservative treatment of acute and chronic non-specific low back pain: a systematic review of randomized controlled trials of the most common interventions / Van Tulder M.W., Koes B.W., Bouter L.M. // Spine. — 1997. — Vol. 22, № 18. — P. 2128-2156. http://dx.doi.org/10.1097/00007632-199709150-00012
11. Association of the Japanese Orthopaedic Association Score with the Oswestry Disability Index, Roland-Morris Disability Questionnaire, and Short-Form 36 / Fujiwara A., Kobayashi N., Saiki K. [et al.] // Spine. — 2003. — Vol. 28. — P. 1601-1607. http://dx.doi.org/10.1097/01.BRS.0000077510.95462.39
12. Eubanks J. Prevalence of lumbal facet arthrosis and its relationship to age, sex and race: an anatomic study of cadaveric speciments / M. Lee, E. Casinelli //Spine. — 2007. — Vol. 32, № 19. — P. 2058-2062. http://dx.doi.org/10.1097/BRS.0b013e318145a3a9
13. Hirabayashi K. Operative results and postoperative progression of ossification among patients with ossification of cervical posterior longitudinal ligament / K. Hirabayashi, J. Miyakawa, K. Satomi [et al.] // Spine. — 1981. — Vol. 6. — P. 354-364. http://dx.doi.org/10.1097/00007632-198107000-00005

/81-1.jpg)