Ураження нервової системи, як і раніше, становлять вагому частку в структурі захворюваності населення поряд із серцево-судинною й онкологічною патологією. Хвороби центральної нервової системи, наприклад інсульт, і периферичних нервів, наприклад нейропатії, часто призводять до зниження працездатності хворих та інвалідизації, а тому вимагають своєчасних лікувальних втручань [1, 2].
У переважній більшості випадків порушення в роботі нервової системи пов’язані з двома патологічними процесами: порушенням провідності нервових імпульсів і розвитком дегенеративних змін. Відповідно, для лікаря будуть кращими ті лікарські засоби, що зможуть одночасно коригувати обидві ці ланки патогенезу [1, 2].
Одним із найбільш ефективних засобів подібної дії є іпідакрин (фармакологічна група: антихолінестеразні засоби). За рахунок подвійного ефекту — блокади потенціалзалежних К+-каналів пресинаптичної мембрани й оборотного інгібування ацетилхолінестерази — препарат був здатний допомогти більшості пацієнтів при проведенні наукових досліджень і в рутинній клінічній практиці [3, 4].
Ще однією перевагою є здатність іпідакрину діяти як у центральній нервовій системі, так і на периферії. Більшість інших антихолінестеразних засобів добре працюють або в центральних структурах (наприклад, галантамін), або в периферичних (наприклад, прозерин) [3].
З огляду на велику значимість іпідакрину для неврологічної практики нами був підготовлений цей огляд, мета якого зводилася до висвітлення механізмів дії даного засобу й ефективності його парентеральних лікарських форм.
Механізми дії іпідакрину
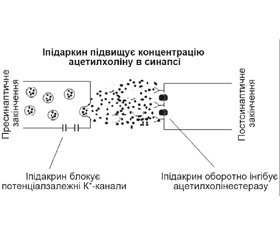
Основним місцем дії іпідакрину є холінергічні синапси центральної й периферичної нервової системи (рис. 1). З одного боку, препарат блокує потенціалзалежні К+-канали пресинаптичної частини, що подовжує стан збудження в пресинапсі. У цих умовах із нього вивільняється більше ацетилхоліну. З іншого боку, препарат оборотно пригнічує ацетилхолінестеразу постсинаптичної мембрани, перешкоджаючи руйнуванню ацетилхоліну. Обидва ефекти — більше вивільнення ацетилхоліну і менше його руйнування — призводять до підвищення концентрації даного медіатора в синаптичній щілині. Природним наслідком цього є покращення передачі нервових імпульсів через холінергічні синапси [5].
/24-1.jpg)
В експериментальному дослідженні [6] були описані результати лікувального впливу іпідакрину при травматичній нейропатії сідничного нерва. Через 1 місяць внутрішньом’язового введення препарату відзначалося відновлення структури мієліну, аксонів, перехватів Ранв’є, ультраструктури леммоцитів. Був зроблений висновок, що іпідакрин стимулює розвиток компенсаторно-відновних процесів і може бути рекомендований для клінічної практики.
Захворювання з порушенням центральної провідності
При захворюваннях центральної нервової системи набуває значення низка додаткових механізмів дії іпідакрину. Поряд з основними механізмами вони забезпечують спостережуваний у клініці лікувальний ефект препарату.
Слабка блокада потенціалзалежних Na+-каналів забезпечує розвиток слабкого седативного ефекту. Виявлено модулюючий вплив іпідакрину на ГАМКергічну й катехоламінову системи, що разом із гальмуванням амілоїдогенезу в головному мозку і М2-агоністичною активністю (її відображенням є зміна довголатентних потенціалів нейронів у СА1 ділянці гіпокампа) забезпечує нейротрофічний ефект. Інгібування псевдохолін-естерази супроводжується покращанням здатності до навчання, пам’яті й зорово-просторових функцій [2, 3].
Парентеральні форми іпідакрину застосовують для лікування таких захворювань, як травматичне ураження головного мозку, енцефалопатії різного генезу (посттравматична, судинна, алкогольна), ішемічний і геморагічний інсульт, при виході з коми, при аксонопатії внаслідок спінальної аміотрофії 1-го і 2-го типу тощо [3].
Нижче наведені приклади використання іпідакрину при різних видах інсульту.
Ішемічний і геморагічний інсульт (гострий період)
Дослідники повідомляють про те, що при призначенні іпідакрину постінсультним хворим найбільш значуща динаміка спостерігається в руховій сфері. При цьому чим раніше розпочати введення препарату, тим більш вираженим буде клінічний ефект. Так, при призначенні іпідакрину в гострому періоді ішемічного інсульту відновлення рухових функцій відбувається в 76 % випадків. А якщо це було зроблено в ранньому відновлювальному періоді, то в 50 % випадків [3].
У відкрите рандомізоване контрольоване дослідження [7] було включено 60 пацієнтів у гострому періоді інфарктів мозку і внутрішньомозкових крововиливів у домінантній півкулі головного мозку з провідним синдромом у вигляді різних афазій. Пацієнтів розподілили на три групи. Перша (n = 20) отримувала базову терапію + 1,5% іпідакрин внутрішньом’язово по 1 мл 1 раз на день. Друга (n = 20) отримувала базову терапію + 1,5% іпідакрин внутрішньом’язово по 1 мл 2 рази на день. Контрольна група одержувала тільки базову терапію без іпідакрину. Лікування починали з 1–2-го дня після надходження до стаціонару, тривалість лікування становила 8–10 днів.
На тлі проведеної терапії в першій групі був відзначений регрес афазії — до помірної вираженості (3,6 ± 0,6 бала, до лікування — тяжка афазія на рівні 5,3 ± 0,5 бала; p < 0,05). На початку у хворих спостерігався тяжкий геміпарез на рівні 1,1 ± 0,4 бала, який під час лікування не зазнав змін.
У другій групі був відзначений регрес афазії — до легкої вираженості (1,7 ± 0,6 бала, до лікування — помірна афазія на рівні 4,5 ± 0,4 бала; p < 0,05), зросла м’язова сила до легкого геміпарезу (4,3 ± 0,3 бала, до лікування — помірний геміпарез на рівні 3,8 ± 0,5 бала; p < 0,05). Автори особливо підкреслюють, що м’язовий тонус вірогідно не збільшувався не тільки в першій, але й у другій групі. Відсутність впливу 1,5% іпідакрину в дозі 2 мл/день на підвищення м’язового тонусу має велике практичне значення, тому що частина ангіоневрологів побоюється саме цього негативного ефекту препарату в гострому періоді лікування інсульту.
Переносимість терапії в обох групах пацієнтів була доброю. У першій групі результати терапії 8 хворих оцінили як задовільні, 12 — як добрі. У другій групі результати терапії 3 пацієнти оцінили як задовільні, 17 — як добрі. Ускладнення від застосування іпідакрину відзначено тільки в одного пацієнта в другій групі у вигляді шкірної висипки на 3-й день призначення. Препарат було відмінено, що супроводжувалося регресом висипки.
Автори зробили висновок про те, що включення іпідакрину в комплексну терапію мозкових інсультів в гострому періоді сприяє більш швидкому регресу основних неврологічних симптомів.
У відкрите дослідження [8] було включено 28 пацієнтів на 2–3-й день після перенесеного інсульту (тип інсультів у роботі не наведено). Усім пацієнтам призначали 0,5% іпідакрин внутрішньом’язово по 1 мл 2 рази на день протягом 10 днів.
У результаті лікування регрес рухових порушень тією чи іншою мірою був зареєстрований у всіх хворих, які перенесли інсульт. Добрий ефект відзначений у 79 % випадків (20 хворих), незначні зміни — у 21 % випадків (8 хворих). Хворі добре переносили препарат, побічних ефектів не відзначалося (іпідакрин не викликав посилення спастичності й підвищення артеріального тиску).
Отже, проведене дослідження підтвердило клінічну ефективність ін’єкційних форм іпідакрину в пацієнтів із руховими порушеннями, які перенесли інсульт. Іпідакрин з перших днів мозкового інсульту впливає на ступінь і темпи відновлення неврологічних розладів, сприяючи більш швидкому й значному зменшенню рухових розладів.
Захворювання з порушенням периферичної провідності
При захворюваннях периферичної нервової системи і нейром’язових захворюваннях набуває значення низка додаткових механізмів дії іпідакрину. Поряд з основними механізмами вони забезпечують спостережуваний у клініці лікувальний ефект препарату.
Слабка блокада потенціалзалежних Na+-каналів забезпечує розвиток слабкого аналгетичного ефекту. Препарат підсилює дію на гладкі м’язи ацетилхоліну, адреналіну, серотоніну, гістаміну й окситоцину за рахунок прямого впливу на міофібрили [2, 8].
Парентеральні форми іпідакрину застосовують для лікування таких захворювань, як нейропатії (травматична, компресійно-ішемічна, діабетична, постгерпетична), радикулопатії, неврити (лицьового, поворотного, слухового та інших нервів), аксонопатії при невральних аміотрофіях, сенсоневральна приглухуватість, міастенія й міастенічні синдроми, нетримання сечі після радикальної простатектомії тощо [3, 9, 10].
Нижче наведені приклади використання іпідакрину для лікування нейропатій і радикулопатій різної етіології.
Нейропатії й радикулопатії
У відкрите контрольоване дослідження [12] було включено 100 пацієнтів із цукровим діабетом 1-го і 2-го типу, які страждали від діабетичної полінейропатії з комбінованим ураженням чутливих, рухових і вегетативних нервів. Пацієнтів розподілили на три групи. Перша (n = 40) отримувала базову терапію + 1,5% іпідакрин внутрішньом’язово по 1 мл 2 рази на день. Друга (n = 40) отримувала базову терапію + 0,5% іпідакрин внутрішньом’язово по 1 мл 2 рази на день. Контрольна група (n = 20) отримувала базову терапію + 0,05% прозерин (неостигмін) підшкірно по 1 мл 2 рази на день. Тривалість лікування становила 3 тижні.
У результаті дослідження було встановлено, що на тлі лікування іпідакрином динаміка вираженості больового синдрому не зазнала вірогідних змін у всіх трьох групах. У першій і другій групах спостерігалося зменшення сенсорних порушень (порушень поверхневої чутливості) порівняно зі станом до лікування (p < 0,01), причому більша доза препарату призводила до більшого ефекту (p < 0,05). У контрольній групі динаміка сенсорних порушень не зазнавала вірогідних змін. У першій і другій групах спостерігалося зменшення рухових порушень порівняно зі станом до лікування (p < 0,05), причому більша доза препарату призводила до більшого ефекту (p < 0,01) (рис. 2). У контрольній групі динаміка рухових порушень не зазнавала вірогідних змін.
У групі хворих, які отримували 1,5% розчин іпідакрину, було відзначено більш значуще, ніж у двох інших групах, збільшення швидкості проведення імпульсу по сенсорним і моторним волокнам і найбільш істотне збільшення амплітуди довільного скорочення досліджуваних м’язів.
Побічні ефекти при застосуванні іпідакрину не відзначались.
Отже, проведене дослідження дозволило виявити вірогідне зменшення сенсорних і рухових порушень, покращання нервової провідності при парентеральному застосуванні іпідакрину в комплексному лікуванні хворих із діабетичною полінейропатією. Зазначені зміни мали дозозалежний характер: вірогідно більший позитивний ефект був отриманий при використанні 1,5% розчину іпідакрину по 1 мл 2 рази на день.
У відкрите контрольоване клінічне дослідження [13] було включено 60 пацієнтів із нейропатією певного нерва або радикулонейропатією. Захворювання розрізнялися за етіологією, включно з демієлінізуючими й інфекційними хворобами. Пацієнтів поділили на дві групи. Основна (n = 30) отримувала базову терапію + 1,5% іпідакрин внутрішньом’язово по 1 мл 1 раз на день. Контрольна група (n = 30) отримувала тільки базову терапію без іпідакрину. Тривалість лікування становила 20 днів.
Під час дослідження було виявлено, що зменшення інтенсивності болю хоча б на 1 бал за візуальною аналоговою шкалою спостерігалося більш часто в групі з іпідакрином (73,3 % пацієнтів) порівняно з контрольною групою (20 % пацієнтів) (p < 0,05). У групі з іпідакрином наростання болю відзначено не було, на той час як у контрольній групі біль посилився в 7 хворих.
Аналогічно збільшення м’язової сили (тобто регрес парезу) хоча б на 1 бал за шкалою MRC Muscle Scale спостерігалося більш часто в групі з іпідакрином (70 % пацієнтів) порівняно з контрольною групою (46,7 % пацієнтів) (значення p не наведено). У групі з іпідакрином парез наростав в 1 хворого, у контрольній групі — у 5 хворих.
Дані електронейроміографії були покращені у 80 % пацієнтів у групі з іпідакрином і 60 % пацієнтів у контрольній групі (значення p не наведено). Негативна динаміка при цьому методі дослідження спостерігалася в 1 хворого в групі з іпідакрином і 3 хворих у контрольній групі.
Під час дослідження не було виявлено істотних побічних ефектів. Найбільш часто зустрічалося невелике збільшення слиновиділення в групі з іпідакрином.
Автори роботи дійшли висновку, що іпідакрин є ефективним засобом у практиці лікування парезів, обумовлених нейропатіями й радикулопатіями. Включення даного препарату в комплекс лікувальних заходів дозволяє підвищити результативність лікування, зменшити тривалість відновного періоду і, що важливо, не супроводжується розвитком м’язових контрактур і інших значущих побічних ефектів. Знеболюючий ефект іпідакрину пов’язаний, мабуть, із блокадою потенціалзалежних Na+-каналів і може привести до зниження використання нестероїдних протизапальних засобів.
Висновки
У наведених вище клінічних дослідженнях була переконливо продемонстрована здатність іпідакрину покращувати функцію центральних і периферичних нервових волокон. В експериментальних дослідженнях була підтверджена здатність препарату зменшувати вираженість пошкоджень нервових структур. У сукупності це дозволяє іпідакрину ефективно боротися з руховими, чутливими й іншими порушеннями при різних захворюваннях нервової системи. У всіх дослідженнях були відзначені безпека й добра переносимість іпідакрину.
Одним із представників парентеральної форми іпідакрину на ринку України є лікарський засіб Медіаторн®, розчин для ін’єкцій, виробництва ПАТ «Галичфарм» (Корпорація «Артеріум»). Поряд із доброю ефективністю й безпекою препарату Медіаторн® важливою перевагою є його ціна — препарат приблизно в 1,5–2 рази доступніший
порівняно з іншими наявними в продажу аналогами.
Отже, з огляду на комплексний характер дії, клінічні й економічні переваги, Медіаторн® є оптимальним препаратом для лікування захворювань нервової системи, при яких потрібна корекція провідності й підтримка цілісності нервових структур.
Конфлікт інтересів. Не заявлений.
Список литературы
1. Neurological disorders: public health challenges // World Health Organization. — 2006. — http://www.who.int.
2. Применение ингибиторов ацетилхолинэстеразы при лечении заболеваний периферической нервной системы / Катунина Е.А., Аванесова О.В., Пестовская О.Р. и др. // Фарматека. — 2009. — № 15. — С. 52-55.
3. Нейромидин в клинической практике / Дамулин И.В., Живолупов С.А., Зайцев О.С. и др. // 2-е изд., перераб. и доп. — М.: Медицинское информационное агентство, 2016. — 60 с.
4. Федин А.Н. Венозная энцефалопатия // Невроньюс. — 2017. — Спецвып. — 20 с.
5. Комплексное лечение пациентов в раннем восстановительном периоде ишемического инсульта с применением препарата нейромидин / Литовченко Т.А., Завальная Е.П., Тондий О.Л., Лебединец В.В. // Український вісник психоневрології. — 2013. — Т. 21, № 3. — С. 27-30.
6. Особенности влияния нейромидина и магнитной стимуляции на нейропластичность при травматической невропатии / Живолупов C.А., Рашидов Н.А., Онищенко Л.С., Самарцев И.Н. // Кайшибаевские чтения: Сборник научных трудов V научно-практической конференции с международным участием, посвященной 80-летию профессора С.К. Кайшибаева. — Алматы, 8–10 октября 2015. — С. 43-48.
7. Пономарев В.В., Шабалина Ю.С., Брилева Е.В. Дозозависимая эффективность нейромидина для коррекции афазий в остром периоде мозгового инсульта // Международные обзоры: клиническая практика и здоровье. — 2013. — № 1. — C. 38-42.
8. Кальменева И.М. Постинсультная реабилитация больных перенесших инсульт // Вестник КазНМУ. Неврология. — 2011.
9. Никитин К.А. Антихолинэстеразная терапия в оториноларингологии // Материалы межрегиональной научно-практической конференции оториноларингологов Сибири и Дальнего Востока с международным участием «Актуальные вопросы оториноларингологии». — Благовещенск, 29–30 июня 2017. — С. 88-96.
10. Консервативное лечение недержания мочи после радикальной простатэктомии / Глыбочко П.В., Аляев Ю.Г., Винаров А.З. и др. // Урология. — 2012. — № 2. — С. 16-18.
11. Живолупов С.А., Бардаков С.Н. Роль ингибиторов ацетилхолинэстеразы в лечении миастении и миастенических синдромов // Нервно-мышечные болезни. — 2015. — № 3. — С. 77-78.
12. Дзяк Л.А., Шульга А.Н., Цуркаленко Е.С. Эффективность применения нейромидина в лечении диабетической полинейропатии // Український вісник психоневрології. — 2007. — Т. 15, № 2. — С. 135-138.
13. Парези при нейропатії та радикулопатії: тактика лікування / Орос М.М., Смоланка В.І., Яцинин Р.Ю., Савицька Н.О. // Міжнародний неврологічний журнал. — 2017. — № 8. — С. 53-58.

/24-1.jpg)
/25-1.jpg)