Поширеність синдрому подразненого кишечника (СПК) серед населення світу становить у середньому 11,2 %. У розвитку СПК відіграють роль генетичні фактори, розлади моторики, порушення вісцеральної чутливості, психосоціальні чинники, зміни кишкової мікробіоти, харчова непереносимість. Зміни способу життя й харчування сучасної людини, зниження фізичної активності, високі інформаційні й психоемоційні навантаження сприяють збереженню й поглибленню проявів СПК [1–4].
При великий варіабельності й нерідко досить інтенсивних суб’єктивних симптомах абдомінальний біль — основний симптом, що викликає найбільшу тривогу в пацієнта. Біль виникає у відповідь на ритмічні або постійні м’язові скорочення, спазми відділів кишки, розтягування кишечника газом, зміни вісцеральної чутливості травного каналу. Біль і неприємні відчуття у хворих із СПК виникають при більш низькому порозі збудливості, ніж у здорових людей. У патогенезі вісцеральної гіперчутливості важливу роль відіграє порушення балансу нейромедіаторів і регуляторних пептидів, таких як серотонін, холецистокінін, мотилін, ендогенні опіати, ендорфіни [4–6].
Поряд із сенсорною та нейром’язовою дисфункціями в розвитку СПК відіграють роль помірно виражені запальні зміни слизової оболонки кишечника, а також порушення якісного й кількісного складу кишкової мікрофлори. Про їх значення в патогенезі СПК свідчить те, що маніфестація захворювання часто відбувається після перенесених кишкових інфекцій, прийому антибіотиків. Больові відчуття в цих випадках можуть бути наслідком зміни складу бактеріальної мікрофлори кишечника, розвитку імунного запалення слизової оболонки кишечника низького ступеня активності (low-grade mucosal inflammation), для якого характерна інфільтрація слизової оболонки товстої кишки прозапальними цитокінами. Тривалий рецидивуючий кишковий біль, що турбує пацієнта протягом багатьох років, змінює звичний спосіб життя, знижує працездатність, вимагає постійної медикаментозної корекції й суттєво погіршує якість життя. Хворі з функціональним болем у животі — акцентуйовані особистості. Незадоволеність лікуванням, відсутність клінічного ефекту від терапії призводять до розвитку депресій, дратівливості, що ще більше ускладнює перебіг захворювання [5–7].
До переліку препаратів, що традиційно застосовуються при лікуванні хворих на СПК, входять спазмолітики й антидепресанти. Застосування спазмолітиків зумовлено тим, що для СПК характерні посилені скорочення кишечника (насамперед сигмоподібної кишки) у відповідь на прийом їжі або стрес, що може пояснити постпрандіальний біль і дискомфорт, а також імперативні позиви на дефекацію. Найбільш часто як перша лінія лікування СПК у європейських країнах застосовуються мебеверин і отилонію бромід, а в США — гіосцин і м’ятна олія в капсулах. Про корисні властивості олії м’яти перцевої відомо ще з часів Гіппократа й Авіценни. М’ята перцева широко використовується в сучасній медицині. На основі м’ятної олії й ментолу виготовляють комплексні препарати: болезаспокійливої дії, що застосовують при невралгії, міозиті, — меновазин і мазі гевкамен, ефкамон; евкатол, інгакамф, пектусин, аерозолі каметон, інгаліпт і камфомен; заспокійливі препарати при неврозах серця, тахікардії, безсонні — корвалол, корвалдин, валокормід, краплі Зеленіна, валідол; літолітичної дії — уролесан, оліметин і фітолізин [2, 8–10].
Олія м’яти перцевої містить ментол, його ефіри та інші біологічно активні речовини, такі як ментол, пінени, лимонен, феландрен, цинеол та інші терпеноїди, крім цього, у ній містяться флавоноїди, кислота урсолова й олеанолова, бетаїн, каротин, гесперидин, дубильні речовини, органічні кислоти, мікроелементи, що стимулюють чутливі рецептори слизових оболонок ротової порожнини й шлунка, рефлекторно зменшують відчуття нудоти, запобігають блюванню, а також мають помірну спазмолітичну, заспокійливу й жовчогінну дію [2, 10].
Сучасна наука виявила, що механізм впливу L-ментолу (головної складової олії м’яти перцевої) на кишечник — це поєднання ряду ефектів: спазмолітичного, розслаблюючого гладку мускулатуру, знеболюючого, протизапального, антимікробного. За даними нещодавніх міжнародних досліджень встановлено вірогідний ефект L-ментолу щодо зняття болю, спазмів, відчуття здуття, порушень випорожнення.
Мета дослідження: вивчення ефективності й переносимості препарату Капсумен у хворих на хронічний запор різного генезу, що призначався в дозі по 1 капсулі 2 рази на день протягом 4 тижнів.
Матеріали та методи
Проведено дослідження 20 хворих на СПК, яким, крім дієтичних рекомендацій, призначався препарат Капсумен, в 1 капсулі якого міститься 170 мг олії м’яти перцевої (L-ментолу 50 мг), у дозі по 1 капсулі 2 рази на день протягом 4 тижнів. Серед обстежених хворих переважали жінки — 14 (70 %) пацієнтів, чоловіків було 6 (30 %). Вік хворих становив від 21 до 52 років. У дослідженнях використовували загальноклінічні методи обстеження: опитування, фізичне обстеження, клінічні, лабораторні, інструментальні, рентгенологічні методи, ультразвукове дослідження органів черевної порожнини. Хворим проводили копрологічне й бактеріологічне дослідження фекалій.
Результати та обговорення
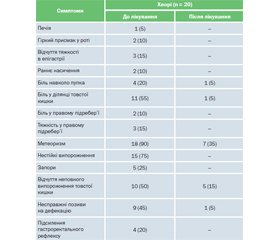
Серед клінічних проявів захворювання домінували скарги, що вказували на наявність в обстежених хворих синдрому подразненого кишечника (табл. 1).
До лікування в 90 % пацієнтів мав місце больовий синдром, біль навколо пупка турбував 20 % хворих, а біль, локалізований у ділянці товстої кишки, спостерігався в 55 % обстежених пацієнтів. У більшості хворих мав місце метеоризм — 90 % випадків. Порушення випорожнення спостерігались у 100 % хворих. У більшості обстежених хворих — 75 % — характер випорожнень був невизначеним, тобто запори чергувалися з послабленням, а інколи з нормальними випорожненнями; у 25 % мали місце запори; 50 % хворих скаржились на наявність відчуття неповного випорожнення товстої кишки, 45 % — на несправжні позиви на дефекацію, 20 % — на підсилення гастроректального рефлексу. Після лікування в більшості хворих зникли або зменшились клінічні прояви захворювання. Крім цього, покращилась переносимість харчових продуктів, що дозволило хворим розширити раціон харчування, зокрема збільшити вживання свіжих овочів і фруктів. Хворі добре переносили препарат, у жодному випадку не спостерігалось негативних побічних явищ.
Важливе значення для захворювань кишечника має стан кишкової мікробіоти. Відомо, що мікробіота впливає на численні процеси в організмі людини. Нормальна мікрофлора є фактором природної резистентності організму, чинить сильну антагоністичну дію щодо інших, у тому числі патогенних мікроорганізмів, сприяє розвитку неспецифічної й опосередковано-специфічної резистентності. Мікрофлора бере участь у порожнинному травленні, посилює перистальтику шлунково-кишкового тракту й сприяє збільшенню активності травних ферментів. Кишкова мікробіота впливає на функцію мозку, поведінкові реакції людини, а також є активним учасником метаболічних процесів. Дані щодо складу мікробіоценозу наведені в табл. 2.
/8_u.jpg)
До лікування в обстежених хворих було виявлено порушення родового складу кишкової мікрофлори. Спостерігалось зниження кількості представників облігатної флори. Так, до лікування кількість lg КУО/г Escherichia і Bifidobacterium була в 1,4 раза нижчою, ніж у здорових осіб; Lactobacillus — в 1,3 раза нижчою; Enterococcus — у 1,3 раза нижчою (р < 0,05 у всіх випадках). Щодо вмісту представників факультативної мікрофлори у фекаліях хворих на хронічний запор, то спостерігається збільшення їх вмісту в фекаліях. Кількість lg КУО/г Enterobacter збільшилася у 2,8 раза; Staphylococcus — в 1,6 раза; Klebsiella — у 2,3 раза; Clostridium — в 1,3 раза; Proteus — у 2,5 раза; Citobacter — в 1,7 раза; Candida — в 1,3 раза (р < 0,05 у всіх випадках).
Визначення вмісту у фекаліях хворих на хронічний запор представників облігатної й факультативної кишкової мікрофлори після лікування показало збільшення кількості lg КУО/г Escherichia і Bifidobacterium в 1,2 і 1,3 раза відповідно; Lactobacillus — в 1,2 раза (р < 0,05 у всіх випадках) і зменшення вмісту lg КУО/г Enterococcus в 1,2 раза, Staphylococcus — в 1,3 раза; Klebsiella — в 1,4 раза; Clostridium — в 1,3 раза; Proteus — в 1,4 раза; Citobacter — в 1,4 раза; Candida — в 1,4 раза порівняно з вмістом у фекаліях до лікування (р < 0,05 у всіх випадках).
Позитивний вплив на мікробіоценоз кишечника обумовлений поліфункціональною дією масла м’яти перцевої, що включає нормалізуючий вплив на рухову й секреторну функцію шлунково-кишкового тракту, покращення відтоку жовчі, процесів травлення.
Висновок
На підставі отриманих даних щодо позитивного впливу препарату Капсумен на клінічні прояви СПК, а саме зменшення метеоризму, больового синдрому, порушень випорожнення, а також результатів бактеріологічного дослідження фекалій можна зробити висновок про ефективність і безпеку застосування препарату м’яти перцевої Капсумен у лікуванні хворих на СПК.
Список литературы
1. Буторова Л.И., Калинин А.В. Синдром раздраженного кишечника: патогенетические подходы к лечению абдоминальной боли // Фарматека. — 2011. — № 12. — С. 8-10.
2. Вайс Р.Ф. Фитотерапия: Руководство: Пер. с нем. / Р.Ф. Вайс, Ф. Финтельманн. — М.: Медицина, 2004. — 552 с.
3. Ивашкин В.Т., Полуэктова Е.А. Синдром раздраженного кишечника: патофизиологические и клинические аспекты проблемы // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2015. — № 1. — С. 4-16.
4. Полуэктова Е.А., Кучумова С.Ю., Шептулин А.А., Ивашкин В.Т. Лечение синдрома раздраженного кишечника с позиций современных представлений о патогенезе заболевания // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2013. — № 1. — С. 57-65.
5. Ситкин С.И. Воспаление, микробиота, висцеральная гиперчувствительность — новые и «старые» терапевтические мишени при синдроме раздраженного кишечника // Клинические перспективы гастроэнтерологии, гепатологии. — 2014. — № 3. — С. 43-52.
6. Сamilleri M., Bueno L., Andersen V., De Ponti F., Choi M., Lembo A. Pharmacologic, pharmacokinetic and pharmacogenomic aspects of functional gastrointestinal disorders // Gastroenterology. — 2016. — 150. — 1319-1331.
7. Lowel R.M., Ford A.C. Global prevalence of and risk factors for irritable bowel syndrome: a meta-analysis // Clin. Gastroenterol., Gepatol. — 2012. — Vol. 10. — P. 712-721.
8. Клінічна фармакологія: Підручник для студентів і лікарів / [Абдуєва Ф.М., Бичкова О.Ю., Бондаренко І.О. та ін.]; за загальною редакцією М.І. Яблучанського та В.М. Савченка. — Х.: ХНУ імені В.Н. Каразіна, 2011. — 405 с.
9. Ковалев В.Н., Попова Н.В., Кисличенко В.С. и др. Практикум по фармакогнозии. Учебное пособие для студентов высших учебных заведений. — Х.: Изд-во НФаУ; Золотые страницы, 2003. — 510 с.
10. Лесиовская Е.Е. Доказательная фитотерапия: Учебник. — М.: Ремедиум, 2014. — 224 с.
11. American College of Gastroenterol monograph on the management of irritable bowel syndrome and chronic idiopathic constipation / A.C. Ford, P. Moayyedi, B.E. Lacy [et al.] // Am. J. Gastroenterol. — 2014. — Vol. 109. — P. S2-S26.
12. Chey W.D. Irritable bowel syndrome: a clinical review / W.D. Chey, J. Kurlander, S. Eswaran // JAMA. — 2015. — Vol. 313(9). — P. 949-958.
13. Drossman D.A., Hasler W.L. Rome IV — Functional GI Disorders: Disorders of Gut-Brain Interaction // Gastroenterology. — May 2016. — Vol. 150, Issue 6. — P. 1257-1261.
14. Talley N.Y., Jones M., Nuyts G., Dubois D. Risk factors for chronic constipation based on a general practice sample // Am. J. Gastroentеrol. — 2003. — 98. — 1107-1111.

/8_u.jpg)