Журнал «Практическая онкология» Том 2, №1, 2019
Вернуться к номеру
Випадок псевдоангіоматозної стромальної гіперплазії
Авторы: Галішина Г.О.
Спеціалізований мамологічний центр ПП «Перша приватна клініка», м. Київ, Україна
Рубрики: Онкология
Разделы: Справочник специалиста
Версия для печати
Псевдоангіоматозна стромальна гіперплазія (PASH) — це рідкісне доброякісне фіброзне ураження, в основі якого лежить патологічне розростання мезенхімальної тканини з клітинною вистілкою, що імітує судини. В статті наведено випадок PASH у жінки 25 років з історією спостереження.
Псевдоангиоматозная стромальная гиперплазия (PASH) — это редкое доброкачественное фиброзное поражение, в основе которого лежит патологическое разрастание мезенхимальной ткани с клеточной выстилкой, имитирующей сосуды. В статье приведен случай PASH у женщины 25 лет с историей наблюдения.
Pseudoangiomatous stromal hyperplasia is a rare benign fibrous lesion with underlying pathological growth of mesenchymal tissue with a cellular lining mimicking the blood vessels. The article presents a case of pseudoangiomatous stromal hyperplasia in a 25-year-old woman with follow-up.
псевдоангіоматозна стромальна гіперплазія; доброякісні пухлини молочних залоз
псевдоангиоматозная стромальная гиперплазия; доброкачественные опухоли молочных желез
pseudoangiomatous stromal hyperplasia; benign tumors of the mammary glands
Вступ
Псевдоангіоматозна стромальна гіперплазія (PASH) є доброякісним мезенхімальним захворюванням [1]. Уперше було описано в 1986 році Vuitch et al. [2] як судинне проліферативне ураження. Це рідкісне непухлинне ураження, що найчастіше проявляється в пременопаузі та має прямий зв’язок з гормональним статусом, що підтверджують імуногістохімічні дослідження, в 95 % випадків [1] вони мали позитивні естроген- і прогестерон-рецептори. Достеменно причини виникнення PASH невідомі, але є дані, що в 73 % випадків жінки приймали оральні контрацептиви або замісну гормональну терапію [3], середня тривалість прийому препаратів від 10 (комбіновані оральні конт–рацептиви) до 13 років (замісна гормональна терапія). За даними досліджень [4], в патогенезі важливу роль відіграє аномальна гіперреактивність міофібробластів на ендогенні й екзогенні гормони.
Приблизно на грудень 2018 року [5] в літературі описано 220 випадків PASH, з них усього 2 — у чоловіків (1 трансгендер та 1 з гінекомастією).
Виділяють такі види псевдоангіоматозної стромальної гіперплазії:
1. Гістологічно [3]:
— прості;
— фасцикулярно-проліферативні;
— асоційовані з іншими захворюваннями (наприклад, гінекомастія, карцинома, атипова гіперплазія, фіброаденома).
2. Клінічно [6]:
— дифузні;
— вузлові.
3. За локалізацією:
— одно- та двобічні;
— власне молочної залози чи аксилярної ділянки.
Найчастіше PASH проявляться утворенням, що пальпується аналогічно фіброаденомі [3, 7], але відомі випадки, коли вона була абсолютно асимптомною [4, 8] та виявлена лише за допомогою інструментальних методів. Відомі поодинокі випадки, коли були скарги на локальний біль та кров’янисті виділення з соска [9]. За результатами ультразвукового дослідження [10, 11], PASH проявляється гіпоехогенним утворенням з гетерогенною структурою (у 83 % випадків) та паралельною орієнтацією, нечітким контуром (62 %). За даними мамографії — високоінтенсивна тінь з нечітким контуром (тобто немає чітких рентгенологічних критеріїв для постановки діагнозу) [3] або локальна асиметрія [9]. За BIRADS зазвичай виставляли категорію 4 або 5. У 83 % випадків [11] для постановки діагнозу достатньо Core biopsy. Середній розмір утворень становив 4,2 см (від 0,8 до 11 см) [3]. Диференціювати необхідно з фіброаденомою, філоїдною пухлиною, гамартомою, ангіосаркомою, локальним фіброзом та низькодиференційованою ангіо–саркомою [12].
Гістологічно PASH характеризується наявністю проліферуючих міофібробластів, що вистилають щілиноподібні простори з анастомозами, що імітують кровоносні судини [1].
Щодо менеджменту проблеми в літературі існують три варіанти:
1. Хірургічний: секторальна резекція у випадках вузлової форми [3] або мастектомія при дифузних формах [4]. Ризик виникнення рецидиву становить 7 % [1].
2. Спостереження: у випадках, коли відсутнє збільшення в розмірах у динаміці [10].
3. Прийом тамоксифену описаний в літературі [13], але потребує додаткових досліджень.
Опис клінічного випадку
Пацієнтка, 25 років, звернулась зі скаргами на утворення в правій молочній залозі, яке змінювало розміри залежно від фази менструального циклу.
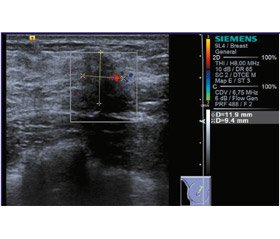
З анамнезу відомо, що гормональні контрацептиви не приймала, травми та хронічні захворювання заперечує, спадковий анамнез не обтяжено. За результатами об’єктивного огляду в правій молочній залозі виявлено щільне утворення розміром 2 см, безболісне, помірно рухоме, регіональні лімфатичні вузли мають фізіологічні властивості. За результатами ультразвукового дослідження (УЗД) в обох молочних залозах (рис. 1) виявлені гіпоехогенні утворення з нечіткими, нерівними контурами, посиленим перинодальним кровотоком, вертикальною орієнтацією щодо шкіри. За даними еластографії — мають високу щільність з характерними для гідрофільних включень мозаїчними зонами та ознаки перифокальної інфільтрації, виставлена категорія US-BIRADS 4C. У диференційно-діагностичному ряду розглянуті: карцинома, локальний аденоз, радіальний рубець, філоїдна пухлина. Виконано Core biopsy обох утворень голкою 14-10G, отримані стовпчики сіро-жовтого кольору відправили на гістологічне дослідження. Мікроскопічний опис препарату: матеріал представлений тільки фіброзною та жировою тканиною, визначаються численні щілиноподібні порожнини, що місцями анастомозують між собою, щілини вистелені міофібробластами, які імітують ендотеліальні клітини. В одному препараті визначається один проток, який вистелений двошаровим епітелієм без ознак атипії. Естроген-рецептор (DACO, клон EP1) — негативна реакція. Прогестерон-рецептор (DACO, клон PgR 636) — позитивна реакція у 90 % клітин протокового епітелію високої інтенсивності.
Обрано тактику спостереження: за 12 місяців спостереження розміри і структура утворень стабільні за результатами УЗД, суб’єктивні скарги не наростають.
Обговорення
У даної пацієнтки виявлено два утворення в обох молочних залозах, одне з яких не проявлялось клінічно, а стало УЗ-знахідкою. За стандартами виконана морфологічна верифікація та визначені позитивні гормональні рецептори. Прийнято рішення про консервативне ведення випадку через невеликі розміри утворень та відсутність тенденції до збільшення.
Висновки
1. Обов’язкова морфологічна верифікація з визначенням гормональних рецепторів.
2. Променеві методи діагностики не дозволяють чітко визначити патологію.
3. Індивідуальний підхід у виборі метода лікування.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
1. Bowman E., Oprea G., Okoli J. Pseudoangiomatous stromal hyperplasia (PASH) of the breast: a series of 24 patients // Breast J. — 2012. — 18. — Р. 242-247.
2. Vuitch M.F., Rosen Р.Р., Erlandson R.A. Pseudoangiomatous hyperplasia of mammary stroma // Hum. Pathol. — 1986. — 17. — Р. 185-191.
3. Marco Ferreira, Constance T. Albarracin, Erika Resetkova. Pseudoangiomatous stromal hyperplasia tumor: a clinical, radiologic and pathologic study of 26 cases // Modern Pathology. — 2007. — Vol. 21, № 2. — P. 201.
4. Powell C.M., Cranor M.L., Rosen P.P. Pseudoangiomatous stromal hyperplasia (PASH). A mammary stromal tumor with myofibroblastic differentiation // Am. J. Surg. Pathol. — 1995. — 19. — Р. 270-277.
5. Ko S.Y., Koh M.J. Bilateral diffuse tumorous pseudoangiomatous stromal hyperplasia treated with bilateral mastectomy in a 40-year-old woman // Radiol. Case Rep. — 2018. — 13(6). — Р. 1271-1275.
6. Rosa G., Dawson A., Jordi Rowe J. Does Identifying Whether Pseudoangiomatous Stromal Hyperplasia (PASH) Is Focal or Diffuse on Core Biopsy Correlate With a PASH Nodule on Excision? // International Journal of Surgical Pathology. — 2017. — 25(4). — Р. 292-297.
7. Okoshi K., Ogawa H., Suwa H. et al. A case of nodular pseudoangiomatous stromal hyperplasia (PASH) // Breast Cancer. — 2006. — 13. — Р. 349-353.
8. Sean D. Raj, Vivek G. Sahani, Beatriz Elena Adrada, Marion Elizabeth Scoggins, Constance Albarracin, Piyanoot Woodtichartpreecha, Flavia E. Posleman Monetto, Gary J. Whitman. Pseudoangiomatous Stromal Hyperplasia of the Breast (PASH): Multimodality Review with Pathologic Correlation // Current Problems in Diagnostic Radiology. — 2016.
9. Rafeek N., Dev B., Thambidurai L., Satchidanandam A. Tumoral pseudoangiomatous stromal hyperplasia: Radiological and pathological correlation with review of literature // Egyptian Journal of Radiology and Nuclear Medicine. — 2017. — 48(1). — Р. 147-152.
10. Gormlaith C. Hargaden, Eren D. Yeh, Dianne Georgian-Smith, Richard H. Moore, Elizabeth A. Rafferty, Elkan F. Halpern, Grace T. McKee. Analysis of the Mammographic and Sonographic Features of Pseudoangiomatous Stromal Hyperplasia // American Journal of Roentgenology. — 2008. — 191(2). — Р. 359-363.
11. Сhoi Y.J., Ko E.Y., Kook S. Diagnosis of pseudoangiomatous stromal hyperplasia of the breast: ultrasonography findings and different biopsy methods // Yonsei Med. J. — 2008 Oct 31. — 49(5). — Р. 757-64.
12. Wendie A. Berg // Diagnostic Imaging. — 2007. — IV-2. — Р. 66-69.
13. Pruthi S., Reynolds C., Johnson R.E., Gisvold J.J. Tamoxifen in the management of pseudoangiomatous stromal hyperplasia // Breast J. — 2001 Nov-Dec. — 7(6). — Р. 434-9.

/40-1.jpg)