Журнал «Здоровье ребенка» Том 14, №5, 2019
Вернуться к номеру
Досвід клінічного застосування респіраторного пробіотика Бактобліс у дітей із секреторним середнім отитом
Авторы: Гавриленко Ю.В.
Національна медична академія післядипломної освіти імені П.Л. Шупика, м. Київ,Україна
Рубрики: Педиатрия/Неонатология
Разделы: Справочник специалиста
Версия для печати
Секреторний середній отит (ССО) у дітей залишається на сьогодні поширеним захворюванням лор-органів серед хворих різних вікових груп. Причина його виникнення — продовження гострого середнього отиту (ГСО), перебіг гострого післявірусного риносинуситу, гіпертрофія аденоїдних вегетацій та інші. Дане захворювання характеризується стійкою наявністю рідини в порожнині середнього вуха, зниженням слухової функції, різними скаргами пацієнтів на відчуття у вусі. Було проведено обстеження й подальше спостереження за 22 дітьми, хворими на ССО, які протягом 30 днів отримували терапію пероральним пробіотиком Бактобліс. Після проведеного лікування дітей було оцінено епізоди ГСО, проаналізовано результати тональної аудіометрії, комплексної тимпанометрії, ендоскопії носа й носоглотки, отоскопії, мікроотоскопії та обстеження піднебінних мигдаликів. Також було оцінено переносимість, побічну дію прийому респіраторного пробіотика. Отримані результати дослідження вказують на добрий профіль безпеки, вірогідне зменшення епізодів ГСО і позитивний ефект лікування за усіма проаналізованими клінічними даними. Застосування перорального пробіотика Бактобліс може відігравати певну роль у зниженні частоти виникнення й ступеня тяжкості перебігу ССО в дітей, що покращує якість життя пацієнтів.
Секреторный средний отит (ССО) у детей остается на сегодня распространенным заболеванием лор-органов среди больных разных возрастных групп. Причина его возникновения — продолжение острого среднего отита (ОСО), течение острого послевирусного синусита, гипертрофия аденоидных вегетаций и другие. Данное заболевание характеризуется устойчивым наличием жидкости в полости среднего уха, снижением слуховой функции, различными жалобами пациентов на ощущения в ухе. Было проведено обследование и дальнейшее наблюдение за 22 детьми, больными ССО, которые в течение 30 дней получали терапию пероральным пробиотиком Бактоблис. После проведенного лечения детей были оценены эпизоды ОСО, проанализированы результаты тональной аудиометрии, комплексной тимпанометрии, эндоскопии носа и носоглотки, отоскопии, микроотоскопии и обследования небных миндалин. Также были оценены переносимость, побочные действия приема респираторного пробиотика. Полученные результаты исследования указывают на хороший профиль безопасности, достоверное уменьшение эпизодов ОСО и положительный эффект лечения по всем проанализированным клиническим данным. Применение перорального пробиотика Бактоблис может играть определенную роль в снижении частоты и степени тяжести ССО у детей, улучшает качество жизни пациентов.
Secretory otitis media (SOM) in children remains a common ENT disease among patients of different age groups today. Its cause is the continuation of acute otitis media (AOM), the course of acute post-viral rhinosinusitis, adenoid hypertrophy, etc. This disease is characterized by the persistent presence of fluid in the middle ear cavity, decreased auditory function, various complaints of patients on sensations in the ear. An examination and follow-up of 22 children with SOM was performed, they received therapy with Bactoblis oral probiotic for 30 days. After the treatment of children, episodes of AOM were evaluated, tonal audiometry, comprehensive tympanometry, endoscopy of the nose and nasopharynx, otoscopy, microotoscopy and examination of the palatine tonsils were analyzed. The tolerability, side effects of respiratory probiotic were also evaluated. The results of the study indicate a good safety profile, a significant reduction in AOM episodes and a positive treatment effect according to all the clinical data analyzed. The use of an oral probiotic Bactoblis may play a certain role in reducing the incidence and severity of SOM in children, which improves patients’ quality of life.
гострий середній отит; секреторний середній отит; діти; пробіотики; Бактобліс
острый средний отит; секреторный средний отит; дети; пробиотики; Бактоблис
acute otitis media; secretory otitis media; children; probiotics; Bactoblis
Вступ
Гострий середній отит (ГСО) — це одна з найчастіших проблем дитячого віку, яку необхідно вирішувати не тільки дитячим отоларингологам, але й педіатрам, сімейним лікарям. За даними літератури, близько 70 % дітей до трьохрічного віку переносять один раз ГСО, а 80–90 % дітей дошкільного віку мають принаймні один епізод секреторного середнього отиту (ССО) [1]. Відомо, що основними бактеріальними збудниками ГСО є Streptococcus pneumoniae, Haemophilus influenzae, Moraxella catarrhalis і Streptococcus pyogenes, що часто мають транстубарний шлях поширення інфекції від носової частини глотки до порожнини середнього вуха через слухову трубу, викликаючи виражені запальні реакції.
Досить часто при ССО наявний безсимптомний стійкий ексудат у порожнині середнього вуха, який виникає на тлі ГСО, ГПРС. Дане захворювання часто зникає спонтанно, але в деяких випадках, особливо коли має місце двобічний процес, який присутній понад 2 місяці, може вимагатися оперативне лікування в дитячому віці з уведенням тимпаностомічної трубки для дренажу, щоб уникнути проблем зі стійким зниженням слуху або переходом у хронічний процес [2].
Антибіотики, протизапальні препарати й кортикостероїди не усувають накопичений ексудат у середньому вусі, саме тому вони не можуть бути широко рекомендовані до застосування. За даними авторів встановлено, що діти, які схильні до розвитку отиту, переносять більше бактеріальних збудників у мікробіоті носової частини глотки й менше потенційно-інтерферентних мікроорганізмів, таких як альфа-гемолітичні стрептококи, негемолітичні стрептококи, види Prevotella й Peptostreptococcus [3, 4]. При цьому встановлено, що деякі штами альфа-гемолітичних стрептококів пригнічують розмноження патогенних бактерій in vitro, а застосування назального спрею з альфа-гемолітичними стрептококами в дітей, схильних до отиту, знижує ризик рецидиву ГСО й розвитку ССО.
Крім того, дослідниками встановлено, що спрей-терапія альфа-гемолітичними стрептококами в дітей зі встановленим ССО може зменшити кількість рідини в середньому вусі, тим самим зменшуючи проблеми зі слухом і надаючи можливість уникнути хірургічного втручання в багатьох випадках. Протягом останніх років було досліджено багато пероральних стрептококів, що здатні перешкоджати розмноженню патогенів, які мешкають у ротовій порожнині й носоглотці. Серед них найбільш ретельно вивченим є пероральний пробіотик Streptococcus salivarius K12 (Бактобліс). Даний штам продукує два характерні лантибіотики, що кодуються мегаплазмідом і називаються саліварицин А2 і саліварицин В, вони здатні гальмувати розмноження S.pyogenes, S.pneumoniae, M.catarrhalis, які беруть участь у патогенезі ГСО й бактеріального фаринготонзиліту в дітей і дорослих [5, 6]. Нещодавні клінічні дослідження, які проводилися в дорослих і дітей, продемонстрували, що лікування пероральним пробіотиком Бактобліс вірогідно знижує кількість рецидивів бактеріального фаринготонзиліту й ГСО [7].
Тому клінічний інтерес викликає визначення ефективності й переносимості пробіотика Бактобліс при лікуванні дітей із захворюваннями середнього вуха для встановлення можливого захисного ефекту з точки зору зменшення рецидивів ГСО і прогресування ССО.
Мета проведеного дослідження полягала в оцінці ефективності, профілю безпеки й переносимості пробіотика Бактобліс при застосуванні його протягом 30 днів дітям, хворим на ССО, за наявності ексудату в середньому вусі щонайменше протягом 3 місяців, здатності препарату захищати від рецидиву ГСО, спостереження за регресом ССО за допомогою тональної аудіометрії, комплексної тимпанометрії, ендоназальної ендоскопії, отоскопії, мікроотоскопії й обстеження піднебінних мигдаликів (ПМ).
Матеріали та методи
Клінічні дослідження пацієнтів були проведені на базі кафедри дитячої оториноларингології, аудіології та фоніатрії Національної медичної академії післядипломної освіти (НМАПО) імені П.Л. Шупика.
Тональна аудіометрія
Проводилася на аудіометрі MА-13 на частотах від 250 до 8000 Гц для аналізу визначення порогів слуху. За потреби застосовували кістковий шлях (частоти від 250 до 4000 Гц). Використовувана методика була беззвучною, а поріг вважався найменшою інтенсивністю, при якій у 100 % випадків дитина відповідала на наявність звуку. Середні тональні пороги на частотах 250–2000 Гц для дітей класифікували як норму (оцінка = 0; до 15 дБ); зниження слуху легкого ступеня внаслідок порушення передачі звуку (оцінка = 1; від 16 до 70 дБ; зниження слуху тяжкого ступеня внаслідок порушення передачі звуку (оцінка = 2, понад 71 дБ).
Комплексна тимпанометрія
Для оцінки стану середнього вуха використовувався тимпанометр Otometrics (Interacustic, Данія). Тимпанограма оцінювалася за трьома типами умов: тип А (нормальний стан); тип В (наявність ексудату в середньому вусі); тип С (порушення функції слухової труби).
Мікроотоскопія
Дані, одержані за результатами мікроотоскопії, були класифіковані відповідно до чотирьох ступенів: нормальна барабанна перетинка (оцінка = 0); матовоподібна барабанна перетинка (оцінка = 1); матовоподібна й втягнута барабанна перетинка (оцінка = 2); потовщена, з рівнем рідини барабанна перетинка (оцінка = 3).
Ендоназальна ендоскопія
Ендоназальне ендоскопічне обстеження проводили за допомогою прямого чи кутового ендоскопа Karl Storz з оглядом внутрішньоносових структур, склепіння носової частини глотки, глоткового отвору слухової труби з тубарними валиками.
Обстеження піднебінних мигдаликів
Об’єм ПМ класифікували відповідно до затверджених критеріїв таким чином: ПМ ледь помітні позаду передньої дужки у мигдаликовій ямці (оцінка = 0); ПМ помітні за передньою дужкою (оцінка = 1); гіпертрофовані ПМ розташовані на три чверті шляху до середньої лінії (оцінка = 2); ПМ повністю ускладнюють прохідність дихальних шляхів (оцінка = 3).
Статистичний аналіз
Різницю між двома групами клінічних змінних — до і після терапії пробіотиком Бактобліс — визначали за допомогою двостороннього критерію Манна — Уїтні, а різниця між показниками до і після тимпанометрії визначалася за допомогою критерію Фішера. Статистичні розрахунки були здійснені з використанням програмного забезпечення IBM SPSS 17.0, Statisticа 8.0, Microsoft Office Excel 2010.
Результати та обговорення
Протягом 2019 року було обстежено 22 амбулаторних хворих дитячого віку із ССО, які перебували на амбулаторному лікуванні у лор-відділенні міської дитячої клінічної лікарні № 1 міста Києва, на базі якого розташована кафедра дитячої оториноларингології, аудіології і фоніатрії НМАПО імені П.Л. Шупика. Хлопчиків було 12, дівчаток — 10. Віковий діапазон дітей становив від 2 до 6 років, середній вік — 3,5 ± 1,4 року. Усі пацієнти в період лікування приймали пероральний пробіотик Бактобліс (пакетики-саше). Склад на 1 пакетик-саше 1,5 г: діючі речовини: пробіотик Streptococcus salivarius K12; вітамін D3 8 мкг. Додаткові речовини: мальтодекстрин; фруктоолігосахариди; ароматизатор. Починаючи з Т = 0 до Т = 30 кожен пацієнт приймав пакетик-саше Бактобліс щовечора, безпосередньо перед сном. Вироблення слини зазвичай знижується у вечірні години, що покращує ефективність пероральної колонізації.
Серед 22 включених пацієнтів 7 повідомили про алергію в анамнезі, 5 хворих із 22 залучених до дослідження мали позитивний результат бактеріологічного посіву з ПМ на S.pyogenes. Ці ж пацієнти також мали позитивний результат бакпосіву на мікрофлору й залишалися безсимптомними наприкінці дослідження, що свідчить про те, що вони є здоровими носіями. Проте жоден інший пацієнт не мав позитивного результату посіву на S.pyogenes наприкінці дослідження. Статистичний аналіз отриманих даних у дітей до і після лікування пробіотиком Бактобліс подано в табл. 1.
Як видно з табл. 1, пероральне застосування респіраторного пробіотика Бактобліс сприяло вірогідному зменшенню деяких клінічно значущих результатів. А саме: частота випадків ГСО, розрахована як кількість епізодів на місяць на одну дитину, знижувалась на 71 % після лікування порівняно з відповідною частотою випадків, розрахованою за кількістю епізодів, що сталися в попередньому році.
Отоскопічні дані барабанної перетинки при мікроотоскопії покращилися на 65 %, а закладеність вуха знижувалася на 60 %.
Аналіз отриманих даних тимпанометрії в дітей із ССО до і після застосування перорального пробіотика Бактобліс наведено в табл. 2.
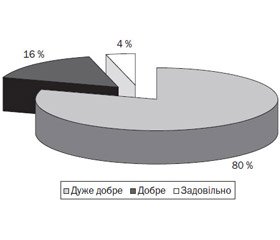
Як видно з табл. 3, результати проведеної тимпанометрії в дітей із ССО істотно покращилися, зокрема щодо наявності ексудату в середньому вусі, який відзначали в Т = 30 лише у двох випадках, з обох сторін. Відсутні релевантні відмінності щодо порушення функції слухової труби. Стосовно переносимості терапії респіраторним пробіотиком Бактобліс слід зазначити, що пробіотичне лікування продемонструвало дуже добрий профіль безпеки, без будь-яких пов’язаних із ним побічних ефектів чи випадків виключення пацієнтів із дослідження. Ці дані наведені на рис. 1.
Отже, можна сформулювати дві гіпотези. Перша полягає в тому, що пероральна терапія пробіотиком Бактобліс, можливо, зменшила популяції відповідних збудників у мікробіоті носоглотки. А друга гіпотеза полягає в тому, що лікування респіраторним пробіотиком Бактобліс у дітей із ССО могло стимулювати вроджений імунітет, сприяючи виведенню патогенних бактерій із середнього вуха. Отримані результати вказують на те, що стимуляція антибактеріальних імунних ефекторних механізмів, а не бактеріальне втручання може бути відповідальною за спостережувані клінічні переваги перорального застосування пробіотика Бактобліс.
Висновки
У даному неконтрольованому дослідженні, проведеному за участі дітей із діагнозом рецидивуючого ГСО й безсимптомного ССО, ми використовували Бактобліс, що добре зарекомендував себе. Отримані нами результати демонструють, що даний пероральний пробіотик: 1) має добрий профіль безпеки при застосуванні в дітей, схильних до розвитку отиту, які страждають від безсимптомного ССО; 2) має опосередкований захисний ефект щодо зменшення рецидивів ГСО; 3) за результатами спостереження за хворими, які приймали препарат Бактобліс, встановлено покращання клінічних симптомів і особливостей перебігу захворювання, характерних для дітей із ССО.
Проте це дослідження перш за все доповнює загальний профіль безпеки штамів S.salivarius К12 при рецидивуючих інфекціях верхніх дихальних шляхів, а також у дітей, хворих на ССО, які мають порушення функції слухової труби за наявності ексудату середнього вуха. Позитивні результати слід розглядати лише як відправну точку для подальшої оцінки ролі штамів S.salivarius К12 у дітей із ГСО та/або ССО.
Конфлікт інтересів. Не заявлений.
1. Гавриленко Ю.В. Раціональна терапія: місцеве лікування гострого середнього отиту. Современная педиатрия. 2016. № 6(78). С. 19-23.
2. Лайко А.А., Заболотний Д.І., Борисенко О.М. та ін. Хронічні хвороби середнього вуха. К.: Логос, 2018. 325 с.
3. Di Pierro F., Di Pasquale D., Di Cicco M. Oral use of Streptococcus salivarius K12 in children with secretory otitis media: preliminary results of a pilot, uncontrolled study. Int. J. Gen. Med. 2015. 8. 303-308. doi:10.2147/IJGM.S92488.
4. Леженко Г.О., Абатуров О.Є., Пашкова О.Є. Роль ендогенних антимікробних пептидів у бактеріальній колонізації носоглотки в дітей із гіперплазією ретроназальної мигдалини. Здоровье ребенка. 2016. № 6(74). С. 74-80. doi:10.22141/2224-0551.6.74.2016.82136.
5. Wescombe P.A., Hale J.D., Heng N.C., Tagg J.R. Developing oral probiotics from Streptococcus salivarius. Future Microbiol. 2012. 7(12). 1355-1371. doi:10.2217/fmb.12.113.
6. Di Pierro F., Colombo М., Zanvit А., P. Risso Р., Rottoli A.S. Use of Streptococcus salivarius K12 in the prevention of streptococcal and viral pharyngotonsillitis in children. Drug Healthc Patient Saf. 2014. 6. 15-20. doi:10.2147/DHPS.S59665.
7. Крючко Т.А. Можливості застосування лантибіотиків у профілактиці рекурентних інфекцій верхніх дихальних шляхів у дітей. Здоровье ребенка. 2017. Т. 12. № 8. С. 2-7.

/31-2.jpg)
/31-1.jpg)