Вступ
Сучасні військові конфлікти характеризуються збільшенням частки поліструктурних пошкоджень кінцівок щодо інших анатомічних ділянок, що обумовлено застосуванням у війнах початку XXI сторіччя індивідуальних комплексів захисту тулуба та голови. Так, згідно з аналізом структури поранень під час АТО частка поранень кінцівок сягає до 64 %, тоді як поранення тулуба становлять до 20 %. У той же час за весь період АТО не змінюється тенденція переважання кількості уражень нижніх кінцівок до верхніх — в середньому 2,4 до 1 відповідно, що спонукає до вивчення перебігу ранової хвороби бойових ушкоджень саме нижніх кінцівок. Одним із найбільш тяжких патологічних станів, що лежать в основі більшості ускладнень вогнепальних поранень кінцівок та можуть призводити до стійкої інвалідизації. є компартмент-синдром (КС), або місцевий гіпертензивний ішемічний синдром (МГІС). Значний відсоток незадовільних результатів лікування у вигляді гнійно-некротичних ускладнень, контрактур суміжних суглобів, порушення функцій периферичних нервів та вогнепального остеомієліту, що часто стає підставою до виконання ампутації ураженої кінцівки, робить актуальним питання вивчення помилок під час діагностики та лікування МГІС на фоні вогнепальних ушкоджень нижніх кінцівок (ВУНК) із метою профілактики розвитку ускладнень.
Матеріали та методи
Нами проаналізований результат лікування 58 хворих на МГІС на фоні вогнепальних поранень та переломів кісток нижніх кінцівок під час проведення АТО на Сході України.
Усі пацієнти були чоловічої статі віком від 21 до 62 років (середній вік — 45,8 ± 3,3 року). За характером уражуючого фактора в 34 (60,5 %) випадках МГІС розвинувся на фоні вогнепальних кульових переломів довгих трубчастих кісток, в 15 (26,5 %) — після мінно-вибухової травми з переломом кісток кінцівок та в 9 (13 %) — на фоні множинних осколкових поранень м’яких тканин нижніх кінцівок.
Залежно від локалізації МГІС переважало ураження гомілки — 31 (55 %), стегна — 23 (39 %), сідничної ділянки — 2 (3,4 %), стопи — 2 (3,4 %). Розвиток КС на суміжному з ураженим сегментом кінцівки діагностований у 5 (8,6 %) постраждалих: у 2 випадках — при вогнепальних переломах верхньої третини гомілки та в 3 — при внутрішносуглобовому переломі метаепіфізів стегнової та великогомілкової кісток.
У 49 (86,8 %) випадках МГІС розвинувся на фоні вогнепальних багатоуламкових переломів, з яких у 12 (20 %) випадках розвитку МГІС передувало пошкодження судинно-нервових пучків. Так, за даними медичної документації, 2 (3,4 %) пацієнтам виконувалась автовенозна пластика стегнової артерії, у 2 (3,4 %) випадках — підколінної, в 3 (7,8 %) — задньої та у 2 (3,4 %) — передньої великогомілкової артерій. Клінічні прояви пошкодження периферичних нервів при МГІС зустрічались у 18 (31 %) поранених. Ізольовані пошкодження сідничного та стегнового нервів відмічалися у 2 (3,4 %) випадках, великогомілкового — у 4 (5,1 %), малогомілкового нерва — в 10 (17 %) та їх поєднання — в 3 (5,1 %) випадках.
Час від моменту отримання поранення до надходження на етап спеціалізованої травматологічної допомоги коливався від декількох годин до 2–5 діб, у зв’язку з чим ми спостерігали випадки розвитку МГІС у м’язово-фасціальних футлярах кінцівок у стадії як оборотних, так і необоротних порушень кровообігу.
Наявність щільного набряку м’яких тканин, блідість шкірних покровів, ослаблення або відсутність капілярного відклику, порушення чутливості в проєкції стоп ураженої кінцівки потребували виключення МГІС. Для вимірювання підфасціального тиску ми застосовували серійний прилад фірми Stryker. Обов’язковим є вимірювання тиску у всіх м’язово-фасціальних футлярах ураженого сегмента. Отримання показників у межах 30–40 мм рт.ст., що були меншими за рівень діастолічного артеріального тиску, було одним із показань щодо виконання первинної (ПХО) або повторної хірургічної обробки вогнепальної рани за невідкладними показаннями. Хірургічна обробка при вогнепальних пораненнях потребує беззаперечного виконання базових її принципів: широкого розсічення рани, висічення нежиттєздатних тканин, ревізії судинно-нервових структур та фасціотомії всіх м’язово-фасціальних футлярів на всьому протязі ураженого сегмента.
Фасціотомні рани після перенесеного МГІС характеризуються вираженим паравульнарним набряком, рясною сукровичною ексудацією та схильністю до інфікування, що робить процес їх лікування дуже складним. З метою покращання результатів лікування додатково впроваджено застосування ультразвукової кавітації вогнепальних ран та систем їх вакуум-асоційованого закриття. Ультразвуковий дебридмент рани та посилення репаративних процесів у рані під впливом терапії керованим негативним тиском (NPWT-терапії) сприяють активному росту грануляційної тканини та чіткому відмежуванню нежиттєздатних тканин. Застосування NPWT-терапії дозволяє забезпечити постійну й адекватну евакуацію ранового ексудату та зменшення інтерстиційного набряку, стимулювання формування грануляційної тканини в оптимально вологому рановому середовищі, запобігає її реінфікуванню, розвитку перехресних інфекцій та антибіотикорезистентних штамів у лікарні.
Здебільшого перебіг лікування супроводжувався розвитком гнійно-некротичних ускладнень з боку операційних ран, що потребувало виконання повторних хірургічних обробок. У 4 випадках була виконана ампутація ураженого сегмента.
По-друге, перебіг травматичної хвороби потребував корекції водно-електролітного балансу, анемії, гіпопротеїнемії, нирково-печінкового градієнта, що, зі свого боку, потребувало розміщення пацієнтів в умовах відділення реанімації, проведення гемодіалізу у зв’язку з розвитком у поранених гострої ниркової недостатності та курсів ГБО, що значно покращує репаративні процеси в рані та показники гомеостазу.
Був один летальний випадок, що пов’язаний із розвитком поліорганної недостатності на фоні переважаючої гострої ниркової недостатності у зв’язку з перенесеним тяжким компартмент-синдромом обох гомілок.
Розвиток стійких контрактур у суглобах ураженої кінцівки та збереження клінічних проявів пошкодження периферичних нервів потребували тривалого реабілітаційного лікування, виконання етапних реконструктивних оперативних втручань.
Значна кількість ускладнень, що супроводжує перебіг МГІС, спонукала нас до аналізу помилок та можливих причин розвитку ускладнень.
Результати та обговорення
Найбільш часто МГІС розвивався на фоні вогнепального поранення верхньої третини гомілки в поєднанні з уламковим переломом її кісток, що спостерігалось у 18 (31 %) випадках. У 12 (21 %) пацієнтів МГІС діагностовано на фоні пошкодження периферичних нервів. Розвиток МГІС на фоні шокового стану пораненого спостерігався в 10 (17 %) постраждалих. І нарешті, повторні хірургічні обробки у 22 (37 %) поранених продемонстрували відсутність адекватної фасціотомії на ураженому сегменті, що не дозволяло отримати необхідного декомпресивного ефекту. В цю ж групу увійшли пацієнти після відновлення пошкоджених магістральних судин (4 — 7 %), яким не була виконана профілактична фасціотомія на ураженому та суміжному сегментах.
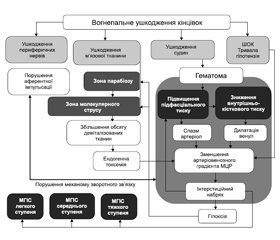
Цілком логічно, що розвиток ускладнень пов’язаний із неврахуванням у схемі лікування патологічних процесів, які лежать в основі розвитку МГІС при вогнепальному ушкодженні (рис. 1).
На рис. 1 ми навели основні ланцюги розвитку МГІС при вогнепальних ушкодженнях, що утворюються при ушкодженні м’язової тканини, судин, нер-вових стовбурів та супроводжуються шоковим станом або тривалою гіпотензією з формуванням порочних кіл, які потенціюють один одного та створюють умови для підвищення підфасціального тиску.
Міжм’язова гематома, що утворюється при ушкодженні судин, створює умови для відносного зменшення обсягу кістково-фасціального футляра та компресії ушкодженого м’яза. Збільшення підфасціального тиску супроводжується зниженням внутрішньокісткового тиску. Спазм артеріол та дилатація венул призводять до зменшення артеріовенозного градієнта та розвитку інтерстиційного набряку, що збільшує обсяг ураженого м’яза в замкненому просторі кістково-фасціального футляра та супроводжується поступовим зростанням підфасціального тиску, створюючи перше порочне коло. Таким чином, збільшення обсягу кістково-фасціального футляра за рахунок гематоми або набряку м’яза є передумовою розвитку МГІС.
У той же час порушення функціонування мікроциркуляторного русла призводить до гіпоксії м’язової тканини, в якій найбільш уразливою є зона молекулярного струсу та парабіозу, що утворюються по ходу ранового каналу. Відсутність адекватного капілярного кровопостачання збільшує обсяг ішемізованих тканин ушкодженого м’яза і, як наслідок, ендогенну токсемію. Токсичне ураження ендотелію капілярів погіршує функцію мікроциркуляторного русла та призводить до анаеробного кліткового метаболізму в уражених тканинах, збільшення інтерстиційного набряку та гіпоксії з формуванням другого порочного кола.
З наведеного вище стає зрозумілим факт переважання розвитку МГІС при ушкодженнях на рівні верхньої третини гомілки, що становив майже 40 % всіх простежених випадків, що, ймовірно, обумовлено особливостями анатомічного розташування судинно-нервових пучків щодо кістково-фасціальних футлярів на цьому рівні. Збільшення тиску в підфасціальному просторі призводить до стиснення судинно-нервових структур унаслідок невідповідності резерву збільшення обсягу футляра у зв’язку з відносною нееластичністю фасції та збільшення обсягу ураженого м’яза.
Нагадуємо, що ключовим фактором у розвитку МГІС є різниця між діастолічним артеріальним та внутрішньом’язовим тиском, тобто артеріальний тиск оказує безпосередній вплив на перфузійний тиск ушкодженого м’яза. Тому іншою патогенетично обумовленою ланкою розвитку МГІС є стан, що супроводжується шоком або тривалою гіпотензією. Тому група поранених, стан яких супроводжується гіпотензією, потребує особливої уваги хірурга та обов’язкового динамічного спостереження щодо розвитку МГІС.
У той же час периферичні нерви, що проходять через футляр, в якому підвищений підфасціальний тиск, також перебувають у стані ішемії. Це проявляється скаргами на порушення периферичної чутливості та є однією з діагностичних ознак розвитку МГІС. Але порушення аферентної імпульсації внаслідок вогнепального пошкодження периферичного нерва може згладжувати та маскувати характерні для МГІС скарги на нестерпний біль розриваючого характеру. Також подібна ситуація виникає при порушенні свідомості та коматозному стані пораненого.
Таким чином, порушення механізму зворотного зв’язку внаслідок пошкодження периферичних нервів, кома, тривала гіпотензія та шок створюють сприятливі умови для формування порочних кіл розвитку МГІС, в основі яких лежить підвищення підфасціального тиску, а єдиним патогенетично обґрунтованим методом лікування МГІС при ВУНК є декомпресійна фасціотомія.
Ураховуючи наведене вище, ми проаналізували помилки діагностичного та лікувального етапів, розподіливши їх на дві основні групи: стратегічні та тактичні.
Стратегічні помилки — група помилок, що пов’язані з неврахуванням етіопатогенетичних механізмів розвитку МГІС при ВУНК, які з високою часткою вірогідності призводять до розвитку ускладнень (табл. 1).
Тактичні помилки — помилки, пов’язані з дефектами виконання певних елементів комплексного лікування поранених із ВНУК, що призводить до розвитку та прогресування МГІС (табл. 2).
Стратегічні помилки, що, на нашу думку, могли призвести до розвитку МГІС, були виявлені в 33 (56,6 %) пацієнтів. Частіше ускладнення розвивалось на фоні відмови від фасціотомії всіх КФФ при вогнепальних пораненнях кінцівок, що відмічалося в 10 (17,2 %) випадках, при цьому кількість оборотних та необоротних змін була однаковою — 5 (8,6 %) випадків (табл. 1). Група пацієнтів із розвитком МГІС на фоні вогнепальних переломів була меншою — 8 (13,7 %) хворих, але кількість необоротних змін була більшою та становила 6 (10,3 %) випадків, серед яких більша частина — випадки розвитку МГІС після вогнепальних переломів на рівні верхньої та середньої третини гомілки — 4 (6,8 %). Окремо звертають на себе увагу 9 (15,5 %) випадків розвитку МГІС у пацієнтів, які мали поєднані тяжкі поранення голови, тулуба та кінцівок, що супроводжувались явищами шоку або тривалої гіпотензії. При цьому кількість необоротних змін у м’яких тканинах становила 7 (12 %) випадків. Як правило, пацієнтам цієї групи хірургічна обробка ран кінцівок виконувалась другим етапом після виконання оперативного втручання, направленого на збереження вітальних функцій.
/116.jpg)
Загальна кількість тактичних помилок становила 66 випадків у 58 пацієнтів із МГІС нижніх кінцівок, що обумовлено тим, що в деяких випадках зустрічалась комбінація двох чи трьох помилок в одного пацієнта. Найбільш часто зустрічались помилки, пов’язані з порушенням виконання техніки фасціотомії КФФ, — 37 (56 %) випадків, серед яких переважали необоротні зміни в м’язах ураженого сегмента — 28 (42,4 %) (табл. 2). Найбільш часто ми спостерігали ознаки МГІС після фасціотомії, що не забезпечують адекватного декомпресійного ефекту, які відмічалися в 10 випадках (27 %) від усіх простежених випадків МГІС (табл. 3). Як правило, визначалось розсічення фасції на протязі до 2–3 см навколо раннього каналу. Фасціотомія лише одного футляра в проекції вхідного отвору ранового каналу мала місце в 18 (31 %) випадках, що в поєднанні зі збереженням цілісності фасції інших трьох КФФ залишало ризик розвитку МГІС вкрай високим.
Структура тактичних помилок, пов’язаних із порушенням техніки виконання фасціотомії, наведена в табл. 3. Найбільш часто зустрічались помилки у вигляді фасціотомії лише одного футляра ураженого сегмента, що мало місце в 18 (31 %) випадках, та фасціотомії, що не забезпечували адекватного декомпресійного ефекту — 10 (27 %) пацієнтів.
З метою вивчення статистично вірогідного впливу стратегічних та тактичних помилок на тяжкість перебігу МГІС ми вирішили дослідити силу зв’язку в парах «фактор ризику — наслідок» за допомогою методу «багато польових таблиць», де досліджуваний фактор ризику — це стратегічна або тактична помилка, а наслідок — наявність чи відсутність необоротних ішемічних змін у м’язах ураженого сегмента.
Як видно з табл. 1, загальна кількість стратегічних помилок, які, на нашу думку, могли стати причиною розвитку МГІС, мала місце в 33 (56,6 %) випадках, при цьому кількість оборотних та необоротних змін становила відповідно 11 (18,8 %) та 22 (37,9 %).
Для визначення вірогідності отриманих результатів в табл. 4 проведений аналіз із використанням непараметричних статистичних критеріїв за методом критерію χ2 Пірсона та визначенням сили зв’язку за допомогою коефіцієнта кореляції Пірсона (С). Розрахунки виконувались за допомогою online-калькулятора програми medstatistic.ru.
Так, аналіз даних табл. 4 дозволив отримати такі результати: значення критерію χ2 = 4,090 із рівнем значимості критерію p < 0,05 та коефіцієнтом кореляції С = 2,257, що відповідає середній силі зв’язку між показниками та свідчить про те, що кореляційний зв’язок у парі «стратегічні помилки — необоротні зміни в м’яких тканинах» є статистично значимим.
Таким чином, ми можемо стверджувати, що при ВУНК, що супроводжуються розвитком МГІС, стратегічні помилки лежать в основі розвитку необоротних ішемічних змін у 22 (37,9 %) випадках (р < 0,05).
Для статистичної обробки впливу тактичних помилок на розвиток ускладнень з табл. 2 нами обрана група пацієнтів з однорідними помилками, які пов’язані з порушенням техніки виконання фасціотомії, що було визначено в 37 (63,7 %) пацієнтів (табл. 3). При цьому загальна кількість оборотних та необоротних змін становила відповідно 9 (15 %) та 28 (48 %) випадків.
Аналіз даних табл. 5 також потребував використання непараметричних статистичних критеріїв за методом критерію χ2 Пірсона, але з поправкою Єйтса, внаслідок того, що в таблиці один із показників мав величину меншу за 10: 7 (12 %) — кількість випадків розвитку необоротних змін, при яких не було визначено тактичних помилок.
Критерій χ2 з поправкою Єйтса дорівнює 8,346 з рівнем значимості критерію p < 0,01 та коефіцієнтом кореляції Пірсона (С) = 0,543, що відповідало відносно сильній силі зв’язку між досліджуваними парами показників та свідчить про те, що кореляційний зв’язок в парі «порушення техніки виконання фасціотомії» між ними є статистично значимим.
Таким чином, ми можемо стверджувати, що тактична помилка «порушення техніки фасціотомії» призводила до розвитку необоротних змін у м’язах ураженого сегмента при МГІС у 28 (48 %) випадках (p < 0,01).
Наведені вище дані демонструють, що стратегічні і тактичні помилки, що виявлені в поранених із необоротними формами МГІС при ВУНК, здебільшого пов’язані з відмовою від виконання фасціотомії або технічними помилками під час її виконання.
На нашу думку, це пов’язано з недостатньою обізнаністю лікарів хірургів та травматологів, які першими приймають хворого з пораненням кінцівок, внаслідок браку інформації на шпальтах сучасних медичних видань відносно показань до виконання фасціотомії, техніки та обсягу оперативного втручання.
Наполягаємо, що ефективною є лише фасціотомія всіх КФФ на протязі всього сегмента. Найбільш оптимальним є виконання фасціотомії з просвіту ранового каналу з метою зменшення обсягу хірургічної агресії. Але в разі, коли локалізація вхідного чи вихідного отвору ранового каналу не дозволяє виконати адекватну фасціотомію, остання повинна бути виконана через окремий доступ відповідно до анатомічних орієнтирів КФФ на кожному сегменті з урахуванням проекції судинно-нервових структур. З цією метою доцільне застосування фасціотомів різної довжини. Використання різного виду ножиць не завжди дозволяє повноцінно виконати підшкірну фасціотомію в дистальних відділах сегмента та супроводжується підвищеним ризиком ятрогенного ушкодження судинно-нервових структур.
Окремої уваги потребують стани, що супроводжуються шоком або тривалою гіпотензією. Зниження рівня артеріального тиску на фоні поєднаної вогнепальної травми голови, тулуба та кінцівок створює умови, при яких артеріовенозний градієнт тиску в підфасціальному просторі стає рівним або меншим за внутрішньомязовий, що створює передумови до латентного перебігу розвитку МГІС. В нашому дослідженні кількість таких випадків становила 9 (15,5 %), серед яких переважали необоротні зміни в м’язах ураженого сегмента — 7 (12 %).
Як правило, хірургічна обробка ран кінцівок таким пацієнтам виконується в другу чергу, після завершення операції, направленої на збереження вітальних функцій та, на жаль, часто без дотримання необхідних стандартів, визначених при лікуванні вогнепальних ран кінцівок. Невеликі за обсягом та площею ранові дефекти, відсутність кровотечі та вираженого набряку сегмента кінцівок внаслідок артеріальної гіпотензії або шоку маскують клінічний перебіг МГІС. З іншого боку, недостатня хірургічна настороженість чергових лікарів та недостатня інформованість щодо особливостей патогенетичних механізмів розвитку МГІС при пораненнях кінцівок створюють умови для розвитку необоротних ішемічних змін уражених сегментів.
На нашу думку, пацієнтам із шоковим станом повинна виконуватись превентивна підшкірна фасціотомія навіть за відсутності клінічних або інструментальних ознак підвищення підфасціального тиску. Відходження від цього стандарту є дуже загрозливим у плані розвитку компартмент-синдрому.
Таким чином, розвиток та прогресування МГІС при ВУНК із високим ступенем вірогідності пов’язаний із неврахуванням етіопатогенетичного механізму розвитку ускладнення та порушенням виконання техніки фасціотомії футлярів ураженого сегмента, які ми вважаємо стратегічною та тактичною помилками.
Висновки
1. Аналіз результатів лікування пацієнтів із МГІС при ВУНК дозволив виділити групу стратегічних та тактичних помилок, які статистично вірогідно впливали на розвиток КС.
2. Визначена група стратегічних помилок, що пов’язані з неврахуванням етіопатогенетичних механізмів розвитку МГІС, вірогідно впливає на розвиток необоротних ішемічних змін при МГІС у 22 (37,9 %) випадках (р < 0,05).
3. Визначена група тактичних помилок, які пов’язані з порушенням техніки фасціотомії, призводила до розвитку необоротних змін у м’язах ураженого сегмента при МГІС у 28 (48 %) випадках (p < 0,01).
4. Отримані дані свідчать про потребу в продовженні досліджень у даній проблемі, популяризації інформації щодо ризиків розвитку КС при вогнепальних пошкодженнях кінцівок, техніки фасціотомій тощо.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.

/114.jpg)
/116.jpg)
/117.jpg)