Резюме
Актуальність. Хвороба рухового нейрона, або бічний аміотрофічний склероз (БАС), насамперед характеризується руховими порушеннями, а також супроводжується широким діапазоном немоторних симптомів. Серед немоторних симптомів слід виділити больовий синдром, що залишається недостатньо дослідженим. Метою нашого дослідження було визначення частоти виникнення больового синдрому на ранніх стадіях хвороби рухового нейрона, виявлення найбільш частої локалізації болю. Матеріали та методи. Обстежено 49 пацієнтів з БАС від 27 до 79 років, середній вік яких становив 57 років. Діагноз базувався на переглянутих Ель-Ескоріальських критеріях. Візуально-аналогова шкала (ВАШ) була використана для визначення інтенсивності болю, а розширена переглянута шкала оцінки БАС (ALSFRS-R) — для моніторингу прогресування хвороби. Результати. Больові відчуття були виявлені у 69 % пацієнтів, причому їх наявність не залежала від статі і віку обстежених. Найбільш частими дескрипторами больового синдрому були ниючі, тягнучі, смикаючі, а також пекучі відчуття. Хвороба статистично значуще прогресувала повільніше (р = 0,01) у пацієнтів без болю (40,4 ± 4,4 бала) порівняно з пацієнтами з наявністю больових відчуттів (36,5 ± 4,9 бала) за шкалою ALSFRS-R. Було відзначено, що біль в основному локалізувався в верхніх кінцівках (38 %), нижніх кінцівках (27 %) і попереково-крижовій ділянці (15 %). Наявність больового синдрому вірогідно залежала від дебюту захворювання. Ризик виникнення болю у пацієнтів із шийним дебютом був у 1,5 раза вищим. При бульбарному дебюті хворі вкрай рідко вказували на наявність больових відчуттів (4,0 ± 5,5 %). Висновки. Больовий синдром слід виявляти вже на ранніх стадіях хвороби мотонейрона. Оскільки наявність болю у пацієнтів корелює з більш швидким прогресуванням хвороби, лікувальні заходи слід коригувати з урахуванням даного симптому. Гетерогенність больових відчуттів вимагає додаткового вивчення і відповідного планування реабілітаційних процедур.
Актуальность. Болезнь двигательного нейрона, или боковой амиотрофический склероз (БАС), прежде всего характеризуется двигательными нарушениями, а также сопровождается широким диапазоном немоторных симптомов. Среди немоторных симптомов следует выделить болевой синдром, который остается недостаточно исследованным. Целью нашего исследования было определение частоты встречаемости болевого синдрома на ранних стадиях болезни двигательного нейрона, выявление наиболее частой локализации боли. Материалы и методы. Обследовано 49 пациентов с БАС от 27 до 79 лет, средний возраст которых составлял 57 лет. Диагноз базировался на пересмотренных Эль-Эскориальских критериях болезни двигательного нейрона. Визуально-аналоговая шкала (ВАШ) была использована для определения интенсивности боли, а расширенная пересмотренная шкала оценки БАС (ALSFRS-R) — для мониторинга прогрессирования болезни. Результаты. Болевые ощущения были выявлены у 69 % пациентов, причем их наличие не зависело от пола и возраста обследуемых. Наиболее частыми дескрипторами болевого синдрома были ноющие, тянущие, дергающие, а также пекущие ощущения. Болезнь статистически значимо прогрессировала значительно медленнее (р = 0,01) у пациентов без боли (40,4 ± 4,4) по сравнению с пациентами с наличием болевых ощущений (36,5 ± 4,9 балла) по шкале ALSFRS-R. Было отмечено, что боль в основном локализовалась в верхних конечностях (38 %), нижних конечностях (27 %) и пояснично-крестцовой области (15 %). Наличие болевого синдрома достоверно зависело от дебюта заболевания. Риск возникновения боли у пациентов с шейным дебютом был в 1,5 раза выше. При бульбарном дебюте больные крайне редко отмечали наличие болевых ощущений (4,0 ± 5,5 %). Выводы. Болевой синдром следует выявлять уже на ранних стадиях болезни двигательного нейрона. Поскольку наличие боли у пациентов коррелирует с более быстрым прогрессированием болезни, лечебные мероприятия следует корректировать с учетом этого симптома. Гетерогенность болевых ощущений требует дополнительного изучения и соответствующего планирования реабилитационных процедур.
Background. Motor neuron disease, or amyotrophic lateral sclerosis (ALS), is primarily characterized by progressive motor deficit and various non-motor symptoms. One of such symptoms is pain syndrome, which continues to be poorly understood and often not detected by clinicians. The purpose of our study was to determine the frequency of pain syndrome in the early stages of motor neuron disease and the anatomical localization of pain. Materials and methods. We examined 49 ALS patients aged 27 to 79 years (on average 56.7 years). The ALS diagnosis was based on the revised El Escorial criteria. The visual analog scale was used to determine the intensity of pain, and the ALS functional rating scale (ALSFRS-R) — to monitor disease progression. Results. In this study, 69 % of patients had experienced pain. The presence of pain reported by ALS patients was not sex and age dependent. The most frequent descriptors of pain syndrome reported by the patients were nagging, pulling, throbbing, and burning sensations. The disease progresses statistically slowly in patients without pain (40.4 ± 4.4 points) compared to those with pain sensations (36.5 ± 4.9 points, p = 0.01) according to ALSFRS-R. We found that pain was mainly localized in the upper extremities (38 %), lower extremities (27 %) and lower back (15 %). The presence of pain syndrome depended significantly on the onset of the disease. The risk of pain in patients with the onset in the neck was 1.5 times higher. Patients with bulbar onset rarely complained about pain (4.0 ± 5.5 %). Conclusions. Clinicians should detect pain syndrome in the early stages of motor neuron disease. Since the presence of pain in ALS patients correlates with a more rapid disease progression, therapeutic measures should be adjusted to the presence of such symptom. Pain heterogeneity requires additional study and appropriate planning of rehabilitation.
Вступ
Хвороба рухового нейрона, або бічний аміотрофічний склероз (БАС), — це фатальне швидкоінвалідизуюче нейродегенеративне захворювання, при якому вражаються переважно альфа-мотонейрони спинного мозку, мотонейрони стовбура мозку і первинної моторної кори [1].
Захворюваність на БАС зростає в усьому світі. За даними Глобального фонду аналізу хвороб за період з 1990 по 2016 рік, смертність від хвороби рухового нейрона збільшилася на 8 %, найбільша кількість пацієнтів була зареєстрована в країнах з високим рівнем доходу на душу населення.
Результати показали, що в 2016 році 330 918 осіб у всьому світі страждали від хвороби рухового нейрона. Поширеність серед всіх вікових груп становила 4–5 випадків на 100 000 населення на рік. Однією з перших ознак ураження центральних мотонейронів при БАС може бути втрата спритності, що виражається в повільності, недолугості при виконанні тонких, звичних рухових актів. Іншими ознаками є підвищення м’язового тонусу, сегментарних рефлексів, поява ознак паралічу і патологічних кистьових і стопних знаків.
Загибель периферичних мотонейронів призводить до появи парезів, гіпорефлексії, атрофії скелетних м’язів, фасцикуляцій і іноді болісних м’язових крампі. Парези найчастіше виникають локально й асиметрично, спочатку у верхніх або нижніх кінцівках, послідовно поширюючись на сусідні м’язові групи. Атрофії зазвичай переважають в м’язах-розгиначах. Бульбарний і псевдобульбарний синдроми відносять до частих ознак хвороби рухового нейрона, що виникає як на ранніх, так і на пізніх стадіях захворювання. Вони можуть проявлятися дисфонією, дизартрією, дисфагією, фасцикуляціями й атрофією язика, насильницьким сміхом або плачем, рефлексами орального автоматизму, а також синдромом оральної гіперсекреції. Клінічна варіабельність і неухильне прогресування симптоматики, значні порушення дихання і ковтання на різних стадіях хвороби, БАС-асоційована атрофія та кахексія, відсутність специфічних біомаркерів, паліативний характер доступної терапії зумовлюють виникнення суспільних і етичних дилем при веденні хворих із термінальними стадіями БАС, що не мають однозначних шляхів розв’язання. Усі ці чинники вимагають від лікаря вирішення найбільш складних проблем клінічної й експериментальної неврології.
Доступні наукові дані, що пояснюють етіологію хвороби, украй мізерні і потребують додаткових досліджень. До факторів ризику БАС у чоловіків відносять зайнятість у сільському господарстві, будівництві, лісовому господарстві, захоплення рибальством і полюванням. Ці професії і хобі можуть бути пов’язані з надмірними фізичними навантаженнями, а також впливом таких токсичних речовин, як свинець, інші важкі метали, дизельне паливо [2]. Численні дані вказують на статистично значуще збільшення ризику виникнення хвороби мотонейрона при безпосередньому контакті з важкими металами, а також пестицидами в сільському господарстві [3]. Відзначається високий ризик виникнення цього грізного захворювання у професійних гравців у футбол [4].
Сімейні форми хвороби мотонейрона зустрічаються приблизно у 10 % хворих, у переважній більшості випадків захворювання вважається спорадичним [5]. Діагностичні тести для хвороби мотонейрона знаходяться в стадії розробки, хоча в багатьох випадках генетичні дослідження, електронейроміографія і ней-ровізуалізація можуть істотно допомогти в постановці діагнозу.
Концепція вибіркового ураження мотонейронів, що панує протягом останніх десятиліть, ставиться під сумнів. Накопичується все більше даних про залучення чутливих нейронів на певних етапах розвитку патологічного процесу. Так, зокрема, гістологічні дослідження вказують на те, що у деяких хворих на БАС до патоморфологічного процесу можуть залучатися периферичні чутливі нерви, спінальні ганглії і задні канатики спинного мозку [6]. За допомогою нейрорадіологічних і електрофізіологічних методів досліджень спинного мозку можна виявити субклінічний сенсорний дефіцит приблизно у 85 % пацієнтів із хворобою мотонейрона [7]. Ці та інші факти залучення екстрамоторних систем у патологічний процес при БАС змушують клініцистів і дослідників звернути увагу на немоторні прояви хвороби.
У низці випадків при хворобі мотонейрона у пацієнтів, крім больових відчуттів різного характеру, виявляють когнітивні порушення, безсоння, загальну слабкість, депресію, тривогу [8–11]. При обстеженні хворих на БАС виявленню й оцінці больового синдрому лікарями приділяється недостатньо уваги, оскільки захворювання традиційно вважається безболісним [12]. Частота больового синдрому у пацієнтів із БАС, за даними різних джерел, може варіювати від 51 до 85 % [13, 14]. Нерідко біль істотно знижує якість життя хворих на БАС [14]. Висока частота цих немоторних проявів хвороби, її причини, медикаментозна і немедикаментозна терапія вимагають додаткового дослідження.
Матеріали та методи
До даного дослідження нами були включені 49 пацієнтів із хворобою мотонейрона (28 (57 %) чоловіків і 21 (43 %) жінка), середній вік яких становив 56,7 ± 11,0 року. Діагностика БАС базувалася на переглянутих Ель-Ескоріальських клініко-діагностичних критеріях і визначалася як клінічно вірогідний БАС.
Критеріями відбору були: клінічно та інструментально вірогідний БАС, інформована згода пацієнта, відсутність симптомів деменції згідно з МКБ-10.
Критеріями виключення служили: відсутність інформованої згоди пацієнта, клінічно й інструментально непідтверджений БАС, згідно з наведеними вище критеріями, а також симптоми деменції.
Візуально-аналогова шкала (ВАШ) використовувалась для визначення інтенсивності болю. Пацієнт оцінював больові відчуття на відрізку, що дорівнює 10 см, діапазон оцінок становив від 10 до 0, де 10 балів — це найсильніший біль, якій хворий коли-небудь відчував, а 0 — повна відсутність болю. Розширена переглянута шкала оцінки БАС (ALSFRS-R) була використана для моніторингу динаміки прогресування захворювання [16].
При локальній болючості, скутості в суглобах і різних відділах хребта проводилося додаткове магнітно-резонансне томографічне дослідження.
Статистичні дані оброблялися з використанням Statistics 6.1. Перевірка розподілу показників проводилася за допомогою критерію Колмогорова — Смирнова. Для опису нормально розподілених показників використовували середнє значення і середньоквадратичне відхилення (М ± SD), при розподілі, відмінному від гаусового, — медіану і квартилі (Me, IQR: Q1–Q3). При описі частотних характеристик використовували частоту і 95% довірчий інтервал (P ± 95% ДI). Для порівняння 2 груп застосовувався критерій Стьюдента (t) або Манна — Уїтні (U), кількох груп — критерій Краскела — Уолліса (χ22). Порівняння частот проводили за допомогою таблиць спряженості. На статистично значущі відмінності вказує критерій хі-квадрат Пірсона (χ2), на щільність зв’язку — коефіцієнт чотирьохпольової кореляції (φ) або, в разі недихотомічних змінних, ʋ Крамера (ʋ), відносний ризик наведено з 95% довірчим інтервалом (RR ± 95% ДI). Розбіжності вважалися значущими при р ≤ 0,05.
Результати та обговорення
Із 49 пацієнтів з БАС у 34 (69,4 %) відзначалися больові відчуття різного ступеня інтенсивності. Наявність больового синдрому у пацієнтів не залежала від статі і становила для чоловіків 68 % (19/9) випадків, для жінок — 71 % (15/6). Середній вік пацієнтів із больовим синдромом становив 54,9 ± 10,8 року і статистично значуще не відрізнявся від віку пацієнтів, які не мали болісних відчуттів, — 60,9 ± 12,1. Середнє значення функціональної шкали оцінки прогресування захворювання (ALSFRS-R) у пацієнтів із больовим синдромом становило 36,5 ± 4,9 бала, а без болю — 40,4 ± 4,4 бала, що відрізняється на статистично значущому рівні (t = 2,67, p = 0,01). Пацієнти вказували на появу болю у таких ділянках, як нижні кінцівки, поперекова ділянка, тулуб, плечовий пояс, верхні кінцівки, шия та голова.
Найчастіше у пацієнтів з БАС біль локалізувався переважно у верхніх кінцівках (кисть, передпліччя, плече) — 38,0 ± 16,3 %, нижніх кінцівках (стопа, гомілка, стегно) — 27,0 ± 14,8 %, а також в поперековій ділянці — 15,0 ± 11,9 % (рис. 1).
Пацієнти описували свої больові відчуття як ниючі — 11 з 34 (32,4 ± 15,7 %), тягнучі — 10 з 34 (29,4 ± 15,3 %), смикаючі — 6 з 34 (17,6 ± 12,8 %), пекучі — 4 з 34 (11,8 ± 10,8 %). Колючий, стискаючий і пульсуючий характер болю відзначали поодинокі пацієнти (2,9 ± 10,2 %).
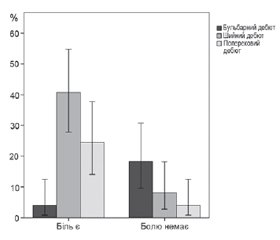
Наявність больового синдрому статистично значуще корелювала з типом дебюту БАС (χ2 = 17,5, ʋ = 0,59, р = 0,001). Вкрай рідко больовий синдром відзначався при бульбарному дебюті хвороби мотонейрона — 2 з 49 (4,0 ± 5,5 %), найчастіше біль відчували пацієнти з шийним дебютом — 20 з 49 (41,0 ± 13,8 %), а при поперековому дебюті біль виявлявся у 12 із 49 (25,0 ± 12,0 %) (рис. 2). У пацієнтів з шийним дебютом ризик появи болю був в 1,5 раза вищим (χ2 = 4,3, φ = 0,3, р = 0,04; RR = 1,49, 95% ДI 1,01–2,20).
Бали за ВАШ і функціональною шкалою (ALSFRS-R) від дебюту БАС статистично значуще не залежали. Однак у пацієнтів з шийним дебютом при відсутності болю бал за функціональною шкалою статистично значуще був нижчим (Me = 38,0, IQR 35,0–38,8) порівняно з іншим дебютом (Me = 42,0, IQR 40,0–44,0; U = 4,5, p = 0,02), хоча, за літературними даними [16], розширена переглянута шкала оцінки БАС має валідну структуру і внутрішню зваженість. Бал за ВАШ становив для бульбарного дебюту 3,5 ± 0,7, для шийного — 5,5 ± 1,6, для поперекового — 5,4 ± 2,1.
У нашій вибірці 19 з 49 пацієнтів мали тривалість захворювання більше 2 років, однак наявність больового синдрому й інтенсивність болю не залежали від терміну захворювання (рис. 3), на відміну від бала за функціональною шкалою, що при 1–2-річному перебігу хвороби статистично значуще був вищим (U = 169,5, p = 0,02; Me = 40,0, IQR 34,8–43,0), ніж при 3–4-річному (Me = 37,0, IQR 31,0–39,0).
Висновки
Наші дані продемонстрували, що біль при хворобі мотонейрона є досить частим симптомом і не залежить від статі і віку обстежених хворих. У групі пацієнтів із больовим синдромом відзначено більш швидке прогресування характерних моторних симптомів БАС порівняно з пацієнтами, які не мали больових відчуттів.
Біль найчастіше локалізувався в верхніх і нижніх кінцівках, а також у поперековій ділянці. За зменшенням частоти виникнення у хворих відзначалися ниючі, тягнучі, смикаючі, пекучі болі, а стискаючі, колючі та пульсуючі болі зустрічалися з приблизно однаковою частотою і досить рідко. Нами було відзначено, що при бульбарному дебюті больові відчуття у пацієнтів були практично відсутні.
Аналіз результатів дослідження показав, що тривалість захворювання не впливала на наявність і інтенсивність больового синдрому.
Для поглиблення наших уявлень про механізми виникнення болю і його вплив на якість життя пацієнтів з БАС необхідні подальші дослідження вчених і практикуючих лікарів. Необхідна розробка стандартизованого опитувальника болю для даної категорії хворих. Виявлення та лікування больового синдрому слід визнати важливим вектором паліативної допомоги при даному захворюванні.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Список литературы
1. Conradi S., Ronnevi L.O. Selective vulnerability of alpha motor neurons in ALS: relation to autoantibodies toward acetylcholinesterase (AChE) in ALS patients. Brain. Res. Bull. 1993. 30(3–4). Р. 369-71.
2. Aisha S., Hansen J., Kioumourtzoglou M.A. et al. Study of occupation and amyotrophic lateral sclerosis in a Danish cohort. Occup. Environ. Med. 2018 Sep. 75(9). Р. 630-638.
3. Malek A.M., Barchowsky A., Bowser R. et al. Environmental and Occupational Risk Factors for Amyotrophic Lateral Sclerosis: A Case-Control Study. Neurodegener. Dis. 2014. 14. Р. 31-38.
4. Chio A., Calvo A., Dossena M., Ghiglione P. et al. ALS in Ita-lian professional soccer players: the risk is still present and could be soccer-specifi. Amyotroph. Lateral. Scler. 2009 Aug. 10(4). Р. 205-9.
5. Majoor-Krakauer D., Willems P.J., Hofman A. Genetic epidemiology of amyotrophic lateral sclerosis. Clin. Genet. 2003. 63. Р. 83-101.
6. Wakabayashi K., Horikawa Y., Oyake M. et al. Sporadic motor neuron disease with severe sensory neuronopathy. Acta Neuropathol. 1998 Apr. 95(4). Р. 426-30.
7. Iglesias C., Sangari S., El Mendili M.M. et al. Electrophysiological and spinal imaging evidences for sensory dysfunction in amyotrophic lateral sclerosis. BMJ Open. 2015 Feb. 24. 5(2).
8. Chiò A., Moglia C., Canosa A. et al. A Cognitive impairment across ALS clinical stages in a population-based cohort. Neurology. 2019 Aug. 13. Pii. Р. 10.121.
9. Lo Coco D., Fatigue L.V. Sleep, and nocturnal complaints in patients with amyotrophic lateral sclerosis. Eur. J. Neurol. 2012 May. 19(5).
10. Prado L., Bicalho I.C., Vidigal-Lopes M. et al. Depression and anxiety in a case series of amyotrophic lateral sclerosis: frequency and association with clinical features. Einstein (Sao Paulo). 2017 Jan-Mar. 15(1). Р. 58-6.
11. Аkerblom Y., Jakobsson L.B., Zetterberg L. et al. The multiple faces of pain in motor neuron disease: a qualitative study to inform pain assessment and pain management. Disabil. Rehabil. 2019 Apr. 24. Р. 1-10.
12. Handy C.R., Krudy C., Boulis N. Pain in Amyotrophic La-teral Sclerosis: A Neglected Aspect of Disease. Neurol. Res. Int. 2011 May. 3.
13. Rivera I., Ajroud-Driss S., Casey P. et al. Prevalence and characteristics of pain in early and late stages of ALS. Amyotroph Lateral Scler Frontotemporal Degener. 2013 Sep. 14(5–6). Р. 369-72
14. Wallace V.C., Ellis C.M., Burman R. et al. The evaluation of pain in amyotrophic lateral sclerosis: a case controlled observational study. Amyotroph. Lateral Scler. Frontotemporal. Degener. 2014 Dec. 15(7–8). Р. 520-7.
15. Scott J., Huskisson E.C. Graphic representation of pain. Pain. 1976. 2(2). Р. 175-184.
16. Castrillo-Viguera C., Grasso D., Simpson E. et al. Clinical significance in the change of decline in ALSFRS-R. Amyotrophic Lateral Sclerosis. 2010. Volume 11. Issue 1–2.
/95.jpg)

/96.jpg)
/96_2.jpg)