Журнал «Почки» Том 9, №3, 2020
Вернуться к номеру
Продовжена тривала діуретична терапія
Авторы: Іванов Д.Д.
Національна медична академія післядипломної освіти імені П.Л. Шупика, м. Київ, Україна
Рубрики: Нефрология
Разделы: Справочник специалиста
Версия для печати
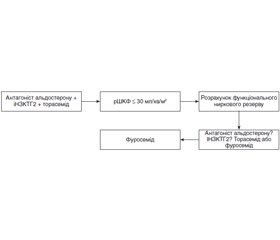
Розглянуті практичні аспекти призначення діуретичної терапії при хронічній хворобі нирок (ХХН), цукровому діабеті (ЦД) і серцевій недостатності (СН) — як окремих нозологіях, так і при їх комбінації. Незважаючи на те, що ці захворювання мають різну етіологію, хронічна затримка рідини є загальним проявом при їх прогресуванні. Починаючи з 2020 року комбінована діуретична терапія антагоністом альдостерону та петльовим діуретиком доповнена інгібіторами натрійзалежного котранспортера глюкози 2-го типу (іНЗКТГ2) при ХХН, ЦД і хронічній СН зі зниженою фракцією викиду. Така тактика демонструє кращу дегідратацію, збільшення виживаності пацієнтів і зниження серцево-судинної смертності. Проте зниження швидкості клубочкової фільтрації (ШКФ) супроводжується зменшенням ефективності позначених ліків. Такою межею є ШКФ менше за 30 мл/хв/м2, хоча існують індивідуальні коливання. Можливим рішенням питання індивідуалізації продовження потрійної тривалої діуретичної терапії є визначення функціонального ниркового резерву. Його збереження та контроль калію крові дозволяє продовжувати потрійну терапію. Інакше пацієнт вимушений відміняти антагоніст альдостерону, іНЗКТГ2, переходити з торасеміду на фуросемід і готуватись до нирково-замісної терапії.
Рассмотрены практические аспекты назначения диуретической терапии при хронической болезни почек (ХБП), сахарном диабете (СД) и сердечной недостаточности (СН) — как отдельных нозологиях, так и при их комбинации. Несмотря на то, что эти заболевания имеют разную этиологию, хроническая задержка жидкости является общим проявлением при их прогрессировании. С 2020 года комбинированная диуретическая терапия антагонистом альдостерона и петлевым диуретиком дополнена ингибиторами натрийзависимого котранспортера глюкозы 2-го типа (иНЗКТГ2) при ХБП, СД и хронической СН со сниженной фракцией выброса. Такая тактика демонстрирует лучшую дегидратацию, увеличение выживаемости пациентов и снижение сердечно-сосудистой смертности. Однако снижение скорости клубочковой фильтрации (СКФ) сопровождается уменьшением эффективности упомянутых лекарств. Такой гранью является СКФ менее 30 мл/мин/м2, хотя существуют индивидуальные различия. Возможным решением вопроса индивидуализации продолжения тройной длительной диуретической терапии является определение функционального почечного резерва. Его сохранение и контроль калия крови позволяет продолжать тройную терапию. В противном случае пациенту необходимо отменять антагонист альдостерона и иНЗКТГ2, переходить с торасемида на фуросемид и готовиться к почечно-заместительной терапии.
The practical aspects of prescribing diuretic therapy in chronic kidney disease, diabetes mellitus and heart failure, both as separate nosologies and in their combination, are considered. Although these diseases have different etiologies, chronic fluid retention is a common manifestation as they progress. Since 2020, combined diuretic therapy with an aldosterone antagonist and a loop diuretic has been supplemented with sodium-glucose cotransporter-2 inhibitor for chronic kidney disease, diabetes mellitus and chronic heart failure with reduced ejection fraction. This approach demonstrates better dehydration, increased patient survival, and reduced cardiovascular mortality. However, a decrease in the glomerular filtration rate is accompanied by a decrease in the effectiveness of these agents. This border line is glomerular filtration rate less than 30 ml/min/m2, although there are individual differences. A possible solution for the individualization of the continuation of triple long-term diuretic therapy is to determine the functional renal reserve. Its maintenance and control of blood potassium allows the triple therapy to be continued. Otherwise, the patient needs to cancel an aldosterone antagonist and sodium-glucose cotransporter-2 inhibitor, switch from torasemide to furosemide and prepare for renal replacement therapy.
хронічна хвороба нирок; цукровий діабет; серцева недостатність; антагоніст альдостерону; інгібітори натрійзалежного котранспортера глюкози 2-го типу; петльові діуретики
хроническая болезнь почек; сахарный диабет; сердечная недостаточность; антагонист альдостерона; ингибиторы натрийзависимого котранспортера глюкозы 2-го типа; петлевые диуретики
chronic kidney disease; diabetes mellitus; heart failure; aldosterone antagonist; sodium-glucose cotransporter-2 inhibitors; loop diuretics
Висновки
1. Mullens W., Damman K., Harjola V.P. et al. Застосування діуретиків при застійній серцевій недостатності: офіційна заява Асоціації серцевої недостатності Європейського товариства кардіологів. Pochki. 2019. № 1. Р. 53-71. DOI: 10.22141/2307-1257.8.1.2019.157796.
2. Важливі положення для нефрологічної практики. Американська діабетична асоціація. Стандарти медичної допомоги при діабеті. Pochki. 2020. № 1. Р. 61-67. DOI: 10.22141/2307-1257.9.1.2020.196919.
3. Іванов Д. Діуретики в сучасній нефрології. Pochki. 2019. № 2. Р. 60-64. DOI: 10.22141/2307-1257.8.2.2019.166668.
4. https://www.fda.gov/news-events/press-announcements/fda-approves-new-treatment-type-heart-failure
5. Use of sodium-glucose co-transporter 2 inhibitors and risk of serious renal events: Scandinavian cohort study. BMJ. 2020. 369. DOI: https://doi.org/10.1136/bmj.m1186 (Published 29 April 2020).
6. Jardine M.J., Zhou Z., Mahaffey K.W. et al. CREDENCE Study Investigators. Renal, Cardiovascular, and Safety Outcomes of Canagliflozin by Baseline Kidney Function: A Secondary Analysis of the CREDENCE Randomized Trial. J. Am. Soc. Nephrol. 2020 May. № 31(5). Р. 1128-1139. DOI: 10.1681/ASN.2019111168.
7. https://www.medscape.com/viewarticle/929866
8. Иванов Д.Д. Маркетинговый ход: преимущества торасемида медленного высвобождения? Ліки України. 2017. № 6(212). С. 43-47.
9. Ivanov D., Savytska L., Kulachek V. The association of kidney stress test with water salt loading with estimated glomerular filtration rate decline in patients with chronic kidney disease stage 1–3. Archives of the Balkan Medical Union. Balkan Medical Union. 2019 Sept. Vol. 54. № 3. Р. 11-17.

/10.jpg)