За последние десятилетия медицина и фармакология совершили огромный прорыв в различных направлениях: многие проблемы при использовании последних достижений поддаются решению и многие болезни отступают. Однако проблема боли до сих пор остается одной из наиболее актуальных, в том числе боли в спине, которая, согласно выводам экспертов ВОЗ, по масштабам сопоставима с пандемией и является серьезной медицинской и социально-экономической проблемой.
По данным эпидемиологических исследований, проведенных в США и странах Западной Европы, распространенность боли в спине достигает 40–80 %, а ежегодная заболеваемость — 5 % [1]. Она является второй по частоте после респираторных заболеваний причиной обращения к врачам и третьей причиной госпитализации. Около 25 % взрослого населения в разных странах мира хотя бы раз в жизни отсутствовали на работе из-за боли в спине [2]. У 50 % пациентов выраженность боли в спине снижается через 1 неделю, у 40 % улучшение наступает через 8 недель, оставшиеся 7–10 % больных продолжают испытывать боль на протяжении 3 месяцев и более [3].
У 85 % пациентов боль в спине является неспеци-фической, как правило, обусловленной дегенеративно-дистрофическими заболеваниями позвоночника — остеохондрозом и остеоартрозом с последующим вовлечением в процесс связок, мышц, сухожилий и фасций. Также немаловажное значение имеет функционально обратимое блокирование межпозвоночных суставов, которое может предшествовать развитию остеохондроза и остеоартроза, возникает в уже пораженных суставах и сопровождается болью в спине [4, 5].
В терапии острой и хронической боли в спине применяются различные немедикаментозные и медикаментозные методы лечения, однако по-прежнему золотым стандартом являются нестероидные противовоспалительные препараты (НПВП), оказывающие непосредственное воздействие на патогенез боли [6].
Боль в спине: от патогенеза к патогенетической терапии
Международная ассоциация по изучению боли (IASP) определяет боль как «неприятное сенсорное и эмоциональное переживание, связанное с истинным или потенциальным повреждением ткани или описываемое в терминах такого повреждения» [7]. С точки зрения патогенеза ее возникновение происходит при активации ноцицепторов — первичных чувствительных нейронов, реагирующих на повреждающие стимулы [6, 7]. Периферические терминали ноцицепторов представлены свободными нервными окончаниями, на мембране которых идентифицированы особые белковые структуры — рецепторы, реагирующие на повреждающие механические, термические и химические раздражители. Среди химических раздражителей большое значение при активации ноцицепторов имеют алгогены: брадикинин, гистамин, серотонин, АТФ, лейкотриены, простагландины, субстанция Р, нейрокинин А. Эти вещества, связываясь с рецепторами, повышают проницаемость Са2+ и Na+ через ионные каналы, что приводит к возбуждению ноцицепторов [7].
В свою очередь, появление ноцицептивной импульсации в пораженных дисках, связках, суставах позвоночника сопровождается активацией альфа- и гамма-мотонейронов спинного мозга, вызывая спазм мышц, иннервируемых данным сегментом, что влечет за собой локальную ишемию, раздражение ноцицептивных рецепторов и, в конечном итоге, формирование порочного круга: боль — спазм мышц — боль [5].
Также ноцицептивная импульсация по спиноталамическому и спиноретикулоталамическому пути поступает в ядра таламуса, гипоталамуса, лимбическую систему, чувствительную кору, где формируется сложная системная ответная реакция. Она представлена нисходящей антиноцицептивной (антиболевой) системой, которую формируют кора, подкорковые структуры и нейротрансмиттеры нисходящей системы — моноамины, в том числе аминокислоты (глицин), катехоламины, серотонин, а также эндорфины, энкефалины, соматостатин, кальцитонин.
Согласно международным рекомендациям EULAP, NICE, при лечении острой и хронической неспецифической боли в спине препаратами первой линии являются нестероидные противовоспалительные препараты. Центральный механизм действия НПВП — блокада циклооксигеназы-2 (ЦОГ-2) и снижение синтеза простагландинов, важнейших медиаторов воспаления, что обеспечивает патогенетическое влияние этого класса анальгетиков на развитие и хронизацию боли. НПВП снижают сенситизацию периферических ноцицепторов, замедляют хемотаксис клеток воспалительного ответа, подавляют процессы ангиогенеза и гетеротопической оссификации, уменьшают синтез цитокинов, факторов роста и металлопротеиназ, препятствуют активации остеокластов. Такое многоплановое воздействие имеет особую ценность для контроля боли при хронических заболеваниях позвоночника — остеохондрозе и остеоартрите [10].
Принципиальное значение может иметь и воздействие НПВП на центральные механизмы передачи болевого импульса, так как стойкое и мощное ноцицептивное возбуждение сенсорных нейронов сопровождается гиперэкспрессией ЦОГ-2 в ЦНС. Данному механизму придается большое значение в развитии центральной сенситизации, ответственной за формирование синдрома хронической боли [14].
Выбор нестероидных противовоспалительных препаратов для лечения боли в спине: все ли НПВП одинаковы?
Все НПВП не только обладают лечебным действием, но и вызывают довольно большой спектр нежелательных явлений. Побочные эффекты при приеме НПВП во многом связаны с преимущественным торможением той или иной изоформы ЦОГ. Для традиционных неселективных НПВП, блокирующих ЦОГ-1 и ЦОГ-2, существует опасность развития патологии верхних отделов ЖКТ, характеризующейся наличием эрозий, язв и гастроинтестинальных катастроф — кровотечений и перфорации (НПВП-гастропатия). Риск появления данных осложнений у лиц, регулярно принимающих НПВП, возрастает по сравнению с популяцией более чем в 4 раза и составляет примерно 0,5–1 эпизод на 100 пациентов в год. Пациенты, регулярно принимающие НПВП, погибают от подобных осложнений в 2–3 раза чаще, чем люди, не получающие каких-либо НПВП [11, 12].
Эти данные послужили основой для разработки новых НПВП — умеренно селективных (этодолак, мелоксикам, нимесулид) и специфических, или высокоселективных (коксибы), ингибиторов ЦОГ-2. Умеренно селективные и специфические ингибиторы ЦОГ-2 оказывают незначительное влияние на образование простагландина в слизистой оболочке желудочно-кишечного тракта, поэтому при их применении риск гастроинтестинальных осложнений значительно ниже по сравнению с использованием традиционных НПВП.
В то же время и между более новыми представителями класса НПВП есть отличия по профилю безопасности. Специфические ингибиторы ЦОГ-2, селективно блокируя ЦОГ-2, способны нарушать баланс факторов, влияющих на свертывание крови, — синтез тромбоксана А2 и простациклина, что определяет протромботический эффект. У пациентов с болезнями сердечно-сосудистой системы это чревато повышением риска тромбоэмболических осложнений, таких как инфаркт миокарда и ишемический инсульт [13].
Поэтому в настоящее время считается, что умеренно селективные ингибиторы ЦОГ-2, к которым относится этодолак, характеризуются оптимальным соотношением эффективности, гастроинтестинальной и кардиоваскулярной безопасности. В отличие от высокоселективных ингибиторов фермента, они не полностью подавляют ЦОГ-2-зависимый синтез простациклинов эндотелием сосудов, показывают достаточный противовоспалительный и аналгезирующий эффект и, что немаловажно, не вызывают одновременной полной блокады ЦОГ-1 и ЦОГ-2 при применении в комбинации с ацетилсалициловой кислотой [15].
Этодолак (Этол Форт, Nobel) — рациональный выбор при лечении острой и хронической боли в спине
Этодолак (Этол Форт, Nobel) — производное пираноиндолуксусной кислоты, рацемат право- и левовращающих энантиомеров (R- и S-этодолак). Биологически активен только S-этодолак, обладающий способностью блокировать ЦОГ-2, что приводит к формированию противовоспалительного и обезболивающего эффекта. Гастропротективное действие обеспечивает R-этодолак, за счет чего препарат имеет низкую гастротоксичность. По мнению экспертов, каждый энантиомер выполняет свою индивидуальную функцию, в комплексе обеспечивая как эффективность, так и желудочно-кишечную безопасность этодолака [1].
Этодолак относится к умеренно селективным ингибиторам ЦОГ-2, таким как мелоксикам и нимесулид: соотношение ингибирующих концентраций ЦОГ-2/ЦОГ-1 для него составляет около 2 : 1 [17]. Он обладает благоприятными фармакологическими свойствами — практически 100% биодоступностью и быстрым всасыванием: Cmax достигается примерно через 1 ч после перорального приема. Период полувыведения этодолака, который почти полностью метаболизируется в печени, составляет порядка 7 ч (от 3,5 до 10 ч) [16, 18]. Этодолак используется с 1985 г. и в настоящее время является наиболее востребованным препаратом для лечения боли и воспаления во многих развитых странах мира, таких как США, Великобритания, Франция, Япония, Южная Корея [19].
Механизм действия этодолака, как и других НПВП, заключается в ингибировании синтеза простагландинов. Однако, помимо этого, этодолак влияет на продукцию и действие окислительных радикалов и других компонентов нейтрофильной активации, блокирует синтез брадикинина, что усиливает обезболивающий и противовоспалительный эффект [21]. Кроме того, важной особенностью этодолака является то, что он проникает через гематоэнцефалический барьер и выключает болевые TRPA1-рецепторы нейронов задних рогов спинного мозга, тем самым предотвращая или уменьшая центральную сенситизацию. Поэтому этодолак является полезным для лечения и острой боли, и мигрени, воспалительной боли с нейропатическим компонентом (аллодинии) и, что важно, эффективен в предотвращении хронизации болевого синдрома [47, 48].
Также большим преимуществом при использовании этодолака является отсутствие отрицательного влияния на суставной хрящ. Напротив, за счет ингибирования интерлейкина-1, -5 и фактора апоптоза хондроцитов, подавляющих активность металлопротеиназ, этодолак оказывает выраженное протективное действие в отношении суставного хряща, что особенно важно для пациентов с заболеваниями суставов, в том числе при поражении суставного аппарата позвоночника [22].
Этодолак обладает выраженным анальгетическим и противовоспалительным действием, сопоставимым с традиционными НПВП, что позволяет эффективно применять данный препарат даже в случаях, когда предшествующее использование других НПВП не давало клинического эффекта. Одним из основных преимуществ этодолака перед другими НПВП является быстрое начало аналгезии — в течение 30 минут после приема (Tmax — 60 минут) и ее продолжительность 12 ч (T1/2 — 7 ч), что приравнивается к применению некоторых внутримышечных форм НПВП. Согласно проведенным исследованиям, выраженный анальгетический эффект этодолака (30 минут) развивается значительно быстрее, чем у кетопрофена, напроксена, пироксикама (1 час) и диклофенака (2 часа) [49, 50].
Также несомненным преимуществом этодолака является минимальный риск возникновения побочных эффектов, что особенно важно при длительном назначении препарата, а также для лечения пациентов пожилого возраста и имеющих сопутствующие заболевания (артериальную гипертензию, сахарный диабет, хронические заболевания желудочно-кишечного тракта) [37].
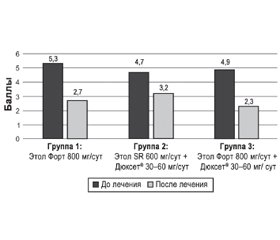
Нередко при хронической боли в спине назначаются трициклические антидепрессанты (амитриптилин) и ингибиторы обратного захвата норадреналина и серотонина (флуоксетин, дулоксетин), что связано с их влиянием на нисходящие антиноцицептивные системы (норадренергическую, серотонинергическую), функцию ионных каналов, рецепторы N-метил-D-ас-партата (NMDА). Однако недавно опубликованный метаанализ девяти крупных исследований ставит под сомнение преимущество антидепрессантов — селективных ингибиторов обратного захвата серотонина (СИОЗС) — перед плацебо в терапии хронической боли в спине [38]. Кроме того, многие исследователи подчеркивают низкую эффективность СИОЗС флуоксетина, пароксетина при хронической боли в спине [39, 40]. Из антидепрессантов имеет доказательную базу и считается эффективным в лечении хронического болевого синдрома СИОЗС дулоксетин. Профессор М.М. Орос [51] в своем исследовании показал, что для лечения болевого синдрома и предотвращения его хронизации у пациентов с подострой болью в спине целесообразно рекомендовать применение препаратов этодолака: Этол Форт в дозе 800 мг/сут в два приема или этодолак пролонгированного действия Этол SR 1 таблетка 600 мг в сутки (обезболивает 24 часа) (рис. 1), а также комбинированной терапии этодолаком с антидепрессантом дулоксетином (препарат Дюксет® по 30–60 мг/сут), особенно у пациентов с выраженными показателями тревожности (рис. 2).
/101.jpg)
При хронической боли в спине могут применяться антиконвульсанты — габапентин и прегабалин [41, 42]. Но результаты исследований их применения при неспецифической вертеброгенной боли в спине весьма неоднозначны. В исследовании McCleane у 80 больных с хронической болью в нижней части спины отмечалось недостоверное снижение числа баллов по визуальной аналоговой шкале (ВАШ) в конце курса терапии при назначении прегабалина [43]. В других работах было показано, что при болях в спине прегабалин более эффективен в комбинации с НПВП или опиоидными анальгетиками, нежели в качестве монотерапии [44–46].
При болевых синдромах в области спины и выраженном мышечном спазме с НПВП эффективно применяются миорелаксанты центрального действия, например этодолак с тиоколхикозидом (Тиозид).
Сравнительное исследование безопасности и эффективности комбинации этодолака с миорелаксантом тиоколхикозидом и комбинации этодолака с миорелаксантом толперизоном у пациентов с острой болью в пояснице и мышечно-скелетным спазмом [52] показало значительное клиническое улучшение в обеих группах пациентов: как в снятии боли, так и в снятии спазма мышц.
Профиль безопасности комбинации этодолака 400 мг 2 раза в сутки с тиоколхикозидом 8 мг в сутки был выше по сравнению с комбинацией этодолака 400 мг 2 раза в сутки с толперизоном 300 мг в сутки.
Эффективность этодолака с тиоколхикозидом была выше по сравнению с комбинацией этодолака с толперизоном.
Неблагоприятных событий в группе этодолака с тиоколхикозидом было меньше по сравнению с группой этодолака с толперизоном.
Рекомендовано использовать комбинацию этодолака с тиоколхикозидом у пациентов с острой болью в пояснице и мышечным спазмом.
Таким образом, только этодолак при неспецифической вертеброгенной боли в спине оказывает непосредственное воздействие на патогенез боли и воспаления, а его эффективность и безопасность подтверждена многочисленными клиническими исследованиями.
Доказательная база эффективности этодолака при лечении боли в спине
Имеется широкая доказательная база, подтверждающая высокую эффективность и благоприятный профиль безопасности этодолака при стоматологических, ортопедических операциях и других хирургических вмешательствах, травмах, онкологической боли, ревматических заболеваниях суставов, остеоартрозе, а также при острой и хронической неспецифической боли в спине.
В двух масштабных наблюдательных исследованиях, проведенных французскими учеными, была подтверждена эффективность и хорошая переносимость этодолака. В ходе этой работы этодолак был назначен более чем 55 000 пациентов с ревматоидным артритом, остеоартритом и спондилоартритом. Необходимая доза препарата определялась лечащими врачами в зависимости от клинической ситуации и варьировала от 200 до 600 мг/сут, длительность приема составляла до 6 недель. Существенное улучшение состояния было отмечено у 33 % больных ревматоидным артритом, 42 % — спондилоартритом и 50 % — остеоартритом. При этом общее число нежелательных реакций составило 11 %, из которых лишь 6 случаев были серьезными. Суммарно 89 % пациентов оценили переносимость этодолака как хорошую или очень хорошую [27].
Существенное снижение выраженности боли в нижней части спины при назначении этодолака было показано в работе М. Hatori и S. Kokubun [23] с участием 88 пациентов с люмбоишиалгией. Применение этодолака в течение 2 недель привело к выраженному снижению боли у 54 пациентов.
Эффективность и безопасность этодолака в дозе 800–1200 мг в сутки изучалась у пациентов с болевым синдромом, обусловленным грыжами межпозвоночных дисков поясничного отдела позвоночника. 200 пациентов принимали препарат в течение 14–21 дня. В ходе исследования было установлено, что полноценный анальгетический эффект был достигнут у 179 пациентов. Препарат действовал через 30–45 минут после приема, а эффект обезболивания сохранялся до 12 часов. Авторами была отмечена высокая анальгетическая активность этодолака, сочетающаяся с хорошим профилем безопасности, что позволило им рекомендовать препарат для купирования болевых синдромов в неврологии и нейрохирургии [25].
В исследовании Д.И. Жабасовой [26] оценивалась эффективность и безопасность лечения этодолаком боли в спине, вызванной вертеброгенными заболеваниями, сопровождающимися корешковым синдромом. Все пациенты предъявляли жалобы на боль в спине, усиливающуюся при движении, чихании, кашле, с иррадиацией в ногу. В течение 14–21 дня они получали этодолак 800–1200 мг 2 раза в день.
Результаты исследования продемонстрировали регресс болевого и рефлекторно-тонического синдрома у 65 % пациентов на 3-и — 5-е сутки, у остальных — на 7–10-е сутки применения этодолака. При этом авторы исследования отмечали не только высокую эффективность препарата, но и его хорошую переносимость.
В исследовании, проведенном М. Arriagada и R. Arinoviche [24], сравнивали эффективность и безо-пасность этодолака и пироксикама у 61 пациента с острой болью в нижней части спины. Согласно полученным данным, применение обоих НПВП в течение 7 дней позволило существенно снизить интенсивность боли, функциональных нарушений, спазма паравертебральных мышц и проблем со сном. При этом число нежелательных реакций на фоне использования этодолака было достоверно меньшим, чем при приеме пироксикама.
С.Г. Сова [21] было проведено сравнительное исследование эффективности этодолака и целекоксиба в лечении вертеброгенного пояснично-крестцового радикулита. Основную группу исследования составили 30 пациентов, которые получали лечение этодолаком по 400 мг 2 раза в сутки, а группу сравнения — 30 больных, которые принимали целекоксиб по 200 мг 2 раза в сутки. В ходе исследования пациентам проводились рентгенография позвоночника в прямой и боковой проекции и денситометрия, а также рутинные лабораторные исследования (общий анализ крови и мочи, биохимическое исследование крови, ревмопробы). Пациентов обследовали на 1, 2, 7 и 12-й дни.
В первый, второй и седьмой дни наблюдения пациенты основной и контрольной группы оценивали интенсивность боли и ее динамику по визуально-аналоговой шкале одинаково. На 12-й день исследования пациенты основной группы оценивали интенсивность болевых ощущений значительно ниже, чем больные группы сравнения (р < 0,05).
Побочные эффекты наблюдались у пяти пациентов основной группы (16,7 %) и у четырех больных из группы сравнения (13,3 %). Таким образом, в данном исследовании этодолак в дозе 800 мг/сут по количеству побочных реакций практически не уступал высокоселективному ингибитору ЦОГ-2 целекоксибу в дозе 400 мг/сут, а по выраженности и длительности анальгетического эффекта достоверно превосходил его.
В исследовании В.В. Поворознюка и соавт. [28], проведенном в отделении возрастных изменений опорно-двигательного аппарата ГУ «Институт геронтологии им. Д.Ф. Чеботарева НАМН Украины», было обследовано и пролечено 26 пациентов в возрасте от 45 до 75 лет с болью в нижней части спины на фоне остеохондроза пояснично-крестцового отдела позвоночника в стадии обострения. Пациентов методом простой рандомизации разделили на две группы по 13 человек: основную и сравнения. В составе комплексного лечения пациенты основной группы принимали этодолак (Этол Форт, Nobel) в дозе 400 мг per os дважды в сутки в течение 14 дней, пациенты группы сравнения — диклофенак в дозе 75 мг per os дважды в сутки в течение 14 дней.
Результаты исследования показали, что прием этодолака способствует достоверному уменьшению степени выраженности вертебрального болевого синдрома, улучшению функциональной и повседневной активности, качества жизни пациентов уже на 7-е сутки лечения, что подтверждено результатами анализа показателей опросников Мак-Гилла, Роланда — Морриса, Освестри, Euro-Qol5D, 4-составной ВАШ. При этом количество и степень выраженности побочных эффектов в обеих группах не отличались от описанных в литературе.
В работе Г.М. Авдей и соавт. [29] приняли участие 44 пациента с вертеброгенными болями в спине, 30 из которых получали этодолак по 400 мг 2 р/день и 10 — кеторолак 0,01 г 2 р/день. Курс лечения составил 7 дней. Была установлена высокая анальгетическая эффективность этодолака, сопровождающаяся улучшением жизнедеятельности пациентов, изменением болевого поведения, уменьшением тревожности и депрессии, превосходящая по этим параметрам группу контроля.
Для эффективного и безопасного лечения хронической боли в спине препарат Этол Форт (этодолак) применяется в стандартной дозе 400 мг 2 раза в сутки после еды. При остром воспалении и боли Этол Форт назначают в дозе 400 мг 3 раза в сутки. Максимальная суточная доза составляет 1200 мг. Для больных с массой тела менее 60 кг суточная доза препарата составляет 20 мг/кг [21]. Вызывает интерес пролонгированная форма этодолака. Этодолак SR (Этол SR) не только обезболивает в течение 24 часов, его применение позволяет избежать побочных эффектов, связанных с высокой концентрацией. Он имеет улучшенный профиль безопасности для ЖКТ и большую противовоспалительную эффективность при хронических воспалительных состояниях, способствует соблюдению пациентом режима противовоспалительной активности и обеспечивает больший успех терапии хронической боли у пациентов с ревматоидным артритом, остеоартритом, другими хроническими воспалительными процессами в суставах и позвоночнике [53].
Этодолак: доказанная гастроинтестинальная, кардиоваскулярная и почечная безопасность
Одним из важнейших достоинств этодолака является низкий риск осложнений со стороны ЖКТ. Это подтверждает метаанализ 29 рандомизированных клинических исследований (РКИ), проведенный Y. Chen и соавт. [30]. Суммарный риск серьезных осложнений со стороны ЖКТ при использовании этодолака был в 3 раза ниже, чем на фоне приема неселективных НПВП, и в 2 раза меньше была частота развития эндоскопических язв.
Низкая частота развития НПВП-гастропатии при использовании этодолака подтверждена в серии эндоскопических исследований. Так, L. Laine и соавт. [31] сравнили действие плацебо, этодолака 800 мг/сут и напроксена 1000 мг/сут на слизистую оболочку желудка у 52 здоровых добровольцев, принимавших эти препараты в течение 4 недель. Общая площадь эрозий слизистой оболочки желудка на момент окончания исследования в группе этодолака была сопоставима с группой плацебо и гораздо меньше, чем в группе напроксена.
Большой интерес представляет исследование кишечной кровопотери, связанной с приемом этодолака. Р. Leese [32] сравнил кровопотерю из органов ЖКТ (с помощью эритроцитов, меченных 51Cr) у 30 здоровых добровольцев, использовавших это лекарство в дозах 600 и 1200 мг/сут и напроксен 1000 мг/сут. Через 21 день приема НПВП объем кровопотери был достоверно меньше в группах добровольцев, получавших разные дозы этодолака, чем в группе напроксена: 0,38; 0,45 и 1,2 мл/сут соответственно.
Частота кардиоваскулярных осложнений при использовании этодолака оценивалась в метаанализе, включающем 25 популяционных исследований кардиоваскулярных осложнений, связанных с НПВП (18 независимых популяций). Было установлено, что риск развития данной патологии для этодолака находится на умеренном уровне — 1,55 [44].
Влияние этодолака на функцию почек оценивалось в ходе серии РКИ при остеоартрите и ревматоидном артрите (n = 2629). Было показано, что этот препарат не вызывает ренальных осложнений у лиц без исходной патологии почек и не способствует прогрессированию умеренной и слабовыраженной почечной недостаточности [34]. Отсутствие значимого негативного действия этодолака (в том числе в высоких дозах) на функцию почек при сроке приема от 4 до 14 дней было показано в двух исследованиях, проведенных в группах здоровых добровольцев [35, 36].
Выводы
Боль в спине — широко распространенная в мире проблема. У 85 % пациентов боль в спине является неспецифической, как правило, обусловленной дегенеративно-дистрофическими заболеваниями позвоночника — остеохондрозом и остеоартрозом с последующим вовлечением в процесс связок, мышц, сухожилий и фасций.
В терапии острой и хронической неспецифической боли в спине препаратами первой линии являются НПВП, что регламентируется международными руководствами EULAP, NICE. У пациентов с высоким риском нежелательных явлений со стороны ЖКТ и сердечно-сосудистой системы (ССС) предпочтительнее рекомендовать умеренно селективные НПВП.
Этодолак (Этол Форт, Этол SR) — умеренно селективный, сбалансированный по соотношению эффективности, удобства применения и безопасности препарат группы НПВП. В пользу этодолака говорят длительная серия масштабных клинических испытаний и большой опыт применения этого лекарственного средства в реальной клинической практике многих развитых стран мира. Важным преимуществом этодолака (Этол Форт, Этол SR) является быстрый обезболивающий эффект и низкий риск нежелательных реакций со стороны ССС и ЖКТ (низкий риск как диспепсий, так и потенциально опасных осложнений, таких как язвы и кровотечения). Основной точкой приложения этодолака (Этол Форт) следует считать контроль боли при острых болях и этодолака пролонгированного действия (Этол SR) — при хронических болях в спине.
Список литературы
1. Пизова Н.В. Боль в спине: что мы знаем и что должны знать? https://www.spinabezboli.ru/bol_v_spine_chto_doljni_znat.
2. Поворознюк В.В. Боль в нижней части спины: современный взгляд на проблему. Здоровье Украины. 2015. № 3.
3. Попелянский Я.Ю., Штульман Д.Р. Болезни нервной системы. М.: Медицина, 2001. С. 293-316.
4. Морозова О.Г. Современные подходы к лечению боли в спине. http://www.medicus.ru/manualtherapy/patient/sovremennye-podhody-k-lecheniyu-boli-v-spine-28055.phtml.
5. Баринов А.Н. Сегментарные механизмы формирования мышечного спазма, спастичности и хронизации боли. Врач. 2012. № 5.
6. Курушина О.В., Барулин А.Е. Современные аспекты лечения болей в спине. РМЖ. 2012. № 10. С. 528.
7. Кукушкин М.Л. Боль в спине: мишени для патогенетической терапии. РМЖ. 2011. № 30. С. 1862.
8. Насонов Е.Л. Нестероидные противовоспалительные препараты (перспективы применения в медицине). М.: Анко, 2000.
9. Каратеев А.Е., Яхно Н.Н., Лазебник Л.Б. и др. Применение нестероидных противовоспалительных препаратов: клинические рекомендации. М.: ИМА-ПРЕСС, 2009.
10. Ali A., Arif A.W., Bhan C. et al. Managing Chronic Pain in the Elderly: An Overview of the Recent Therapeutic Advancements. Cureus. 2018. Sep 13. 10 (9).
11. Каратеев А.Е., Насонова В.А. Развитие и рецидивирование язв желудка и двенадцатиперстной кишки у больных, принимающих нестероидные противовоспалительные препараты: влияние стандартных факторов риска. Тер. арх. 2008. № 5. С. 62-66.
12. Насонов Е.Л., Лазебник Л.Б., Беленков Ю.Н. и др. Применение нестероидных противовоспалительных препаратов: клинические рекомендации. М.: Алмаз, 2006.
13. Johnson A., Nguyen T., Day R. Do nonsteroidal anti-inflammatory drugs affect blood pressure? A meta-analysis. Ann. Intern. Med. 1994. Vol. 121. P. 289-300.
14. Ho P.M., Maddox T.M., Wang L. et al. Risk of adverse outcomes associated with concomitant use of clopidogrel and proton pump inhibitors following acute coronary syndrome. JAMA. 2009 Mar 4. Vol. 301 (9). 937-944.
15. Сулик Р.В. Купирование хронического болевого синдрома у пациентов с заболеваниями опорно-двигательного аппарата. Український медичний часопис. 2012. № 6 (92). XI/XI.
16. Balfour J.A., Buckley M.M. Etodolac. A reappraisal of its pharmacology and therapeutic use in rheumatic diseases and pain states. Drugs. 1991 Aug. 42 (2). 274-99.
17. Warner T.D., Giuliano F., Vojnovic I. et al. Nonsteroid drug selectivities for cyclo-oxygenase-1 rather than cyclo-oxygenase-2 are associated with human gastrointestinal toxicity: a full in vitro analysis. Proc. Natl. Acad. Sci USA. 1999 Jun 22. 96 (13). 7563-8.
18. Brocks D.R., Jamali F. Etodolac clinical pharmacokinetics. Clin. Pharmacokinet. 1994 Apr. 26 (4). 259-74.
19. Tirunagari S.K., Derry S., Moore R.A., McQuay H.J. Single dose oral etodolac for acute postoperative pain in adults. Cochrane Database Syst. Rev. 2009 Jul 8. CD007357. doi: 10.1002/14651858.CD007357.pub2.
20. Inoue N., Nogawa M., Ito S. et al. Nonsteroidal anti-inflammatory drugs: «Etodolac» — an old drug, new possibilities». Biol. Pharm. Bull. 2011. Vol. 34 (5). P. 655-659.
21. Сова С.Г. Эффективность и безопасность этодолака в лечении вертеброгенных болевых синдромов. Здоровье Украины. Неврология. 2012. № 2.
22. Каратеев А.Е. Этодолак: хорошо известен и активно используется в разных странах мира. Пора бы и нам? Научно-практическая ревматология. 2019. 57 (4). 468-473.
23. Hatori M., Kokubun S. Clinical use of etodolac for the treatment of lumbar disc herniation. Curr. Med. Res. Opin. 1999. 15 (3). 193-201. doi: 10.1185/03007999909114091.
24. Arriagada M., Arinoviche R. Etodolac versus piroxicam in the treatment of acute lumbago. Double-blind study. Rev. Med. Chil. 1992 Jan. 120 (1). 54-8.
25. Ирысов К.Б. Этодин-форте в лечении больных с грыжами поясничных межпозвонковых дисков. https://www.medcentre.com.ua/articles/Effektivnost-etodina-fort-v-25173.
26. Жабасова Д.И. Применение препарата Этодин Форт в неврологической практике амбулаторных больных. Медицина. 2012. № 2.
27. Benhamou C.L. Large-scale open trials with etodolac (Lodine) in France: an assessment of safety. Rheumatol. Int. 1990. 10 Suppl. 29-34. doi: 10.1007/BF02274753.
28. Поворознюк В.В., Орлик Т.В., Крочак С.П., Парахіна Т.В. Оцінка ефективності та безпечності етодолаку в лікуванні болю у нижній частині спини. Ортопедия, травматология и протезирование. 2013. № 3 (592). С. 55-60.
29. Авдей Г.М., Кулеш С.Д., Шумскас М.С. и др. Эффективность препарата Этодин Форт у пациентов с вертеброгенным болевым синдромом. Неврология и нейрохирургия. Восточная Европа. 2012. № 1 (13).
30. Chen Y.F., Jobanputra P., Barton P. et al. Cyclooxygenase-2 selective non-steroidal anti-inflammatory drugs (etodolac, meloxicam, celecoxib, rofecoxib, etoricoxib, valdecoxib and lumiracoxib) for osteoarthritis and rheumatoid arthritis: a systematic review and economic evaluation. Health Technol. Assess. 2008 Apr. 12 (11). 1-278.
31. Laine L., Sloane R., Ferretti M., Cominelli F. A randomized double-blind comparison of placebo, etodolac, and naproxen on gastrointestinal injury and prostaglandin production. Gastrointest. Endosc. 1995 Nov. 42 (5). 428-33.
32. Leese P. Comparison of the effects of etodolac SR and napro-xen on gastro-intestinal blood loss. Curr. Med. Res. Opin. 1992. 13 (1). 13-20.
33. Varas-Lorenzo C., Riera-Guardia N., Calingaert B. et al. Myocardial infarction and individual nonsteroidal anti-inflammatory drugs meta-analysis of observational studies. Pharmacoepidemiol. Drug Saf. 2013 Jun. 22 (6). 559-70.
34. Brater D.C. Evaluation of etodolac in subjects with renal impairment. Eur. J. Rheumatol. Inflamm. 1990. 10 (1). 44-55.
35. Svendsen K.B., Bech J.N., Sоrensen T.B., Pedersen E.B. A comparison of the effects of etodolac and ibuprofen on renal haemodynamics, tubular function, renin, vasopressin and urinary excretion of albumin and alpha-glutathione-S-transferase in healthy subjects: a placebo-controlled cross-over study. Eur. J. Clin. Pharmacol. 2000 Aug. 56 (5). 383-8.
36. Brater D.C., Brown-Cartwright D., Anderson S.A., Uaamnuichai M. Effect of high-dose etodolac on renal function. Clin. Pharmacol. Ther. 1987 Sep. 42 (3). 283-9.
37. Сорока Н.Ф. Этодолак (Этодин Форт) — проверенный временем и клинической практикой нестероидный противовоспалительный препарат. https://cyberleninka.ru/article/n/etodolak-etodin-fort-proverennyy-vremenem-i-klinicheskoy-praktikoy-nesteroidnyy-protivovospalitelnyy-preparat.
38. Urquhart D.M., Hoving J.L., Assendelft W.W. et al. Antidepressants for nonspecific low back pain. Cochrane Database Syst. Rev. 2008. CD001703. Р. 2.
39. Dickens C., Jayson M., Sutton С. et al. The relationship between pain and depression in a trial using paroxetine in sufferers of chronic low back pain. Psychosomatics. 2000. 41. 490-9.
40. McQuay H.J. et al. A systematic review of antidepressants in neuropathic pain. Pain. 1996. 68. 217-27.
41. Dworkin R.H., О’Connor A.B., Backonja M. et al. Pharmacologic management of neuropathic pain: evidence-based recommen- dations. Pain. 2007. 132. 23. 7-51.
42. Hansson P., Fields H., Hill R., Marchettini P. Neuropathic Pain: Pathophysiology and Treatment, Progress in Pain Research and Management. Seattle, WA: IASP Press, 2002. 21. 151-67.
43. McCleane G.J. Does Gabapentin have an analgesis effect on background movement and refferedpain?A randomized, double-blind, placebo-controlled study. Pain Clinic. 2001. 13. 103-7.
44. Gatti A., Sabato A.F., Occhioni R. et al. Controlled-release oxycodone andpregabalin in the treatment of neuropathic pain: resultsofa multicenter Italian study. Eur. Neurol. 2009. 61. 129-37.
45. Romano C.L., Romano D., Bonora C., Mineo G. Pregabalin, cele-coxib, and their combination for treatment of chronic low-back pain. J. Orthop. Traumatol. 2009. 10 (4). 185-91. Epub. 2009, 18.
46. Pota V., Maisto M., Pace M.C. et al. Association ofbuprenorphine TDS and pregabalin in the treatment of low back pain. Eur. Pain. 2007. 11. S83.
47. Nassini R., Materazzi S., Benemei S., Geppetti P. The TRPA1 channel in inflammatory and neuropathic pain and migraine. Rev. Physiol. Biochem. Pharmacol. 2014. 167. 1-43.
48. Inoue N., Ito S., Nogawa M., Tajima K., Kyoi T. Etodolac blocks the allyl isothiocyanate-induced response in mouse sensory neurons by selective TRPA1 activation. Pharmacology. 2012. 90 (1–2). 47-54.
49. Castellsague J., Riera-Guardia N., Calingaert B. Individual NSAIDs and upper gastrointestinal complications: a systematic review and meta-analysis of observational studies (the SOS project). Drug Saf. 2012. № 35 (12). P. 1127-1146.
50. Baumert P.W. Acute inflammation after injury. Quick control speeds rehabilitation. Postgrad. Med. 1995. 97 (2). 35-42.
51. Орос М.М., Сабовчик А.Я., Грабар В.В., Яцинин Р.Ю. Підгострий біль у спині: підходи до медикаментозного лікування як профілактика хронізації болю. Міжнародний неврологічний журнал. 2019. № 5 (107).
52. Tanu Garg, Vijay K. Yadav. Сравнительное исследование безопасности и эффективности этодолака с тиоколхикозидом и толперизона с этодолаком у пациентов с острой болью в пояснице и с мышечно-скелетным спазмом. International Journal of Basic & Clinical Pharmacology. 2003.
53. Бисваджит Рухидас, Раджат Рэй, Дебджоти Наскар, Биплаб Кумар Чакра, Кумар Чаттерджи. Фармакологические и токсикологические исследования микросфер гумми-катира, нагруженных этодолаком, полученных методом испарения эмульсионного растворителя W1/O/W2 у крыс. Braz. J. Pharm. Sci. 2017. № 4. Vol. 53.
/101.jpg)