Журнал «Практическая онкология» Том 3, №2, 2020
Вернуться к номеру
Ризик-менеджмент венозного тромбоемболізму в онкохірургії: практичні рішення для клінічної роботи
Авторы: Тлустова Т.В.
Рубрики: Онкология
Разделы: Справочник специалиста
Версия для печати
8 вересня 2020 року відбувся онлайн-вебінар «Ризик-менеджмент венозного тромбоемболізму в онкохірургії: практичні рішення для клінічної роботи», який провели Сергій Олександрович Дубров, д.м.н., професор, президент Асоціації анестезіологів України, і Богдан Олегович Матвійчук, д.м.н., професор, завідувач кафедри хірургії ФПДО Львівського національного медичного університету. Спікери висвітлили питання венозного тромбоемболізму (ВТЕ) в різних популяціях хірургічних пацієнтів, особливо приділивши увагу онкохірургічним пацієнтам. Були обговорені різні групи ризиків ВТЕ та геморагічних ускладнень. Наведені практичні приклади застосування наявних на сьогодні рекомендацій щодо зменшення ризиків ВТЕ в онкохірургічних пацієнтів.
Актуальність проблеми венозного тромбоемболізму в різних популяціях пацієнтів хірургічного профілю
Венозний тромбоемболізм — більш реальна загроза, ніж ми собі уявляємо. Згідно зі статистичними даними:
— ВТЕ — це 1 з 4 смертей, пов’язаних з тромбозом;
— ВТЕ — це одна з найголовніших причин смерті в лікарні, розвитку якої можна запобігти;
— 60 % усіх випадків ВТЕ трапляються під час або після госпіталізації.
З усіх випадків ВТЕ близько 20 % випадків зустрічаються в онкологічних пацієнтів. ВТЕ посідає друге місце серед причин летальності хворих з онкологічною патологією після прогресування безпосередньо онкологічного процесу. Розвиток ВТЕ у хворих із пухлинами збільшує ризик їх смерті у 2–6 разів. Незважаючи на те, що у світовій літературі можна знайти близько 30 консенсусних документів з ВТЕ в онкології, дослідження вказують на те, що практична їх реалізація є недостатньою (особливо в стаціонарних хворих).
Щорічна захворюваність на ВТЕ у пацієнтів з онкопатологією становить приблизно 1/250. З усіх онкологічних пацієнтів 15 % мають симптоматичний ВТЕ, у 50 % знаходять ВТЕ при автопсії. Порівняно з пацієнтами без раку онкологічні пацієнти мають вищий ризик першого та повторного ВТЕ, вищий ризик кровотечі при застосуванні антикоагулянтів і вищий ризик смерті.
Найбільшу частоту ВТЕ при різних онкологічних захворюваннях спостерігають при солідних пухлинах (47 %), нирковій карциномі (43 %), гліомі високого ступеня (26 %), множинній мієломі (28 %) тощо.
Фактори ризику ВТЕ у хірургічних пацієнтів можна поділити:
— на пов’язані з хірургічним втручанням;
— пов’язані з особливостями пацієнта.
До факторів ВТЕ, пов’язаних із хірургічним втручанням, належать: обсяг і тривалість хірургічного втручання, інтраопераційне положення на операційному столі, тип анестезії, післяопераційна іммобілізація.
Операції високого ризику:
— великі хірургічні втручання — операції тривалістю понад 45 хвилин;
— операції на черевній або грудній порожнині (наприклад, великі абдомінальні/тазові втручання або хірургічні операції з приводу раку);
— операції тривалістю ≥ 2 години;
— ургентна операція або планова операція (ризик під час ургентної операції вищий, ніж при плановій);
— післяопераційна іммобілізація протягом ≥ 4 днів, а також критичний стан пацієнта, якій перебуває на постільному режимі (наприклад, великі опіки, політравми, ураження мозку або хребта).
Операції низького ризику: незначні амбулаторні втручання (наприклад, планове лікування грижі, хірургія щитоподібної залози, незначне видалення шкіри, каротидна ендартеректомія).
Фактори ризику ВТЕ у загальній хірургії
Високий ризик ВТЕ:
— велика загальна хірургічна операція, вік пацієнта понад 60 років;
— велика загальна хірургічна операція, вік пацієнта 40–60 років, ВТЕ в анамнезі або інші фактори ризику (наприклад, тромбофілія).
Середній ризик ВТЕ:
— велика загальна хірургічна операція, вік пацієнта 40–60 років;
— мала загальна хірургічна операція, вік пацієнта понад 60 років;
— мала загальна хірургічна операція, вік пацієнта 40–60 років, ВТЕ в анамнезі або інші фактори ризику (наприклад, тромбофілія).
Низький ризик ВТЕ:
— мала загальна хірургічна операція, вік пацієнта 40–60 років;
— велика хірургічна операція, вік пацієнта менше за 40 років.
До факторів ризику ВТЕ, які пов’язані із особливостями пацієнта, належать:
— вік понад 60 років;
— ожиріння;
— анамнез ВТЕ;
— злоякісне захворювання;
— вагітність;
— замісна терапія естрогенами;
— запальне захворювання кишки;
— спадкові тромбофілічні стани.
Найбільш вагомим фактором з усіх наведених є вік понад 60 років. У госпіталізованих пацієнтів частота ТЕЛА збільшується з віком і втричі перевищує цей показник у загальній популяції.
Збільшення індексу маси тіла (ІМТ) вище від нормального значення пов’язане з підвищенням ризику розвитку ВТЕ. За даними дослідження NHS, відносний ризик розвитку неспровокованої ТЕЛА, не пов’язаний з попереднім хірургічним втручанням, травмою або раком, збільшується приблизно на 8 % на кожні 1 кг/м2 індексу маси тіла й наближається до майже 6-кратного (р < 0,001) збільшення в осіб з індексом маси тіла понад 35 кг/м2.
Фактори ризику ВТЕ в онкологічних пацієнтів можна розподілити на 4 групи:
1) фактори ризику, пов’язані з онкологічним захворюванням;
2) фактори ризику, пов’язані з проведенням лікування онкологічного захворювання;
3) фактори ризику, які залежать від пацієнта;
4) інші фактори.
Фактори ризику ВТЕ, пов’язані з онкологічним захворюванням:
— локалізація пухлини;
— гістологічний тип пухлини;
— стадія пухлини;
— ступінь злоякісності;
— початковий період після діагностики.
Фактори ризику ВТЕ, пов’язані з лікуванням:
— хірургічне лікування;
— променева терапія;
— хіміотерапія;
— антиангіогенні препарати;
— імуномодулюючі препарати;
— гормональна терапія;
— стимулятори еритропоезу;
— гемотрансфузія;
— катетеризація центральної судини.
Фактори ризику ВТЕ, які залежать від пацієнта:
— вік;
— вага, індекс маси тіла;
— рухливість;
— супутні захворювання;
— прихильність щодо профілактичних заходів.
Інші фактори ризику:
— кількість лейкоцитів;
— кількість тромбоцитів;
— анемія;
— тромбофілія.
Найбільш ґрунтовно предиктори розвитку тромбозу описані в тріаді Virchow — патофізіологічні стани, що сприяють розвитку ВТЕ: гіперкоагуляція, пошкодження ендотелію судин, венозний стаз.
Особливості тріади Virchow у хворих на онкологічні захворювання:
— пошкодження ендотелію судин: хірургічна операція/травма, хіміотерапія, променева терапія, постійний катетер, погане харчування, тютюнопаління;
— гіперкоагуляція: злоякісна пухлина/макрофаги, клітини запалення/білки й прокоагулянти, ангіогенез, хіміотерапія;
— венозний стаз: вік, малорухливий спосіб життя, ожиріння, хронічна недостатність функції серця, печінки, нирок, венозна недостатність/компресія, лімфедема.
Практична оцінка тромботичного ризику в хірургічних пацієнтів
У всіх пацієнтів під час госпіталізації або у пацієнтів, які вже проходять стаціонарне лікування, необхідно індивідуально оцінювати ризики розвитку венозного тромбоемболізму й кровотечі. Для оцінки ризику ВТЕ в хірургії використовується шкала Caprini — валідна шкала оцінки ризику розвитку ВТЕ-ускладнень у пацієнтів хірургічного профілю. Шкала Caprini легка в користуванні й доступна для об’єктивної оцінки ризику ВТЕ.
Фактори розвитку великих геморагічних ускладнень
Перша група — загальні фактори ризику розвитку великих геморагічних ускладнень:
— активна кровотеча;
— велика кровотеча в анамнезі;
— відомі неліковані порушення гемостазу;
— тяжка ниркова або печінкова недостатність;
— тромбоцитопенія;
— гострий інсульт;
— неконтрольована системна гіпертензія;
— люмбальна пункція або спінальна анестезія протягом попередніх 4 годин або наступних після процедури 12 годин;
— супутнє застосування антикоагулянтів, антитромбоцитарних препаратів або тромболітичних засобів.
Друга група — фактори ризику розвитку великих геморагічних ускладнень, пов’язані зі характером оперативного втручання:
— абдомінальна хірургія: чоловіча стать, рівень гемоглобіну < 130 г/л у періопераційному періоді, малігнізація, комплексна хірургія ≥ 2 процедури, тяжка резекція або понад один анастомоз;
— панкреатодуоденектомія: сепсис, неспроможність анастомозу в ділянці підшлункової залози, кровотеча;
— резекція печінки: кількість сегментів, супутня резекція позапечінкових органів, первинна злоякісна пухлина печінки, низький рівень гемоглобіну перед операцією і тромбоцитів;
— кардіальна хірургія: застосування аспірину, застосування клопідогрелю протягом 3 днів перед операцією, ІМТ понад 25 кг/м2, незапланована хірургія, накладання 5 або більше шунтів, похилий вік, ниркова недостатність, хірургічне втручання, за винятком аортокоронарного шунтування;
— торакальна хірургія: пневмонектомія або розширена резекція;
— втручання, що можуть мати особливо тяжкі наслідки геморагічних ускладнень: краніотомія, спінальна травма, реконструктивні процедури вільним клаптем.
Згідно із отриманими результатами метааналізу рандомізованих досліджень у загальній хірургії, які порівнюють низькомолекулярні гепарини (НМГ) із плацебо або нефракціонованим гепарином (НФГ), встановлено, що частота розвитку ВТЕ частіше спостерігається в онкологічних пацієнтів, ніж у неонкологічній хірургії: 1,2 % проти 1,8 % відповідно. Крім того, в онкологічній хірургії встановлений значно вищий ризик великих кровотеч — у 4 рази більший, ніж у неонкологічній хірургії.
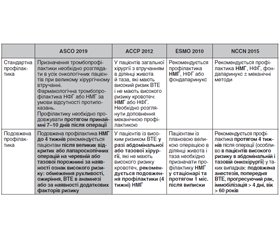
Огляд сучасних клінічних рекомендацій з профілактики ВТЕ в онкологічних пацієнтів
У 2019 році опубліковані міжнародні клінічні протоколи з лікування й профілактики ВТЕ в пацієнтів із раком Консультативної групи Міжнародної ініціативи з питань тромбозу та раку (ITAC).
Профілактика ВТЕ в пацієнтів з онкологічними захворюваннями при хірургічному втручанні:
1. Рекомендовано застосування НМГ один раз на добу (якщо кліренс креатиніну становить ≥ 30 мл/хв) або НФГ у низьких дозах тричі на добу для запобігання післяопераційному ВТЕ в пацієнтів з онкологічними захворюваннями. Фармакопрофілактику слід розпочинати за 2–12 год перед операцією і продовжувати щонайменше протягом 7–10 днів. Відсутні дані, що дозволяють зробити висновки стосовно переваг одного типу НМГ над іншим.
2. Існує недостатньо даних на підтримку фондапаринуксу як альтернативи НМГ для профілактики післяопераційного ВТЕ у пацієнтів з онкологічними захворюваннями.
3. Рекомендується застосування найвищої профілактичної дози НМГ для запобігання післяопераційному ВТЕ в пацієнтів з онкологічними захворюваннями.
4. Подовжена профілактика (4 тижні) НМГ для запобігання післяопераційному ВТЕ після великої лапаротомії в пацієнтів з онкологічними захворюваннями показана пацієнтам із високим ризиком розвитку ВТЕ і низьким ризиком виникнення кровотечі.
5. Подовжена профілактика (4 тижні) НМГ для запобігання ВТЕ у пацієнтів з онкологічними захворюваннями, яким проводиться лапароскопія, рекомендована так само, як і при лапаротомії.
6. Механічні методи не рекомендовані як монотерапія, за винятком ситуацій, коли фармакологічні методи протипоказані.
7. Фільтри нижньої порожнистої вени не рекомендовані для рутинної профілактики.
Профілактика й лікування венозного тромбоемболізму в пацієнтів з раком: оновлення клінічних практичних рекомендацій Американського товариства клінічної онкології:
1. Госпіталізованим пацієнтам, які мають активне злоякісне новоутворення та гостре захворювання або знижену рухливість, слід запропонувати фармакологічну тромбопрофілактику за відсутності кровотечі або інших протипоказань.
2. Госпіталізованим пацієнтам, які мають активне злоякісне новоутворення без додаткових факторів ризику, може бути запропонована фармакологічна тромбопрофілактика за відсутності кровотечі або інших протипоказань Активним вважається рак, діагностований протягом попередніх 6 місяців; рецидивуючий, місцево-поширений або метастатичний рак; рак, лікування якого відбувається протягом 6 місяців; рак крові в стадії неповної ремісії.
3. Рутинну фармакологічну тромбопрофілактику не слід пропонувати пацієнтам, які госпіталізовані виключно для проведення незначних процедур або інфузії хіміотерапії, а також пацієнтам, які підлягають трансплантації стовбурових клітин/кісткового мозку.
4. Усім пацієнтам із злоякісним захворюванням при великому хірургічному втручанні слід запропонувати фармакологічну тромбопрофілактику або з НФГ, або з НМГ за відсутності протипоказань через активну кровотечу, високий ризик кровотечі тощо.
5. Профілактику слід починати передопераційно.
6. Механічні методи можна застосовувати на додаток до фармакологічної тромбопрофілактики, але не слід застосовувати як монотерапію для профілактики ВТЕ, за винятком випадку, коли фармакологічні методи протипоказані через активну кровотечу або високий ризик кровотечі.
7. Комбіноване застосування фармакологічної і механічної профілактики може підвищити ефективність, особливо в пацієнтів з дуже високим ризиком.
8. Фармакологічну тромбопрофілактику в пацієнтів, які підлягають великому хірургічному втручанню з приводу раку, слід продовжувати щонайменше від 7 до 10 днів. Подовжена профілактика НМГ до 4 тижнів після операції рекомендується пацієнтам, які перенесли велику відкриту або лапароскопічну операцію на черевній або тазовій порожнині з приводу раку, які мають ознаки високого ризику, такі як обмежена рухливість, ожиріння, анамнез ВТЕ, або додаткові фактори ризику. В умовах хірургічних втручань з низьким ризиком рішення щодо відповідної тривалості тромбопрофілактики слід приймати індивідуально в кожному конкретному випадку.
9. Застосування антикоагулянтів не рекомендується для покращання виживання пацієнтів з раком без ВТЕ.
Були розглянуті 2 клінічні випадки з точки зору ризик-менеджменту ВТЕ в онкохірургії
Перший клінічний випадок. Хвора віком 58 років, вага — 71 кг, зріст — 168 см, ІМТ — 25,4, була госпіталізована планово з раком низхідної ободової кишки (аденокарцинома помірного ступеня диференціації). Пацієнтка перенесла правобічну геміколектомію з приводу раку сліпої кишки у 2001 році. Має супутнє захворювання — В-клітинну хронічну лімфолейкемію. За даними комп’ютерної томографії: пухлина низхідної ободової кишки Т4N2M0. Лабораторні показники: лейкоцити крові — 30 • 109/л, гемоглобін — 95 г/л. Пацієнтці планується лівобічна геміколектомія, D3-лімфодисекція.
За шкалою Caprini ризик ВТЕ визначено як високий.
Ризик розвитку геморагічних ускладнень у даному випадку низький.
Стратегія профілактики ВТЕ — фармакопрофілактика й рання мобілізація пацієнтки.
Режим фармакологічної профілактики — еноксапарин 40 мг підшкірно за 12 годин до операції і наступне введення через 12 годин після операції, надалі — кожні 12 годин.
У цієї пацієнтки були показання до подовженої профілактики венозного тромбоемболізму протягом 4 тижнів.
Другий клінічний випадок. Пацієнтка віком 52 роки, вага 120 кг (ІМТ 40 кг/м2), якій планується проведення лапароскопічної гістеректомії з приводу великої фіброміоми матки. Орієнтовна тривалість операції понад 1 год. Додатково встановлено: на нижніх кінцівках — варикозно розширені підшкірні вени, в анамнезі — супутній цукровий діабет, приймає метформін.
За шкалою Caprini ризик визначено як високий.
Ризик розвитку геморагічних ускладнень у даному випадку низький.
Стратегія профілактики ВТЕ — фармакопрофілактика.
Режим фармакологічної профілактики з урахуванням ваги пацієнтки — еноксапарин 40 мг 2 рази на добу, тобто кожні 12 годин.
Тривалість медикаментозної профілактики в даному випадку — 10–15 діб після виписки зі стаціонару.
Отже, доза і тривалість профілактичного лікування повинні відповідати ступеню ризику ВТЕ в кожного конкретного пацієнта для належного запобігання розвитку післяопераційних ВТЕ-ускладнень як на етапі госпітального лікування, так і після виписки із стаціонару. Рутинна профілактика знижує захворюваність, смертність і витрати на медичне обслуговування в госпіталізованих пацієнтів із ризиком розвитку тромбозу глибоких вен і ТЕЛА.

/30.jpg)