Газета «Новости медицины и фармации» №13 (734), 2020
Вернуться к номеру
Ревматическая полимиалгия: объединяя усилия европейских ревматологических обществ
Авторы: Пузанова О.Г.(1), Мошковская Ю.О.(2), Соболь В.О.2
(1) — Киевский медицинский университет, г. Киев, Украина
(2) — Национальный медицинский университет имени А.А. Богомольца, г. Киев, Украина
Рубрики: Ревматология
Разделы: Справочник специалиста
Версия для печати
Введение
Постарение популяции диктует необходимость усиления доказательной базы специфических гериатрических синдромов, ревматических заболеваний (РЗ) с поздним дебютом и РЗ пожилого возраста. Особого внимания международного сообщества ревматологов, интернистов, врачей общей практики заслуживает ревматическая полимиалгия (РП) — второе по распространенности после ревматоидного артрита воспалительное РЗ, развивающееся почти исключительно в возрасте старше 50 лет, чаще в 70–79, у женщин в 2–3 раза чаще, чем у мужчин, и не имеющее специальных диагностических тестов [1–3]. В отсутствие последних диагноз РП остается клиническим диагнозом исключения, что последовательно отражено в разработках Европейской антиревматической лиги (EULAR) и Американской коллегии ревматологов (ACR) 2012 и 2015 г. [4, 5], а также в рекомендациях Немецкого ревматологического общества (DGRh), Австрийского общества ревматологии и реабилитации (ÖGR), Швейцарского ревматологического общества (SGR) и других научно-медицинских ассоциаций и организаций 2018 г. [6].
Актуальность совершенствования методов лечения РП обусловлена и прямой связью типичных для этого заболевания остроты и выраженности полимиалгического синдрома с проблемой безопасности приема нестероидных противовоспалительных средств (НПВС) в пожилом возрасте. Важной клинической ассоциацией РП, требующей неотложной консультации ревматолога и эскалации доз глюкокортикоидов (ГК), является гигантоклеточный артериит (ГКА) и связанный с ним повышенный риск развития необратимой слепоты и аортальных осложнений. Остается открытым вопрос сопряженности РП со злокачественными опухолями — как фактора риска (ФР) их развития или паранеопластического синдрома [7–16].
Целью публикации является общая характеристика и обсуждение основных положений и доказательной базы рекомендаций (руководства) по ведению РП Немецкого, Австрийского и Швейцарского ревматологических обществ 2018 г.
Рекомендации DGRh/ÖGR/SGR (2018) по ведению РП
В обсуждаемом руководстве [6] указано на недостаточную изученность этиологии и патогенеза РП и такие возможные ФР ее развития, как «генетические, инфекционные, процессы старения иммунной и сосудистой систем и эндокринные нарушения». Со ссылкой на С. Dejaco и F. Muratore и соавт. (2016) [8, 15] отмечена «возможная связь более выраженных системных, суставных и околосуставных симптомов воспаления с предсуществующим васкулитом». По итогам систематического обзора F. Buttgereit и соавт. (2016) [7], самым частым клиническим признаком РП названа двусторонняя боль в плечах (95 %), другими типичными симптомами — остро или подостро возникшая боль в шее или тазовом поясе и выраженная утренняя скованность, возможными проявлениями — артриты и теносиновиты проксимальных суставов (плечевых, тазобедренных) и дистальных (суставов кисти, коленных), а также конституциональные признаки — лихорадка, ухудшение аппетита, слабость и/или похудение [8, 14]. Подчеркнуто, что на практике диагноз РП устанавливают при сочетании типичных клинических проявлений с повышенной скоростью оседания эритроцитов (СОЭ) и/или уровнем С-реактивного белка (СРБ), и точность диагноза возрастает при выявлении поддельтовидного бурсита, теносиновита двуглавой мышцы плеча и/или синовита плечевого сустава [7]; круг дифференциальной диагностики включает поздний дебют РА, ГКА, хондрокальциноз, инфекции и злокачественные опухоли [8, 15].
Отмечая важность разработок EULAR/ACR 2012 и 2015 г. [4, 5], в 2018-м немецкие, австрийские и швейцарские эксперты указали на «большое разнообразие подходов к ведению РП в клинической практике в немецкоязычных странах, Европе и мире в целом». В центре их внимания оказался вопрос применения фармакологических и нефармакологических подходов для достижения оптимального соотношения пользы и риска при лечении РП. Целевой группой руководства DGRh/ÖGR/SGR определены «все взрослые пациенты с клиническим подозрением на РП». Разработка предназначена «для всех врачей, занимающихся ведением больных РП, прежде всего ревматологов, а также задействованных представителей не врачебных профессиональных групп… и, возможно, пациентов и их родственников». Ее основу составили рекомендации EULAR/ACR (2015) [5], «адаптированные для немецкоязычных стран» [6].
Ранее нами установлено участие большого количества специальных медицинских сообществ и общественных организаций в разработке, региональной адаптации и внедрении клинических рекомендаций в Германии [17]. Соавторами обсуждаемого руководства DGRh/ÖGR/SGR стали представители Немецкого общества гериатрии (DGG), Немецкой ревматической лиги, Немецкого общества внутренней медицины (DGIM), Немецкого общества ортопедии и хирургической ортопедии (DGOOC), Немецкого общества физической медицины и реабилитации (DRPMR) и Немецкого общества общей медицины (DGAM). Заседания рабочей группы были проведены в апреле 2016 и феврале 2017 г. При разработке общих принципов и специальных рекомендаций использовали формат PICO (Patients, Intervention, Comparison, Outcome), что позволило сформулировать 12 структурированных вопросов по вмешательствам и 10 по прогностическим факторам, а также методики GRADE (Grading of Recommendations Assessment, Development and Evaluation) и QUIPS (Quality-In-Prognosis Studies) — для оценки качества клинических исследований (КИ), посвященных вмешательствам и прогнозу соответственно. Доказательную базу составили 52 первоисточника, учтенные в рекомендациях EULAR/ACR (2015), и 2663 публикации, найденные в период 01.2014–07.2016 (из которых были отобраны три: одна, представившая итоги открытого моноцентрового КИ применения тоцилизумаба у 10 больных РП [18], и две, посвященные ФР неблагоприятных исходов [16, 19]). Поисковые термины были «релевантны названиям РП, используемым с 1970 г.». Поиск проведен в компьютерных базах данных Cochrane Library, Medline, Embase, CINAHL, Web of Science и дополнен электронным и ручным поиском в «серой литературе», а именно реестрах КИ и материалах конгрессов ACR, EULAR, Британского общества ревматологов и международных конгрессов, посвященных РП, ГКА и другим васкулитам; кроме того, были изучены первоисточники опубликованных статей и проведен опрос экспертов на предмет «возможных дальнейших публикаций» [6].
Пять общих принципов (A, B, C, D, E) ведения больных РП в Германии, Австрии и Швейцарии, предложенные рабочей группой DGRh/ÖGR/SGR, приведены в табл. 1. Авторы исходили из того, что РП-подобные заболевания исключены и пациенты находятся под наблюдением ревматолога, но с общими подходами также ознакомлены семейные врачи, ортопеды, гериатры, физиотерапевты, реабилитологи. Необходимость ведения ревматологами именно пациентов с атипичными проявлениями, осложненным течением или частыми рецидивами РП отражает принцип С [6].
Что касается предикторов неблагоприятных исходов, в руководстве приведены итоги ретроспективных исследований A.T. Hancock и соавт. (Великобритания, 2014) [19] и F.G. Yurdakul и соавт. (Турция, 2015) [16]. В первом, включившем 3249 пациентов первичного звена с РП и 12 735 лиц контрольной группы, доказана связь риска развития сердечно-сосудистых событий с возрастом и мужским полом; когорту второго исследования составил 41 пациент, и различий по ответу на ГК на 3-й нед. лечения в зависимости от пола и наличия/отсутствия периферического артрита не было выявлено.
Обсуждая противоречивость доказательств связи РП с наличием и риском развития злокачественных опухолей, авторы руководства DGRh/ÖGR/SGR сослались на шесть источников (проведенный нами анализ показал, что лишь один из них опубликован в 2017 г., тогда как остальные — в 1993–2002 гг.). При этом была отмечена невозможность разработки общей или специальной рекомендации по выявлению опухолей при РП, отличной от общепринятых положений по онкоскринингу в соответствующих возрастных группах [6]. Приведены данные J.E. Naschitz и соавт. (1996–1997) о бóльшей вероятности паранеопластического характера РП при наличии выраженных конституциональных признаков у лиц моложе 50 лет, асимметричности симптомов, недостаточной эффективности ГК, СОЭ < 40 или > 100 мм/ч и наличии периферического артрита [20, 21], а также данные M. Bellan и соавт. (2017) о том, что «наиболее сильными предик–торами» паранеопластической природы РП являются наличие ≥ 6 болезненных суставов, возраст ≥ 75 лет и мужской пол [22]. Обращаясь к принципу С (табл. 1), мы видим, что именно периферический артрит, системные проявления, но и более низкий уровень маркеров воспаления и более молодой возраст (< 60 лет) отнесены к атипичным симптомам и признакам, определяющим ведение пациента ревматологом (в рекомендациях EULAR/ACR — направление на консультацию [5]) и, соответственно, его онкологическую настороженность.
Важной предпосылкой создания руководства DGRh/ÖGR/SGR (2018) на основе рекомендаций EULAR/ACR (2015) и новых доказательств явился систематический обзор F. Buttgereit и соавт. (2016), включивший 20 рандомизированных клинических исследований (РКИ) эффектов лечебных вмешательств (в целом у 1016 пациентов с РП/ГКА) и 30 исследований применения визуализирующих методов для диагностики и/или оценки эффективности терапии (всего 2080 участников). В отношении РП итоги обзора подтвердили эффективность ГК как средств первой линии (в дозе 12,5–25 мг/сут по преднизолону) и полезные эффекты добавления метотрексата, такие как снижение кумулятивной дозы ГК (на 20 %) и частоты рецидивов (на 36 %) [7].
Сопоставив указанные в табл. 1 пять принципов DGRh/ÖGR/SGR с восемью, ранее разработанными EULAR/ACR, отметим как отсутствие значимых различий между ними, так и четкое определение EULAR/ACR ряда исследований «дополнительными» (а именно: содержания в крови белковых фракций, витамина D, тиреотропина, креатинкиназы, антиядерных и антинейтрофильных цитоплазматических антител, тестов на туберкулез, рентгенографии органов грудной клетки) и предложение ими учитывать у больных РП несколько большего перечня сопутствующих болезней (включая недавние переломы, ФР развития глаукомы и ФР развития ПЭ ГК-терапии). Кроме того, индивидуальный план ведения каждого пациента, персонифицированный выбор стартовой дозы и схемы последующего титрования ГК, важность доступа к индивидуальному курсу физических упражнений и быстрого прямого доступа к медицинскому персоналу (при развитии рецидивов или ПЭ терапии) выделены EULAR/ACR как отдельные принципы [1, 5].
Залогом успешного лечения РП в руководстве DGRh/ÖGR/SGR признано совместное принятие решений врачом и соответственно обученным пациентом.
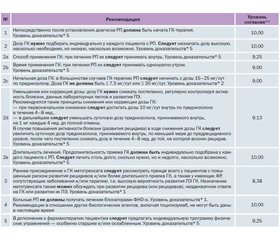
В табл. 2 представлены специальные рекомендации DGRh/ÖGR/SGR по ведению РП — их пять, причем 2-я состоит из пяти подпунктов [6], тогда как ранее EULAR/ACR предложили десять [5]. Их градация в немецкоязычном руководстве соответствует принятой в Германии системе АВ0: А — сильная рекомендация с формулировкой «должно, нужно» (нем.: soll), В — условная рекомендация с формулировкой «следует, может» (нем.: sollte, kann), 0 — «не может быть дано рекомендаций». Как видно из табл. 2, почти по всем положениям достигнут высокий уровень согласия разработчиков (как и по общим принципам), однако в основу 70 % положений (7 из 10) положено экспертное мнение, а не эпидемиологические доказательства. Систематическими обзорами подкреплены две рекомендации (№ 3 и 4), итогами РКИ — одно положение (№ 2с), т.е. 20 и 10 % положений соответственно.
В унисон с позицией EULAR/ACR (2015) в немецкоязычном руководстве указано, что ГК хорошо зарекомендовали себя в клинической практике и остаются средствами 1-й линии терапии РП, поскольку в большинстве случаев приводят к быстрому и выраженному улучшению. В лечении РП не следует использовать НПВС, т.к. потенциальный риск развития ПЭ превышает ожидаемую, обычно небольшую терапевтическую пользу. НПВС и/или анальгетики разрешается применять как дополнительные средства — при наличии боли, обусловленной другой причиной. Специфические рекомендации по анальгетикам не могут быть даны.
Невозможность точнее сформулировать рекомендацию относительно стартовой дозы ГК объяснена тем, что при создании руководства было найдено «слишком мало публикаций высокого уровня доказательности… и слишком много подгрупп пациентов с различным клиническим профилем» [6]. Таким образом, согласовано индивидуальное определение минимальной эффективной дозы с учетом имеющихся ФР развития ПЭ ГК, рецидивов РП и необходимости длительного приема ГК, а также сопутствующих болезней и их лечения, что позволит достичь наилучшего соотношения пользы и риска.
Отметив преобладание в Германии, Австрии, Швейцарии и других немецкоязычных странах назначений ГК внутрь (при РП в частности), авторы руководства указали на «возможность внутримышечного применения метилпреднизолона (МП) — на усмотрение врача» [6]. Доказательную базу этой альтернативы составили успешные результаты применения МП в стартовой дозе 120 мг каждые 3 нед. в двойном слепом сравнительном исследовании В. Dasgupta и соавт. (1998) [23].
При формулировке положения о времени приема ГК авторы обсуждаемого руководства учли «отсутствие КИ по этому вопросу, опирались на клинический опыт и вероятность… развития гипоталамо-гипофизарно-надпочечниковой недостаточности, нарушений циркадных ритмов и сна» и высказались против разделения суточной дозы ГК во всех случаях РП. По их мнению, это возможно в отдельных ситуациях, таких как появление ночных болей при достижении дозы < 5 мг/сут по преднизолону. Приведены данные М. Cutolo и соавт. (2017), изучивших в небольшом КИ (n = 62) эффекты применения при недавно развившейся РП преднизолона с модифицированным высвобождением по сравнению с обычным преднизолоном: на 4-й нед. часть пациентов, ответивших на терапию, в основной группе оказалась большей, чем в контрольной (53,8 % против 40,9 %) [24]. Однако на формулировке рекомендации это доказательство не отразилось [6].
В отношении стартовой дозы ГК DGRh/ÖGR/SGR рекомендует рассматривать назначение бóльших доз (до 25 мг/сут по преднизолону) больным РП с повышенным риском развития рецидивов и низким риском развития ПЭ ГК; меньшим дозам (около 15 мг/сут) следует отдавать предпочтение у пациентов, имеющих СД, остеопороз, глаукому или другие ФР развития ПЭ ГК. Указано, что в немецкоязычных странах Европы не принято начинать лечение РП с дозы 12,5 мг/сут. Подчеркнута необходимость «индивидуального» подхода к снижению дозы ГК в ходе лечения РП и коррекции доз при развитии рецидивов заболевания, что подразумевает учет профиля ФР и результатов клинико-лабораторного мониторинга пациентов, включающего контроль переносимости ГК [6]. При этом руководство DGRh/ÖGR/SGR ссылается на рекомендации EULAR 2010 г. по мониторингу ПЭ низкодозовой ГК-терапии в клинических испытаниях и медицинской практике [25] и более позднюю разработку индекса токсичности ГК (Miloslavsky E.M. и соавт., 2017) [26]. Отмечены принципы скорейшего снижения бóльших стартовых доз (таких как 25 мг/сут) по сравнению с меньшими (15 мг/сут) и поддержания «здоровья костей» на основе рекомендаций немецкоязычных научных обществ остеологии 2009 и 2014 г. [27, 28].
Обращает на себя внимание отсутствие в немецкоязычном руководстве указаний на целесообразность повышения дозы ГК при персистенции симптомов и подтверждении диагноза РП через 2–4 нед. в соответствии с алгоритмом EULAR/ACR (2015) [1, 2, 5].
Что касается метотрексата, то, в отсутствие «типичной клинической ситуации, при которой несомненно показано его назначение», и ссылаясь на публикации 1985–2013 гг. [29–37], авторы руководства DGRh/ÖGR/SGR указали на необходимость индивидуализированного применения этого препарата при РП и целесообразность рассмотрения его прежде всего у женщин, в случаях значительно повышенной СОЭ (> 40 мм/ч), наличия периферического артрита или сопутствующих заболеваний, повышающих риск развития ПЭ ГК [6]. Именно эти факторы считают основными (хотя и не установленными) ФР рецидива/потребности в длительной терапии, а периферический артрит — атипичной манифестацией РП [1, 5], что в итоге предполагает назначение метотрексата именно ревматологом.
Достигнуто общее согласие с тем, что дополнительная терапия метотрексатом должна быть рассмотрена при рецидиве/рецидивах РП, неадекватном ответе на ГК или развитии их ПЭ. Созвучно с разработкой EULAR/ACR (2015) [5] и обзорами F. Buttgereit и C. Dejaco и соавт. (2016) [7, 8], в руководстве для немецкоязычных стран указано, что основу этих положений составили «частично противоречивые» итоги нескольких рандомизированных и одного ретроспективного КИ; кроме того, отмечено лучшее качество исследований, подтвердивших пользу метотрексата при РП (в отношении частоты рецидивов, кумулятивной дозы ГК и возможности их отмены), по сравнению с теми, в которых получили негативные результаты. У лиц с нарушенной функцией почек рекомендовано избегать лечения метотрексатом или тщательно его контролировать. Отмечена слабая доказательная база экономических эффектов метотрексата при РП и невозможность сформулировать рекомендации по применению других традиционных болезнь-модифицирующих антиревматических средств — в связи с отсутствием релевантных КИ [6].
Приведенное в табл. 2 положение № 4 по неприменению ингибиторов фактора некроза опухоли названо «обескураживающим» [6], хотя ранее их также не рекомендовали EULAR/ACR [5]. Авторы объясняют его отсутствием доказательств эффективности этих препаратов при РП и наличием данных о плохой переносимости и высокой стоимости такого лечения. По состоянию на время издания руководства DGRh/ÖGR/SGR (2018) после предшествующей разработки EULAR/ACR (2015) позитивный эффект применения тоцилизумаба подтвердился лишь в одном открытом КИ IIa фазы (Lally L. и соавт., 2016) [18]. Критикуя методологию и статистическую мощность этого исследования, авторы обсуждаемого руководства сочли невозможным сформулировать положение по применению тоцилизумаба при РП. То же было отмечено для препаратов других моноклональных антител — ввиду отсутствия опубликованных результатов проспективных КИ их эффектов [6].
Сохранение мышечной массы и функции и снижение риска падений названы желаемыми целями лечения РП — в отсутствие исследований, подтвердивших пользу физиотерапевтических вмешательств (табл. 2). При этом индивидуализированное применение программ физических упражнений «представляется особенно полезным для пожилых и/или ослабленных больных РП… несмотря на отсутствие доказательств и принимая во внимание настойчивое желание пациентов» [6].
Наконец, отметим отсутствие в немецкоязычном руководстве аналога рекомендации EULAR/ACR (2015) о противопоказании назначения больным РП китайских травяных препаратов Yanghe и Biqi.
В заключительной части руководства DGRh/ÖGR/SGR (2018) констатируется ведущая роль ГК в лечении РП, несмотря на слабость доказательной базы по таким ключевым позициям, как стартовая доза, режим ее снижения и длительность терапии, что связано с неоднородностью подгрупп пациентов. Основу этого документа, созданного с целью поддержки врачей Германии, Австрии и Швейцарии в принятии клинических решений, касающихся ведения больных РП, в том числе персонифицированного, составили изданные тремя годами ранее рекомендации EULAR/ACR и консенсус экспертов указанных стран.
Проведенный нами информационный анализ показал как высокий уровень согласия разработчиков руководства DGRh/ÖGR/SGR по всем общим принципам и специальным рекомендациям, так и преобладание экспертного мнения как основы их формулировок (70 % положений). Важными особенностями и отличиями этой разработки от ее прототипа — рекомендаций EULAR/ACR — являются: усиление внимания к атипичным проявлениям РП (периферическому артриту, системным признакам, более молодому возрасту пациентов и низким показателям воспаления), требующим наблюдения ревматолога и онкологической настороженности; предложение более высокой минимальной стартовой дозы ГК (15, а не 12,5 мг/сут); отсутствие такой опции, как повышение дозы ГК через 2–4 нед. при персистенции симптомов и подтверждении диагноза РП; приведение четкого перечня необходимых диагностических тестов, а также первых доказательств эффектов применения при РП тоцилизумаба; отсутствие рекомендации против назначения ряда средств традиционной китайской медицины.
Сопоставим данную разработку с клинической рекомендацией «Ревматическая полимиалгия» Финской медицинской ассоциации, использование которой как нового клинического протокола, без адаптации, было утверждено приказом Министерства здравоохранения Украины в декабре 2016 г. [38, 39]. Оба медицинских стандарта рекомендуют стартовую дозу преднизолона не ниже 15 мг/сут (одновременно начиная профилактику остеопороза), однако в финском/украинском документе максимальная стартовая доза ГК не превышает 20 мг/сут, и отмечено, что необходимость применения бóльших доз возникает редко; пересмотр диагноза рекомендован при отсутствии симптоматического улучшения через 3–5 дней; снижение дозы предложено начинать через 2–4 нед. «на 2,5 мг ежемесячно, затем медленнее». Исключение латентных злокачественных опухолей названо необязательным у больных с типичной клинической картиной; показаниями к консультации ревматолога определены подозрение на ГКА, атипичная клиническая картина и недостаточный ответ на лечение, и среди них четко описано именно первое — наличие у пациента головной боли, болезненности волосистой части головы, нарушений зрения, перемежающейся боли в челюсти или конечности. «Типичными клиническими данными» определены возраст > 50 лет, СОЭ > 40 мм/ч и «быстрый ответ на 10–20 мг/сут преднизолона в течение 3 дней». Обязательными диагностическими тестами названы лишь СОЭ, СРБ и общий анализ крови с определением содержания тромбоцитов; остальные исследования немногочисленны (щелочная фосфатаза, креатинкиназа, ревматоидный фактор, антитела к циклическому цитруллинированному пептиду, ультразвуковое исследование плечевых и тазобедренных суставов — как полезный компонент начальных исследований, биопсия височной артерии — при подозрении на ГКА) и приведены в аспекте дифференциальной диагностики, круг которой включает РА, спондилоартриты, васкулиты, заболевания соединительной ткани, полимиозит, остеоартрит, адгезивный капсулит, фибромиалгию, гипотиреоз, вирусные инфекции, депрессию, миеломную болезнь, другие злокачественные опухоли. Лечебная тактика при обострении РП предполагает возврат к более высокой дозе ГК. Адъювантная терапия метотрексатом предложена при недостаточном ответе на ГК или развитии их ПЭ; его возможной альтернативой назван азатиоприн — в отличие от руководств DGRh/ÖGR/SGR и EULAR/ACR. Еще одной особенностью нового клинического протокола является рекомендация контролировать лишь небольшой перечень параметров при ведении больных РП: СОЭ, содержание в крови СРБ, форменных элементов, креатинина, глюкозы и электролитов [39]. Выявленные различия между рекомендациями DGRh/ÖGR/SGR и Финской медицинской ассоциации (т.е. новым украинским клиническим протоколом) можно объяснить их приоритетным предназначением (для ревматологов и специалистов первичного звена соответственно) и особенностями методологии их разработки, а также экономическими факторами.
Заключение
Единые рекомендации немецкого, австрийского и швейцарского ревматологических обществ и других научно-медицинских ассоциаций и организаций (DGRh/ÖGR/SGR, 2018), разработанные для преодоления различий в подходах к ведению больных РП в указанных странах Европы на основе адаптации рекомендаций EULAR/ACR (2015), пересмотра их первоисточников и более 2,6 тыс. новых доказательств, опубликованных в 2014–2016 гг., представляют большой интерес в условиях постарения популяции, миграции медицинских кадров и необходимости повышения качества медицинской помощи пациентам пожилого возраста с синдромом полимиалгии и РП в частности.
Содержание общих принципов и специальных рекомендаций DGRh/ÖGR/SGR по ведению РП в целом соответствует прототипу, однако имеет особенности, касающиеся стартовых доз ГК и их коррекции, перечня диагностических тестов и информации, касающейся применения тоцилизумаба и средств традиционной китайской медицины.
Перспективу усиления доказательной базы ведения РП в клинической практике отражает тот факт, что более 2/3 рекомендаций DGRh/ÖGR/SGR базируется на мнении экспертов. При этом лечение больных РП, как правило, сопряжено с проблемами коморбидности, переносимости обезболивающей и противовоспалительной терапии и своевременного выявления ГКА (что освещается также в украинском протоколе) и злокачественных опухолей (что четче представлено в немецкоязычном руководстве).
Систематическое изучение медико-технологических документов по стандартизации медицинской помощи, разработанных в развитых странах на основе доказательного и консенсусного подходов, является необходимой предпосылкой развития системы национальных медицинских стандартов, способствует их гармонизации и регулярному обновлению и открывает перспективы повышения качества медицинской помощи пациентам с заболеваниями костно-мышечной системы в Украине.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов и финансовой поддержки, гонораров и других форм вознаграждения при подготовке данной статьи.
Список литературы
Список литературы находится в редакции

/4_m.jpg)
/4_m2.jpg)