Вступ
Депресія є одним з найпоширеніших психічних розладів, що робить вагомий внесок в глобальний тягар психопатології [1–3]. Незважаючи на широкий спектр апробованих антидепресантів, досягти бажаного ефекту лікування вдається не завжди. Купірування гострої депресивної симптоматики реєструється в 60–70 % хворих, ремісії вдається досягти лише в 20–40 % пацієнтів [4]. На сучасному етапі розробки та вдосконалення методів терапії депресивних розладів усе більше уваги приділяється участі нейротрансмітерів, перш за все моноамінів, у патогенезі захворювання й особливостям впливу антидепресивних засобів на ці ланки [5].
Розробка антидепресантів, що взаємодіють як із серотонінергічними, так і з норадренергічними рецепторами, тобто з подвійним механізмом дії, призвела до створення нового класу препаратів — селективних інгібіторів зворотного захвату серотоніну та норадреналіну (СІЗЗСН). Поява антидепресантів із подвійним механізмом дії супроводжувалася суттєвим підвищенням ефективності лікування депресивних станів [6–8].
Одним із СІЗЗСН є венлафаксин — перший серед тимоаналептиків третього покоління. Однак механізм дії венлафаксину фактично полягає в потрійному впливі, оскільки він пригнічує активність не лише серотоніну та норадреналіну, а й дофаміну.
Сьогодні доведена дозозалежність терапевтичного ефекту венлафаксину. Завдяки широкому діапазону терапевтичної дії венлафаксин послідовно включає в спектр своєї нейрохімічної активності серотонінергічні, норадренергічні та дофамінергічні рецептори [9]. При порівнянні ефективності венлафаксину з антидепресантами групи СІЗЗС в метааналізі 34 рандомізованих подвійних сліпих досліджень, що включали хворих на депресивні розлади різного ступеня вираженості, були встановлені статистично значущі переваги венлафаксину як засобу для досягнення ремісії [10].
Відзначено високу ефективність венлафаксину при широкому спектрі депресивних станів у рамках рекурентного й біполярного афективного розладів [11], а також при генералізованій тривозі, соматогенній та постінсультній депресії [12]. Виявлений факт більшої ефективності венлафаксину порівняно з СІЗЗС в терапії тяжких депресій прямо пов’язують з наявністю подвійного механізму дії препарату [13]. Підкреслюються сприятливий профіль переносимості й невисока частота побічних ефектів у процесі терапії венлафаксином [11].
В Україні з’явився венлафаксин ізраїльського виробництва (компанія «Асіно») — Лафаксин XR, який випускається у формі таблеток пролонгованої дії, що містять 75 і 150 мг венлафаксину. Препарат повністю відповідає всім критеріям якості та біоеквівалентності, а інноваційна схема пролонгованого вивільнення забезпечує стабільну концентрацію препарату в плазмі крові та згладжування піків концентрації, що сприяє досягненню кращого комплаєнсу і зниженню ризику розвитку побічних ефектів, а отже, забезпечує кращу переносимість порівняно зі звичайною (IR) формою [14]. При цьому в низьких дозах (до 150 мг/добу) препарат діє як інгібітор зворотного захвату серотоніну, при підвищенні дози (до 225 мг/добу) — серотоніну і норадреналіну, у разі подальшого збільшення дози (до 375 мг/добу) — серотоніну, норадреналіну і дофаміну [15].
Разом із вищезазначеним у рамках проведеного нами дослідження визначені характерні особливості в системах периферичних катехоламінів у хворих на депресивні розлади, які мають діагностичну та прогностичну значущість і демонструють їх узгоджену та взаємопов’язану динаміку, специфічну для окремої форми депресивного розладу. Виявлено, що норадреналін є прогностичним фактором перебігу депресивних розладів та свідчить про хронізацію розладу. У пацієнтів із депресивними епізодами та рекурентними депресивними розладами вміст норадреналіну вірогідно нижчий, ніж в осіб без психічних розладів (на 43,00 і 48,00 % відповідно) [16].
Метою даного дослідження була оцінка ефективності венлафаксину XR — таблетки пролонгованої дії 75 мг в терапії пацієнтів із рекурентними депресивними розладами.
Матеріали та методи
У дослідженні взяли участь 42 пацієнти з рекурентними депресивними розладами різного ступеня тяжкості (серед них 6 пацієнтів із легким епізодом, 27 — із помірним епізодом та 9 — із тяжким епізодом без психотичних симптомів). Діагноз був встановлений з урахуванням критеріїв МКХ-10 (F 33.0, 33.1, 33.2). Середній вік групи обстежених становив 42,58 ± 6,97 року. Середня тривалість захворювання від його першої маніфестації дорівнювала 6,8 року, середня кількість перенесених до включення в дослідження депресивних епізодів була 3,7. Тривалість поточного депресивного епізоду до початку прийому досліджуваного препарату в середньому становила 4,3 міс. Усі пацієнти отримували венлафаксин XR в дозі 75 мг на добу з кроком титрування 2 тижні до 225 мг на добу, що зумовлене спектром нейрохімічної активності препарату та залученням бажаних нор-адренергічних ефектів зазначеного дозування.
Особливості клінічного стану пацієнтів та його динаміка оцінювалися до лікування (день 1), у процесі терапії (день 42), а також після завершення лікування (день 90). Проводився постійний моніторинг небажаних явищ та аналіз їх зв’язку з препаратом, що досліджується.
Використовувався комплексний підхід, що включав такі методи: клініко-психопатологічний (вивчення скарг, клінічного анамнезу, катамнезу, психопатологічного стану та його динаміки); психодіагностичний на базі шкали депресій Центру епідеміологічних досліджень (CES-D) [17] та шкали депресії Гамільтона (HDRS) [17]; методи математичної статистики.
Результати та обговорення
Структура клініко-психопатологічних проявів депресивного спектра в пацієнтів із рекурентними депресивними розладами на момент першої оцінки характеризувалася наявністю афективних, мотиваційно-вольових, когнітивних, психомоторних та соматичних порушень (табл. 1). Аналіз отриманих даних свідчить про те, що у всіх 100,00 % обстежених провідним симптомом був пригнічений настрій. Серед мотиваційно-вольових проявів найчастіше спостерігалися зменшення активності та ініціативи (90,48 %) і відчуття відсутності перс-пективи (83,33 %), а в структурі когнітивних порушень — зниження концентрації уваги (88,06 %) та психічна виснаженість (80,95 %). Психомоторні порушення в групі обстежених були представлені переважно ретардацією (57,14 %), соматичні — фізичною стомлюваністю (80,95 %) та розладами сну (78,57 %).
/86.jpg)
У результаті терапії венлафаксином XR було виявлене суттєве поліпшення психічного стану пацієнтів. При оцінці клініко-психопатологічної симптоматики на 42-й та 90-й день терапії спостерігалося вірогідне зменшення інтенсивності всього спектра показників порівняно з вихідними даними (р < 0,001). Обстеження пацієнтів на момент закінчення 90-денного курсу лікування виявило, що незначне зниження фону настрою, що не доходив до ступеня депресії, зберігалося лише в 14,29 % осіб, зниження концентрації уваги — в 11,90 % осіб, зменшення активності та ініціативи — у 9,52 %, фізична стомлюваність — у 7,14 % та ретардація — лише в 4,76 % осіб.
Аналіз клініко-психопатологічних особливостей обстежених пацієнтів був доповнений даними шкали депресій Центру епідеміологічних досліджень США (CES-D) [17]. Шкала CES-D належить до суб’єктивних та призначена для виявлення та оцінки тяжкості депресії. Необхідно враховувати, що шкала CES-D є інструментом самодіагностики й відображає сприйняття пацієнтами власної хвороби та, як наслідок, якості їхнього життя.
На момент першого обстеження за шкалою CES-D діагностовані переважно розлади помірного ступеня тяжкості (54,76 % хворих) (табл. 2). Розлади тяжкого та легкого ступеня тяжкості виявлені в 33,33 та 11,91 % пацієнтів відповідно. При цьому діагноз тяжкого депресивного епізоду з урахуванням критеріїв МКХ-10 був встановлений лише в 21,43 % обстежених, що може свідчити про суб’єктивну переоцінку тяжкості свого стану в 11,90 % пацієнтів цієї категорії. Середнє значення балів за шкалою CES-D у групі обстежених для розладів легкого, помірного та тяжкого ступенів тяжкості становило 21,20; 27,57 та 36,57 бала відповідно.
На 42-й день терапії венлафаксином XR зареєстроване вірогідне зменшення відсотка клінічних проявів тяжкого депресивного епізоду (9,52 % осіб; р < 0,005). На момент завершальної оцінки (день 90) за шкалою в обстежених пацієнтів відзначалися показники, що відповідають розладам лише легкого ступеня тяжкості та субклінічним проявам депресії в 14,29 та 85,71 % осіб відповідно.
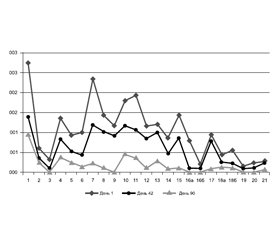
Більш детальний аналіз середнього значення балів за пунктами шкали CES-D наведений на рис. 1.
Найбільші показники у групі обстежених при першій оцінці відзначалися за такими пунктами: 12 — «Я не почуваю себе щасливою людиною» (2,06 ± 0,67 бала), 10 — «Я відчуваю занепокоєння, страхи» (1,92 ± 0,63 бала), 3 — «Незвжаючи на допомогу друзів та членів моєї родини, мені не вдається позбутися почуття туги» (1,88 ± 0,69 балів), 16 — «Життя не дає мені задоволення» (1,86 ± 0,78 бала). При завершальній оцінці за пунктами шкали CES-D показники 1–14 та 16–20 були вірогідно меншими, ніж при першому обстеженні (t ≥ 3,714). Отримані дані свідчать, що в результаті терапії досліджуваним препаратом у пацієнтів цієї категорії відзначалося суттєве полегшення суб’єктивного відчуття тяжкості свого стану та підвищення й відновлення самооцінки.
Для об’єктивізації оцінки клінічної структури епізоду та його редукції в динаміці використовувалася психометрична шкала депресії Гамільтона [17]. За шкалою HDRS було встановлено, що стан переважної більшості пацієнтів (64,29 %) на 1-й день оцінки відповідав помірному депресивному епізоду. У той же час тяжкому та легкому депресивним епізодам відповідав стан 21,43 та 14,28 % осіб відповідно. На 42-й день терапії частка хворих на тяжкий депресивний епізод зменшилася в > 2 рази, на 90-й день терапії ознак тяжкого епізоду в групі обстежених не виявлено. При цьому на 42-й день у результаті проведеної терапії досліджуваним препаратом середнє значення балів для тяжкого та помірного депресивних епізодів знизилося на > 30 %.
Детальний аналіз середнього значення балів за пунктами шкали HDRS наведений на рис. 2.
У хворих із рекурентними депресивними розладами до терапії відзначалися такі найбільші показники: 1 — депресивний настрій (2,75 ± 0,52 бала), 7 — робота та діяльність (2,34 ± 0,93 бала), 11 — соматична тривога (1,93 ± 0,75 бала), 10 — психічна тривога (1,80 ± 0,67 бала), 15 — іпохондричні розлади (1,57 ± 0,82 бала).
Оцінка стану пацієнтів у динаміці продемонструвала, що вираженість клінічних проявів за переважною більшістю пунктів шкали HDRS (60,87 %) — 1, 3–8, 10–15 та 18б — уже на 42-й день лікування вірогідно зменшилася порівняно з першим обстеженням (t ≥ 2,2030), що переконливо свідчить про ефективність обраної терапії. Найбільше зниження проявів депресії спостерігалося за пунктами: 1 — депресивний настрій, 7 — робота та діяльність, 11 — соматична тривога, 10 — психічна тривога (t ≥ 10,4486, t ≥ 6,0217, t ≥ 5,6152 та t ≥ 4,7404 відповідно). Таким чином, оцінка стану пацієнтів на 42-й день терапії венлафаксином XR свідчить про суттєве підвищення їх соціальної адаптації.
Під час дослідження проводився моніторинг небажаних явищ на всіх етапах терапії. На фоні прийому венлафаксину XR серйозних небажаних явищ у пацієнтів не виявлено. Серед зареєстрованих побічних ефектів, що, можливо, пов’язані із прийомом досліджуваного препарату, визначені: незначне підсилення тривоги (11,90 % осіб), нудота транзиторного характеру (9,52 %), вегетативні прояви несистемного характеру (4,76 %). Варто зазначити, що вказані небажані явища редукувалися самостійно, додаткова терапія не застосовувалася, доза досліджуваного препарату не змінювалася.
Висновки
Таким чином, результати клінічного застосування венлафаксину XR при рекурентних депресивних розладах показали його високу антидепресивну активність. У 88,10 % хворих мав місце чіткий позитивний терапевтичний ефект зі зменшенням ступеня тяжкості клінічної симптоматики (за HDRS) на 50 % і більше.
Завдяки широкому спектру антидепресивної дії, а також хорошій переносимості Лафаксин XR може бути рекомендований як препарат вибору при лікуванні тяжких і помірних депресивних епізодів. Препарат із вираженою антидепресивною активністю збалансованої дії Лафаксин XR (венлафаксин) на сучасному етапі розвитку психофармакотерапії по праву може бути віднесений до високоефективних представників класу антидепресивних сполук.
Конфлікт інтересів. Не заявлений.
Список литературы
1. Depression. The treatment and Management of depression in adults (updated edition). National Clinical Practice Guideline 90. Режим доступу: www.nice.org.uk/guidance/cg90/evidence/full-guidance-243833293
2. Терапия антидепрессантами и другие методы лечения депрессивных расстройств. Доклад Рабочей группы CINP на основе обзора доказательных данных. Под ред. В.Н. Краснова. М., 2008. 215 С.
3. Марута Н.О., Панько Т.В., Федченко В.Ю., Семікіна О.Є. Клініко-психопатологічні прогностичні фактори перебігу первинних депресивних розладів. Психічне здоров’я. 2017. Т. 2, вип. 51. С. 117-119.
4. Бауэр М., Пфенниг А., Северус Э., Вайбрау П.С., Ангст Ж., Мюллер Х.-Ю. Клинические рекомендации Всемирной федерации обществ биологической психиатрии по биологической терапии униполярных депрессивных расстройств. Часть 1: Острое и продолженное лечение униполярных депрессивных расстройств по состоянию на 2013 год. Современная терапия психических расстройств. 2015. 4. 33-39.
5. Дробижев М.Ю., Овчинников А.А., Кикта С.В. Механизмы действия антидепрессантов и патогенез психических расстройств. В чем соответствия? Социальная и клиническая психиатрия. 2017. 27 (3). Р. 94-101.
6. Thase M.E., Entsuah A.R., Rudolph R.L. Remission rates during treatment with venlafaxine or selective serotonin reuptake inhibitors. Br. J. Psychiatry. 2001. 178. Р. 234-241.
7. Vermeiden M.L., Mulder P.G., van den Broek W.W., Bruijn J.A. A double-blind randomized study comparing plasma level-targeted dose imipramine and high-dose venlafaxine in depressed inpatients. J. Psychiatr. Res. 2013. 47. 10. Р. 1337-1342.
8. Entsuah A.R. et al. Response and remission rates in different subpopulations with major depressive disorder administered Venlafa-xine, selective serotonin reuptake, or placebo. J. Clin. Psychiatry. 2001. 62. 11. Р. 869-877.
9. Вельтищев Д.Ю. Эффективность венлафаксина (велаксин) при лечении депрессии: результаты современных исследований. Журнал неврологии и психиатрии. 2013. 11. Р. 79-81.
10. Nemeroff C.B., Entsuah R., Benattia I., Demitrack M., Sloan D.M., Thase M.E. Comprehensive analysis of remission with venlafaxine versus SSRI. Biol. Psychiatr. 2008. 63. Р. 424-434.
11. Ястребов Д.В. Терапевтически резистентные депрессии в клинике пограничной психиатрии. Журнал неврологии и психиатрии. 2011. 111. 4. С. 47-50.
12. Мосолов С.Н., Костюкова Е.Г., Городничев А.В., Тимофеев И.В., Ладыженский М.Я., Сердитов О.В. Клиническая эффективность и переносимость препарата венлафаксин (велаксин) при лечении умеренной и тяжелой депрессии. Трудный пациент. 2007. 11. С. 72-78.
13. Barak Y., Swartz M., Barcuch Y. Venlafaxine or a second SSRI: switching after treatment failure with an SSRI among depressed inpatients: a retrospective analysis. Progr. Neuropsychopharmacol. & Biol. Psychiat. 2011. Vol. 35. P. 1744-1747.
14. Бурчинский С.Г. Венлафаксин в лечении депрессивных расстройств: от фармакологии к фармакотерапии. НейроNews. Здоров’я України. 2015. № 7. С. 30-34.
15. Smith D., Dempster C., Glanville J. et al. Efficacy and tole-rability of venlafaxine compared with selective serotonin reuptake inhibitors and other antidepressants: a meta-analysis. Br. J. Psychiatry. 2002. 180. Р. 396-404.
16. Федченко В.Ю. Фактори прогнозу формування, перебігу та виходу депресивних розладів (клініко-психопатологічні, патопсихологічні та біохімічні підходи). Автореф. дис... д-ра мед. наук. Харків, 2019. 43 с.
17. Смулевич А.Б. Депрессии при соматических и психических заболеваниях. М.: Медицинское информационное агентство, 2003. 209 с.
/87.jpg)

/86.jpg)
/87_2.jpg)
/88.jpg)